PLCD4基因作为胃腺癌转移诊断标志物的用途的制作方法
本发明涉及生物技术领域,具体地涉及plcd4基因在胃腺癌转移的诊断、治疗中的用途。
背景技术:
胃癌是源于胃粘膜上皮细胞的恶性肿瘤,主要为腺癌。2008年全球新诊断出胃癌近100万例,病死人数74万,是全世界发病率第四、致死率第二的癌症,是一种临床上常见的恶性肿瘤。虽然胃癌全球总发病率有所下降,但有将近三分之二的胃癌病例集中在经济欠发达国家和地区,中国及其他东亚国家高发。据《生命时报》2014年发布的最新版“中国癌症地图”。我国每年新发肿瘤病例约为3120000例,平均每天8550例,每分钟有6人被诊断为癌症,有5人死于癌症。而根据世界卫生组织的调查显示,我国属于胃癌高发区,辽宁、山东、甘肃、江苏、福建等省情况更为严重。在临床上,尽管早期胃癌的治疗己经取得了重大进步,常用外科手术切除加区域淋巴结清扫及术后放化疗支持,然而晚期胃癌的长期生存率仍然很低。很多文献及研究表明,肿瘤的侵袭、转移导致了大部分胃癌患者的死亡并在胃癌的不良预后中扮演关键角色。胃癌的侵袭、转移是一个多基因调控、多因子参与、多步骤进行的复杂的生物学过程,一般认为癌细胞的运动和侵袭能力是产生转移的重要条件。但对于晚期胃癌,其侵袭和转移潜在的分子机制尚不明确。因而寻找可靠的肿瘤预后的标志性因子,并找到能够有效抑制肿瘤转移和侵袭的分子靶点,改善肿瘤的预后,是近年来研究的热点,也是肿瘤研究中的一个重点和难点。因此,迫切的需要鉴别胃癌进展期的重要分子,研发新的药物作用靶点,为肿瘤的治疗和患者的预后提供有价值的帮助。
近年来,研究发现了与胃腺癌转移相关的基因标志物,如申请号:201710823744.7,申请号:201710823754.0,申请号:201710823753.6申请号:201710823745.1申请号:201710822660.1公开的。肿瘤是一种多基因触发型疾病,与众多基因的表达异常相关,为了提高肿瘤诊断的精确性,需要将多基因联合诊断,由于目前发现的用于胃腺癌转移的基因标志物不多,因此需要开发更多的标志物以用于临床诊断。
技术实现要素:
本发明的目的之一在于提供一种通过检测plcd4基因表达差异来实现胃腺癌转移诊断的方法。
本发明的目的之二在于提供一种通过促进plcd4基因表达来治疗胃腺癌转移的方法。
本发明的目的之三在于提供一种用于筛选胃腺癌转移治疗药物的方法。
本发明的目的之四在于提供一种用于治疗胃腺癌转移的药物。
为了实现上述目的,本发明采用了如下技术方案:
本发明提供了检测plcd4的试剂在制备胃腺癌转移诊断工具中的应用。
进一步,所述检测plcd4的试剂包括检测plcd4基因表达量的试剂。
更进一步,所述检测plcd4的试剂包括能够定量plcd4基因mrna的试剂,和/或能够定量plcd4蛋白的试剂。
本发明的定量plcd4基因mrna的试剂可基于使用核酸分子的已知方法来发挥其功能:如pcr、如southern杂交、northern杂交、点杂交、荧光原位杂交(fish)、dna微阵列、aso法、高通量测序平台等。使用该试剂可以定性地、定量地、或半定量地实施分析。
进一步,所述pcr方法为已知方法,例如,arms(amplificationrefractorymutationsystem,扩增不应突变系统)法、rt-pcr(逆转录酶-pcr)法、嵌套pcr法等等。扩增的核酸可以通过使用点印迹杂交法、表面等离子共振法(spr法)、pcr-rflp法、原位rt-pcr法、pcr-sso(序列特异性寡核苷酸)法、pcr-ssp法、ampflp(可扩增片段长度多态性)法、mvr-pcr法、和pcr-sscp(单链构象多态性)法来检测。
所述能够定量plcd4基因mrna的试剂可以是plcd4基因或转录本的特异性引物,也可以是plcd4基因或转录本的特异性识别探针,或同时包括引物和探针。
上面所述的plcd4基因或转录本的特异性引物包括实时定量pcr中使用的特异扩增plcd4基因的引物。在本发明的的具体实施例中,所述引物序列如seqidno.1和seqidno.2所示。
引物可以通过化学合成来制备,通过使用本领域技术人员知道的方法参考已知信息来适当地设计,并通过化学合成来制备。
探针可以通过化学合成来制备,通过使用本领域技术人员知道的方法参考已知信息来恰当设计,并通过化学合成来制备,或者可以通过从生物材料制备含有期望核酸序列的基因,并使用设计用于扩增期望核酸序列的引物扩增它来制备。
本发明的定量plcd4蛋白的试剂可基于使用抗体的已知方法来发挥其功能:例如,可以包括elisa、放射免疫测定法、免疫组织化学法、western印迹等。
本发明的定量plcd4蛋白的试剂包括特异性结合plcd4蛋白的抗体或其片段。可以使用任何结构、尺寸、免疫球蛋白类别、起源等的抗体或其片段,只要它结合靶蛋白质即可。本发明的检测产品中包括的抗体或其片段可以是单克隆的或多克隆的。抗体片段指保留抗体对抗原的结合活性的抗体一部分(部分片段)或含有抗体一部分的肽。抗体片段可以包括f(ab′)2、fab′、fab、单链fv(scfv)、二硫化物键合的fv(dsfv)或其聚合物、二聚化v区(双抗体)、或含有cdr的肽。本发明的定量plcd4蛋白的试剂可以包括编码抗体或编码抗体片段的氨基酸序列的分离的核酸,包含该核酸的载体,和携带该载体的细胞。
抗体可以通过本领域技术人员公知的方法来获得。例如,制备保留整个或部分靶蛋白质的多肽或整合编码它们的多核苷酸的哺乳动物细胞表达载体作为抗原。使用抗原免疫动物后,从经过免疫的动物获得免疫细胞并融合骨髓瘤细胞以获得杂交瘤。然后从杂交瘤培养物收集抗体。最后可以通过使用被用作抗原的plcd4蛋白或其部分对获得的抗体实施抗原特异性纯化来获得针对plcd4蛋白的单克隆抗体。可以如下制备多克隆抗体:用与上文相同的抗原免疫动物,从经过免疫的动物收集血液样品,从血液中分离出血清,然后使用上述抗原对血清实施抗原特异性纯化。可以通过用酶处理获得的抗体或通过使用获得的抗体的序列信息来获得抗体片段。
标记物与抗体或其片段的结合可以通过本领域普遍知道的方法来实施。例如,可以如下荧光标记蛋白质或肽:用磷酸盐缓冲液清洗蛋白质或肽,添加用dmso、缓冲剂、等准备的染料,然后混合溶液,再于室温放置10分钟。另外,标记可使用商品化的标记试剂盒,诸如生物素标记试剂盒,如生物素标记试剂盒-nh2、生物素标记试剂盒-sh(dojindolaboratories);碱性磷酸酶标记试剂盒诸如碱性磷酸酶标记试剂盒-nh2、碱性磷酸酶标记试剂盒-sh(dojindolaboratories);过氧化物酶标记试剂盒诸如过氧化物酶标记试剂盒-nh2、过氧化物酶标记试剂盒-nh2(dojindolaboratories);藻胆蛋白标记试剂盒诸如藻胆蛋白标记试剂盒-nh2、藻胆蛋白标记试剂盒-sh、b-藻红蛋白标记试剂盒-nh2,b-藻红蛋白标记试剂盒-sh、r-藻红蛋白标记试剂盒-nh2、r-藻红蛋白标记试剂盒sh(dojindolaboratories);荧光标记试剂盒诸如荧光素标记试剂盒-nh2、hilytefluor(tm)555标记试剂盒-nh2、hilytefluor(tm)647标记试剂盒-nh2(dojindolaboratories);及dylight547和dylight647(technochemicalcorp.)、zenon(tm)、alexafluor(tm)抗体标记试剂盒、qdot(tm)抗体标记试剂盒(invitrogencorporation)和ez-标记物蛋白质标记试剂盒(funakoshicorporation)。为了正确标记,可以使用适宜的仪器来检测经过标记的抗体或其片段。
本发明的用于检测plcd4基因表达量检测的样品的获得是本领域的常规技术,优选可选择非侵入性或具有最低程度侵入性的方法获得。
所述的样品可以是(但不限于):外周血、骨髓、淋巴结、腹腔清洗液、胃壁细胞或胃液。在本发明的具体实施方案中,所述样品来自受试者的组织。
本领域技术人员公知,肿瘤组织的细胞会脱落到体液中,这些脱落的细胞称之为循环肿瘤细胞,循环肿瘤细胞的性质同肿瘤组织中肿瘤细胞的性质相同,因此检测体液中尤其是血液中循环肿瘤细胞的性质就可以代表肿瘤组织的性质。就本发明而言,通过检测肿瘤组织中plcd4基因表达可以用于诊断胃腺癌转移,可以容易得出也可以通过检测循环肿瘤细胞中plcd4基因表达来诊断胃腺癌转移。
本发明还提供了一种用于胃腺癌转移诊断的工具,所述工具能够检测plcd4基因表达量。
进一步,所述工具包括能够定量plcd4基因mrna的试剂,和/或能够定量plcd4蛋白的试剂。
通常,所述的试剂存在于适当的容器中。可使用稀释剂如去离子水将每种所述引物或探针调整到至少一种需要量的浓度,分装于容器中。
进一步,所述能够定量plcd4基因mrna的试剂包括实时定量pcr中使用的特异扩增plcd4基因的引物,所述引物序列如seqidno.1和seqidno.2所示。
进一步,所述用于胃腺癌转移诊断的工具包括但不限于芯片、试剂盒、试纸、或高通量测序平台;高通量测序平台是一种特殊工具,随着高通量测序技术的发展,对一个人的基因表达谱的构建将成为十分便捷的工作。通过对比疾病患者和正常人群的基因表达谱,容易分析出哪个基因的异常与疾病相关。因此,在高通量测序中获知plcd4基因的异常与胃腺癌转移相关也属于使用了本发明的plcd4的新用途,同样在本发明的保护范围之内。
本发明的试剂盒中还可包括用于提取核酸的试剂,用于pcr的试剂,用于染色或显色的试剂等。例如,这些试剂包括但不限于:抽提液、扩增液、杂交液、显色液、洗液等。
此外,所述的试剂盒中还可包括描述检测胃腺癌转移的方法的说明书等。
本发明所述的试剂盒可包含适于实用(如针对于不同的检测方法)的多种不同的试剂,并不限于目前所列举的试剂,只要是基于plcd4基因或转录本的检测来判断胃腺癌转移的试剂均包含在本发明范围内。
本发明还提供了一种胃腺癌转移诊断的方法,所述方法包括如下步骤:
(1)获取受试者的样品;
(2)检测受试者样品中plcd4基因表达水平;
(3)将测得的plcd4基因表达水平与受试者的疾病相关性关联起来。
(4)与正常对照相比,plcd4基因表达水平在统计学上降低,表明受试者被判断胃腺癌已经发生转移、或者预测胃腺癌转移的受试者预后不良、或者评估胃腺癌转移的受试者已经复发。
本发明还提供了一种胃腺癌转移的治疗方法,所述方法包括促进plcd4基因的表达,或促进plcd4蛋白的表达或增强plcd4蛋白的活性。
本发明还提供了一种肿瘤药物的筛选方法,可以通过在对癌细胞添加测试药物后或在对肿瘤模型动物施用测试药物后的某个时期测量plcd4基因或者plcd4蛋白的表达水平来测定肿瘤药物改善肿瘤预后的效果。更具体地说,当plcd4基因或者plcd4蛋白的表达水平在添加或施用测试药物后升高时或者恢复正常水平时,可选择该药物作为改善肿瘤预后的治疗药物。
本发明还提供了一种治疗胃腺癌转移的药物,所述药物包含plcd4的激动剂。
本发明的plcd4基因或plcd4蛋白的激活剂不受限制,只要是可以促进或者增强plcd4或涉及plcd4上游或下游途径的物质的表达或活性,且对于治疗肿瘤有效的药物即可。
所述激活剂还包括包含携带plcd4基因的载体或者宿主细胞。
本发明的激活剂一方面可以用于补充内源性的plcd4蛋白的缺失或不足,通过提高plcd4蛋白的表达,从而治疗因plcd4蛋白缺乏导致的胃腺癌。另一方面可以用于增强plcd4蛋白的活性,从而治疗胃腺癌。
本发明还提供了上述激动剂在制备治疗胃腺癌转移的药物中的应用。
本发明的激动剂可以通过本领域任何已知的方式配制药物组合物来使用。这种组合物包含活性成分,加上一种或多种药物可接受的载体、稀释剂、填充剂、结合剂及其它赋形剂,这依赖于给药方式及所设计的剂量形式。本领域枝术人员已知的治疗惰性的无机或有机的载体包括(但不限于)乳糖、玉米淀粉或其衍生物、滑石、植物油、蜡、脂肪、多羟基化合物例如聚乙二醇、水、蔗糖、乙醇、甘油,诸如此类,各种防腐剂、润滑剂、分散剂、矫味剂。保湿剐、抗氧化剂、甜味剂、着色剂、稳定剂、盐、缓冲液诸如此类也可加入其中,这些物质根据需要用于帮助配方的稳定性或有助于提高活性或它的生物有效性或在口服的情况下产生可接受的口感或气味,在这种组合物中可以使用的制剂可是其原始化合物本身的形式,或任选地使用其药物学可接受的盐的形式,本发明的激动剂可以单独给药,或以各种组合给药,以及与其它治疗药剂一起结合形式给药。如此配制的组合物根据需要可选择本领域技术人员已知的任何适当的方式把激动剂进行给药。使用药物组合物时,是将安全有效量的本发明的抑制剂施用于人,其中口服安全有效量通常至少约100微克/千克体重。当然,具体剂量还应考虑给药途径、病人健康状况等因素,这些都是熟练医师技能范围之内的。
本发明的药物可根据需要制备成各种剂型。包括但不限于,经皮、粘膜、鼻、口颊、舌下或经口使用的片剂、溶液剂、颗粒剂、贴剂、膏剂、胶囊剂、气雾剂或栓剂。
本发明的药物的施用途径不受限制,只要它能发挥期望的治疗效果或预防效果即可,包括但不限于静脉内,腹膜内,眼内,动脉内,肺内,口服,小泡内,肌肉内,气管内,皮下的,通过皮肤,通过胸膜,局部的,吸入,通过粘膜,皮肤,肠胃,关节内,心室内,直肠,阴道,颅骨内,尿道内,肝内,瘤内。在某些情况下,可以系统地给药。在某些情况下是局部地给药。
本发明的药物的剂量不受限制,只要获得期望的治疗效果或者预防效果即可,可以依据症状、性别、年龄等来恰当的确定。本发明的治疗药物或预防药物的剂量可以使用例如对疾病的治疗效果或者预防效果作为指标来确定。
本发明的“plcd4基因”(chromosome2,nc_000002.12(218606873..218637186))序列可以ncbi数据库中进行查询。
在本发明的上下文中,“胃腺癌转移诊断”包括判断受试者是否已经发生胃腺癌转移、判断受试者是否存在胃腺癌转移的风险、判断胃腺癌转移患者是否已经复发转移。
本文所用的“治疗”涵盖患有相关疾病或病症的哺乳动物例如人类中治疗相关的疾病或疾病状态,并且包括:
(1)预防疾病或疾病状态在哺乳动物中发生,尤其是当该哺乳动物易感于所述疾病状态,但尚未被诊断出患有这种疾病状态时;
(2)抑制疾病或疾病状态,即阻止其发生;或者
(3)缓解疾病或疾病状态,即使疾病或疾病状态消退。
术语“治疗”通常涉及治疗人类或动物(例如,被兽医所应用),其中可达到某些预期的治疗效果,例如,抑制病症的发展(包括降低发展速度、使发展停止)、改善病症和治愈病症。还包括作为预防措施(例如预防)的治疗。对还没有发展为病症但有发展为该病症危险的患者的用途,也包括在术语“治疗”中。
本发明的优点和有益效果:
本发明首次发现了plcd4基因表达与胃腺癌转移相关,通过检测受试者组织中plcd4的表达,可以判断受试者是否患有胃腺癌转移、或者判断受试者是否存在患有胃腺癌转移的风险,从而指导临床医师给受试者提供预防方案或者治疗方案。
本发明发现了一种新的分子标记物-plcd4基因,相比传统的检测手段,基因诊断更及时、更特异、更灵敏,能够实现胃腺癌转移的早期诊断,从而降低胃腺癌转移的死亡率。
附图说明
图1显示利用基因芯片检测plcd4基因在胃腺癌组织中的表达;
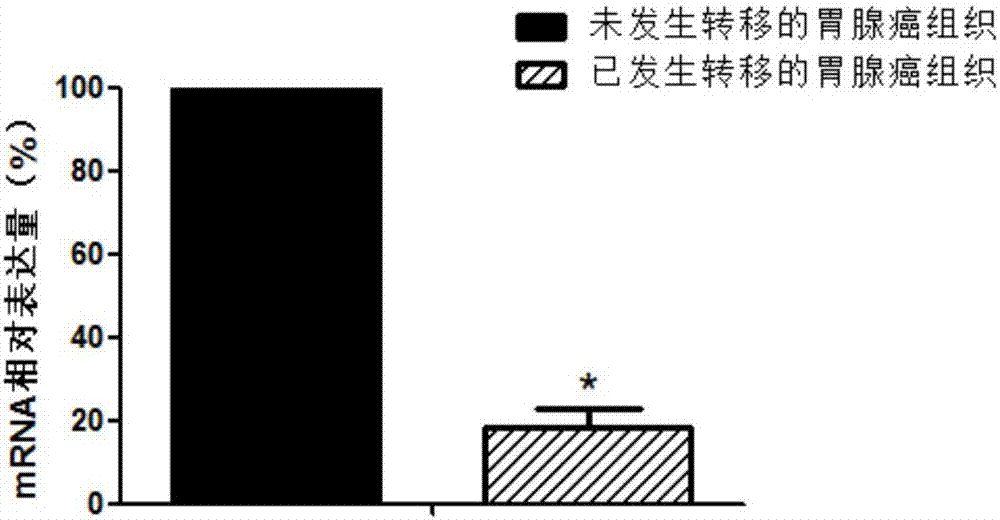
图2显示利用qpcr检测胃腺癌组织中plcd4基因的表达。
具体的实施方式
下面结合附图和实施例对本发明作进一步详细的说明。以下实施例仅用于说明本发明而不用于限制本发明的范围。实施例中未注明具体条件的实验方法,通常按照常规条件,例如sambrook等人,分子克隆:实验室手册(newyork:coldspringharborlaboratorypress,1989)中所述的条件,或按照制造厂商所建议的条件。
实施例1plcd4基因的差异表达
1、样本获取:8例胃腺癌组织(包括4例有转移样本和4例无转移样本)上述样本为胃腺癌患者的手术切除标本。上述所有标本的取得均通过组织伦理委员会的同意。组织样本的临床资料包括:性别、年龄、肿瘤大小、病理分级(edmonson)、转移与否、复发与否等。上述样本液氮保存。
2、胃腺癌转移组织rna的获取
利用norgenrna提取试剂盒提取组织rna。
组织裂解:
1)在较少rnase干扰的清洁区,使用含适量液氮的研钵称取离体组织样本约20mg,用杵棒研磨至粉末状;
2)将样本转移到一个不含rna酶的2ml的离心管中;
3)加入300μllysissolution,置于匀浆器内,充分研磨1-5min;
4)12000g,4℃,离心10min,转移上清至新的1.5ml的离心管中;
5)加入600μlrnase-freewater,用漩涡器混匀;
6)加入20μl蛋白酶k,在55℃温浴15min,不断涡旋混匀;
7)14000g,室温,离心1min,使细胞碎片沉淀于离心管底部,取上清转移到另外一个不含rna酶1.5ml的离心管中;
8)加入450μl的95%乙醇,涡旋混匀;
rna吸附:
9)取650μl含乙醇的裂解液加到离心柱中,14000g离心1min;
10)弃下层,重置收集管于柱上;
11)依照裂解液的容量,重复9)~10)步;
12)加入400μlwashsolution,14000g离心2min;
13)弃下层,将柱置于一新的收集管上;
dnase处理:
14)加入100μlenzymeincubationbuffer和15μldnasei,14000g离心1min;
15)将收集管中的溶液重新移入柱中;
16)室温放置15min;
rna洗涤:
17)加入400μlwashsolution,14000g离心1min,弃下层,重置收集管于柱上;
18)加入400μlwashsolution,14000g离心2min,弃收集管;
rna洗脱:
19)把柱子放入1.7mlelution管中;
20)加入30μlelutionbuffer;
21)200g离心2min,使溶液充分与柱结合,然后14000g离心1min。
通过nanodropnd-1000读取260nm和280nm处的吸光度值(a)测定rna溶液的纯度。经1%甲醛变性琼脂糖凝胶电泳,紫外透射光下观察,检测rna的完整性。
3、基因芯片杂交及扫描
总rna经线性化扩增后,cy3-utp标记,荧光标记后的crnas采用rneasyminikit纯化,用amhion的rnafragmentationreagents对标记好的crnas进行片段化处理。采用美国agilent公司的人全基因表达谱芯片(4x44k基因),在芯片杂交炉中65℃杂交17h,然后洗脱、染色,最后用agilentdnamicroarrayscanner扫描仪扫描。
4、芯片数据处理与分析
杂交后的芯片经芯片扫描仪读取数据点后,将数据导入分析软件,对于两组比值的自然对数绝对值大于2.0或小于0.5的基因作为差异表达基因。
5、统计学处理
采用spss13.0统计软件进行数据分析,组间差异比较采用单因素方差分析法,p<0.05差异有显著性意义。
6、结果
结果显示(如图1所示),与未发生转移的胃腺癌组织相比,已发生转移的胃腺癌组织中plcd4基因的mrna水平显著降低,差异具有统计学意义(p<0.05)。
实施例2差异表达基因的大样本验证
1、按照实施例1的方法收集80例胃腺癌组织(包括40例有转移样本和40例无转移样本)上述样本为胃腺癌患者的手术切除标本。上述所有标本的取得均通过组织伦理委员会的同意。组织样本的临床资料包括:性别、年龄、肿瘤大小、病理分级(edmonson)、转移与否、复发与否等。
2、组织总rna提取
步骤同实施例1。
3、逆转录
利用takara公司的逆转录试剂盒进行rna的逆转录。
4、qpcr
(1)引物设计
根据genbank中plcd4基因和gapdh基因的编码序列设计qpcr扩增引物,由上海生工生物工程技术服务有限公司合成。具体引物序列如下:
plcd4基因:
正向引物为5’-gaatatgccttcagtctt-3’(seqidno.1);
反向引物为5’-ttagtcaatgccttatagaa-3’(seqidno.2),
gapdh基因:
正向引物为5’-tttaactctggtaaagtggatat-3’(seqidno.3);
反向引物为5’-ggtggaatcatattggaaca-3’(seqidno.4)。
(2)按照表1配制pcr反应体系:
其中,sybrgreen聚合酶链式反应体系购自invitrogen公司。
表1pcr反应体系
(3)pcr反应条件:95℃5min,(95℃15s,60℃40s)*40个循环。以sybrgreen作为荧光标记物,在lightcycler荧光定量pcr仪上进行pcr反应,通过融解曲线分析和电泳确定目的条带,δδct法进行相对定量。
2.4统计学方法
实验都是按照重复3次来完成的,结果数据都是以平均值±标准差的方式来表示,采用spss13.0统计软件来进行统计分析的,干扰plcd4基因表达组与对照组之间的差异采用t检验,认为当p<0.05时具有统计学意义。
2.5结果
如图2所示,与未发生转移的胃腺癌组织相比,已发生转移的胃腺癌组织中plcd4基因的mrna水平显著降低,差异具有统计学意义(p<0.05)。
上述实施例的说明只是用于理解本发明的方法及其核心思想。应当指出,对于本领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以对本发明进行若干改进和修饰,这些改进和修饰也将落入本发明权利要求的保护范围内。
序列表
<110>贵州省人民医院
<120>plcd4基因作为胃腺癌转移诊断标志物的用途
<160>4
<170>siposequencelisting1.0
<210>1
<211>18
<212>dna
<213>人工序列(artificialsequence)
<400>1
gaatatgccttcagtctt18
<210>2
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>2
ttagtcaatgccttatagaa20
<210>3
<211>23
<212>dna
<213>人工序列(artificialsequence)
<400>3
tttaactctggtaaagtggatat23
<210>4
<211>20
<212>dna
<213>人工序列(artificialsequence)
<400>4
ggtggaatcatattggaaca20
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于片状锶铁氧体双重放大的乳腺癌易感基因免疫传感器的制备方法
- 基于pcr引物3’末端核苷酸双脱氧修饰的乳腺癌易感基因snp快速、灵敏检测方法
- 用于乳腺癌易感基因BRCA1和BRCA2的Long-range PCR检测的引物组、方法及试剂盒的制作方法
- 一种基于纳米银及纳米铜联合构建的双通道乳腺癌易感基因传感器的制备方法及应用
- 预测乳腺癌结果的nano46基因和方法
- Brca基因易感snp位点检测组合物的制作方法
- 3d热乳癌检测的制作方法
- 基于微流控芯片的基因治疗乳腺癌的药物的制备方法
- 一种检测原发性肝细胞癌的易感基因的荧光定量pcr基因分型方法及其试剂盒的制作方法
- Akr1b10基因蛋白作为乳腺癌诊断标志物和药物靶标的制作方法