一种集成式细胞三维动态培养微器件及其制作方法与流程
本发明属于微加工技术和3d微打印成型技术领域,涉及一种集成式细胞三维动态培养微器件及其制作方法,该集成式细胞三维动态培养微器件用于细胞三维动态培养、药物筛选、组织工程等。
技术背景
作为生物体的基本单元,细胞对于揭示生命规律、疾病的诊断、药物的筛选等具有重要意义。进行细胞研究的关键在于细胞的培养,进行细胞体外培养时应尽可能的复现细胞在体微环境。
传统的细胞体外培养器件通常选择培养皿、培养瓶或培养板,属于静态培养,与细胞在体生长环境相差较大。近些年出现了微流控细胞培养技术,实现了细胞的动态灌注式培养,使得细胞在体生活的微环境的体外模拟和控制成为可能,然而这种培养方式为二维动态培养,不能模拟细胞在体的三维空间环境。随着科技的发展,3d打印技术在生物医学工程中的应用受到了人们的重视。如今,利用3d打印技术成型的细胞培养三维支架在细胞培养中得到了广泛应用。三维支架实现了细胞在体外的三维培养,但这种三维培养方式是静态的,无法模拟在体细胞生活的流动微环境。
技术实现要素:
本发明的目的在于,提供一种可供细胞体外三维动态培养的微器件及其制作方法,构建更贴近于在体细胞生长的动态稳定微环境。采用微加工技术制作细胞进样层和中间过渡层,中间过渡层具有通孔结构,用来连接细胞进样层和三维培养层,细胞通过细胞进样层上的细胞进样通道进入培养池内。采用微加工技术和3d微打印技术制作三维培养层,其制作过程如下:首先用微加工的方法制备三维培养层的微通道结构,然后在三维培养层上方贴附pvc双面胶膜掩模层,用3d微打印的方法在培养池区域进行细胞培养三维支架的区域打印,最后采用激光切割的方法去除掩模层和多余支架,得到该集成式细胞三维动态培养微器件的三维培养层。培养池内集成细胞培养三维支架模拟在体细胞生活所处的细胞外基质,使得细胞的生长、繁殖、铺展和生理表征更贴近于体内情况。
本发明的技术方案:
一种集成式细胞三维动态培养微器件,所述的集成式细胞三维动态培养微器件包括三层结构,自上而下依次为细胞进样层1、中间过渡层10和三维培养层14;
所述的细胞进样层1,其上布置有培养液进样孔2、培养池对准孔6、废液排出孔8、细胞储存池a4和细胞储存池b9;所述的培养池对准孔6有多个,所述的细胞储存池a4、培养池对准孔6和细胞储存池b9位于同一条直线上,细胞储存池a4和细胞储存池b9位于培养池对准孔6的两端;所述的培养池对准孔6间通过细胞流通通道3顺次连接,所述的细胞储存池a4通过细胞进样通道5与相邻的培养池对准孔6相连接,所述的细胞储存池b9通过细胞出样通道7与相邻的培养池对准孔6相连接;培养液进样孔2和废液排出孔8位于垂直于细胞储存池a4、培养池对准孔6和细胞储存池b9所在的直线上,培养液进样孔2和废液排出孔8分别位于直线的两侧;
所述的中间过渡层10,其上布置有培养液进样通孔11、培养池连通孔12和废液排出通孔13;所述的培养池连通孔12有多个且位于同一条直线上,培养池连通孔12与细胞进样层1的培养池对准孔6一一对应;所述的培养液进样通孔11和废液排出通孔13分别与细胞进样层1的培养液进样孔2和废液排出孔8对应;
所述的三维培养层14,其上布置有培养液储存池15、三维培养池17和废液储存池19;所述的三维培养池17有多个且位于同一条直线上;所述的培养液进样通道16有多个,分别用于连通培养液储存池15和三维培养池17,使培养液从培养液储存池15进入三维培养池17;所述的废液出样通道18有多个,分别用于连通废液储存池19和三维培养池17,使废液从三维培养池17进入废液储存池19;所述的培养液储存池15与中间过渡层10的培养液进样通孔11相对应;所述的废液储存池19与中间过渡层10的废液排出通孔13相对应;所述的三维培养池17与中间过渡层10的培养池连通孔12相对应;培养液进样孔2、培养液进样通孔11和培养液储存池15的形状和大小均相同,废液排出孔8、废液排出通孔13和废液储存池19的形状和大小均相同,培养池对准孔6、培养池连通孔12和三维培养池17的形状和大小均相同,便于后续的对准键合;所述的三维培养池17,内部集成细胞培养三维支架20,为细胞的粘附、铺展、增殖及生理表达提供了支持。
所述的培养液进样孔2、培养液进样通孔11、培养液储存池15、废液排出孔8、废液排出通孔13和废液储液池19,具有相同的尺寸,直径为1-2mm。
所述的培养池对准孔6、培养池连通孔12和三维培养池17,具有相同的尺寸和形状,形状为正方形、正六边形、正八边形、正十边形、正十二边形或圆,多边形的内切圆直径为2-5mm。
所述的细胞进样通道5和细胞出样通道7,通道的深度为60-100um,通道的宽度为100-300um。
所述的培养液进样通道16和废液出样通道18,通道宽度为300-500um。
所述的细胞培养三维支架20的纤维直径为10-30um,纤维之间的距离为100-400um。
一种集成式细胞三维动态培养微器件的制作方法,所述的细胞进样层1、中间过渡层10和三维培养层14,采用热固性聚合物聚二甲基硅氧烷pdms、热塑性聚合物聚甲基丙烯酸甲酯pmma、聚苯乙烯ps或聚碳酸酯pc材料制作基底;
所述的细胞进样层1和中间过渡层10的制作过程如下:首先在平整的基底上均匀旋涂一层负胶bn-303或bn-308以增加后续su-8胶与基底的结合性,烘干后全曝光;再旋涂一层su-8胶,前烘后采用光刻图形化su-8胶,再经显影液处理即得到su-8胶模具;将烘干后的su-8胶模具置于干燥塔内密封好,用三甲基氯硅烷做脱模剂,熏蒸30分钟,有利于后续的脱模;以脱模剂处理后的su-8胶模具为模板,在甩胶机上旋涂热固性聚合物pdms,烘干后即将su-8胶模具上的图形转移到热固性聚合物pdms上,或采用热压的方法将su-8胶模具上的图形转移到热塑性聚合物pmma、ps或pc上;其中中间过渡层10使用热固性聚合物pdms时厚度不大于su-8胶模具上微柱的高度,以形成通孔;
所述的细胞进样层1,采用微流控芯片专用打孔器在培养液进样孔2和废液排出孔8的对应位置打出通孔;
所述的三维培养层14,先通过微加工方法制作微通道结构,再用3d微打印方法在三维培养池17区域集成细胞培养三维支架20;其制作过程如下:首先切割pvc双面胶模制作掩模层,将pvc双面胶模粘贴在三维培养层14上实现图案化;所述的掩模层覆盖除三维培养池17外所有的三维培养层14区域,且容易从三维培养层14上剥离,便于后续的键合;然后以图案化的三维培养层14作为接收装置,利用3d打印方法在三维培养层14上进行区域微打印,使成型的细胞培养三维支架20完全覆盖三维培养池17;接着,用激光切割机沿着三维培养层14上的三维培养池17的轮廓切割打印成型的细胞培养三维支架20,分离三维培养池17内外的支架结构;最后,去除胶模和残余的支架,只保留集成到三维培养池17内部的细胞培养三维支架20,即制得三维培养层14;
所述的三维培养池17中的细胞培养三维支架20,采用3d微打印的静电直写设备制作,其材料具有良好的生物相容性、生物可降解性和良好的机械力学性能,细胞与细胞培养三维支架20很好的相容,并在支架上生长、繁殖、铺展;
所述的静电直写设备包括计算机控制单元21、ccd高速摄像机22、金属打印喷头23、橡胶管24、精密注射泵25、高压直流电源26、收集装置聚合物芯片27、x-y轴移动平台28和接收基底29;所述的接收基底29固定在x-y轴移动平台28上,随平台进行x-y轴的移动;所述的收集装置聚合物芯片27固定在接收基底29上;所述的计算机控制单元21和ccd高速摄像机22共同控制x-y轴移动平台28的坐标位移;所述的精密注射泵25通过橡胶管24与金属打印喷头23连接,用于溶液的挤出和打印;所述的高压直流电源26的正极与金属打印喷头23相连,负极与x-y轴移动平台28相连,地线与大地相接,使金属打印喷头23和接收基底29之间形成高压电场;
所述的细胞培养三维支架20的具体成型过程如下:用掩模层图形化三维培养层14后,将其固定在接收基底29上,开启3d打印机,打开高压直流电源26,此时在金属打印喷头23和接收基底29间形成高压电场;当精密注射泵25通过橡胶管24按给定流量供给打印溶液,金属打印喷头23的打印溶液受力形成泰勒锥,用泰勒锥的近场射流开始打印,同时x-y轴移动平台28按给定速度快速移动,即在收集装置聚合物芯片27上成型细胞培养三维支架20;用激光沿着三维培养池17的轮廓切割,去除掩模层和残余支架,制得三维培养池17中的细胞培养三维支架20;
所述的集成式细胞三维动态培养微器件的三层结构通过氧等离子体处理或者热压方法键合在一起;所述的氧等离子体键合方法具体为:当三层结构选用的材料均为pdms时,键合面经过氧等离子体处理后表面产生亲水性基团羟基-oh,当键合面贴在一起时,羟基间发生反应生成牢固的氧键-o-和水h2o,因此三层结构之间牢固的粘在一起,形成永久性的键合;所述的热压方法键合具体为:当三层结构均为热塑性的材料pmma、ps或pc时,首先通过紫外处理去掉材料表面的疏水基团,使材料变得亲水,然后通过加热加压的方式使材料达到玻璃化温度,经过保温保压和降温降压的过程将三层结构键合在一起;
所述的键合过程中,细胞进样层1、中间过渡层10、三维培养层14之间需要对准,所述的对准过程采用可视化的显微成像技术,将对准过程呈现在计算机屏幕上,通过调整上下平台间的位置使芯片层之间实现对准;
所述的细胞培养微器件在键合好之后通入无水乙醇以保持封闭通道及培养池内表面的亲水性,为后续的细胞培养起到消毒灭菌的作用。
所述的细胞培养三维支架20采用天然可降解高分子材料壳聚糖、明胶,或者合成可降解高分子材料聚乳酸pla、聚己内酯pcl,或者混合材料如聚己内酯和聚氧化乙烯的混合物pcl/peo、聚己内酯和聚乳酸的混合pcl/pla作为成型材料。
本发明的有益效果:本发明提出了微加工技术与3d打印技术相结合的微器件制作方法,设计制作了一种集成式细胞三维动态培养微器件,该器件的培养池内成型了细胞培养三维支架,这种三维支架内部形成了三维互通的微通道结构,模拟体内细胞生活的空间结构,同时通过封闭的微通道网络为支架内的细胞提供实时的换液,极大程度模拟了细胞在体生活微环境,更有利于研究体内细胞的生理特征。该集成式细胞三维动态培养微器件的发明制作促进了细胞体外培养技术的发展。
附图说明
图1是本发明集成式细胞三维动态培养微器件的三维结构图。
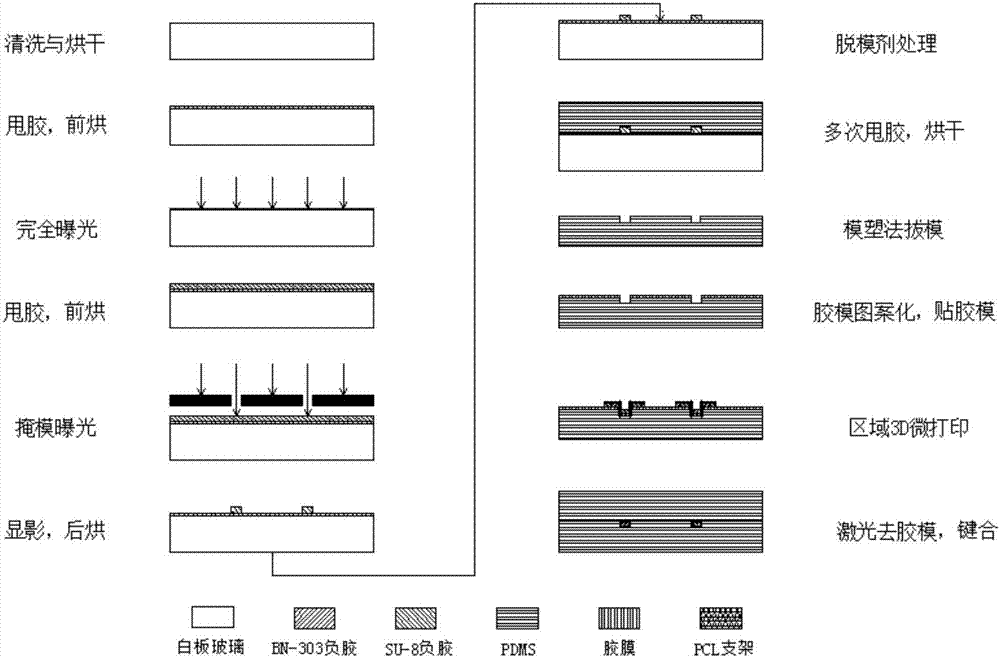
图2是本发明集成式细胞三维动态培养微器件制作工艺流程图。
图3是本发明中细胞进样层1的二维俯视图。
图4是本发明中三维培养层14的二维俯视图。
图5是图4中m的局部放大图。
图6是进行3d微打印的静电直写设备。
图中:1细胞进样层;2培养液进样孔;3细胞流通通道;4细胞储存池a;5细胞进样通道;6培养池对准孔;7细胞出样通道;8废液排出孔;9细胞储存池b;10中间过渡层;11培养液进样通孔;12培养池连通孔;13废液排出通孔;14三维培养层;15培养液储存池;16培养液进样通道;17三维培养池;18废液出样通道;19废液储存池;20细胞培养三维支架;21计算机控制单元;22ccd高速摄像机;23金属打印喷头;24橡胶管;25精密注射泵;26高压直流电源;27收集装置聚合物芯片;28x-y轴移动平台;29接收基底。
具体实施方式
以下结合附图和技术方案,进一步说明本发明的具体实施方式。
如图1所示,一种用于构建细胞体外三维培养动态稳定微环境的细胞培养微器件,该微器件由三层结构组成,分别为细胞进样层1、中间过渡层10和三维培养层14,细胞进样层1位于最上层,中间过渡层10位于中间,三维培养层14位于底层。细胞进样层1上的培养液进样孔2与中间过渡层10上的培养液进样通孔11以及三维培养层14上的培养液储存池15具有相同的尺寸,直径为1-2mm,本实施例中为2mm;细胞进样层1上的废液排出孔8和中间过渡层10上的废液排出通孔13以及三维培养层14上的废液储液池19具有相同的尺寸,直径为1-2mm,本实施例中为2mm;中间过渡层10上培养池连通孔12的大小形状与培养池对准孔6、三维培养池17相同,形状可以为正方形、正六边形、正八边形、正十边形、正十二边形或圆,多边形的内切圆直径为2-5mm,本实施例中为内切圆直径2mm的正八边形;细胞进样层1的细胞进样通道5与细胞出样通道7呈对称分布,通道的深度为60-100um,通道的宽度为100-300um,本实施例中细胞进出样通道的深度和宽度分别为60um和300um;三维培养层14上的培养液进样通道16和废液出样通道18的宽度为300-500um,本实施例中选择500um;培养池中的细胞培养三维支架20的纤维直径为10-30um,本实施例中为10um;细胞培养三维支架20纤维之间的距离为100-400um,本实施例中纤维间距为400um。所述的多个三维培养池17共同集成到一个培养液进样通道上,实现细胞的高通量培养。
所述的集成式细胞三维动态培养微器件的细胞进样层、中间过渡层和三维培养层的制作材料相同,均为热固性聚合物聚二甲基硅氧烷pdms或者热塑性聚合物聚甲基丙烯酸甲酯(pmma)或聚苯乙烯(ps)或聚碳酸酯(pc)。当使用热固性聚合物聚二甲基硅氧烷(pdms)时,微通道的结构成形选择微加工技术;当使用热塑性聚合物聚甲基丙烯酸甲酯(pmma)或聚苯乙烯(ps)或聚碳酸酯(pc),结构成形选择热压技术。不论何种成形技术,均需要模具。集成式细胞三维动态培养微器件的三层结构均采用以su-8胶为材料的模具。制作过程如下:首先在平整的玻璃片上均匀旋涂一层负胶bn-303或bn-308以增加后续su-8胶与基底的结合性,其厚度为0.5-2.0um,烘干后再旋涂一层su-8胶。对于细胞进样层,其厚度与细胞进样通道的深度相同,为60-100um,本实施例为60um;对于中间过渡层,su-8胶的厚度为300-600um,本实施例为300um;对于三维培养层,其厚度与培养液进样通道的深度相同,为60-100um,本实施例为100um。前烘后采用光刻技术图形化su-8胶,经过显影得到su-8胶模具,这种模具具有制作简单、成本低的优点;将烘干后的模具置于干燥塔内,用三甲基氯硅烷熏蒸半小时,有利于后续的脱模。模具制作好之后,本实施例选择热固性聚合物聚二甲基硅氧烷pdms作为微器件材料,用甩胶机旋涂聚二甲基硅氧烷pdms,置于85℃热板烘干,制备微器件的三层结构,其中中间过渡层使用的pdms材料厚度小于等于su-8模具上的微柱的高度,以形成通孔。采用微流控芯片专用打孔器在培养液进样孔和废液排出孔对应位置打出通孔。
所述的三维培养层先通过微加工技术制作微通道结构,然后在培养池区域利用3d微打印技术集成细胞培养三维支架,三维支架采用天然可降解高分子材料壳聚糖、明胶,或者合成可降解高分子材料聚乳酸pla、聚己内酯pcl,或者混合材料如聚己内酯和聚氧化乙烯的混合物pcl/peo、聚己内酯和聚乳酸的混合物pcl/pla作为成型材料。其制作过程如下:用激光切割机切割胶模制作掩模层,将胶模粘贴在三维培养层上实现图案化,胶模的厚度为50-100um,本实施例为50um,所述的掩模层需要覆盖三维培养层上除培养池外所有的区域,且容易从三维培养层上剥离,便于后续的键合;本实施例选择合成可降解高分子材料聚己内酯pcl作为细胞培养三维支架的成型材料,以图案化的三维培养层为接收装置,利用静电直写技术在培养池区域进行细胞培养三维支架的区域打印,使成型的细胞培养三维支架完全覆盖培养池,区域打印的面积为20x20um-40x40um,本实施例为40x40um;用激光沿着培养池轮廓切割打印成型的细胞培养三维支架,分离培养池内外的支架结构,激光切割机的电流为2.5-3.0ma,为保护pdms本实施例为2.5ma;去除胶模和残余支架,只保留集成在培养池内部的细胞培养三维支架,即可制得所需的三维培养层。
所述的合成可降解高分子材料聚己内酯pcl具有良好的生物相容性、生物可降解性和良好的机械特性,细胞可在三维支架上粘附、铺展和增殖,降解后生成co2和h2o。所述的静电直写技术需要先将聚己内酯pcl溶于冰乙酸,60℃磁力搅拌3-4h来制备打印溶液,溶液浓度为50%-80%,本实施例为70%。在洁净室中进行3d微打印——静电直写机制备聚己内酯pcl细胞培养三维支架,其具体实施如下:将70%w/v的聚己内酯/冰乙酸混合液填装精密注射泵上的注射器内,经橡胶管连接至金属打印喷头,注射器体积为1.0-2.0ml,本实施例为1.0ml,精密注射泵的流量为1-2ul/min,本实施例选择2ul/min;打印喷头与接收基底的距离为2-5mm,本实施例为3mm;施加的直流电压为1.5-3.0kv,本实施例为3.0kv;利用计算机控制单元盒ccd高速摄像机控制x-y轴移动平台的速度为100-300mm/s,本实施例为300mm/s;按打印需求在收集装置聚合物芯片上可打印三维支架的纤维直径为10-30um,间距为100-400um,本实施例三维支架的纤维直径为10um,间距为400um。由于冰乙酸极易挥发,加速了细胞培养三维支架的成型,成型的三维支架需要紫外灭菌和一系列的消毒处理。
最后,所述的细胞进样层、中间过渡层和三维培养层通过氧等离子体处理或者热压的方法键合在一起。所述的氧等离子体处理键合方法具体为当三层结构选用的材料均为pdms时,键合面经过氧等离子体处理后表面产生亲水性基团羟基(-oh),当键合面贴在一起时,羟基间发生反应生成牢固的氧键(-o-)和水(h2o),因此三层结构之间牢固的粘在一起,形成永久性的键合;所述的热压键合具体为当三层结构均为热塑性的材料(pmma或ps或pc)时,首先通过紫外处理去掉材料表面的疏水基团,使材料变得亲水,然后通过加热加压的方式使材料达到玻璃化温度,经过保温保压和降温降压的过程将三层结构键合在一起。本实施例选择氧等离子体处理进行键合,键和参数为20w,50s。键合过程中,细胞进样层与中间过渡层之间需要对准,中间过渡层与三维培养层之间需要对准,所述的对准过程采用可视化的显微成像技术,将对准过程呈现在计算机屏幕上,通过调整上下平台间的位置使芯片层之间实现对准。本发明制作的集成式细胞三维动态培养微器件实现了hela细胞的三维动态培养。
- 还没有人留言评论。精彩留言会获得点赞!