苯并二硫环戊二烯衍生物的制备方法与流程
本发明属于有机合成化学技术,特别是涉及一种苯并二硫环戊二烯衍生物的制备方法。
背景技术:
苯并二硫环戊二烯(bdt)是一类具有良好的生物活性分子,常常表现出了较强的抗乙肝病毒(jlabelledcompdrad.2012,55,197)、抗结核分枝杆菌(bioorgmedchemlett.2008,18,3706)以及抗腹泻等活性(j.med.chem.2004,47,5265)。同时,苯并二硫环戊二烯作为精细化工产品的重要中间体,在食品、农药、日用化学品、涂料、纺织、印染、造纸、感光材料、高分子材料等领域有着广泛的用途。然而,从天然物质中往往只能分离得到极少量的苯并二硫环戊二烯类化合物,而且花费昂贵。因此,这些物质的人工合成因此而具有特别重要的意义。当前,苯并二硫环戊二烯的合成方法一直是有机合成化学的重要研究课题之一(chem.sci.2013,4,2892;j.org.chem.1990,55,4693;org.biomol.chem.2010,8,1293;synthesis.1999,1,43;j.org.chem.2013,50,467;j.am.chem.soc.2014,136,7257)。但是这些公开的催化体系通常使用具有刺激性气味的硫酚或其衍生物作为“硫源”,同时它们还普遍存在着底物范围窄,反应条件苛刻,产物产率低等诸多缺点,缺乏实用价值。因此,发展一种简单实用的合成苯并二硫环戊二烯的方法具有着重要的意义。
技术实现要素:
发明目的:针对上述现有技术存在的问题,本申请提供了一种环境友好、价格低廉、操作简单、反应条件温和,并且原料简单易得的苯并二硫环戊二烯衍生物的制备方法。
技术方案:本发明所述的一种如下式(2)所示苯并二硫环戊二烯衍生物的制备方法,
取s8和2-溴硫代酰胺,加入铜催化剂,并以1,10-菲啰啉为配体,碳酸铯为碱,在非水溶剂系统中,反应得到苯并二硫环戊二烯类化合物;其中,r'选自氢、烷基或卤素,r选自芳基、烷基或稠芳环。
优选的,所述非水溶剂选自甲苯、1,2-二氯乙烷、1,4-二氧六环、n,n-二甲基甲酰胺、乙腈、氯仿和二甲基亚砜中的一种或多种。
其中,在所述优选的溶剂中,在极性质子性溶剂中n,n-二甲基甲酰胺(dmf)效果最佳;极性非质子性溶剂中甲苯效果最佳。
所述铜催化剂选自氯化铜、溴化铜、氯化亚铜、溴化亚铜、碘化亚铜和醋酸铜中的一种或多种。优选的,所述铜催化剂为碘化亚铜。
进一步的,所述铜催化剂和1,10-菲啰啉的用量为0.1~1当量,所述碱的用量为1~2当量。其中“当量”是指以底物s8和2-溴硫代酰胺最少的一个量为标准量。
所述反应时间为1~2h,反应温度为20-100℃。
进一步的,所述s8和2-溴硫代酰胺的摩尔比为1~3:1,优选1.5:1。
优选的,一种苯并二硫环戊二烯衍生物的制备方法,反应式如下:
取s8和2-溴硫代酰胺(1),加入催化剂氯化亚铜,以1,10-菲啰啉为配体,碳酸铯为碱,在n,n-二甲基甲酰胺溶剂系统中,100℃条件下反应1-2h得到苯并二硫环戊二烯类化合物(2)。
有益效果:本发明使用简单、易得的工业原料s8在温和的条件下,与2-溴硫代酰胺反应,得到苯并二硫环戊二烯类化合物,丰富了苯并二硫环戊二烯的合成方法,为苯并二硫环戊二烯类化合物的合成提供了一种廉价易得、环境友好的合成方法,反应体系绿色环保,产物易分离纯化,适用于合成各种高度官能化的苯并二硫环戊二烯类化合物,特别适用于大规模的工业生产,可以高效、高收率地制得高纯度的苯并二硫环戊二烯类化合物。
附图说明
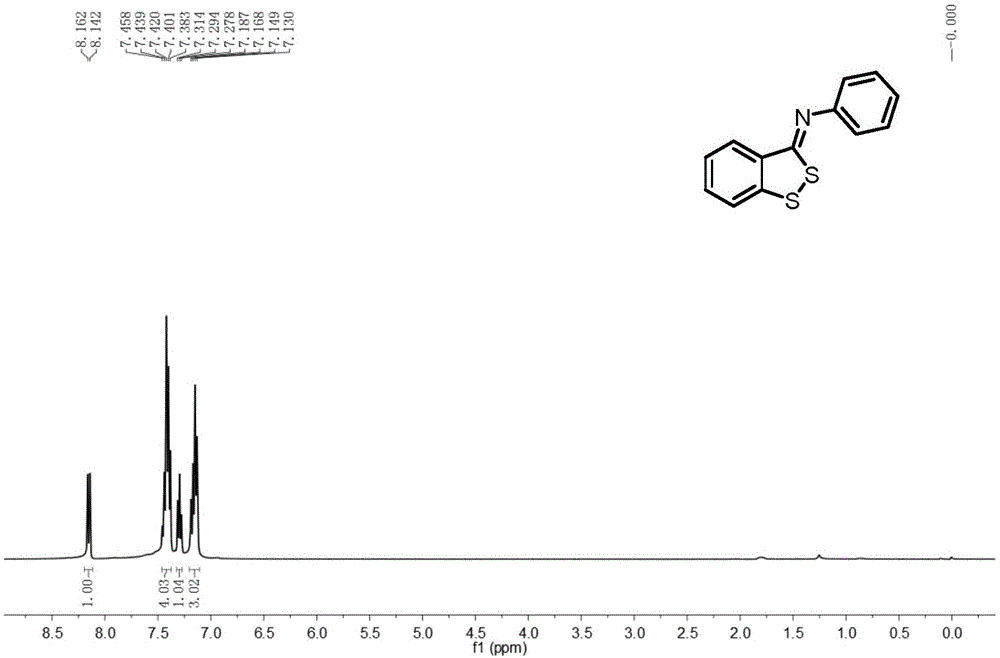
图1为苯并二硫环戊二烯衍生物2a的1h-nmr的核磁共振谱;
图2为苯并二硫环戊二烯衍生物2a的13c-nmr的核磁共振谱;
图3为苯并二硫环戊二烯衍生物2b的1h-nmr的核磁共振谱;
图4为苯并二硫环戊二烯衍生物2b的13c-nmr的核磁共振谱;
图5为苯并二硫环戊二烯衍生物2c的1h-nmr的核磁共振谱;
图6为苯并二硫环戊二烯衍生物2c的13c-nmr的核磁共振谱;
图7为苯并二硫环戊二烯衍生物2d的1h-nmr的核磁共振谱;
图8为苯并二硫环戊二烯衍生物2d的13c-nmr的核磁共振谱。
具体实施方式
下面结合实施例对本申请作出详细说明。
a)原料来源:
实施例中采用的原料2-溴硫代酰胺是通过2-溴酰胺与p2s5反应合成。具体反应条件如下:在室温条件下,二氯甲烷为溶剂,将2-溴酰胺与p2s5(物质量比1:1)混合搅拌3~4h,将反应液倾入冰水中(300ml),静置过夜,抽滤得到棕黄色固体2-溴硫代酰胺(90~99%的收率)。另外,申请书中所需的催化剂、溶剂等均是商业上可购易得原料。
b)实施例:
实施例1:苯并二硫环戊二烯衍生物2a的制备,实验结果见表1。
向带有磁力搅拌装置的50ml史莱克瓶中加入甲苯(10ml)、n-苯基-2-溴硫代苯甲酰胺1a(0.291g,1.0mmol)和s8(0.036g,1.2mmol),加入碘化亚铜(0.019g,0.1mmol),1,10-菲啰啉(0.036g,0.2mmol),碳酸铯(0.326g,1.0mmol)搅拌均匀后,将其放入100℃油浴中继续搅拌。tlc检测底物消失,反应结束。将反应液倾入饱和氯化钠水溶液中(10ml),用二氯甲烷(3×10ml)萃取,合并有机相,然后用水(3×10ml)反洗有机相,经过无水氯化钙干燥、抽虑、减压蒸馏等步骤得到粘稠的固体,最后经过硅胶柱层析(洗脱液为v石油醚:v乙酸乙酯=20:1)得到黄色固体,经过nmr、ms证实为苯并二硫环戊二烯类化合物2a,其收率为93%。
谱图解析数据2a:
yellowsolid,m.p.143-144℃;1h-nmr(400mhz,cdcl3)δ8.15(d,j=8.0hz,1h),7.46-7.38(m,4h),7.31-7.28(m,1h),7.19-7.13(m,3h);13c-nmr(cdcl3,100mhz)δ166.3,151.5,145.3,132.6,131.8,129.7,126.8,125.4,125.1,123.3,119.8;hrms(apci)m/zcalculatedforc13h9ns2[m+h]+:244.0249found:244.0265.
实施例2
用1b代替实施例1中的1a,其中,各个物料用量为:1b(0.306g,1.0mmol)和s8(0.036g,1.5mmol),加入碘化亚铜(0.19g,1mmol),1,10-菲啰啉(0.108g,0.6mmol),碳酸铯(0.65g,2.0mmol);所述非水溶剂选择dmf(10ml)。
其他条件同实例1,实验结果见表1。
谱图解析数据2b:
yellowsolid,m.p.164-165℃;1h-nmr(400mhz,cdcl3)δ8.15(d,j=8.8hz,1h),7.47-7.42(m,2h),7.32-7.28(m,1h),7.21(d,j=8.0hz,2h),7.05(d,j=7.2hz,2h),2.35(s,2h);13c-nmr(cdcl3,100mhz)δ164.8,147.9,144.2,133.8,131.7,130.7,129.2,125.7,124.4,122.3,118.8,20.0;hrms(apci)m/zcalculatedforc14h11ns2[m+h]+:258.0406found:258.0411.
实施例3
用1c代替实施例1中的1a,其中,各个物料用量为:1c(0.312g,1.0mmol)和s8(0.072g,3mmol),加入碘化亚铜(0.19g,1mmol),1,10-菲啰啉(0.18g,1mmol),碳酸铯(0.65g,2.0mmol);所述非水溶剂选择dmf(10ml)。
其他条件同实例1,实验结果见表1。
谱图解析数据2c:
yellowsolid,m.p.173-174℃;1h-nmr(400mhz,cdcl3)δ8.18-8.15(m,1h),7.52-7.47(m,2h),7.37-7.33(m,1h),7.16-7.12(m,2h),6.99-6.95(m,2h),3.84(s,3h);13c-nmr(cdcl3,100mhz)δ165.6,157.1,145.1,144.7,132.9,131.7,126.8,125.5,123.4,121.4,114.8,55.5;hrms(apci)m/zcalculatedforc14h11nos2[m+h]+:274.0355found:274.0381.
实施例4
用1d代替实施例1中的1a,其中,各个物料用量为:1d(0.312g,1.0mmol)和s8(0.036g,1.5mmol),加入碘化亚铜(0.095g,0.5mmol),1,10-菲啰啉(0.09g,0.5mmol),碳酸铯(0.65g,2.0mmol);所述非水溶剂选择dmf(10ml)。
其他条件同实例1,实验结果见表1。
谱图解析数据2d:
yellowsolid,m.p.206-207℃;1h-nmr(400mhz,cdcl3)δ8.15(d,j=8.0hz,1h),7.55-7.48(m,2h),7.40-7.34(m,3h),7.09(d,j=8.4hz,2h);13c-nmr(cdcl3,100mhz)δ166.1,148.9,144.4,131.5,131.0,129.3,128.8,125.8,124.6,122.3,120.4;hrms(apci)m/zcalculatedforc13h8clns2[m+h]+:277.9859found:277.9894.
实施例5
用1e代替实施例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据2e:
yellowsolid,m.p.168-169℃;1h-nmr(400mhz,cdcl3)δ7.94(d,j=0.8hz,1h),7.27-7.18(m,4h),7.06-7.04(m,2h),2.37(s,3h),2.33(s,3h);13c-nmr(cdcl3,100mhz)δ166.0,148.9,142.1,135.4,134.6,131.0,132.7,130.2,126.5,122.8,119.7,21.0,20.6;hrms(apci)m/zcalculatedforc15h13ns2[m+h]+:272.0562found:272.0585.
实施例6
用1f代替实施例1中的1b,其他条件同实例1,实验结果见表1。
谱图解析数据2f:
yellowsolid,m.p.186-187℃;1h-nmr(400mhz,cdcl3)δ7.96(s,1h),7.39-7.34(m,4h),7.10-7.06(m,2h),2.45(s,3h);13c-nmr(cdcl3,100mhz)δ167.5,150.1,142.5,135.9,133.5,132.7,130.3,129.9,126.7,123.0,121.4,20.8;hrms(apci)m/zcalculatedforc14h10clns2[m+h]+:292.0016found:292.0038.
实施例7
用1g代替实施例1中的1c,其他条件同实例1,实验结果见表1。
谱图解析数据2g:
yellowsolid,m.p.222-223℃;1h-nmr(400mhz,cdcl3)δ8.14(d,j=0.8hz,1h),7.46-7.38(m,2h),7.25-7.23(d,j=8.0hz,2h),7.07-7.04(m,2h),2.38(s,3h);13c-nmr(cdcl3,100mhz)δ164.0,148.5,143.3,135.3,134.7,132.0,131.8,130.3,126.4,124.1,119.8,21.1;hrms(apci)m/zcalculatedforc14h10clns2[m+h]+:292.0016found:292.0034.
实施例8
用1h代替实施例1中的1b,其他条件同实例1,实验结果见表1。
谱图解析数据2h:
yellowsolid,m.p.253-254℃;1h-nmr(400mhz,cdcl3)δ8.13(d,j=2.0hz,1h),7.50-7.47(m,1h),7.43-7.38(m,3h),7.19-7.07(m,2h);13c-nmr(cdcl3,100mhz)δ165.3,149.4,143.5,134.4,132.2,132.1,130.7,129.9,126.4,124.1,121.3;hrms(apci)m/zcalculatedforc13h7cl2ns2[m+h]+:311.9470found:311.9493.
实施例9
用1i代替实施例1中的1c,其他条件同实例1,实验结果见表1。
谱图解析数据2i:
yellowsolid,m.p.193-194℃;1h-nmr(400mhz,cdcl3)δ8.20(d,j=3.6hz,1h),7.82(d,j=8.0hz,1h),7.77(d,j=7.6hz,1h),7.54-7.49(m,3h),7.39-7.34(m,3h),7.31-7.27(m,1h),7.19(dd,j=8.0hzand1.6hz,1h),3.93(s,2h);13c-nmr(cdcl3,100mhz)δ166.2,150.5,145.4,145.0,143.2,141.4,139.1,132.8,131.8,126.9,126.8,126.4,125.5,125.0,123.4,121.0,119.6,118.7,116.8,37.1;hrms(apci)m/zcalculatedforc20h13ns2[m+h]+:332.0562found:332.0569.
实施例10
用1j代替实施例1中的1a,其他条件同实例1,实验结果见表1。
谱图解析数据2j:
yellowsolid,m.p.116-117℃;1h-nmr(400mhz,cdcl3)δ8.66(dd,j=4.8hzand1.6hz,1h),8.36(dd,j=7.6hzand1.6hz,1h),7.40(d,j=8.4hz,2h),7.33-7.30(m,1h),7.08(d,j=8.8hz,2h);13c-nmr(cdcl3,100mhz)δ166.2,162.3,152.3,147.5,133.7,129.8,128.9,125.4,120.4,119.1;hrms(apci)m/zcalculatedforc12h7cln2s2[m+h]+:278.9812found:278.9840.
表1实施例1-10制备所得苯并二硫环戊二烯衍生物及收率
- 还没有人留言评论。精彩留言会获得点赞!
- 一种具有抗氧化活性的芳基苯并呋喃类化合物及其制备方法和应用与流程
- 一种含苯并双环酮与乙氧磺隆的除草组合物及其应用的制造方法与工艺
- 一种6‑氯呋喃[3,2‑B]吡啶的合成方法与流程
- 一类苯并吡喃类化合物及其应用的制造方法与工艺
- 一种以二苯并环庚烯为核心的化合物及其在有机电致发光器件上的应用的制造方法与工艺
- 一种含苯并双环酮与乙草胺的除草组合物及其应用的制造方法与工艺
- 一种含苯并双环酮与噁草酮的除草组合物及其应用的制造方法与工艺
- 分解二噁英前体的催化剂筛选系统及其使用方法与流程
- 一种无卤热固性树脂组合物以及含有它的预浸料、层压板和印制电路板的制造方法与工艺
- 一种以二联二苯并五元杂环为骨架的有机化合物及其在OLED上的应用的制造方法与工艺