结构光照明的双光子荧光显微系统与方法与流程
本发明涉及光学显微领域,具体涉及一种结构光照明的双光子荧光显微系统与方法。
背景技术:
生物组织内的化学组分、分子结构携带着反映生理构造和生命过程的重要信息,检测并分析其化学成分和微结构信息是揭开生物体奥秘和认识病理过程的重要途径。光学显微成像是检测生物组织的重要方法,光学相干层析成像、共聚焦激光扫描显微成像、超分辨显微成像和双光子显微成像等光学成像技术和设备已经在生物学领域取得了巨大的成就。
然而生物组织对从紫外到近红外波段光波的强散射特性导致光束传播路径受到扰动而无法有效聚焦,同时被入射光激发的荧光也因为散射使得高灵敏高精度探测受到了巨大挑战。因此,光学成像方法在生物组织内部成像的深度非常有限,难以满足对深层组织非侵入无创成像检测的需求。
针对这一问题,科学家从生物组织处理和成像方法改进这两个方向进行了探索。一是通过对样本处理:近年来发展起来的生物组织透明化技术,如透明脑,通过改变组织的光学特性来提高其透明度、降低散射性,可提高光束穿透深度;二是通过对光学系统的改进,代表性技术包括多光子荧光成像技术和自适应成像技术,前者采用长波长激发光,提高了入射光组织内的穿透深度。后者利用相位调制器对光学误差进行矫正,通过利用部分散射光以提高其穿透深度。
目前的多光子荧光成像技术能够将生物组织的成像深度提高到毫米级,然而荧光信号微弱且信噪比比较低;而自适应光学成像技术的成像速率还有待提高。
技术实现要素:
本发明结合双光子显微成像深度大和结构光照明技术对荧光收集效率高灵敏度强的特点,提出了一种结构光照明的双光子荧光显微系统与方法,很好地解决了信噪比低和成像速率低的问题,为生物组织深层无创成像提供一种可行性技术。
本发明采用的技术方案如下:
一、一种结构光照明的双光子荧光显微系统:
系统包括飞秒激光器、电光强度调制器、扩束镜、相位调制器、扫描模块、扫描镜、场镜、二色镜、物镜、样品架、三轴平移台、滤光片、第三透镜和光电倍增管(PMT)。电光强度调制器、扩束镜和相位调制器沿飞秒激光器发出的光束依次布置在飞秒激光器前方,飞秒激光经电光强度调制器的功率调制、扩束镜的扩束和相位调制器的相位调制后入射到扫描模块中。
所述飞秒激光器发出的飞秒激光束通过扫描模块、Z向扫描台、相位调制器后,光束在空间上被分为两束,这两束光在圆形光束约束下形状互补、面积相等,两束光束强度相同。
所述的扫描模块包括同轴布置的第一振镜、第一透镜、第二透镜和第二振镜,四个光学器件构成4f系统,经相位调制器相位调制后的光束经第一振镜反射偏转角度后,依次经第一透镜和第二透镜后入射到第二振镜,再经第二振镜反射偏转角度后入射到所述扫描镜,第一振镜和第二振镜的旋转轴电机均与NI采集卡连接。两个振镜的驱动电路板均与采集卡连接,采集卡与计算机连接,由计算机发出控制信号经由采集卡到达振镜的驱动电路板,从而控制振镜的偏转范围和速度。两个振镜分别使光线沿x轴和y轴扫描,因此聚焦光斑可对照射区域的样品进行二维平面扫描。
扫描模块的出射光再依次经过扫描镜、场镜、二色镜和物镜后照射到固定在样品架的样品上,物镜安装在Z向扫描台上,Z向扫描台能够带动物镜沿z轴方向移动,样品架安装在三轴平移台上,通过三轴平移台调整样品架的位置;光电倍增管(PMT)接收从样品的照射区域发射的荧光信号,转换成电信号并解调处理后将样品的荧光图像显示在计算机显示器上。
光电倍增管探测到的荧光信号转换为电信号后将被解调处理。信号解调的方案有两种,对应不同的硬件设置。
第一种,所述的解调模块包括NI采集卡和主控计算机,扫描模块和光电倍增管均与NI采集卡连接,NI采集卡和Z向扫描台连接到主控计算机。该方案下,荧光信号由光电倍增管接收转换成电信号,再经由采集卡传输到计算机,信号进行傅里叶变换处理,选择前面相位调制器设定的调制频率进行滤波,从而解调出所需信号。
第二种解调,增加一路光信号检测,所述的解调模块包括同轴布置的平板玻璃、聚焦镜、小孔和光电二极管以及用于解调的锁相放大器、NI采集卡和主控计算机,平板玻璃安装在所述相位调制器和所述扫描模块之间,经相位调制器相位调制后的光束经平板玻璃发生透射和反射,接着依次经同轴布置的第聚焦镜、小孔后入射到光电二极管(PD),光电二极管和光电倍增管(PMT)均连接到锁相放大器,扫描模块经NI采集卡后和Z向扫描台一起连接到主控计算机,光电二极管探测的信号作为参考信号,光电倍增管接收的信号为被测信号,锁相放大器筛选出被测信号中与参考信号同频(或倍频)的分量,作为有效信号输出到计算机中。
二、一种结构光照明的双光子荧光显微方法:
(1)飞秒激光器发出脉冲激光光束;
(2)依次经电光强度调制器调节出射功率、扩束镜准直扩束后入射到相位调制器,飞秒激光束通过相位调制器后,光束在空间上被分为两束,这两束光在圆形光束约束下形状互补、面积相等,第一光束与第二光束强度相同。例如,图3所示的分光图案,一个中心圆(第二光束)与互补的外周圆环(第一光束),面积等大。相位调制器具备快速时间响应,可以具有最高10MHz的调制频率。第一光束不被调制,第二光束被调制有相对第一光束周期变化的相位延迟,两束光的相位差在0~2π范围内周期变化。;
(3)两束激光经扫描模块后入射到扫描镜,再依次经场镜、二向色镜和物镜后聚焦到样品架上的样品,样品能够被激发光激发出荧光。两束光在聚焦点处会发生干涉,由于第二光束有相对第一光束的随时间周期变化的相位延迟,所以当两束光同相位时,发生相长干涉,聚焦光斑焦点体积内的的光强度达到最大值;当两束光相差为π时,两束光发生相消干涉,聚焦光斑的大部分光强度分布在焦点体积外侧,这样的情形等效于焦斑移动,同样的,样品被激发出的荧光也具有相同的光强分布变化;
(4)样品被激发出来的荧光再依次经过物镜收集、二向色镜反射、滤光片过滤和透镜聚焦后进入光电倍增管(PMT)中,物镜连接有Z向扫描台,使得物镜可沿z轴移动;
(5)上述过程(3)中,激光通过扫描模块对样品表面区域进行扫描,探测样品表面被激发出的荧光信号。通过Z向扫描台调整物镜沿光束方向的位置对样品不同深度处进行扫描,探测样品不同深度处被激发出的荧光信号。这些荧光信号被光电倍增管(PMT)收集并通过解调处理后即获得样品不同深度处的荧光显微图像。
所述的步骤(5)中,荧光信号解调的方案有两种,如前文所述。
样品表面显微信号和样品深度显微信号经NI采集卡发送到主控计算机中,主控计算机接收信号进行傅里叶变换处理,根据相位调制器预先设定的调制频率进行滤波,解调出所需信号进行显微成像。
在相位调制器和所述扫描模块之间平板玻璃使得光束反射,反射光束再依次经聚焦镜、小孔后入射到光电二极管(PD)中,光电二极管(PD)采集获得参考光信号,参考光信号、样品表面显微信号和样品深度显微信号一起输入到锁相放大器进行解调。
所述的扫描模块包括同轴布置的第一振镜、第一透镜、第二透镜和第二振镜,经相位调制器相位调制后的光束经第一振镜反射偏转角度后,依次经第一透镜和第二透镜后入射到第二振镜,再经第二振镜反射偏转角度后入射到所述扫描镜,主控计算机发送电机控制信号经NI采集卡发送到所述扫描模块的第一振镜和第二振镜进而控制扫描探测;主控计算机发送控制信号到Z向扫描台,控制物镜的移动。
所述样品固定于载玻片上,并由样品架夹持,样品架固定在三轴平移台上,通过三轴平移台调节样品的空间位置。
所述的相位调制器包括同轴依次布置的半波片、电光相位调制器、沿水平方向并排拼接的两个偏振分光镜和一片偏振片,进入相位调制器的光束经半波片偏振方向旋转角度后入射到电光相位调制器,电光相位调制器将光束分解成水平方向和竖直方向的两个偏振分量,再入射到两个偏振分光镜拼接形成端面的中间使得调制的光束透过,然后经偏振片形成一路含偏振方向一致的两束光的光束。
本发明飞秒激光器出射的脉冲激光经扩束准之后由特制的相位调制器将光束在空间上分成两束偏振光,这两束光横向剖面上的形状在圆形光束约束下形状互补,沿原来传播方向互相平行,且彼此之间有一个随时间变化的相位差,经过扫描系统后有透镜聚焦在成像面上,可得经过频率调制的荧光信号,对荧光信号进行解调处理可得到信噪比大大提升的显微图像。
本发明的有益效果是:
本发明为生物组织深层无创成像提供了一种可行的方式,对荧光信号的解调能得到信噪比大大提升的显微图像,效率高灵敏度强;同时本发明采用相位调制的方法来调制聚焦光斑的能量分布,解调过程耗时极短,可以对样品进行实时清晰成像,成像速率高。
本发明适合于厚生物样本组织成像,大大提高信噪比,能够在传统多光子方法无法清楚识别的深度重建衍射极限分辨率,为精准光刺激需求提供可以种切实可行的方案。
附图说明
为了更加详细而具体地解释本发明,结合以下附图进行描述。附图展示了本发明系统的结构图,列出了元件编号并作相应解释;附图通过列举非局限性的例子展示了结构光照明对激光束进行调制的分光束方案。
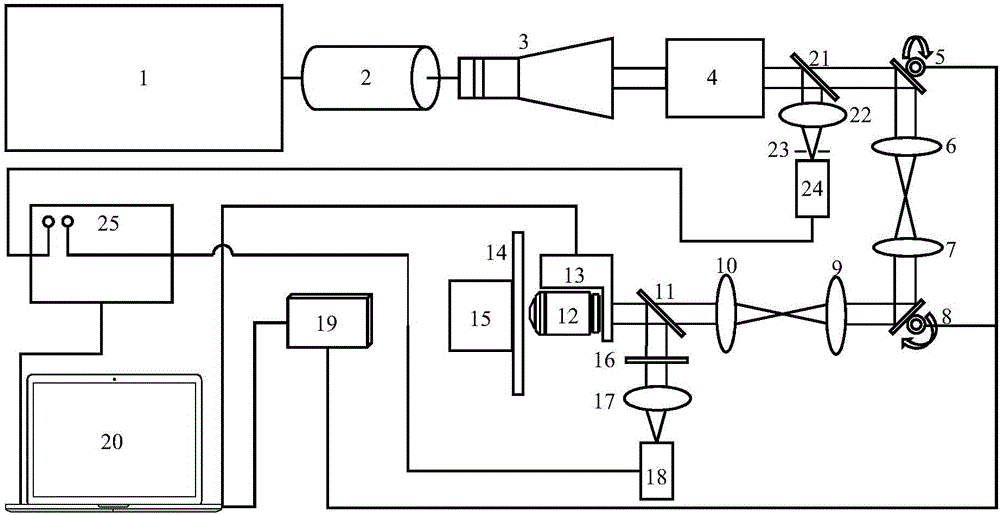
图1是本发明实施例1的结构光照明的双光子荧光显微系统结构示意图;
图2是本发明实施例2的结构光照明的双光子荧光显微系统结构示意图;
图3是本发明实施例的空间光相位调制的分光束方案举例——中心圆与互补的外周圆环;
图4是普通双光子显微方法的荧光强度曲线和本发明结构光照明的双光字荧光显微方法的荧光曲线对比,这三条曲线是仿真结果,设定激发光波长为900nm,焦点深度为1000μm;
图5是普通双光子荧光显微系统对荧光小球成像的仿真图和本发明结构光照明的双光子荧光显微系统对荧光小球成像的仿真图。
图中:飞秒激光器1,电光强度调制器2,扩束镜3,相位调制器4,第一振镜5,第一透镜6,第二透镜7,第二振镜8,扫描镜9,场镜10,二色镜11,物镜12,Z向扫描台13,样品架14,三轴平移台15,滤光片16,第三透镜17,光电倍增管18,数据采集卡19,计算机20;平板玻璃21,聚焦镜22,小孔23,光电二极管24,锁相放大器25。
具体实施方式
下面结合附图对本发明实施例进行详细描述。
本发明的实施例及其具体过程如下:
实施例1
如图1所示,系统包括飞秒激光器1、电光强度调制器2、扩束镜3、相位调制器4、第一振镜5、第一透镜6、第二透镜7、第二振镜8、扫描镜9、场镜10、二色镜11、物镜12、Z向扫描台13、样品架14、三轴平移台15、滤光片16、第三透镜17、光电倍增管(PMT)18、数据采集卡19和计算机20;
电光强度调制器2、扩束镜3和相位调制器4沿飞秒激光器1发出的光束依次布置在飞秒激光器1前方,飞秒激光器1发出的光经电光强度调制器2功率调制、扩束镜3扩束和相位调制器4相位调制后入射到扫描模块中,扫描模块的出射光依次经扫描镜9、场镜10、二色镜11和物镜12后照射到样品架14的样品上,物镜12安装在Z向扫描台13上,样品架14安装在三轴平移台15上,通过三轴平移台15调整样品架14的位置和姿态。样品被激发出的荧光经过物镜收集和二色镜11反射,再依次经滤光片16、透镜17入射到光电倍增管(PMT)18中。
电光强度调制器为自由空间光电光调制器,光束从中间入射,中心出射,根据发出的波长和样品组织的种类,通过调节电压来控制飞秒脉冲激光的出射功率。
扫描模块包括同轴布置的第一振镜5、第一透镜6、第二透镜7和第二振镜8,四个光学元件构成4F系统。经相位调制器4相位调制后的光束经第一振镜5反射偏转角度后,依次经第一透镜6和第二透镜7后入射到第二振镜8,再经第二振镜8反射偏转角度后入射到所述扫描镜9,第一振镜5和第二振镜8的驱动电路板均与NI采集卡19连接,由NI采集卡19输出振镜的控制信号,实现二维扫描。
解调模块包括NI采集卡19和主控计算机20,扫描模块和光电倍增管(PMT)18均与NI采集卡19连接,NI采集卡19和Z向扫描台13连接到主控计算机20。
实施过程如下:
(1)飞秒激光器1发出脉冲激光,光束穿过电光强度调制器后出射功率可被改变,例如,飞秒激光初始功率2W,经过电光调制器后出射功率变为初始功率的15%~20%。之后光束再经扩束镜3进行扩束,例如,将光束直径从1mm扩展到约5mm。
(2)扩束后的激光通过相位调制器4时,光束在空间上被分为两束,这两束光在圆形光束约束下形状互补、面积相等,第一光束与第二光束强度相同。例如,图3所示的分光图案,一个中心圆(第二光束)与互补的外周圆环(第一光束),面积等大。相位调制器具备快速时间响应,可以具有最高10MHz的调制频率。第一光束不被调制,第二光束被调制有相对第一光束周期变化的相位延迟,两束光的相位差在0~2π范围内周期变化,例如,调制信号可以是10kHz的方波。
相位调制器具备快速时间相应和很高的调制频率(~MHz)。激光经过相位调制器后,一半光束被调制,另一半未被调制,被调制光相对未调制光有随时间变化的相位延迟,如用一定频率的正弦信号周期改变调制光束的相位,使两个半区的光束之间的相差经历从0到2π的周期变化。
(3)两束光进入扫描光路中,扫描模块包括两个振镜和两个透镜,构成4f系统。振镜的驱动电路板与采集卡连接,由计算机件通过采集卡输出控制信号来控制振镜的摆角范围和摆动速度。两个振镜分别使光线沿x轴和y轴扫描。
(4)从扫描模块出射的光束依次通过扫描镜、场镜、二色镜和物镜聚焦到样品上,样品能够被激发光激发出荧光。两束光在聚焦点处会发生干涉,由于第二光束有相对第一光束的随时间周期变化的相位延迟,所以当两束光同相位时,发生相长干涉,聚焦光斑焦点体积内的的光强度达到最大值;当两束光相差为π时,两束光发生相消干涉,聚焦光斑的大部分光强度分布在焦点体积外侧,这样的情形等效于焦斑移动,同样的,样品被激发出的荧光也具有相同的光强分布变化。又因为扫描模块的设置,聚焦光斑可由振镜控制对样品进行二维扫描;
(5)样品被激发出来的荧光依次再经过物镜收集、二向色镜反射、滤光片过滤和透镜聚焦后进入光电倍增管PMT中,物镜可以是奥林巴斯的XLUMPLFLN20XW,PMT可以是日本滨松的H7422P-40。相位调制器使得焦点周围的激发光实现了强度调制,因此被激发出的荧光也具有调制光强度,PMT接收的荧光信号包含了直流分量和交流分量,将光电转换后的电信号通过采集卡输入计算机,在计算机上对信号做傅里叶变换,以分别提取直流信号与交流信号,交流信号的频率与相位调制器的调制频率一致。交流信号与直流信号之和等同于普通双光子荧光显微信号。
上述过程(4)中,通过扫描模块的设置激发光能够进行样品表面区域的扫描,探测样品表面被激发出的荧光信号;又通过Z向扫描台调整物镜沿z轴的位置可使激发光对样品不同深度处进行扫描,探测样品不同深度处被激发出的荧光信号。这些荧光信号被光电倍增管(PMT)收集并通过解调处理后即获得样品不同深度处的荧光显微图像,这些不同深度处样品的荧光图像可以通过算法处理构建样品三维结构的图像。
实施例2
如图2所示,系统包括飞秒激光器1、电光强度调制器2、扩束镜3、相位调制器4、第一振镜5、第一透镜6、第二透镜7、第二振镜8、扫描镜9、场镜10、二色镜11、物镜12、Z向扫描台13、样品架14、三轴平移台15、滤光片16、第三透镜17、光电倍增管(PMT)18、数据采集卡19、计算机20、平板玻璃21、第四透镜22、小孔23、光电二极管(PD)和锁相放大器25扫描模块;
实施过程如下:
(1)飞秒激光器1发出脉冲激光,光束穿过电光强度调制器后出射功率可被改变,例如,飞秒激光初始功率2W,经过电光调制器后出射功率变为初始功率的15%~20%。之后光束再经扩束镜3进行扩束,例如,将光束直径从1mm扩展到约5mm。
(2)扩束后的激光通过相位调制器4时,光束在空间上被分为两束,这两束光在圆形光束约束下形状互补、面积相等,第一光束与第二光束强度相同。例如,图3所示的分光图案,一个中心圆(第二光束)与互补的外周圆环(第一光束),面积等大。相位调制器具备快速时间响应,可以具有最高10MHz的调制频率。第一光束不被调制,第二光束被调制有相对第一光束周期变化的相位延迟,两束光的相位差在0~2π范围内周期变化,例如,调制信号可以是10kHz的方波。
(3)两束光继续先前传播,遇到平板玻璃21后分成两路,一路经过平板玻璃反射,依次通过第四透镜22聚焦、小孔23滤波后被光电二极管(PD)收集,PD将光信号转换成电信号输入锁相放大器25中作为参考信号。另一路光束透过平板玻璃继续传输至扫描模块。
(4)两束光进入扫描光路中,扫描模块包括两个振镜和两个透镜,构成4f系统。振镜的驱动电路板与采集卡连接,由计算机上的软件通过采集卡输出控制信号来控制振镜的摆角范围和摆动速度。两个振镜分别使光线沿x轴和y轴扫描。
(5)从扫描模块出射的光束依次通过扫描镜、场镜、二色镜和物镜聚焦到样品上,样品能够被激发光激发出荧光。两束光在聚焦点处会发生干涉,由于第二光束有相对第一光束的随时间周期变化的相位延迟,所以当两束光同相位时,发生相长干涉,聚焦光斑焦点体积内的的光强度达到最大值;当两束光相差为π时,两束光发生相消干涉,聚焦光斑的大部分光强度分布在焦点体积外侧,这样的情形等效于焦斑移动,同样的,样品被激发出的荧光也具有相同的光强分布变化。又因为扫描模块的设置,聚焦光斑可由振镜控制对样品进行二维扫描;
(6)样品被激发出来的荧光依次再经过物镜收集、二向色镜反射、滤光片过滤和透镜聚焦后进入光电倍增管PMT中,物镜可以是奥林巴斯的XLUMPLFLN20XW,PMT可以是日本滨松的H7422P-40。相位调制器使得焦点周围的激发光实现了强度调制,因此被激发出的荧光也具有调制光强度,PMT接收的荧光信号包含了直流分量和交流分量,将光电转换后的电信号输入锁相放大器中,锁相放大器将对此信号进行滤波,筛选出与参考信号同频率(或倍频)的交流信号输出,锁相放大器与计算机连接,计算机接收到样品荧光信号的交流分量。
以上两个实施例的区别在于对探测荧光信号的解调处理,实施例1直接对荧光信号的作傅里叶变换处理,可提取其中的直流分量和交流分量;而实施例2中则通过设置参考光的方式利用锁相放大器筛选出荧光信号中的交流信号,信号解调的目的是一致的。双光子显微镜在观察厚生物组织的时候,由于生物组织对荧光的散射作用,导致收集到的荧光信号非常微弱且信噪比差。而基于本发明的双光子荧光因为强度被调制,因此能够在荧光检测端提取所时间变化的荧光信号交流分量,从而大大提高荧光信号的信噪比,可对生物组织内部大深度处进行无损清晰成像。
如图4是普通双光子显微方法的荧光强度曲线和本发明结构光照明的双光子荧光显微方法的荧光曲线对比,调制图案为中心圆加互补的外周圆环(如图3所示)。这三条曲线是仿真结果,设定激发光波长为900nm,焦点深度为1000μm。从图中可以看出,在对仿真样品1000μm处成像是,相比于普通双光子显微的荧光信号,本发明的荧光信号在1000μm处的光强与其他深度处的光强差距更大,因此信噪比更大。图5是普通双光子荧光显微系统和本发明结构光照明的双光子荧光显微系统对荧光小球成像的仿真对比图,(a)为普通双光子荧光图像,(b)为本发明系统荧光图像,对比可以发现本系统具有出色的噪声抑制能力。
综上,本发明创新点主要有两点,一是利用相位调制器对飞秒激光进行分光束调制(理论上分光束方案有无数种,只要两束光面积相等,形状互补即可),使得聚焦光斑在焦点体积内强度分布被调制;二是采用两种解调荧光信号的方式,解调时间极短,因此可以保证实时成像需要的成像速率。本发明将拓展生物组织清晰成像的深度,并为脑组织光遗传学研究提供切实可行的无损非入侵式光刺激方法。
- 还没有人留言评论。精彩留言会获得点赞!