一种注射用人胰岛素脂质体及其制备方法与流程
本发明涉及医药
技术领域:
,具体涉及一种注射用人胰岛素脂质体及其制备方法。
背景技术:
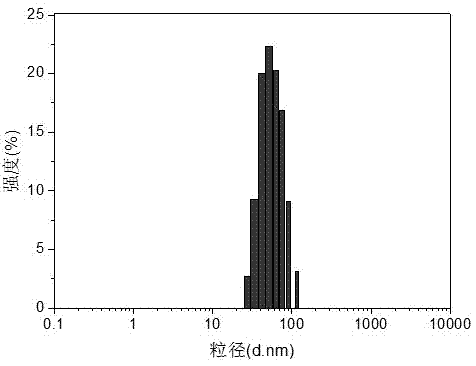
:糖尿病是一种由遗传和环境因素相互作用而引起的临床综合症,其基本病理特征为绝对或相对性胰岛素分泌不足所引起的代谢紊乱。糖尿病现已成为一种常见病、多发病,是一种严重危害人类健康的疾病。随着人们生活水平的提高,社会老龄化人口的增多,糖尿病的发病率在逐年上升。据国际糖尿病联盟统计,目前全球糖尿病患者人数为3.66亿,预计2030年将达到5.52亿,相当于每年增加一千万名患者。在我国,糖尿病的患病率在近10年翻了近两倍。2010年,我国成人糖尿病的患病率为9.7%,患者总数已超过9000万,成为世界第一糖尿病大国;同时,糖尿病前期的糖耐量受损人群达到了1亿4千8百万人,患病率为15.5%。防治糖尿病已成为临床上严重的、紧迫的医疗保健问题之一,日益为人们所重视。对于胰岛细胞病变,不能分泌胰岛素,需要补充外援胰岛素,相关的并发症也比较多的Ⅰ型糖尿病患者而言,胰岛素是唯一的治疗药物。此外,还有30%~40%的Ⅱ型糖尿病患者虽然自身能够分泌胰岛素,但由于分泌量不足或者不能有效地利用胰岛素,最终也需要使用胰岛素来治疗。人类应用的很大一部分胰岛素皆来源于动物。从动物脏器提取的猪、牛胰岛素受脏器来源的限制,而且由于一级结构的差异,带来免疫原性问题,可能导致一系列的副作用。90年代至今,重组人胰岛素成功研发上市,重组人胰岛素是利用生物工程技术,获得的高纯度的生物合成人胰岛素,其氨基酸排列顺序及生物活胜与人体本身的胰岛素完全相同,安全无毒副作用。脂质体(liposomes)是一种类似生物膜结构的双分子层微小囊泡,具有生物膜特性和药物传输能力,胰岛素以脂质体包裹方式给药有利于提高生物利用度和患者用药依从性,脂质体的内水相能保护胰岛素的结构和构象,而外部亲脂层有助于改善跨生物膜屏障吸收性能在胰岛素脂质体中,胰岛素被包裹在脂质体内部,可抵抗蛋白酶的降解,脂质体的磷脂双分子层还可以控制胰岛素的释放,达到比较平稳的降低血糖。现有报道方法制备的胰岛素脂质体冻干粉粒径较大,通过注射进入体内后容易被体内巨噬细胞吞噬,并且注射部位容易出现炎症问题。技术实现要素:本发明的目的是,提供了一种注射用人胰岛素脂质体制剂,具体地是将人胰岛素用含有抗氧剂的脂质体骨架材料和稳定剂载体形成的脂质体载体包封得到的冻干制剂,制成的注射用人胰岛素脂质体有效地降低了给药频率。本发明提供了一种注射用人胰岛素脂质体的制备方法。本发明提供的一种注射用人胰岛素脂质体,其为冻干粉针剂,该制剂包括以下重量份的物质:重组人胰岛素10份脂质体骨架材料50-100份稳定剂10-50份冻干保护剂50-100份抗氧剂1-20份所述重量份可以是ug、mg、g、kg等医药领域公知的含量单位。所述的脂质体骨架材料选自大豆磷脂、蛋黄磷脂、氢化大豆磷脂、氢化蛋黄磷脂、聚乙二醇-磷脂酰胆碱、聚乙二醇-磷脂酰乙醇胺、聚乙二醇-二硬脂酰磷脂酰胆碱中的一种或几种。所述的稳定剂选自胆固醇、豆甾醇、谷甾醇、聚山梨醇、胆酸钠、去氧胆酸钠、十八胺中的一种或几种。所述的冻干保护剂选自氯化钠、甘露醇、葡萄糖、乳糖、聚乙烯吡咯烷酮、蔗糖、甘氨酸、山梨醇、海藻糖、右旋糖酐的一种或几种。所述的冻干保护剂为海藻糖和甘露醇的重量比为1:1的混合物。所述的抗氧剂选自亚硫酸氢钠、焦亚硫酸钠、硫代硫酸钠、谷胱甘肽、抗坏血酸棕桐酸酯、L-半胱氨酸、维生素E、叔丁基对羟基茴香醚中的一种或几种。一种制备上述注射用人胰岛素脂质体的方法,包括以下步骤:a.将脂质体骨架材料和稳定剂溶解于有机溶剂中,置于旋转薄膜蒸发仪上减压除尽有机溶剂,获得磷脂膜,加入缓冲盐溶液搅拌溶解,获得空白脂质体溶液;b.将人胰岛素溶解于注射用水,与所得的空白脂质体溶液混合均匀,冰浴超声30~60分钟,再加入冻干保护剂、抗氧剂充分溶解后,用微孔滤膜过滤;c.将上述步骤b所得溶液进行喷雾干燥,无菌条件下进行分装,制得注射用人胰岛素脂质体。所述的有机溶剂选自乙醇、异丙醇、甲醇、丁酮、丙酮、乙酸乙酯、氯仿、二氯甲烷或甲酸乙酯中的一种或几种。所述的有机溶剂为体积比3:1的异丙醇和乙醇的混合溶剂。所述的缓冲盐为pH值为5.0~6.0的磷酸-磷酸氢二钠缓冲液。本发明所公开的人胰岛素脂质体具有延长药物作用时间,避免频繁注射,提高患者顺应性;血药浓度稳定,峰谷波动小,降低不良反应;避免药物的肝首过效应的优点。本发明能够把脂质体粒径控制在200nm范围以内,载药能力高,提高了人胰岛素的生物利用度,并且良好的缓解了注射部位的炎症问题。附图说明图1实施例1制备的人胰岛素脂质体DLS图;图2实施例2制备的人胰岛素脂质体DLS图;图3实施例3制备的人胰岛素脂质体DLS图;图4实施例1制备的人胰岛素脂质体体外释放-时间曲线;图5实施例2制备的人胰岛素脂质体体外释放-时间曲线;图6实施例3制备的人胰岛素脂质体体外释放-时间曲线;图7实施例1制备的人胰岛素脂质体给药后第1天血糖浓度-时间曲线;图8实施例2制备的人胰岛素脂质体给药后第2天血糖浓度-时间曲线;图9实施例3制备的人胰岛素脂质体给药后第3天血糖浓度-时间曲线;图10实施例3制备的人胰岛素脂质体给药后第4天血糖浓度-时间曲线;图11实施例3制备的人胰岛素脂质体给药后第5天血糖浓度-时间曲线;图12实施例3制备的人胰岛素脂质体给药后第6天血糖浓度-时间曲线;图13实施例3制备的人胰岛素脂质体给药后第7天血糖浓度-时间曲线。具体实施方式下面结合实施例对本发明作进一步的说明,但是不应作为对本发明的限制。实施例1:1.将氢化蛋黄磷脂5500g和聚山梨醇2800g在5L体积比为3:1的异丙醇和乙醇的混合溶剂中使其完全溶解,混合均匀,形成脂质溶液。置于旋转薄膜蒸发仪上减压除尽异丙醇和乙醇,获得磷脂膜,加入pH5.0的磷酸-磷酸氢二钠缓冲液搅拌溶解,获得空白脂质体溶液;2.将人胰岛素1000g溶解于注射用水,与所得的空白脂质溶液混合均匀,冰浴超声处理50min,再加入海藻糖2500g、甘露醇2500g和维生素E500g充分溶解后,微孔滤膜过滤;3.将上述步骤(2)所得溶液进行喷雾干燥,无菌条件下进行分装,制得注射用人胰岛素脂质体。实施例2:1.将氢化大豆磷脂15000g和聚山梨醇2000g在10L二氯甲烷中使其完全溶解,混合均匀,形成脂质溶液。置于旋转薄膜蒸发仪上减压除尽二氯甲烷,获得磷脂膜,加入pH5.5的磷酸-磷酸氢二钠缓冲液搅拌溶解,获得空白脂质体溶液;2.将人胰岛素2000g溶解于注射用水,与所得的空白脂质溶液混合均匀,冰浴超声处理60min,再加入葡萄糖12000g和抗坏血酸棕桐酸酯1000g充分溶解后,微孔滤膜过滤;3.将上述步骤(2)所得溶液进行喷雾干燥,无菌条件下进行分装,制得注射用人胰岛素脂质体。实施例3:1.将大豆磷脂10000g、蛋黄磷脂10000g和聚山梨醇5000g在15L乙酸乙酯中使其完全溶解,混合均匀,形成脂质溶液。置于旋转薄膜蒸发仪上减压除尽乙酸乙酯,获得磷脂膜,加入pH6.0的磷酸-磷酸氢二钠缓冲液搅拌溶解,获得空白脂质体溶液;2.将人胰岛素3000g溶解于注射用水,与所得的空白脂质溶液混合均匀,冰浴超声处理60min,再加入山梨醇20000g和维生素亚硫酸氢钠1000g充分溶解后,微孔滤膜过滤;3.将上述步骤(2)所得溶液进行喷雾干燥,无菌条件下进行分装,制得注射用人胰岛素脂质体。图1-3是实施例1-3制备的人胰岛素脂质体DLS图,从图可以看出,本发明所示方法制备的脂质体粒径均一,且均控制在200nm范围以内,注射使用后未发现注射部位的炎症问题;图4-6是实施例1-3制备的人胰岛素脂质体体外释放-时间曲线,药物作用时间长,生物利用度高;图7-13是给药后第1-7天血糖浓度-时间曲线,从图可以看出,注射后血药浓度稳定,峰谷波动小。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1