一种含有组氨酸去乙酰化酶抑制剂衍生物的抗肿瘤药物的制作方法
本发明涉及抗肿瘤药物技术领域,具体地,涉及一种含有组氨酸去乙酰化酶抑制剂衍生物的抗肿瘤药物。
背景技术:
癌症是危害人类生命健康的重大疾病之一。据世界卫生组织最新数据显示,预计到2020年前,全球癌症发病率将增加50%,而对于癌症的治疗手段,有效性和局限性并存,治愈率偏低。目前,中国新发癌症病人和癌症死亡病人分别为全球的20%和24%。癌症己经成为中国城市居民的第一位死因和农村居民的第二位死因,仅次于心脑血管病。
目前,对癌症治疗方法主要有手术治疗、放射治疗和化学药物治疗。手术治疗作为最传统的治疗方法,对大部分尚未发生转移的肿瘤有一定的治疗效果,但是对于原发病灶已经转移的患者,单纯的手术治疗存在较大的局限性。在这种情况下,手术切除就必须和其它治疗手段联合起来。而放射疗法在破坏或消灭癌细胞的同时,也损害了正常细胞,导致副作用。使用小分子药物杀死肿瘤细胞的化学疗法也是癌症的传统治疗方法之一,但其非选择性的特点使得它们对正常组织和细胞也具有一定的杀伤,从而造成明显的毒副作用,如广谱抗癌药阿霉素(doxorubicin,dox),会引起非常强烈的心脏毒性。更为重要的是,长期使用化疗药物会导致肿瘤细胞对化疗药物产生耐药性,这是导致癌症临床治疗失败的重要原因。因此,克服肿瘤细胞对化疗药物产生的耐药性及促进化疗药物的高效低毒,对增强恶性肿瘤患者化疗的疗效及预后至关重要。
癌症的发展与一些外在的变化是密不可分的,比如异常的组氨酸去乙酰化酶活动。组氨酸去乙酰化酶抑制剂(hdacs)包括结构不同的化合物,是一组有针对性的抗癌药物。其主要是通过增加细胞内组蛋白的乙酰化程度,提高p21等基因的表达水平等途径,抑制肿瘤细胞的增殖,诱导细胞分化和(或)凋亡。组氨酸去乙酰化酶抑制剂能够抑制肿瘤细胞迁移、侵袭、转移和具有抗肿瘤血管生成的作用,其不良反应相对较小,实用性较强,已成为肿瘤靶向治疗的研究新热点。
科研人员通过各种体内、外实验对hdac抑制剂的药理作用进行了系统的研究,部分hdac抑制剂已经进入临床研究阶段,并显示出良好的疗效。研究人员通过药化合成的方式对现有抗肿瘤疾病药物进行结构修饰,得到效果更特异、副作用更小的新型肿瘤疾病治疗药物。组氨酸去乙酰化酶抑制剂(saha)在抗肿瘤等方面具有很好的疗效,但它有一定的副作用,如恶心、呕吐、反应血液系统异常及qt间期延长,还可能造成一过性的血小板减少或骨髓抑制。
因此,急需开发一种抗肿瘤作用更明显,耐受性好,治疗剂量低,可以减轻治疗过程产生的副作用的抗肿瘤疾病药物。
技术实现要素:
针对现有技术的上述不足,本发明提供一种含有组氨酸去乙酰化酶抑制剂衍生物的抗肿瘤药物,以解决上述的技术问题;
本发明的另一个目的是提供一种组氨酸去乙酰化酶抑制剂衍生物5-苯甲酰氨基戊基硒氰酸(tc1)的制备方法和应用。
组氨酸去乙酰化酶抑制剂(saha)是食品药品管理局批准的第1个可以用于临床的hdacs药物,发明人通过对saha进行结构改造,将saha中的-conhon功能基团替换成-secn功能基团,得到一种新的组氨酸去乙酰化酶抑制剂衍生物的化合物5-苯甲酰氨基戊基硒氰酸(tc1),通过分子对接实验发现,tc1与蛋白结合的方式与saha是一致的,说明tc1发挥功能的方式与saha也是一致的。
一种含有组氨酸去乙酰化酶抑制剂衍生物的抗肿瘤药物,包括含有有效量的组氨酸去乙酰化酶抑制剂衍生物、可药用载体和赋型剂,所述赋型剂包括pbs、生理盐水和磺丁基-β-环糊精中的一种或多种;所述组氨酸去乙酰化酶抑制剂衍生物为5-苯甲酰氨基戊基硒氰酸(tc1),分子式为c13h16n2ose,分子量为295.24,结构式如下:
以上所述的5-苯甲酰氨基戊基硒氰酸在制备抗肿瘤药物中的应用。
优选地,以上所述5-苯甲酰氨基戊基硒氰酸在制备抗肿瘤药物中的应用中,包括在前列腺癌、结肠癌、肺癌、宫颈癌、胃癌、恶性脑胶质瘤、乳腺癌、鼻咽癌、肝癌和肾癌的预防药物与治疗药物中的应用。
优选地,所述5-苯甲酰氨基戊基硒氰酸应用在抗肿瘤药物中,应用剂型为临床上可接受的任一剂型,所述剂型包括经胃肠道给药制剂和非经胃肠道给药制剂。
更优选地,所述经胃肠道给药制剂,包括散剂、片剂、颗粒剂、胶囊剂、乳剂、混悬剂。
更优选地,所述非经胃肠道给药制剂,包括注射剂、喷雾剂、栓剂、贴剂、软膏剂。
一种5-苯甲酰氨基戊基硒氰酸(tc1)化合物的制备方法,包括以下步骤:
s1.将苯胺、6-溴己酰氯和三乙胺在四氢呋喃中室温下反应6~14小时,制得7-溴庚酸苯甲酰胺;
s2.将步骤s1中制得的7-溴庚酸苯甲酰胺和硒氰酸钾在室温下反应12~20小时,制得5-苯甲酰氨基戊基硒氰酸。
相对于现有技术,本发明的有益效果:
1、本发明的新化合物5-苯甲酰氨基戊基硒氰酸tc1是一个非常有效的抗肿瘤药物,具有抑制多种人类肿瘤细胞系生长,并能诱导肿瘤细胞凋亡的作用,实验表明tc1对22种肿瘤细胞株具有广谱的抗肿瘤作用,还能诱导肿瘤细胞凋亡,且tc1抑制肿瘤的能力明显强于saha;在肿瘤抑制裸鼠模型试验中,tc1化合物显示出对前列腺癌细胞pc3,胃癌细胞bcg-823和s180细胞具有明显抑制肿瘤生长的作用,同时没有明显的副作用;对小鼠的急性毒理试验也显示未观察到明显毒性,所有受试小鼠生长良好,无一死亡。
2、细胞毒性试验中显示,大多数人体肿瘤细胞对tc1敏感,不同浓度tc1培养基培养的22种肿瘤细胞,其ec50都小于2μg/ml,明显低于saha的浓度,证明tc1能广泛抑制人体肿瘤细胞生长,但对正常细胞株的抑制作用不明显。
3、诱导肿瘤细胞凋亡试验中,采用annexin-v和pi联合染色法检测,发现正常细胞av和pi均低染,凋亡细胞av和pi均高染,表明tc1和saha均具有极强的诱导肿瘤细胞凋亡的能力,且tc1的诱导能力明显强于saha。
4、tc1和saha抗肿瘤有效性试验中,结果显示两种药物均能强烈抑制前列腺癌细胞pc3、胃癌细胞bgc-823和s180细胞三种肿瘤细胞,化合物saha对pc3、bgc-823和s180三种细胞的抑制率(tgi)分别为18.66%、25.14%和29.17%;化合物tc1对pc3、bgc-823和s180三种细胞的抑制率(tgi)分别为1.70%、4.51%和3.76%;此外,使用药物处理后,动物并未出现副作用,综合上面数据表明tc1是一种可开发成新抗肿瘤药物的很好的候选药物。
5、tc1和saha给药后对小鼠的急性毒性试验中,灌胃给药后,连续14d观察称重,观察结果显示所有受试小鼠生长良好,无一死亡;试验结束后进行病例分析,均未观察到明显毒性。
6、与saha相比tc1抗肿瘤作用更明显,耐受性好,治疗剂量低,可以减轻治疗过程产生的副作用;可作为抗肿瘤药物的前体药物,优先作为抗恶性实体瘤药物的前提药物;tc1具有被开发成广谱抗肿瘤新药的巨大潜力,具有很大开发前景的广谱抗肿瘤新药。
附图说明
图1是化合物tc1和saha分别诱导人前列腺癌pc3细胞,胃癌ags细胞,肺癌a549细胞凋亡(24小时)的示意图。
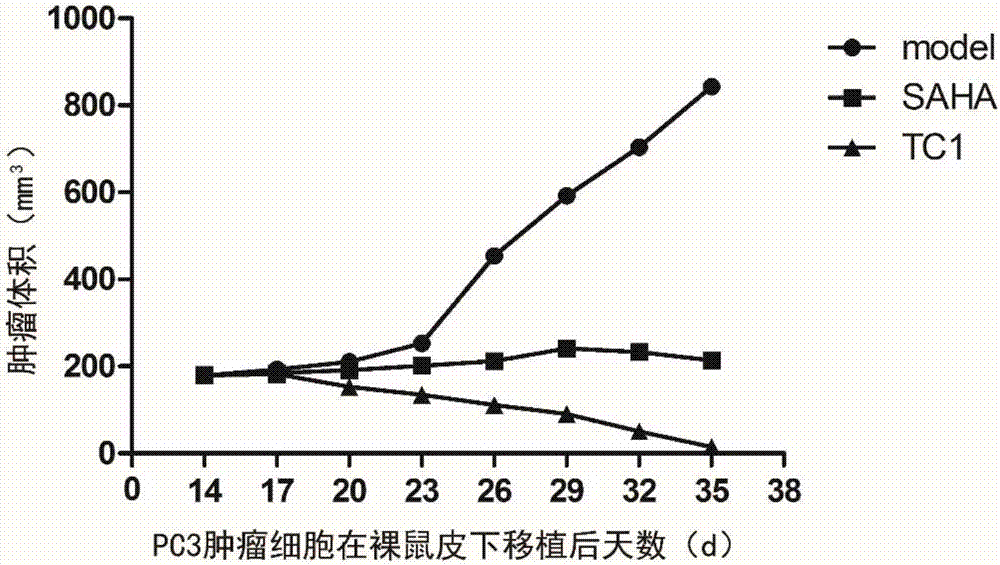
图2是化合物tc1、saha和模型组治疗皮下接种的前列腺癌(pc3)肿瘤细胞的肿瘤体积大小—移植后天数的曲线图。
图3是化合物tc1、saha和模型组治疗皮下接种的胃癌(bgc-823)肿瘤细胞的肿瘤体积大小—移植后天数曲线图。
图4是化合物tc1、saha和模型组治疗皮下接种的肉瘤细胞(s180)肿瘤细胞的肿瘤体积大小—移植后天数曲线图。
图5是化合物tc1对小鼠病理检查结果示意图。
图6是化合物saha对小鼠病理检查结果示意图。
具体实施方式
结合以下实施例对本发明作进一步描述。
实施例15-苯甲酰氨基戊基硒氰酸的制备
s1.将139mg苯胺、320mg6-溴己酰氯和455mg三乙胺在20ml四氢呋喃中室温下反应12小时,制得7-溴庚酸苯甲酰胺,7-溴庚酸苯甲酰胺产出率为86.7%;
s2.将297mg7-溴庚酸苯甲酰胺和115mg硒氰酸钾在室温下反应18小时,制得5-苯甲酰氨基戊基硒氰酸,5-苯甲酰氨基戊基硒氰酸产出率为70.0%。
实施例25-苯甲酰氨基戊基硒氰酸应用中不同剂型的制备
1、注射剂的制备
按实施例1的方法先制备得到tc1化合物,将其与20%聚氧乙烯醚蓖麻油混合,溶解到含磷酸二氢钾、磷酸氢二钾、尼泊金酯和羧甲基纤维素钠的水中,制成混悬型注射剂;
也可以将实施例1制备的tc1化合物用少量dmso溶解后,按常规加注射用水,精滤,灌封、灭菌制成注射液。
2、片剂或胶囊剂的制备
按实施例1的方法先制备得到tc1化合物,将其与药剂学意义上的填充剂、崩解剂组成常规的片剂、缓释片剂或胶囊剂;其中填充剂可选乳糖、微晶纤维素、糊精、淀粉等,崩解剂可选羟丙纤维素、交联聚维酮、羧甲基淀粉钠等,也可以选粘合剂、润滑剂或湿润剂。按照重量比,本发明的tc1化合物1份,乳糖或微晶纤维素0.05~0.2份,羟丙纤维素或羧甲基淀粉钠0.05~0.2份,3%聚维酮溶液为粘合剂,适量的硬脂酸镁为润滑剂。
3、口服液的制备
按实施例1的方法先制备得到tc1化合物,按常规口服液制法制得口服液。
实施例3细胞毒性试验
使用人肿瘤细胞系进行细胞毒性分析。人肿瘤细胞系购自atcc细胞库,用含10%fbs(胎牛血清)的dmem培养液,在含5%co2的37℃孵箱中培养;用胰蛋白酶消化汇合的细胞,经培养液洗涤后计数;向96孔培养板的每孔中加入6000-10000个细胞,孵育16小时或24小时;然后向孔内加入不同浓度的saha和tc1化合物。继续培养48小时后,对药物处理组细胞和对照组细胞进行mtt试验,结果如表1所示。
表1tc1和saha体外抑制肿瘤细胞生长
表1数据显示,细胞毒性试验中,大多数人体肿瘤细胞对tc1敏感,不同浓度tc1培养基培养的22种肿瘤细胞,其ec50都小于2μg/ml,均明显低于saha的浓度,证明tc1能广泛抑制人体肿瘤细胞生长,但对正常细胞株的抑制作用不明显。
实施例4tc1和saha诱导肿瘤细胞凋亡试验
采用annexinv(av)和pi联合染色法检测tc1和saha处理后肿瘤细胞出现的细胞凋亡现象,annexinv是一种磷脂结合蛋白与磷脂酰丝氨酸有高度亲和力,它通过细胞外侧暴露的磷脂酰丝氨酸与凋亡早期的细胞的胞膜结合,因此annexinv被作为检测细胞早期凋亡的灵敏指标之一。
在进行凋亡实验时,首先在96孔板中种植1×106个人体肺癌细胞a549、人前列腺癌细胞pc3和胃癌细胞ags;培养24小时后分别加入不同浓度的tc1和saha,其中saha和tc1诱导人肺癌细胞a549(浓度分别为0μg/ml,1μg/ml),人前列腺癌细胞pc3(浓度分别为0μg/ml,2μg/ml),胃癌细胞ags(浓度分别为0μg/ml,1μg/ml),并继续在37℃,5%co2条件下培养24小时,然后终止细胞培养,并用pbs洗涤细胞2次,经胰酶消化,离心收集细胞,用冷却的pbs再次洗涤细胞,再用4℃的结合缓冲液(含14mmnacl和25mmcacl2的0.01mm,ph7.0,hepe/naoh缓冲液)将细胞配制成1×106个/ml。取0.1ml细胞悬液置5ml流式管中,加入av-fitc5μl,再加pi5μl。稍稍混悬细胞置暗处,在20℃-25℃环境中反应15分钟,然后立即在流式细胞仪(facs)上分析。对照组分为空白对照组和阴性对照组,其中空白对照组是未经处理的细胞,排除自发凋亡;阴性对照组是不加染色剂。结果如图1所示。
由图1可知,正常细胞av和pi均低染,凋亡细胞av和pi均高染,表明tc1和saha均具有极强的诱导肿瘤细胞凋亡的能力,且tc1的诱导能力明显强于saha。
实施例5应用肿瘤抑制裸鼠模型进行saha和tc1两种化合物的抗肿瘤有效性试验
1、建立人肿瘤移植裸鼠模型
t细胞缺陷裸小鼠(nu/nu),雄性,6-8周龄,购自广东省动物中心,按照大学动物饲养和使用委员会指南饲养于无病原体环境。将5×106个pc3、bcg823、s180细胞分别悬浮于0.2ml培养基/基质胶(1:1v/v)中,皮下接种到小鼠的侧腹部区域。当肿瘤平均直径达7~8mm时,选出肿瘤大小为200mm3左右的小鼠,分别给予一定浓度的药物处理组和只给生理盐水的对照组。为保证药物处理组和对照组在处理开始时肿瘤体积分布大致相等,将小鼠分成三类:肿瘤体积小(长度<4mm),肿瘤体积中等(4~8mm),肿瘤体积大(>8mm)。对照组,药物处理组中来自相同类别的小鼠数目大致相等。
2、裸小鼠肿瘤移植模型的给药:
在口服给药试验中,用生理盐水配制化合物tc1和saha按10mg/kg给药。当裸鼠肿瘤大小为200mm3左右时开始每日给药,给予单次剂量0.3ml药液,每天1次,持续3周;对照组按同样方法给予生理盐水。小鼠单独饲养,允许自由采食。
3、抗肿瘤效应评价
每3~4天沿两个垂直方向对肿瘤进行测量。肿瘤体积根据以下公式计算:
v=(a2×b)/2
其中a是肿瘤宽度(较小直径),b是长度(较大直径)。每个肿瘤的相对肿瘤体积(rtv)定义为给定时间点的肿瘤体积与处理开始时肿瘤体积的比值。每个处理组计算平均值。根据以下公式计算肿瘤生长抑制值(tgi),判断抗肿瘤活性:
tgi(%)=t/c×100%,
其中t是处理组试验终点(4周)rtv的平均值,c是对照组试验终点rtv的平均值。采用美国国立癌症研究所的最小抗肿瘤活性标准(t/c≤42%)。试验结束时,将肿瘤切除并在甲醛中固定,进行组织学观察。试验结果如图2、3和4所示。
结果显示,两种药物均能强烈抑制前列腺癌细胞pc3、胃癌细胞bgc-823和s180细胞三种肿瘤细胞,化合物saha对pc3、bgc-823和s180三种细胞的抑制率(tgi)分别为18.66%、25.14%和29.17%;化合物tc1对pc3、bgc-823和s180三种细胞的抑制率(tgi)分别为1.70%、4.51%和3.76%;此外,使用药物处理后,动物并未出现副作用,综合上面数据表明tc1是一种可开发成新抗肿瘤药物的很好的候选药物。
实施例6tc1和saha化合物给药后对小鼠的急性毒性试验
tc1和saha药物溶解后采用灌胃给药。取两组4-6周龄的blab/c小鼠,每组10只(雌雄各半),分别将两种化合物以单次剂量100mg/kg灌胃给药,连续14d,每天观察小鼠生长状况。每两天称定体重。试验结束后,将受试小鼠处死,进行病理分析。结果如图5、图6所示。
试验结果显示:tc1和saha对小鼠灌胃给药,连续14d观察、称重,所有受试小鼠生长良好,无一死亡;试验结束后进行病例分析,均未观察到明显毒性。
最后应当说明的是,以上实施例仅用以说明本发明的技术方案,而非对本发明保护范围的限制,尽管参照较佳实施例对本发明作了详细地说明,本领域的普通技术人员应当理解,可以对本发明的技术方案进行修改或者等同替换,而不脱离本发明技术方案的实质和范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种含有组氨酸去乙酰化酶抑制剂衍生物的抗肿瘤药物的制造方法与工艺
- 氨甲酰基吡啶酮HIV整合酶抑制剂的方法和中间体与流程
- 氨甲酰基吡啶酮HIV整合酶抑制剂的方法和中间体与流程
- 一类组蛋白去乙酰化酶抑制剂及其制备方法和用途与流程
- 组蛋白去乙酰化酶抑制剂于改变蜂王浆中MRJP3蛋白质的新颖用途的制造方法与工艺
- 用于治疗疾病的硫酸乙酰肝素生物合成抑制剂的制造方法与工艺
- 酚氧类氮氧化物作为去乙酰化酶抑制剂的抗肿瘤应用的制造方法与工艺
- 作为NADPH氧化酶抑制剂的酰氨基噻二唑衍生物的制造方法与工艺
- 利用组蛋白脱乙酰酶抑制剂治疗白血病的制造方法与工艺
- 组蛋白去乙酰化酶HDAC6的抑制剂在制备防治急性肾损伤药物中的用途的制造方法与工艺
- 含有色氨酸基本骨架的邻苯二胺类选择性组蛋白去乙酰化酶抑制剂及其制备方法和应用
- 一种生产贝利司他中间体的工艺方法
- 组蛋白去乙酰化酶抑制剂治疗β亚科疱疹病毒的新用图
- 一种含有苯甘氨酸的肉桂酰胺类组蛋白去乙酰化酶抑制剂及其制备方法和应用
- 2-(1-(4-氯苯甲酰基)-5-甲氧基-2-甲基-1氢-吲哚-3-基)-n-羟基乙酰胺作为组蛋白去 ...的制作方法
- Hif羟化酶抑制剂的药物制剂的制作方法
- 一种组蛋白去乙酰酶抑制剂2-(1-(4-氯苯甲酰基)-5-甲氧基-2-甲基-1氢-吲哚-3-基-n ...的制作方法
- 一种组蛋白去乙酰酶抑制剂(e)-3-(2-(1-(4-氯苯甲酰基)-5-甲氧基-2-甲基-1氢-吲哚 ...的制作方法
- 广谱的去乙酰化酶抑制剂及其应用
- 广谱的去乙酰化酶抑制剂乙酰化赖氨酸及其应用
- 黄芪丁酰胆碱酯酶抑制活性有效提取物及其组合物的医药用途和制备方法
- 漏芦花丁酰胆碱酯酶抑制活性有效提取物及其组合物的医药用途和制备方法
- 广枣乙酰胆碱酯酶抑制活性有效提取物及其组合物的医药用途和制备方法
- 一种提高千层塔芽孢移栽成活率的方法
- 组蛋白脱乙酰酶抑制剂与免疫调节药物的组合的制作方法
- 具抗记忆错误效果的乙酰胆碱酯酶抑制剂和5-羟色胺受体4(5ht4)激动剂的化合物,其制 ...的制作方法
- 组蛋白脱乙酰酶抑制剂与免疫调节药物的组合的制作方法
- 具抗记忆错误效果的乙酰胆碱酯酶抑制剂和5-羟色胺受体4(5ht4)激动剂的化合物,其制 ...的制作方法
- 一种具有抑制乙酰胆碱酯酶功能的真菌菌株及其应用
- 含有色氨酸基本骨架的邻苯二胺类选择性组蛋白去乙酰化酶抑制剂及其制备方法和应用