一种球状NiMnO3双金属氧化物的合成方法及其应用与流程
本发明涉及储氢材料领域,特别是一种球状NiMnO3双金属氧化物的合成方法及其应用。
背景技术:
随着传统化石能源的日益消耗,环境污染越来越严重。人们已致力于开发一种新能源。氢能是一种理想的二次能源,是未来有发展前景的新型能源之一,受到研究者们的广泛关注。然而,氢的储存是氢能现阶段开发和利用的瓶颈。近年来,以LiBH4为典型代表的轻金属配位金属氢化物成为新兴的储氢材料的研究热点。
纳米限域是将材料填充到纳米孔道里,利用材料和纳米孔道的相互作用促进反应的进行,为化学反应提供一个独特的微环境。LiBH4具有较高的含氢量(18.5wt%)和体积氢密度(121kg/m3),然而,热稳定性好、放氢慢和可逆性差等因素阻碍了LiBH4的实际应用。NiMnO3能够催化LiBH4放氢,改善其热力学和动力学性能,片状的NiMnO3是由相互连接的均一纳米颗粒组成的,颗粒之间的孔道结构为LiBH4的限域提供可能,使得NiMnO3成为可能的限域骨架。另外,NiMnO3还可以对LiBH4的放氢起到催化作用,限域与催化的协同作用使得LiBH4的放氢性能得到更大程度的改善。
技术实现要素:
本发明的目的是针对上述存在的问题,提供一种NiMnO3双金属氧化物的合成方法及其应用,并以此作为LiBH4放氢的催化剂和限域骨架,从而有效降低LiBH4的放氢温度,同时提高其放氢量。
本发明的技术方案:
一种球状NiMnO3双金属氧化物的合成方法,包括以下步骤:
1)将NiCl2·6H2O和MnCl2·4H2O加入浓度为1M的NaHCO3溶液中,NiCl2·6H2O、MnCl2·4H2O与NaHCO3溶液的用量比为2.5mmol:3.5mmol:50mL,混合均匀后搅拌0.5h,得到白色的前躯体溶液;
2)将上述前驱体溶液在3000r/min转数下进行离心,将所得固体分别用蒸馏水、乙醇各洗涤三次,在60℃下干燥5h,然后在高温500℃下煅烧1h,制得成品球状NiMnO3双金属氧化物。
一种所合成的球状NiMnO3双金属氧化物的应用,制备NiMnO3-LiBH4作为LiBH4放氢的催化剂和限域骨架,NiMnO3-LiBH4的制备包括如下步骤:
1)将制备的球状NiMnO3双金属氧化物放入连接希莱克装置的三颈圆底容器中,在真空度-0.1MPa下抽真空1min,然后通入氩气;
2)在氩气氛围保护下的手套箱中,将LiBH4溶于无水四氢呋喃(THF)溶剂中得到LiBH4/THF溶液,LiBH4与无水四氢呋喃的用量比为0.1g:2mL;
3)将上述LiBH4/THF溶液加入含有球状NiMnO3双金属氧化物的三颈圆底容器中,NiMnO3与LiBH4的质量比为1:0.5-2,搅拌3h,然后在60℃下加热48h以除去四氢呋喃溶剂,制得NiMnO3-LiBH4,并转移到手套箱中进行保存。
本发明的优点是:该合成方法反应条件温和、重现性好、工艺简单、成本低;同时负载LiBH4的NiMnO3为介孔结构,具有纳米限域和催化协同效应,对LiBH4的放氢性能有显著的改善。
附图说明
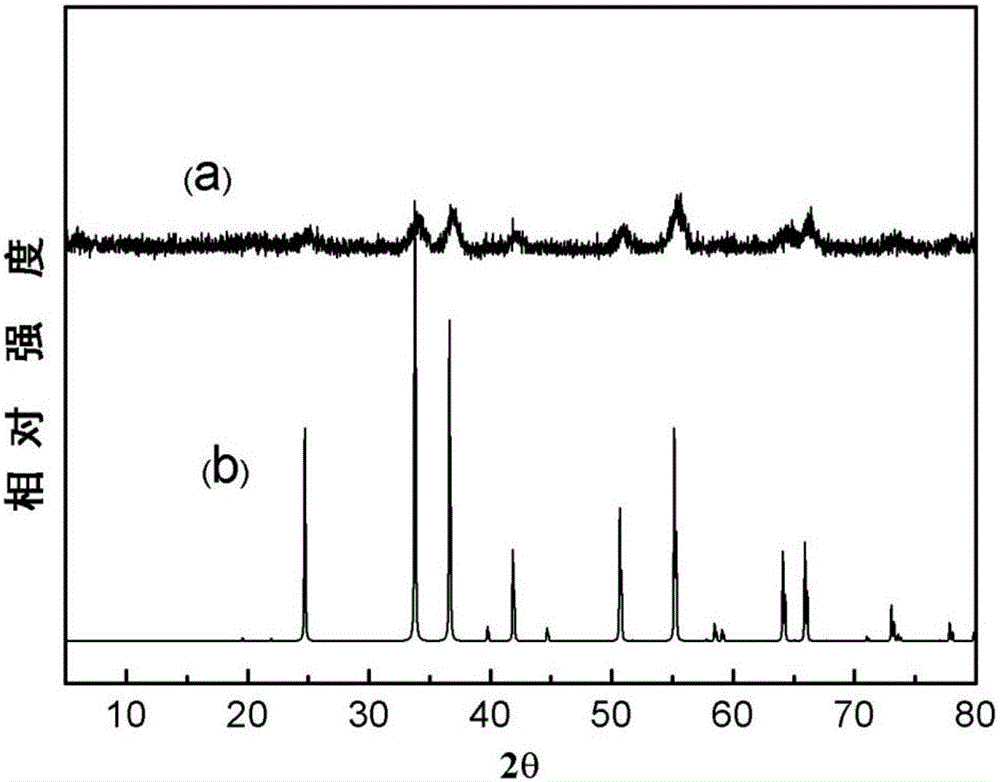
图1为合成的NiMnO3的XRD图,其中:(a)是合成的NiMnO3的XRD图,(b)是NiMnO3的标准卡片图。
图2为合成的NiMnO3的SEM图。
图3为NiMnO3-LiBH4放氢前后的IR图,其中:(a)是放氢前,(b)是放氢后。
图4为纯LiBH4与NiMnO3-LiBH4(1:2)放氢的TPD图,其中:。(a)是纯的LiBH4,(b)是NiMnO3-LiBH4的复合物。
图5为纯LiBH4与NiMnO3-LiBH4(1:2)放氢量曲线,其中:(a)是纯的LiBH4,(b)是NiMnO3-LiBH4的复合物。
具体实施方式
下面结合具体实施例对本发明进一步详细描述
实施例:
一种球状NiMnO3双金属氧化物的合成方法,包括以下步骤:
1)在100mL烧杯中将2.5mmol NiCl2·6H2O和3.5mmol MnCl2·4H2O加入50mL浓度为1M的NaHCO3溶液中,混合均匀后搅拌0.5h,得到白色的前躯体溶液;
2)将上述前驱体溶液在3000r/min转数下进行离心,将所得固体分别用蒸馏水、乙醇各洗涤三次,在60℃下干燥5h,然后在高温500℃下煅烧1h,制得成品球状NiMnO3双金属氧化物。
所得成品与标准卡片JCPDS 75-2089相吻合,其XRD和SEM图分别如图
1和2所示。
一种所合成的球状NiMnO3双金属氧化物的应用,制备NiMnO3-LiBH4作为LiBH4放氢的催化剂和限域骨架,NiMnO3-LiBH4的制备包括如下步骤:
1)将0.2g制备的球状NiMnO3双金属氧化物放入连接希莱克装置的三颈圆底容器中,在真空度-0.1MPa下抽真空1min,然后通入氩气;
2)在氩气氛围保护下的手套箱中,将0.2g LiBH4溶于4mL无水四氢呋喃溶剂中得到LiBH4/THF溶液;
3)将上述LiBH4/THF溶液加入含有球状NiMnO3双金属氧化物的三颈圆底容器中,搅拌3h,然后在60℃下加热48h以除去四氢呋喃溶剂,制得NiMnO3-LiBH4,并转移到手套箱中进行保存。
检测样品NiMnO3-LiBH4放氢性能的方法:
在手套箱中称取70mg的NiMnO3-LiBH4样品,将其放入程序升温脱附放氢(TPD)测试管中,先通半小时氩气,然后从30℃以2℃min-1加热到500℃;流速35.3mLmin-1,用高纯Ar作载气流;放氢结束后,继续通氩气一小时,最后关闭仪器。
图3为NiMnO3-LiBH4放氢前后的IR图,其中:(a)是放氢前,(b)是放氢后。从图3(a)可以看到B-H键的特征弯曲振动峰和伸缩振动峰,表明LiBH4已浸入到NiMnO3中,而图(b)中B-H键的特征吸收峰消失,表明LiBH4已完全分解。
图4为纯LiBH4与NiMnO3-LiBH4(1:2)放氢的TPD图,其中:。(a)是纯的LiBH4,(b)是NiMnO3-LiBH4的复合物。图中表明,NiMnO3-LiBH4复合物的放氢温度明显降低,起始放氢温度在135℃,最大放氢温度在约300℃,相比于纯的LiBH4的起始放氢温度290℃,最大放氢温度440℃相比,明显降低。
图5为纯LiBH4与NiMnO3-LiBH4(1:2)放氢量曲线,其中:(a)是纯的LiBH4(b)是NiMnO3-LiBH4的复合物。图中表明:500℃时,按积分面积计算,NiMnO3-LiBH4的复合物的放氢量高于纯的LiBH4。
- 还没有人留言评论。精彩留言会获得点赞!