放射性标记大麻素受体2配体的制作方法
本发明尤其涉及式(I)的化合物
其中R1是甲基并且其中所述甲基包含至少一个放射性核素。
大麻素受体是一类细胞膜受体,属于G蛋白-偶联受体超家族。目前存在两种已知亚型,称为大麻素受体1(CB1)和大麻素受体2(CB2)。CB1受体具有大的表达范围。其主要表达在中枢神经(即杏仁核小脑,海马体)系统中并且在外周中以较少量表达。由CNR2基因编码的CB2主要在免疫系统的细胞,如巨噬细胞、B细胞和T-细胞上(Ashton,J.C.等Curr Neuropharmacol 2007,5(2),73-80;Miller,A.M.等Br J Pharmacol 2008,153(2),299-308;Centonze,D.,等Curr Pharm Des 2008,14(23),2370-42),和在胃肠系统中(Wright,K.L.等Br J Pharmacol 2008,153(2),263-70)外周表达。CB2受体还存在于脑中,其中它主要发现于小胶质细胞上而非神经元上(Cabral,G.A.等Br J Pharmacol 2008,153(2):240-51)。
对于CB2受体激动剂的兴趣在过去十年间稳步提升(目前有30-40件专利申请/年),原因在于早期化合物中的几种已经在许多人类疾病的临床前模型中显示了具有有益效果的事实,所述疾病包括慢性疼痛(Beltramo,M.Mini Rev Med Chem 2009,9(1),11-25),动脉粥样硬化(Mach,F.等,J Neuroendocrinol 2008,20Suppl 1,53-7),骨质调节(Bab,I.等,Br J Pharmacol 2008,153(2),182-8),神经炎症(Cabral,G.A.等,J Leukoc Biol 2005,78(6),1192-7),缺血/再灌注损伤(Pacher,P.等,Br J Pharmacol 2008,153(2),252-62),系统性纤维化(Akhmetshina,A.等,Arthritis Rheum 2009,60(4),1129-36;Garcia-Gonzalez,E.等,Rheumatology(Oxford)2009,48(9),1050-6),肝纤维化(Julien,B.等,Gastroenterology 2005,128(3),742-55;Munoz-Luque,J.等,J Pharmacol Exp Ther 2008,324(2),475-83)。
缺血/再灌注(I/R)损伤是在诸如卒中,心肌梗死,心肺转流术和其他血管手术,以及器官移植的病症中出现的组织损害的主要原因,并且是使各种病因学的循环休克过程复杂化的终末器官损害的主要机制。所有这些病症特征均在于正常血液供给的中断,导致不充分的组织氧合。再氧合例如再灌注是复原正常组织氧合的最终治疗。但是缺乏来自血液的氧和营养产生其中循环的复原导致进一步组织损害的病症。再灌注损伤的损害原因部分在于损害的组织的炎性反应。由新回流的血液运送到该区域的白细胞响应组织损害释放大量炎性因子如白细胞介素以及自由基。复原的血流再引入细胞内的氧,其损害细胞蛋白,DNA,和质膜。
远端缺血预处理(remote ischemic preconditioning)(RIPC)代表一种利用身体内源保护能力对抗由缺血和再灌注导致的损伤的策略。其描述其中一个器官或组织的暂时性非致死缺血和再灌注给予对在远端器官或组织中“致死”缺血再灌注损伤的随后事件的抗性的有趣现象。尽管提出了几种假设,但器官或组织的暂时性缺血和再灌注通过其给予保护的实际机理目前是未知的。
体液假设提出远端器官或组织中产生的内源物质(如腺苷,缓激肽,阿片样物质,CGRP,内源性大麻素(endocannabinoids),血管紧张素I或一些其他还未确认的体液因子)进入血流并在靶组织中活化其各自受体并从而恢复缺血预处理中涉及的心脏保护的各种细胞内途径。
最近的数据显示内源性大麻素和它们的受体,特别是CB2,可能涉及于预处理中并有助于通过炎症反应的减量调节防止再灌注损伤(Pacher,P.等,Br J Pharmacol 2008,153(2),252-62)。具体地,最近使用CB2工具激动剂的研究显示了该概念用于减少心脏(Defer,N.等,Faseb J 2009,23(7),2120-30),脑(Zhang,M.等,J Cereb Blood Flow Metab 2007,27(7),1387-96),肝(Batkai,S.等,Faseb J 2007,21(8),1788-800)和肾(Feizi,A.等,Exp Toxicol Pathol 2008,60(4-5),405-10)中I/R损伤的功效。
此外,过去数年间,越来越多的文献表明CB2还可以在亚慢性和慢性情况中有意义。CB1和CB2的特定增量调节已经显示在与纤维化有关的慢性疾病的动物模型中(Garcia-Gonzalez,E.等,Rheumatology(Oxford)2009,48(9),1050-6;Yang,Y.Y.等,Liver Int 2009,29(5),678-85)与肌成纤维细胞即作为负责纤维化进程的细胞中的CB2相关表达关联。
CB2受体通过选择性CB2激动剂的活化实际上已经显示在弥散系统性硬化中产生抗纤维化效果(Garcia-Gonzalez,E.等,Rheumatology(Oxford)2009,48(9),1050-6)并且CB2受体已经显现为实验真皮纤维化中(Akhmetshina,A.等,Arthritis Rheum 2009,60(4),1129-36)和在肝病理生理学,包括与慢性肝病相关的纤维发生中(Lotersztajn,S.等,Gastroenterol Clin Biol 2007,31(3),255-8;Mallat,A.等,Expert Opin Ther Targets 2007,11(3),403-9;Lotersztajn,S.等,Br J Pharmacol 2008,153(2),286-9)的关键靶标。
明确地检测组织中的CB2的需求伴随对这种受体的日益增长的兴趣而来。用适当工具评估患者或样品中的CB2表达和受体占有率可以确认表达的靶细胞,允许人类研究中任何CB2配体的剂量寻找(dose finding),或者用于诊断目的。
迄今在用于检测组织中CB2受体蛋白的有效工具中存在不足,这是CB2受体的低表达水平的结果。缺少作为CB2检测工具的特异性抗体的另一个原因可能是因为使用CB2作为免疫原(imunogen)的明显困难。
为了解决该问题,我们探索了使用选择性地与CB2结合的放射性标记配体的可能性。据我们所知,仅存在一种可用的放射性标记CB2配体,称为[3H]-CP55940(Priller,J.等,Molecular Pharmacology 1995,48,288-292)。然而[3H]-CP55940是CB1和CB2受体的非选择性激动剂并且在测试的多种哺乳动物物种中两种受体之间没有区别。因此,为了检测也可能会表达CB1的组织中的CB2,需要利用用于竞争测定的常用同位素3H、用于放射自显影的14C或用于PET示踪技术的11C放射性标记的选择性CB2配体。
第一策略是鉴别相对于CB1对CB2具有高选择性并且与自然存在的大麻素具有结构同源性的配体。CB2激动剂HU-910(在WO 2011/061744中描述)是根据其高选择性并且根据其与在植物中发现的大麻素类化合物的结构相关的性质选择的。尽管HU-910选择性地且竞争性地与已经用[3H]-CP55940标记的CB2受体结合,[3H]-HU-910显示出高度非特异性结合,从而掩蔽与CB2受体的特异性结合位点(其预期代表全部结合位点中的小部分)。在不希望受这种理论约束的情况下,我们把这种现象归因于[3H]-HU-910的高亲油性,引起向膜中的高度分配并且从而引起不能被过量未标记HU-910竞争掉的高度非特异性结合。
因此需要寻找除了效力和选择性之外具有高亲水性的CB2配体,与在化学合成的最终步骤中引入放射性标记的选择方案配合。
如以上所定义的式(I)的化合物意外地被确认具有所需性质并且进而具有大幅降低的非特异性结合。
式(I)的化合物被证实特异性地且选择性地与由重组表达CB2受体的细胞制备的膜结合。此外,式(I)的化合物的结果是特异性地标记脾组织中的CB2受体,所述脾组织是具有CB1和CB2受体二者的高度表达的器官。此外,在从CB2受体缺陷的小鼠中分离的脾组织中,不存在被式(I)的化合物结合。在这种具体情况中,总结合信号不会被过量的未标记的式(I)的化合物(R1=CH3)降低。
式(I)的化合物因此可以例如在组织放射自显影和PET成像中使用,例如,用以评估受体表达和受体占有率,用于人类研究中任何CB2配体的剂量寻找或用于诊断目的。
在本说明书中,术语“放射性核素”定义具有不稳定原子核并且经历放射性衰变的原子的同位素。本发明的具体的放射性核素是[3H]、[11C]和[14C]。
术语“结合常数”是指与配体和受体的结合反应相关的平衡常数。
术语“选择性结合”表征配体与非常有限类型的受体的结合。
本发明因此涉及:
式(I)的化合物,其中所述至少一个放射性核素独立地选自[3H]、[11C]和[14C];
式(I)的化合物,其中R1是C[3H]3、[11C]H3或[14C]H3;
式(I)的化合物,其选自
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-(三氚甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺;
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-([14C]甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺;和
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-([11C]甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺;
式(I)的化合物用于定位患者或样品中CB2受体的用途;
式(I)的化合物用于将患者或样品中CB2受体成像的用途;
式(I)的化合物用于确定另一种化合物是否与CB2受体结合的用途;
式(I)的化合物用于确定另一种化合物是否与CB2受体结合的用途还包括测量所述另一种化合物与所述CB2受体的结合常数;
在CB1受体的存在下的如以上所定义的用途;
式(I)的化合物用于确定疾病是否以CB2受体表达的改变为特征的用途;
式(I)的化合物用于确定疾病是否以CB2受体表达的改变为特征的用途,其中所述疾病是疼痛、动脉粥样硬化(atherosclerosis)、老年性黄斑变性(age-related macular degeneration)、糖尿病性视网膜病(diabetic retinopathy)、青光眼(glaucoma)、糖尿病(diabetes mellitus)、炎症、炎性肠病(inflammatory bowel disease)、缺血-再灌注损伤(ischemia-reperfusion injury)、急性肝衰竭(acute liver failure)、肝纤维化(liver fibrosis)、肺纤维化(lung fibrosis)、肾纤维化(kidney fibrosis)、系统性纤维化(systemic fibrosis)、急性同种异体移植排斥(acute allograft rejection)、慢性同种异体移植肾病(chronic allograft nephropathy)、糖尿病肾病(diabetic nephropathy)、肾小球性肾病(glomerulonephropathy)、心肌病(cardiomyopathy)、心力衰竭(heart failure)、心肌缺血(myocardial ischemia)、心肌梗死(myocardial infarction)、系统性硬化(systemic sclerosis)、热损伤(thermal injury)、烧伤(burning)、肥厚性瘢痕(hypertrophic scars)、瘢痕疙瘩(keloids)、龈炎发热(gingivitis pyrexia)、肝硬化(liver cirrhosis)或肿瘤、骨质调节(regulation of bone mass)、神经变性(neurodegeneration)、卒中(stroke)、短暂性脑缺血发作(transient ischemic attack)或葡萄膜炎(uveitis);
式(I)的化合物,其用于诊断患有疾病的患者或组织;
如以上所定义的用于诊断患有疾病的患者或组织的式(I)的化合物,其中,所述疾病的特征在于与健康受试者或组织中CB2受体的表达相比,所述患者或组织中CB2受体的表达的改变;
如以上所定义使用的化合物,其中所述诊断包括将所述患者或组织中CB2受体的表达与健康受试者或组织中CB2受体的表达进行比较的步骤;
式(I)的化合物用于预测感染疾病的患者是否可能响应于涉及CB2配体施用的治疗的用途;
式(I)的化合物用于预测感染疾病的患者是否可能响应于涉及CB2配体施用的治疗的用途包括:将所述患者中CB2受体的表达与健康受试者或组织中CB2受体的表达进行比较;和
式(I)的化合物用于确定需要向需要其的患者施用的CB2配体的剂量的用途。
本发明进一步涉及用于鉴别与CB2受体结合的化合物的方法,其包括以下步骤:
(a)使疑似与CB2受体结合的化合物与包含CB2受体和式(I)的化合物的样品接触;和
(b)监测所述疑似与CB2受体结合的化合物是否影响式(I)的化合物与CB2受体的结合。
本发明还涉及如以上所定义的方法,其还包括测量所述疑似与CB2受体结合的化合物与CB2受体的结合强度的步骤。
本发明还涉及用于确定化合物是否相对于CB1受体选择性地与CB2受体结合的方法,其包括以下步骤:
(a)使疑似选择性地与CB2受体结合的化合物与包含CB1受体、CB2受体和式(I)的化合物的样品接触;和
(b)监测所述疑似选择性地与CB2受体结合的化合物是否影响式(I)的化合物与CB2受体的结合。
本发明进一步涉及如以上所定义的用于确定化合物是否相对于CB1受体选择性地与CB2受体结合的方法还包括:测量所述疑似选择性地与CB2受体结合的化合物与CB2受体的结合常数。
本发明还涉及用于鉴别作为CB2受体的细胞受体的方法,其包括以下步骤:
(a)使疑似包含CB2受体的样品与式(I)的化合物接触;和
(b)监测是否出现了式(I)的化合物的结合;以及
(c)任选进一步使所述样品与另一种已知CB2配体接触并且监测所述已知CB2配体是否已经将式(I)的化合物从其结合位点置换。
本发明还涉及用于测量动物、患者或样品中当将一定剂量的疑似与CB2受体结合的化合物施用于所述动物或患者或者与所述样品接触时CB2受体被所述化合物占据的百分数的方法,其包括以下步骤:
(a)将式(I)的化合物施用于动物或患者或者与包含至少一种CB2受体的样品接触,所述化合物的量足以占据所述动物、患者或样品的100%CB2受体;
(b)将所述剂量的所述疑似与CB2受体结合的化合物施用于所述动物或患者或者与所述样品接触;
(c)监测式(I)的化合物被所述疑似与CB2受体结合的化合物的置换;和
(d)计算所述至少一种CB2受体被所述疑似与CB2受体结合的化合物占据的百分数。
本发明还涉及用于确定需要向需要其的患者施用的CB2配体的剂量的方法,其包括以下步骤:
(a)确定动物或样品中在将已知在所述动物或样品中提供药理学反应的剂量的所述CB2配体施用于所述动物或者与所述样品接触之后CB2受体被所述CB2配体占据的百分数,包括:
(a1)将足以占据所述动物或样品的100%CB2受体的量的式(I)的化合物施用于所述动物或者与所述样品接触;
(a2)将已知在所述动物或样品中提供所述药理学反应的所述剂量施用于所述动物或与所述样品接触;
(a3)监测式(I)的化合物被所述CB2配体的置换;和
(a4)计算CB2受体被所述CB2配体占据的百分数;
(b)确定在人受试者或样品中给出CB2受体被所述CB2配体占据的相同百分数的所述CB2配体的剂量,包括:
(b1)将足以占据所述人受试者的100%CB2受体的量的式(I)的化合物施用于所述人受试者或者与所述样品接触;
(b2)将一定剂量的所述CB2配体施用于所述人受试者或者与所述样品接触;
(b3)监测式(I)的化合物被所述CB2配体的置换;和
(b4)计算CB2受体被所述CB2配体占据的百分数;
(b5)重复步骤(b2)至(b4),直到在步骤(b4)中也得到在步骤(a4)中计算的CB2受体的百分数;和
(b6)计算已经在步骤(b2)中施用的剂量的加和,从而得到需要向患者施用的所述CB2配体的剂量。
本发明还涉及用于确定疾病是否以CB2受体表达的改变为特征的方法,其包括以下步骤:
(a)将式(I)的化合物与样品接触或者施用于感染所述疾病的受试者以及与健康样品接触或者施用于健康受试者;
(b)监测两个样品中是否出现式(I)的化合物的结合;和
(c)比较两个样品中与所述CB2受体结合的式(I)的化合物的量。
本发明还涉及本发明的方法,其中在监测期间使用放射自显影或正电子发射断层扫描。
本发明进一步涉及药物组合物,其包含式(I)的化合物。
本发明还涉及式(I)的化合物,其用作诊断剂,即用于诊断疾病。
本发明还涉及式(I)的化合物,其用于诊断疼痛、动脉粥样硬化(atherosclerosis)、老年性黄斑变性(age-related macular degeneration)、糖尿病性视网膜病(diabetic retinopathy)、青光眼(glaucoma)、糖尿病(diabetes mellitus)、炎症、炎性肠病(inflammatory bowel disease)、缺血-再灌注损伤(ischemia-reperfusion injury)、急性肝衰竭(acute liver failure)、肝纤维化(liver fibrosis)、肺纤维化(lung fibrosis)、肾纤维化(kidney fibrosis)、系统性纤维化(systemic fibrosis)、急性同种异体移植排斥(acute allograft rejection)、慢性同种异体移植肾病(chronic allograft nephropathy)、糖尿病肾病(diabetic nephropathy)、肾小球性肾病(glomerulonephropathy)、心肌病(cardiomyopathy)、心力衰竭(heart failure)、心肌缺血(myocardial ischemia)、心肌梗死(myocardial infarction)、系统性硬化(systemic sclerosis)、热损伤(thermal injury)、烧伤(burning)、肥厚性瘢痕(hypertrophic scars)、瘢痕疙瘩(keloids)、龈炎发热(gingivitis pyrexia)、肝硬化(liver cirrhosis)或肿瘤、骨质调节(regulation of bone mass)、神经变性(neurodegeneration)、卒中(stroke)、短暂性脑缺血发作(transient ischemic attack)或葡萄膜炎(uveitis)。
式(I)的化合物的合成可以例如根据以下方案实现。
方案1
使用广泛接受的氚-甲基化试剂,比如磺酸[3H]甲酯(例如,4-硝基苯磺酸-[3H]甲酯)或[3H]甲基碘,通过去甲基前体N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺的一步氚-甲基化反应,容易得到目标化合物。这种合成概念的主要优势是可以在合成途径的最后步骤中完成放射性核素的掺入,其通常为履行被称为ALARA(可合理达到的尽可能低的剂量(as low as reasonably achieveable))的辐射保护基本原则的最可行方法。
为了进一步使放射性物质的使用最小化,通常相对于放射性甲基化试剂2-3倍过量使用去甲基前体。
通过应用相同的合成概念并且通过使用已知的[14C/11C]标记的甲基转移试剂,比如[14C/11C]MeI或磺酸[14C/11C]甲酯(例如,三氟甲磺酸[14C/11C]甲基酯、4-硝基苯磺酸[14C/11C]甲酯),可以从相同的前体分子开始制备相应的[14C]-和[11C]标记的衍生物。
尤其是对于[11C]标记策略来说,归因于正电子发射体碳-11的20min的短的半衰期,最重要的是建立短、快速且有效的合成方法。
本发明因此还涉及用于制造式(I)的化合物的方法,其包括使式(A)的化合物
在4-硝基苯磺酸-[3H]-甲酯、[3H]-甲基碘、三氟甲磺酸-[11C]-甲酯、[11C]-甲基碘、4-硝基苯磺酸-[11C]-甲酯、三氟甲磺酸-[14C]-甲酯、[14C]-甲基碘或4-硝基苯磺酸-[14C]-甲酯的存在下反应。
在本发明的方法中,式(A)的化合物有利地在4-硝基苯磺酸-[3H]-甲酯、三氟甲磺酸-[11C]-甲酯或4-硝基苯磺酸-[14C]-甲酯的存在下反应。
本发明的方法有利地在甲苯中进行。
本发明的方法有利地在大约100℃至150℃的温度、尤其是在大约120℃进行。
本发明进一步涉及根据本发明的方法制造的化合物。
现将通过以下没有限制性质的实施例来说明本发明。
实施例
缩写
CAN=CAS登录号;LC=液相色谱法;MS=质谱法;NMR=核磁共振;SEM=平均值的标准误差;THF=四氢呋喃;WT=野生型。
实验
所有反应在氩气氛下在火焰干燥的玻璃器皿中进行。将分析级溶剂用于反应,并且当需要时,在不进行进一步纯化的情况下使用干燥溶剂。除非另外说明,试剂购自声誉良好的供应厂商并且在不进行进一步纯化的情况下使用。所有1H NMR谱在Bruker Advance Ultra Shield 300MHz光谱仪上记录。相对于所述的含氘溶剂报告化学位移。在PE Sciex API 150EX LC/MS涡轮喷雾系统(Turbo Spray System)上记录质谱。使用Isco Combi Flash companion,使用来自多个供应厂商的多种尺寸的预装的二氧化硅柱(230-400目、40-63μm),进行急骤色谱。薄层层析在购自Merck KgaA的预涂布的板(20x 20cm、硅胶F254)上进行并且使用254nm CAMAG UV灯或使用碱性高锰酸钾溶液可视化。使用薄层层析、LCMS和1H NMR的组合来监测所有反应。
实施例1
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-(三氚甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺
a)N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-氟-5-(三氟甲基)苯甲酰胺
向3-叔丁基-1-(环丁基甲基)-1H-吡唑-5-胺(458mg,2.21mmol,CAN 1018679-74-7)和三乙胺(670mg,923μL,6.62mmol)在无水THF(9mL)中的溶液中逐滴加入2-氟-5-(三氟甲基)苯甲酰氯(500mg,333μL,2.21mmol,CAN 207981-46-2)在无水THF(9mL)中的溶液。将粉色悬浮液在环境温度搅拌30分钟并且用1M碳酸氢钠水溶液(70mL)萃取。将水层用乙酸乙酯(3x 70mL)萃取。将有机层合并并且使用硫酸钠干燥,之后在真空中浓缩。通过闪蒸层析(在庚烷中10%至20%乙酸乙酯)将粗物质纯化,得到794.4mg(2.0mmol,91%收率)的作为橙色粉末的标题化合物。
1H NMR(300MHz,氯仿-d)δppm 1.32(s,9H),1.72-2.20(m,6H),2.81(dt,J=14.73,7.37Hz,1H),4.04(d,J=7.06Hz,2H),6.37(s,1H)7.38(dd,J=11.61,8.58Hz,1H),7.80-7.91(m,1H),8.27(d,J=15.95Hz,1H),8.53(dd,J=6.96,2.32Hz,1H)。MS m/z 398.2[M+H]+。
b)N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺
将叔丁醇钾(203mg,1.81mmol)加入至2-甲基丙烷-1,2-二醇(136mg,138μL,1.51mmol,CAN 558-43-0)在无水THF(7mL)中的冰冷的溶液中。将无色悬浮液在0℃搅拌5分钟,使其升温至室温并且搅拌1小时。在0℃下,加入(N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-氟-5-(三氟甲基)苯甲酰胺(400mg,1.01mmol)。将所得的黄色悬浮液在室温下搅拌72h。加入叔丁醇钾(203mg,1.81mmol)并且在70℃继续搅拌2小时。加入1M碳酸氢钠水溶液(50mL)和乙酸乙酯(50mL)并且分层。将水相用乙酸乙酯(2x 50mL)萃取。将有机层合并并且使用硫酸钠干燥,之后在真空中浓缩。通过急骤色谱(在庚烷中30至50%乙酸乙酯)将粗物质纯化,得到334mg(0.714mmol,71%收率)的作为白色粉末的标题化合物。
1H NMR(300MHz,氯仿-d)δppm 1.30(s,9H),1.43(s,6H),1.69-2.05(m,6H),2.77(dt,J=14.63,7.22Hz,1H),4.02-4.19(m,4H),6.19(s,1H),7.13(d,J=8.88Hz,1H),7.75(dd,J=8.68,2.42Hz,1H),8.55(d,J=2.22Hz,1H),9.69(s,1H)。MS m/z 468.3[M+H]+。
c)(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-(三氚甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺
在1ml的螺丝帽小瓶中,将N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺(1.0mg,2.14μmmol)加入至4-硝基苯磺酸-[3H]甲酯(50mCi,0.16mg,0.71μmmol)在无水甲苯(50μL)中的溶液中。将小瓶封闭并且将反应混合物在120℃搅拌2h。之后,通过急骤色谱(二氧化硅,二氯甲烷/甲醇95:5)将粗物质纯化,得到21.4mCi(43%)的>99%放射化学纯度(HPLC:X-Bridge C18,乙腈/甲酸盐缓冲液pH3.0)和85Ci/mmol的比活性的标题化合物。
实施例2
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-([14C]甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺
在2ml的螺丝帽小瓶中,将N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺(209mg,0.45mmol)加入至4-硝基苯磺酸-[14C]甲酯(25mCi,98mg,0.45mmol)在无水甲苯(1.5mL)中的溶液中。将小瓶封闭并且将反应混合物在120℃搅拌20h。在移除溶剂之后,通过急骤色谱(二氧化硅,二氯甲烷/甲醇/三乙胺97:3:0.5)将粗物质纯化,得到8.7mCi(35%)的>99%放射化学纯度(HPLC:X-Bridge C18,水/含有0.05%三乙胺的乙腈)和56mCi/mmol的比活性的标题化合物。
实施例3
(NE)-N-[5-叔丁基-2-(环丁基甲基)-1-([11C]甲基)吡唑-3-亚基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺
通过14N(p,α)11C核反应,在Cyclone 18/9回旋加速器(18-MeV,IBA,比利时)以[11C]CO2的形式制备碳-11。在包括[11C]CO2在镍催化剂上还原为[11C]甲烷和随后的气相碘化的2步反应序列中产生[11C]甲基碘([11C]MeI)。在190℃经过AgOTf/C柱之后,形成更高反应性的三氟甲磺酸-[11C]甲酯(大约30GBq),其鼓泡通过含有N-[5-叔丁基-2-(环丁基甲基)吡唑-3-基]-2-(2-羟基-2-甲基-丙氧基)-5-(三氟甲基)苯甲酰胺(3mg,6.46μmol)和无水甲苯(0.25mL)的3mL反应器小瓶。在5min内将混合物加热至150℃。在用在水(1.5mL)中的30%乙腈稀释后,使用半制备型HPLC(柱:Sunfire C18 5μm;10x 150mm;在大约10min的产物峰)将粗产物纯化。将收集的产物用水(10mL)稀释,捕获在C18筒(Waters,用5mL EtOH和10mL水预处理)上,用水(5mL)洗涤并且用EtOH(0.5mL)洗脱。为了配制最终产物,加入注射用水(9.5mL),得到5%的乙醇浓度。为了质量控制,将等分的配制溶液注射至分析HPLC系统(柱:ACE柱,C18,3μm)中。通过与其非放射性参比化合物的保留时间比较并且通过共同注射,确认11C标记的产物的身份。通过UV峰强度与冷参比化合物的校准曲线的比较,计算产物的比活性。在典型实验中,比活性为≥500GBq/μmol,并且在合成最后的总活性为2±1.00GBq(n=30)。自粒子辐射(bombardment)结束起的总合成时间是大约40min。
实施例4
小鼠中的放射性配体结合
细胞培养
在补充有10%FBS、300μg ml-1潮霉素(hygromycin)和800μg ml-1遗传霉素(geneticin)(G418)的F-12营养混合物(HAM)中培养表达人CB1和人CB2的CHO-K1β-抑制蛋白(arrestin)细胞(DiscoveRx Inc.,Fremont,CA)。细胞于潮湿气氛中在37℃在5%CO2下温育。
放射性配体结合测定
使用玻璃罐和以47,800g在4℃离心30min,在pH 7.4的15mmol L-1Hepes、0.3mmol L-1EDTA、1mmol L-1EGTA、2mmol L-1MgCl2、完全无EDTA蛋白酶抑制剂(Roche Applied Science,Rotkreuz,瑞士)中,将稳定转染的细胞或脾组织均化。之后在相同缓冲液中将片状沉淀物重新均化两次并且离心(47,800g,4℃,30min)。之后在pH 7.4的75mmol L-1Tris、0.3mmol L-1EDTA、1mmol L-1EGTA、12.5mmol L-1MgCl2、250mmol L-1蔗糖中,将最终片状沉淀物以1至3mg mL-1的蛋白质浓度重悬,等分,在干冰上冷冻并且在-80℃储存。
饱和结合
用0.05至2.4nM的式(I)的化合物和40μg的膜蛋白进行饱和结合。使用CP55940(10μM)限定非特异性结合。测定缓冲液由pH 7.4的50mmol.L-1Tris-HCl、5mmol L-1MgCl2、2.5mmol L-1EGTA、和0.1%无脂肪酸BSA组成。通过以250μl/孔的最终体积加入膜来开始测定。将测定物在室温下温育2h,然后在Filtermate细胞收集器(cell harvester)上通过在0.3%聚乙烯亚胺中预浸渍的Packard GF/B过滤器真空过滤并且用洗涤缓冲液(50mmol L-1Tris-HCl、5mmol L-1MgCl2、2.5mmol L-1EGTA和0.5%无脂肪酸BSA,pH 7.4)冲洗。
竞争结合
对于竞争结合来说,或者在存在或不存在逐渐增加的浓度的未标记的式(I)的化合物(R1=CH3)的情况下用0.3nM的[3H]-CP55940,或者在存在或不存在CP55940(10μM)的情况下用1.5nM式(I)的化合物和逐渐增加的量的膜(2.5-80μg),将膜制剂在30℃在0.2mL最终体积的50mmol L-1Tris-HCl、5mmol L-1MgCl2、2.5mmol L-1EGTA、0.1%无脂肪酸BSA和1%DMSO的pH 7.4的缓冲液中温育,轻轻地振荡。通过在0.5%聚乙烯亚胺预浸渍的GF/B过滤板(Packard)上真空过滤接着用2mL的含有0.5%无脂肪酸BSA的冰冷结合缓冲液简短洗涤七次,终止所有结合反应。将板在50℃干燥1h并且使用液体闪烁计数确定所结合的放射性标记。通过四参数逻辑模型使用ActivityBase(ID Business Solution,Ltd.)确定IC50值和Hill斜率。
结果在以下表1和在图1至3中示出。
表1
使用表达人CB2受体的CHO-K1细胞的[3H]-CP55940的放射性配体竞争结合
表1说明了在重组表达人CB1受体和人CB2受体的细胞中并且使用非选择性CB1/CB2放射性配体[3H]-CP55940,未标记的式(I)的化合物(R1=CH3)对于人CB2受体(pKi 8.97)相对于人CB1受体(pKi 5.41)的高结合选择性。
图1:使用小鼠脾组织WT的放射性配体结合(1.5nM[3H]-式(I)的化合物)
图1示出了式(I)的化合物在小鼠脾组织中的高特异性结合。使用逐渐增加的量的膜,非特异性结合保持恒定,但是特异性结合增加。
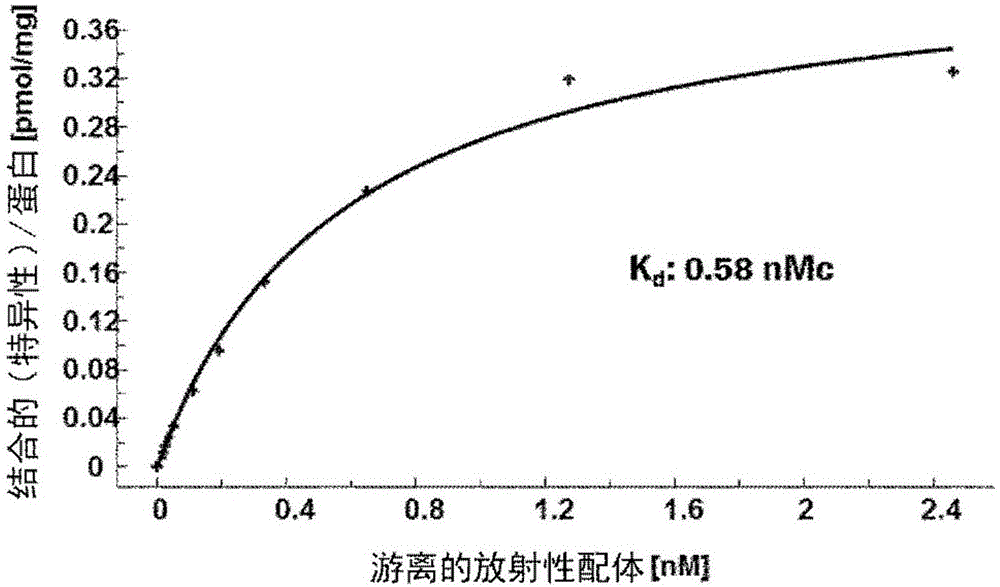
图2:使用小鼠脾组织WT的放射性配体饱和结合([3H]-式(I)的化合物)
图2示出了式(I)的化合物在小鼠脾组织中的特异性结合是可饱和的。对于小鼠CB2受体来说,计算的半数最大亲和性(Kd)是0.58nM,并且在小鼠脾组织中CB2受体表达水平(Bmax)是430fmol/mg。
图3:使用小鼠脾KO(NIH)的放射性配体结合(3[H]-式(I)的化合物)
与图1相比,图3示出了在从CB2缺失的小鼠取得的小鼠脾组织中缺少式(I)的化合物的特异性结合。使用逐渐增加的量的膜,特异性结合仍然不存在,表明与CB2受体的高特异性结合,如在从野生型同窝出生仔畜中取得的小鼠脾组织中证明的。
- 还没有人留言评论。精彩留言会获得点赞!
- 抗kir抗体和抗pd-1抗体的组合用于治疗癌症的制作方法
- 基于结合抑制点击化学反应检测小分子配体靶蛋白的荧光生物传感方法
- 受体配体连接的细胞毒性分子的制作方法
- 一种制备可物理再生蛋白质芯片的方法
- 经修饰的肽,cb受体的配体,用于评估与cb受体结合的试剂盒、体外方法,用于调节cb受体 ...的制作方法
- 对拉伸分子动力学模拟中拉伸方向优化的方法及装置的制作方法
- 鉴别具有治疗性皮脂抑制活性的ahr受体的配体的方法以及所述配体的制作方法
- 空间分辨的配体-受体结合试验的制作方法
- 用于测定分析物与配体的固有结合参数的方法、用于从一群分析物中选择分析物的方法 ...的制作方法
- 测定受体配体间结合常数的压力驱动亲和毛细管电泳方法
- 一种针对cd47的单域抗体的制作方法
- 受体配体连接的细胞毒性分子的制作方法
- 结合到核受体配体多肽的抗psma抗体的制作方法
- 经修饰的肽,cb受体的配体,用于评估与cb受体结合的试剂盒、体外方法,用于调节cb受体 ...的制作方法
- 一种模拟配体分子与靶标受体反应并计算预测该反应的热力学与动力学参数的方法和系统的制作方法
- 鉴别具有治疗性皮脂抑制活性的ahr受体的配体的方法以及所述配体的制作方法
- 具有不同配体和受体的多种生物传感器的统一加工与制造的系统设备的制作方法
- 空间分辨的配体-受体结合试验的制作方法
- 一种基于雄激素受体体外受体-配体结合效应的环境类雄激素的elisa定量检测方法
- 对感化性受体及与其相关的配体进行的调节的制作方法