新型beta‑肾上腺素受体激动剂通用半抗原的合成及应用的制作方法
本发明属于有机合成和分析化学技术领域,涉及一种新型beta-肾上腺素受体激动剂(以下简称beta-激动剂)通用半抗原的合成及其在beta-激动剂多残留检测方面的应用。
背景技术:
beta-肾上腺素受体激动剂,简称beta-激动剂,是动物源性食品中检出率最高、危害最严重的化学性残留危害物,其中最著名的就是克伦特罗(clenbuterol,cl),俗称“瘦肉精”。上世纪80年代,美国脂胺公司的科研人员意外发现,“瘦肉精”能增强动物脂肪分解,促进蛋白质合成,大大缩短肉品上市周期,显著提高胴体瘦肉率、饲料回报率和经济效益。随后在世界各地迅速推广,80年代后期,传入我国并在许多地区的饲料加工企业和养殖业推广使用,很快成为养殖业应用最广泛的“添加剂”。
“瘦肉精”除克伦特罗外,还包括沙丁胺醇(salbutamol,sal)、莱克多巴胺(ractopamine,rac)等20多个结构和性质相类似的化合物。这类化合物进入体内后选择性作用于腺苷酸环化酶,导致人体产生低敏感现象,哮喘发生率和发病程度升高;还可导致内分泌紊乱,诱发染色体畸变及恶性肿瘤,严重时可致人死亡。因此我国和世界上大多数国家都明文禁止“瘦肉精”用作饲料添加剂。
目前,beta-激动剂类兽药残留的检测方法主要包括高效液相色谱法(hplc)、液相色谱-质谱联用法(lc-ms)、气相色谱-质谱联用法(gc-ms)、酶联免疫法(elisa)和荧光免疫法(fia)等。
色谱法是β-激动剂兽药残留的主要检测方法,但是色谱法检测成本高、操作复杂、大量的阴性样品重复检测;而酶联免疫法具有特异性强、样品前处理简单等优点,但特异性强的特点同时也决定了它的致命缺点:一种酶联免疫试剂盒或试纸条只能检测一种兽药残留,而无法检测其它的同类兽药残留,这就是容易出现漏检的原因(如2011年轰动全国的“双汇瘦肉精”事件);此外,随着beta-激动剂多种替代品的出现,如果进行完全检测,一个样品需要使用多种检测产品,大大提高了检测成本和工作时间,失去了快速筛选的意义。
多残留免疫分析能同时检测一类药物残留,其低成本、高通量、快速现场的优点是现有的色谱法和特异性免疫方法无法比拟的,是未来食品安全检测领域的关键技术之一,逐渐引起重视。多残留免疫分析主要有三种方法:通用半抗原、多决定簇抗原和混合抗体。混合抗体法是利用多种特异性抗体实现对多个化合物同时检测的目的;多决定簇抗原是在载体蛋白上偶联多种待测小分子半抗原,制备能识别这些小分子的抗体而进行多残留检测。这两种方法最大的缺点就是重复性差。而通用半抗原具有另外两种方法难以比拟的优点,因此是多残留免疫分析的首选方法,通用半抗原的分子设计与合成是其核心环节。
技术实现要素:
本发明的目的在于提供一类新型beta-激动剂通用半抗原,所述通用半抗原的结构如式i所示:
(i)
其中:
r1和r2各自独立地选自氢原子、羟基、羟甲基、氰基、氨基或氨甲基;
x表示亚甲基或氧原子;
r3表示任意取代的c1-c10的烷基;
r4表示-(ch2)n-y,其中y表示羧基、氨基或者羟基,n为2~6的整数。
本发明提供的beta-激动剂通用半抗原,优选地,具有如式(ii)所示结构:
(ii)
其中,r1为氢原子,r2为氢原子或羟基,r3为环丙基、异丙基或叔丁基。
本发明的另一目的在于提供一种合成如式(i)及式(ii)所示的通用半抗原过程中的中间体的制备方法(路线a),包括以下步骤:
(1)式(iii)化合物酰化得到式(iv)化合物,式(iii)中r1为氢原子,r2为氢原子或羟基,式(iv)中x为氯或溴。酰化试剂可以为氯乙酰氯、氯乙酰溴、溴乙酰氯或溴乙酰溴,在适当的催化剂如三氯化铝、三氟化硼等催化下进行。反应可在适当溶剂如二氯甲烷、三氯甲烷等中于00c到600c的温度下进行。
(iii)(iv)
(2)式(iv)化合物氨化得到式(v)化合物,式(v)中r1为氢原子,r2为氢原子或羟基,r3为环丙基、异丙基或叔丁基。氨化试剂相应地选择为异丙基氨或叔丁基氨,在适当的溶剂如二氯甲烷、三氯甲烷等中于00c到600c的温度下进行。式(iv)中化合物的羧基可用常用保护基团如甲基保护,待羰基还原为羟基之后用常用方法脱去保护基。
(v)
(3)式(v)化合物还原得到式(i)化合物,还原试剂为硼氢化钠,在甲醇或乙醇溶剂中,于00c到300c的温度下进行。
(ii)
本发明还提供了合成如式(i)及式(ii)所示的通用半抗原过程中的中间体的另一种制备方法(路线b),包括以下步骤:
(1)制备如式(vi)所示的n-苄基取代胺,其中r3为环丙基、异丙基或叔丁基。采用苯甲醛与环丙胺、异丙胺或叔丁胺缩合后再还原的方法得到。缩合时可选择甲醇、乙醇等常用溶剂,在100c到500c的温度下进行,缩合产物可不进行分离直接进行下一步还原反应;还原试剂为硼氢化钠,在00c到300c的温度下进行。
(vi)
(2)式(iv)化合物与式(vi)化合物反应得到式(vii)化合物,式(iv)中r1为氢原子,r2为氢原子或羟基,x为氯或溴。在弱碱(如碳酸钾等)作用下于适当溶剂(如乙腈等)适当温度(100c到600c)下进行。式(iv)中化合物的羧基可用常用保护基团如甲基保护,待羰基还原为羟基之后用常用方法脱去保护基。
(iv)(vii)
(3)式(vii)化合物还原得到式(viii)化合物,还原试剂为硼氢化钠,在甲醇或乙醇溶剂中,于00c到300c的温度下进行。
(vii)(viii)
(4)式(viii)化合物还原得到式(i)化合物,还原试剂为氢气加钯/碳催化剂,于00c到300c的温度下进行。
本发明的另一目的还在于提供所述通用半抗原在beta-激动剂多残留检测方面的应用,包括:以所述化合物为半抗原,通过与载体蛋白偶联得到免疫原及包被原;通过动物免疫获得能识别多种肾上腺素受体激动剂的抗体;以及所述抗原、抗体的标记物,包括胶体金标记物、酶标记物和荧光染料标记物。
附图说明
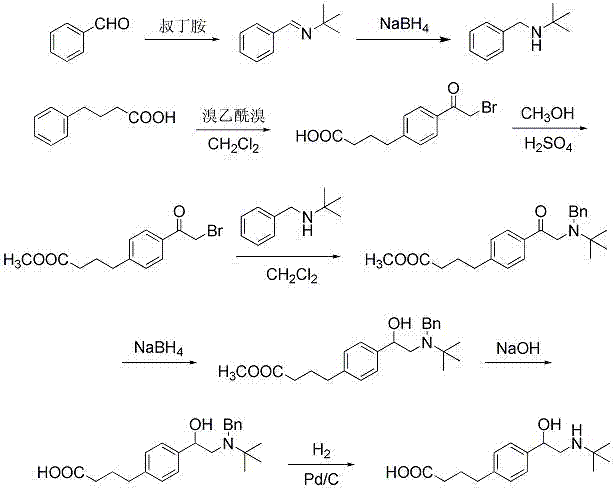
图1为优选通用半抗原4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)的合成路线a;
图2为优选通用半抗原4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)的合成路线b;
图3为本专利涉及的β-肾上腺素受体激动剂通用半抗原的结构通式
具体实施方式
实施例1优选通用半抗原4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)的合成路线a
(1)4-(4-溴乙酰基)苯基丁酸的合成
将8.56g无水氯化铝(64mmol)溶解于150ml二氯甲烷中,加入1.64ml溴乙酰溴(18.7mmol)反应0.5h,再加入2.19g4-苯基丁酸(13.4mmol),常温下反应3-5h。加入150ml水搅拌后用二氯甲烷萃取2-3次,合并有机相后用饱和食盐水洗涤,无水硫酸钠干燥,过滤后减压蒸馏除去溶剂,得产物4-(4-溴乙酰基)苯基丁酸(淡黄色固体)3.5g,产率为91.6%。m/z284,286。1hnmr(cdcl3,400mhz)2.01(m,2h),2.41(t,2h,j=7.2hz),2.77(t,2h,j=7.6hz),4.45(s,2h),7.33(d,2h,j=8.4hz),7.94(d,2h,j=8.4hz).
(2)4-(4-溴乙酰基)苯基丁酸甲酯
将2.85g4-(4-溴乙酰基)苯基丁酸(10mmol)溶解于60ml甲醇中,加入2ml浓硫酸并加热回流3h。减压蒸馏除去甲醇,加入水搅拌后用二氯甲烷萃取2-3次,合并有机相后用饱和食盐水洗涤,无水硫酸钠干燥,过滤后减压蒸馏除去溶剂,得产物4-(4-溴乙酰基)苯基丁酸甲酯(棕黄色液体)2.6g,产率为86.9%。m/z298,300。1hnmr(cdcl3,400mhz)1.97(m,2h),2.39(t,2h,j=7.6hz),2.72(t,2h,j=8.0hz),3.66(s,3h),4.43(s,2h),7.28(d,2h,j=8.0hz),7.91(d,2h,j=8.0hz).
(3)4-(4-(2-叔丁胺基)乙酰基)苯基丁酸甲酯
将0.3g4-(4-溴乙酰基)苯基丁酸甲酯(1mmol)和2.4ml叔丁胺溶解于10ml二氯甲烷中,回流下反应24h。减压蒸馏除去溶剂和过量叔丁胺,加入水搅拌,用二氯甲烷萃取2-3次,合并有机相用饱和食盐水洗涤,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,丙酮/乙酸乙酯(6:1)为淋洗剂,得产物4-(4-(2-叔丁胺基)乙酰基)苯基丁酸甲酯(淡黄色油状液体)152mg,产率为52.3%。m/z292(m++1)。1hnmr(cdcl3,400mhz)1.45(s,9h),1.99(m,2h),2.34(t,2h,j=7.4hz),2.74(t,2h,j=7.6hz),3.68(s,3h),3.91(s,2h),7.34(d,2h,j=8.0hz),8.13(d,2h,j=8.0hz).
(4)4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸甲酯
将80mg4-(4-(2-叔丁胺基)乙酰基)苯基丁酸甲酯(0.27mmol)溶解于1.5ml甲醇中,加入26mg硼氢化钠(0.69mmol),室温下反应2h。加入稀盐酸将ph值调节至4-5,用二氯甲烷萃取2-3次,饱和食盐水洗,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,石油醚/二氯甲烷(5:1)为淋洗剂,得产物4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸甲酯(无色油状液体)57mg,产率为72.1%。m/z294(m++1)。1hnmr(cdcl3,400mhz)1.48(s,9h),1.95(m,2h),2.33(t,2h,j=7.6hz),2.65(t,2h,j=7.6hz),3.00(t,1h,j=11.4hz),3.18(d,1h,j=11.4hz),5.35(m,1h),7.17(d,2h,j=8.0hz),7.38(d,2h,j=8.0hz).
(5)4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)
将45mg4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸甲酯(0.15mmol)溶解于0.5ml甲醇中,加入氢氧化钠溶液(含naoh0.3mmol),室温反应过夜。将反应液用稀盐酸溶液调节ph至5-6,减压蒸馏除去溶剂,用甲醇提取剩余物2-3次,合并提取液后减压蒸干溶剂,用少量丙酮洗涤,得产物4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba,白色固体)36mg,产率为85.7%。m/z280(m++1)。1hnmr(cdcl3,400mhz)1.42(s,9h),1.92(m,2h),2.32(t,2h,j=7.6hz),2.68(t,2h,j=7.6hz),3.05(t,1h,j=11.4hz),3.17(d,1h,j=11.2hz),5.03(m,1h),7.20(d,2h,j=8.0hz),7.34(d,2h,j=8.0hz).
实施例2优选通用半抗原4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)的合成路线b
(1)苄基叔丁胺的合成
将4.8ml苯甲醛(47.1mmol)溶于20ml无水乙醇中,再加入5ml叔丁胺(47.1mmol),室温反应2h。加入1.8g硼氢化钠(47.6mmol),反应1h。用二氯甲烷萃取2-3次,合并有机相后用饱和食盐水洗,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,石油醚/乙酸乙酯(10:1)为淋洗剂,得产物苄基叔丁胺6.2g,产率为80.7%。m/z164(m++1)。1hnmr(cdcl3,400mhz)1.15(s,9h),1.95(brs,1h),3.75(s,2h),7.27(m,3h),7.35(m,2h).
(2)4-(4-溴乙酰基)苯基丁酸甲酯
以与实施例1中步骤(1)—(2)相同的方法合成4-(4-溴乙酰基)苯基丁酸甲酯。m/z298,300.1hnmr(cdcl3,400mhz)1.97(m,2h),2.39(t,2h,j=7.6hz),2.72(t,2h,j=8.0hz),3.66(s,3h),4.43(s,2h),7.28(d,2h,j=8.0hz),7.91(d,2h,j=8.0hz).
(3)4-(4-(2-苄基叔丁胺基)乙酰基)苯基丁酸甲酯
将203mg苄基叔丁胺(1.24mmol)和337mg4-(4-溴乙酰基)苯基丁酸甲酯(1.13mmol)溶解于3ml乙腈中,加入314mg无水碳酸钾(2.27mmol),室温反应过夜。加入水并搅拌后,用二氯甲烷萃取2-3次,合并有机相后用饱和食盐水洗,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,丙酮/乙酸乙酯(10:1)为淋洗剂,得产物4-(4-(2-苄基叔丁胺基)乙酰基)苯基丁酸甲酯(淡黄色油状液体)187mg,产率为43.5%。m/z382(m++1)。1hnmr(cdcl3,400mhz)1.42(s,9h),1.90(m,2h),2.32(t,2h,j=7.6hz),2.65(t,2h,j=7.6hz),3.02(m,4h),3.68(s,3h),7.16-7.20(m,5h),7.39(d,2h,j=7.6hz),8.19(d,2h,j=8.0hz).
(4)4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸甲酯
将74mg4-(4-(2-苄基叔丁胺基)乙酰基)苯基丁酸甲酯(0.2mmol)溶解于1.5ml甲醇中,加入11mg硼氢化钠(0.3mmol),室温下反应1h。加入稀盐酸将ph值调节至4-5,用二氯甲烷萃取2-3次,饱和食盐水洗,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,二氯甲烷/丙酮(5:1)为淋洗剂,得产物4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸甲酯(无色油状液体)41mg,产率为55.1%。m/z384(m++1)。1hnmr(cdcl3,400mhz)1.47(s,9h),1.93(m,2h),2.39(t,2h,j=7.6hz),2.70(t,2h,j=7.6hz),3.08(m,2h),3.70(s,3h),3.78(s,2h),5.05(m,1h),7.16(d,2h,j=7.6hz),7.27-7.32(m,5h),7.41(d,2h,j=8.0hz).
(5)4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸
将45mg4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸甲酯(0.12mmol)溶解于0.5ml甲醇中,加入氢氧化钠溶液(含naoh0.3mmol),室温反应过夜。将反应液用稀盐酸溶液调节ph至5-6,二氯甲烷萃取2-3次,饱和食盐水洗,无水硫酸钠干燥,过滤后浓缩,过硅胶柱纯化,二氯甲烷/乙酸乙酯(5:1)为淋洗剂,得产物4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸(白色固体)39mg,产率89.9%。m/z370(m++1)。1hnmr(cdcl3,400mhz)1.45(s,9h),1.84(m,2h),2.27(t,2h,j=8.0hz),2.60(t,2h,j=7.6hz),3.02(m,2h),3.72(s,2h),5.11(m,1h),7.2-7.24(m,5h),7.30(d,2h,j=7.6hz),7.38(d,2h,j=7.6hz),
(6)4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba)
将37mg4-(4-(2-苄基叔丁胺基)1-羟乙基)苯基丁酸(0.1mmol)和适量钯碳加入到盛有3ml甲醇的反应瓶中,置换空气后,室温反应2h。过滤后浓缩,过硅胶柱纯化,得产物4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba,白色固体)39mg,产率90%。m/z280(m++1)。1hnmr(cdcl3,400mhz)1.42(s,9h),1.92(m,2h),2.32(t,2h,j=7.6hz),2.68(t,2h,j=7.6hz),3.05(t,1h,j=11.4hz),3.17(d,1h,j=11.2hz),5.03(m,1h),7.20(d,2h,j=8.0hz),7.34(d,2h,j=8.0hz).
实施例3化合物4-[4-(2-异丙基胺基-1-羟乙基]苯基丁酸的制备
以4-(4-乙酰基)苯基丁酸甲酯和异丙基苄胺为原料,以与实例2相同的合成方法得到白色固体4-[4-(2-异丙基胺基-1-羟乙基]苯基丁酸。m/z266(m++1)。
实施例4化合物4-[4-(2-环丙基胺基-1-羟乙基]苯基丁酸的制备
以4-(4-乙酰基)苯基丁酸甲酯和环丙基苄胺为原料,以与实例2相同的合成方法得到白色固体4-[4-(2-环丙基胺基-1-羟乙基]苯基丁酸。m/z264(m++1)。
实施例5化合物4-[2-羟基-4-(2-叔丁基氨基-1-羟乙基]苯基丁酸
以2-羟基4-(4-乙酰基)苯基丁酸甲酯和叔丁基苄胺为原料,以与实例2相同的合成方法得到白色固体4-[2-羟基-4-(2-叔丁基氨基-1-羟乙基]苯基丁酸。m/z296(m++1)。
实施例6化合物4-[2-羟基-4-(2-异丙基氨基-1-羟乙基]苯基丁酸
以2-羟基4-(4-乙酰基)苯基丁酸甲酯和异丙基苄胺为原料,以与实例2相同的合成方法得到灰白色固体4-[2-羟基-4-(2-异丙基氨基-1-羟乙基]苯基丁酸。m/z282(m++1)。
实施例7化合物4-[2-羟基-4-(2-环丙基氨基-1-羟乙基]苯基丁酸
以2-羟基4-(4-乙酰基)苯基丁酸甲酯和环丙基苄胺为原料,以与实例2相同的合成方法得到白色固体4-[2-羟基-4-(2-环丙基氨基-1-羟乙基]苯基丁酸。m/z280(m++1)。
实施例84-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸-牛血清白蛋白(tbpba-bsa)偶联物的制备
将74mg4-(4-(2-叔丁胺基)1-羟乙基)苯基丁酸(tbpba,0.2mmol)溶于5-10ml无水乙醇中,加入0.2-0.25mmoln-羟基琥珀酰亚胺(nhs)和0.2-0.25mmol1-[3-(二甲氨基)丙基]-3乙基碳二亚胺碳酸盐(edc),室温下反应3-5h。将上述反应液缓慢加入到5-10ml含有5-10mg/ml牛血清白蛋白(bsa)的磷酸缓冲溶液中,室温反应过夜。将上述反应液用磷酸缓冲溶液透析3-6次,冷冻干燥即可得到tbpba-bsa偶联物冻干粉。
实施例9tbpba多克隆抗体的制备
用tbpba-bsa作为免疫原免疫体重约2kg的健康大白兔。首次免疫时将0.25mg免疫原与等量弗氏完全佐剂混合并充分乳化,背部皮下多点注射。两周后用同样剂量免疫原与等量弗氏不完全佐剂进行乳化并进行加强免疫,每两周加强免疫一次,共加强三次。最后一次免疫10天后对大白兔进行颈静脉采血,放在4℃环境下静置30min,再用硫酸铵多级沉淀法进行纯化,即可得到tbpba多克隆抗体。
实施例10tbpba单克隆抗体的制备
(1)动物免疫
将tbpba-bsa注入到balb/c小鼠体内,免疫剂量为75pg/只,使其产生抗体。
(2)细胞融合和克隆
取免疫balb/c小鼠脾细胞,按5:1(数量配比)比例与sp2/0骨髓瘤细胞融合,采用间接竞争elisa测定细胞上清液,筛选阳性孔。利用有限稀释法对阳性孔进行克隆化,直到筛选得到稳定分泌tbpba单克隆抗体的杂交瘤细胞株。
(3)细胞冻存和复苏
将tbpba单克隆抗体杂交瘤细胞株用冻存液制成1×106个/ml的细胞悬液,在液氮中长期保存。复苏时取出冻存管,立即放入37℃水浴中速融,离心去除冻存液后,移入培养瓶内培养。
(4)单克隆抗体的制备与纯化
增量培养法:将tbpba单克隆抗体杂交瘤细胞株置于细胞培养基中,在37℃条件下进行培养,用辛酸—饱和硫酸铵分级沉淀法纯化,得到tbpba单克隆抗体,-20℃保存。
所述细胞培养基为向rpmi-1640培养基中添加小牛血清和碳酸氢钠,使小牛血清在细胞培养基中的终浓度为20%,使碳酸氢钠在细胞培养基中的终浓度为0.2%;所述细胞培养基的ph为7.4。
上述单克隆抗体还可以采取以下方法制备:将balb/c小鼠腹腔注入灭菌石蜡油0.4ml/只,7天后腹腔注射tbpba单克隆抗体杂交瘤细胞株5×105个/只,7天后采集腹水。用辛酸—饱和硫酸铵分级沉淀法纯化,纯化后的腹水-20℃保存。
实施例11胶体金标记tbpba单克隆抗体的制备
(1)胶体金的制备
在250ml圆底烧瓶中加入氯金酸溶液(0.1%,1ml)和纯净水(99ml),加热至沸腾并不断搅拌。沸腾约2min后迅速加入柠檬酸三钠溶液(1%,2ml),继续搅拌沸腾15min,冷却后用纯净水定容至100ml,用0.2um微滤膜过滤后4℃保存。
(2)金标抗体的制备
取10ml胶体金溶液,加入k2co3缓冲溶液将ph值调节为8.2,室温下加入tbpba单克隆抗体,使抗体终浓度为0.005mg/ml,继续搅拌30min,加入10%bsa溶液至终浓度为1%,再搅拌30min。4000rpm离心30min,弃去上清液,沉淀用缓冲液(含20%蔗糖、1.0%bsa、0.1%peg、0.1%tween20、0.1%nan3的0.01mol/l的pbs溶液)重悬。
实施例12酶标记tbpba-bsa偶联物的制备
将8mg辣根过氧化物酶溶解于2ml纯净水中,加入0.4ml现配制的naio4溶液(l00mmol/l),室温搅拌反应20min;用1mmol/l醋酸盐缓冲液于4℃透析过夜,然后加入2.0ml含有16mgtbpba-bsa的磷酸盐缓冲液(ph=8.6,5mol/l),室温搅拌反应4h;再加入0.1ml现配制的nabh4水溶液(lmol/l),在4℃反应4小时,得到辣根过氧化物酶标记的tbpba-bsa偶联物。
实施例13荧光标记tbpba多克隆抗体的制备
将tbpba多克隆抗体溶于na2co3缓冲溶液(ph=9.0,0.1mol/l),使其浓度为0.01mg/ml,再将异硫氰酸荧光素(fitc)溶于dmso,使其浓度为1mg/ml。按抗体:荧光素=1mg:0.15mg的比例将fitc缓慢加入到抗体溶液中,于暗处4℃反应8h。加入nh4cl溶液(5mol/l)至终浓度为50mmol/l,4℃终止反应2h。将上述反应液用pbs缓冲溶液透析3-6次至溶液澄清,得到fitc标记tbpba多克隆抗体。
- 还没有人留言评论。精彩留言会获得点赞!
- 包含与β-3-肾上腺素能受体激动剂组合的去氨加压素的方法和组合物的制作方法
- 具有毒蕈碱受体拮抗体和β2肾上腺素能受体激动剂两种活性的2-氨基-1-羟乙基-8-羟基 ...的制作方法
- 靶向于肌动蛋白结合蛋白Transgelin-2的化合物及其新用图
- 一种α-2肾上腺素受体和σ受体配体的组合物的制作方法
- 天然植物皂苷功效组分的筛选方法及用图
- 通过玻璃体内和前房内途径用于治疗眼内压和眼部疾病的α-2肾上腺素能激动剂的制作方法
- 用于治疗组织创伤的α-肾上腺素能激动剂的制作方法
- 具有β2肾上腺素能受体激动剂和M3毒蕈碱受体拮抗剂两种活性的2-氨基-1-羟乙基-8-羟 ...的制作方法
- 具有毒蕈碱受体拮抗剂和β2肾上腺素能受体激动剂活性的化合物的制作方法
- 具有毒蕈碱受体拮抗剂和β2肾上腺素能受体激动剂活性的化合物的制作方法