用于选择磷酸酶选择性抑制剂和非选择性磷酸酶抑制剂的方法与流程
本发明公开了一种发现磷酸酶的选择性抑制剂的方法。
发明背景
蛋白的可逆磷酸化事实上控制细胞和生物体功能的所有方面,允许细胞通过激酶和磷酸酶的拮抗作用适应突然的变化。因此,靶向磷酸化提供广泛的治疗切入点,并且激酶已经成为当今对超过3000种已批准的以及实验的药物的药学研究中最常见的药物靶点。然而,虽然靶向磷酸酶原则上应与激酶一样具有吸引力,但磷酸酶的治疗潜力被忽视。
大部分蛋白磷酸化发生在丝氨酸和苏氨酸上,并且选择性的丝氨酸/苏氨酸去磷酸化通过几百种不同的二聚体或三聚体全酶来实现,这些全酶由仅仅几种的催化亚基之一和几百种不同的调节亚基之一组合装配而成(heroes等人,febsjournal,280,584-595,2012)。
出于多种原因,通常已经认为磷酸酶是无成药性的。例如,多种磷酸酶是低聚的。因此,抑制全酶如pp1c的催化部分导致对共享相同催化亚基的多种(例如几百种)全磷酸酶产生抑制,并且可能产生毒性。因为选择性是药物开发的一个重要特性,催化磷酸酶的多功能性已经导致它们被认为是无成药性的。
其次,磷酸酶的调节亚基是固有无序的(bollen等人,2010;choy等人,2012a)并且因此难以表达且不稳定。在大约200种哺乳动物pp1(蛋白磷酸酶1)全磷酸酶中,仅有八种已经得到了结晶。因此缺乏全磷酸酶的结构信息,这意味着基于结构的药物设计不易于应用于这类酶。迄今,可获得结构信息的全磷酸酶仅包含来自调节亚基的短肽(少于大约100个氨基酸)(ragusa:2010hd;;choy等人,2014)并且这些较小的结构使得难以指导药物发现。
此外,基于人工底物的底物水解的酶试验将主要导致发现一般非选择性的催化抑制剂。
因此,需要开发一种一般策略和试验以选择性抑制磷酸酶,并且能够鉴定特定抑制剂,并由此鉴定具有治疗用途的药物。
技术实现要素:
近来,已经展示了选择性抑制丝氨酸/苏氨酸磷酸酶的可行性。发现公开于wo2014108520(medicalresearchcouncil)的一些胍那苄(guanabenz)(tsaytler等人,science,332,91-94,2011;tsaytler和bertolotti,febsjournal,280,766-770,2012)及其衍生物选择性抑制ppp1r15a/gadd34(“r15a”)——一种丝氨酸/苏氨酸蛋白磷酸酶1的应激诱导型调节亚基,并且提出将其用于治疗与蛋白错误折叠应激相关联的疾病。同样地,胍那苄衍生物sephin1(das等人,2015)已经显示选择性抑制ppp1r15a/gadd34。因此已经提出将sephin1作为与蛋白错误折叠应激相关联的疾病的治疗。其它衍生物已经公开于例如wo2016001389a1、wo2016001390a1和wo2014138298a1中,并且据报道具有相似活性。然而,需要改进的选择性试验以确认这些分子是否对r15a抑制是选择性的。
已经偶然鉴定了磷酸酶的其它抑制剂。例如,环孢菌素a和fk506分别结合亲免蛋白、亲环蛋白和fkbp12,并且所得复合物结合钙调磷酸酶——一种异源二聚磷酸酶,包含催化亚基ppp3和两种调节亚基ppp3r1或ppp3r2之一。环孢菌素a是一种磷酸酶抑制剂,但是它通过间接途径完成抑制:环孢菌素不以钙调磷酸酶全磷酸酶的调节亚基为靶标。
已经报道了一种别构wip1磷酸酶(gilmartin等人,2014)。在酶试验中发现了这种抑制剂。迄今,无试验可用于鉴定选择性且别构的磷酸酶抑制剂。
概括地说,虽然先前已经描述了磷酸酶抑制剂,重要的是注意到它们是偶然间被发现。无可用的方法用于普适地鉴定选择性磷酸酶抑制剂。
一种用于鉴定选择性的且别构的磷酸酶抑制剂的方法包括靶向它们的调节亚基。已经偶然鉴定了r15a抑制剂并且提供了以下概念验证:丝氨酸-苏氨酸磷酸酶可通过靶向调节亚基而被选择性抑制(das等人,2015;tsaytler等人,2011)。原则上,相同的范例可用于选择性抑制多种其它pp1全磷酸酶中的一种。然而,磷酸酶的固有无序调节亚基的选择性抑制剂的理性发现是一个未解决的挑战。
本发明提供一种试验方法,用于测定全酶如磷酸酶(即,全磷酸酶)的选择性结合。合适的全磷酸酶包括磷蛋白磷酸酶(ppp)超家族的成员,包括ser/thr蛋白磷酸酶1-7(pp1-7),如例如(heroes等人,febsjournal,280,584-595,2012)所综述。ppp1r15a(也称为gadd34并且本文称为“r15a”)和ppp1r15b(也称为crep并且本文称为“r15b”)是pp1家族的全磷酸酶。
因此,第一方面提供了用于筛选测试化合物以测定该化合物是否选择性地或非选择性地结合全磷酸酶的方法,所述方法包括:
i)提供第一全磷酸酶,其中将所述全磷酸酶捕集/固定;
ii)测试受试化合物结合至所述第一全磷酸酶的能力;
iii)提供第二全磷酸酶,其中将所述第二全磷酸酶捕集/固定;iv)测试相同的受试化合物结合至所述第二全磷酸酶的能力;
v)比较所述受试化合物对所述第一全磷酸酶的结合与所述受试化合物对所述第二磷酸酶的结合
其中选择性结合全磷酸酶的受试化合物将结合至所述第一全磷酸酶而非所述第二全磷酸酶;或者将结合至所述第二全磷酸酶而非所述第一全磷酸酶;或者其中非选择性结合全磷酸酶的化合物将结合至所述第一全磷酸酶和所述第二全磷酸酶这二者。
合适地,依次测试受试化合物结合第一全磷酸酶的能力和相同受试化合物结合第二全磷酸酶的能力,例如使用如本文详述使用单独的芯片、小珠或反应混合物进行测试,分别测定受试化合物对各全磷酸酶的结合亲和力用于比较。
在一个实施方案中,全磷酸酶,即,上述第一和/或上述第二全磷酸酶,是一种低聚酶,包含一个催化亚基和一个或多个调节亚基。存在超过400种磷酸酶,它们实际上调控细胞功能的所有方面,这综述于例如heroes等人(2012)。存在超过200种调节亚基,它们共享一些催化亚基。磷酸酶的调节亚基是固有无序的,即,天然非结构化的(bollen等人,2010;choy等人,2012a),并且仅在结合至它们的催化亚基时趋于变得结构化。此前尚未提供用于鉴定此类天然非结构化分子的抑制剂的方法,因为开发此类方法通常是成问题的。当单独使用时(标记的或未标记的),天然非结构化的磷酸酶的调节亚基一般不稳定或沉淀。因此,单独使用调节亚基从未使得相关生物活性的化合物可被鉴定。
本发明方法使包含调节亚基的复合物(它们是天然非结构化的蛋白)当结合至它们的相互作用伴侣时,能够产生并用于筛选,从而允许新药靶向这类待鉴定的蛋白。
合适地,通过任何可用的方法分离并纯化全磷酸酶。全磷酸酶能够例如在一个合适的表达系统中被表达为亚基,例如细菌、昆虫或哺乳动物细胞表达系统。可通过任何合适的方法例如色谱法纯化亚基。
因为,如上所述全磷酸酶的调节亚基是固有无序的,可能需要用于表达和纯化的特定方法。因此,在一个实施方案中,可标记调节亚基以促进表达和纯化。合适地,调节亚基可标记有两个标签。合适的标签将是本领域内的技术人员熟悉的,并且包括例如亲和标签如麦芽糖结合蛋白(maltosebindingprotein)-标签、组氨酸-标签等。在一个具体实施方案中,为了纯化r15a(和/或r15b),如本文所述mbp-标签可与组氨酸-标签组合使用。有利的是,mbp-标签(麦芽糖结合蛋白(maltosebindingprotein))增加在大肠杆菌中表达的重组蛋白的溶解度。组氨酸-标签也是一种亲和标签。mbp-催化亚基-组氨酸标记的蛋白因此可在2步过程中进行纯化,产生纯的且相对稳定的蛋白,如本文对于mbp-r15a-his的描述。在另一个实施方案中,也可表达催化亚基以包括一个标签如亲和标签。
因此,在一个实施方案中,可通过装配亚基重构全磷酸酶。另选地,不同的亚基可在合适的表达系统(例如细菌、昆虫或哺乳动物细胞)中共表达,并且全酶可通过任何合适的方法(例如色谱法)纯化。
在另一个实施方案中,全磷酸酶可为内源性蛋白,其通过任何合适的方法如色谱法从细胞提取物中纯化。
在一个实施方案的任何方面或本发明的实施方案中,可提供全长亚基的截短形式的调节亚基。合适地,截短形式将保留结合至催化亚基的能力并保留必需的催化功能。例如并且如本文所述,合适的截短形式的r15a和/或r15b保留结合至催化亚基pp1c的能力并且保留它结合eif2α并将其脱磷酸的催化活性。在一个实施方案中,在调节亚基是r15a的情况下,提供它包含氨基酸325-636的截短的片段。在一个实施方案中,在调节亚基是r15b的情况下,提供它包含氨基酸340-698的截短的片段。r15a和r15b的氨基酸序列在图16中给出。有利的是,使用较短的片段能够解决使用全长蛋白时观察到的低蛋白产率和低稳定性问题。然而,本文所述的片段,如r15a和r15b所例示,大于在之前重构的pp1c磷酸酶中的那些,它们仅包含小于100个氨基酸的调节亚基片段(chen等人,2015;choy等人,2015)。在另一个实施方案中,催化亚基可为天然蛋白的截短形式。合适地,此种截短形式将保留它结合调节亚基的能力以及它的催化活性。
在一个实施方案中,对受试化合物结合至上述第一全磷酸酶、上述第二全磷酸酶或上述催化亚基的能力的上述测试通过使用表面等离振子共振(spr)方法测定结合亲和力来完成。
在另一个实施方案中,将全磷酸酶固定在一个表面上。合适的表面是允许进行随后的结合分析的任何表面。例如,上述表面可为芯片如spr(表面等离振子共振(surfaceplasmonresonance))传感器芯片,其适用于spr测量。在其它实施方案中,该表面可为小珠或树脂或例如微板的孔。合适地,通过在表面上的固定重构全磷酸酶。
在另一个实施方案中,使用亲和捕获方法或任何相关的捕获方法来固定全磷酸酶。合适的亲和捕获方法包括使用生物素:链亲和素或其它类似的结合对——例如组氨酸-镍、gst谷胱甘肽等。
在一个实施方案中,全酶的催化亚基例如pp1c首先被固定在芯片上,随后它结合至调节亚基。这如示意图33所示,其中展示了催化亚基a或b。
在一个实施方案中,全磷酸酶可使用亲和标记的亚基在小珠上重构。例如,his-pp1和/或mbp-r15a-his可在小珠上重构。合适的小珠包括直链淀粉小珠。合适地,生物素酰化的蛋白/肽可使用体内生物素酰化在昆虫细胞内生成。在一个实施方案中,在调节亚基和催化亚基上使用的标签可不同。
在另一个实施方案中,根据本发明的任何方面或实施方案对受试化合物对全磷酸酶(或催化亚基)结合的分析在溶液中进行。
在一个实施方案中,根据本发明实施方案的任何方面用于筛选受试化合物的方法还包括一个附加步骤:
vi)提供上述第一和第二全磷酸酶的催化亚基,其中将所述催化亚基捕集/固定;
vii)测试上述候选磷酸酶抑制剂分子结合至所述催化亚基的能力。
受试化合物的结合特性与对全酶的催化结构域的结合的比较可为表征结合分子的选择性或选择性的缺失的重要步骤。在一个实施方案中,所关注的候选物是如下化合物:那些不结合至和/或抑制催化亚基,但是对包含与一个特定调节亚基接合的催化亚基的全磷酸酶具有选择性的化合物。
在包括附加步骤vi)和vii)的试验的上下文中,并且参考图33,结合至a并且是候选的选择性a抑制剂(或活化剂)的化合物将优先结合至芯片a而非b或c。结合至b并且是候选的选择性b抑制剂(或活化剂)的化合物将优先结合芯片b而非a或c。非选择性的结合剂或抑制剂能够结合超过一个芯片。
在另一个实施方案中,上述方法还包括测定选择性或非选择性抑制剂是否单独对催化亚基具有效应(例如在酶试验中),或者是否其中抑制剂对催化亚基无效应,所述抑制剂是调节亚基(即,a或b或以上二者)的抑制剂或活化剂。
在一个实施方案中,用于筛选受试化合物的方法还包括进行验证性分析以在其它试验中测试特定的抑制/活化活性。例如,一种测试抑制剂或活化剂可在酶试验或基于细胞的试验中进行验证以展示靶结合。用于特定全酶活性的合适试验将取决于其中涉及它们的特定细胞途径。技术人员将在关于全酶作为底物与其相互作用的分子的知识中注意到任何具体全酶的合适试验。
可通过在敲除或敲减靶向磷酸酶的细胞中重复相同试验来验证靶结合。敲除细胞可通过常规方法(例如基因敲除或crispr/cas敲除)产生,并且基因沉默可通过任何合适的方法诸如sirna来实现。在不存在靶的情况下,选择性化合物将在细胞中无效应。
受试化合物合适的进一步验证可通过在生物试验中进行的验证。可使用任何揭示靶的生物活性的合适的试验。例如,如果该靶涉及信号转导,信号转导途径的诱导可通过任何方法(例如基于抗体的方法、流式细胞术等)进行监控。磷酸酶抑制剂或活化剂将改变信号转导途径。任何其它生物试验可用于监控靶的抑制或活化。例如如果靶活性影响细胞生长,该试验可为生长试验,它可为凋亡试验(如果靶活性对细胞存活是重要的),它可为免于化学物质的保护(如果该途径涉及免于化学物质的保护)等。
合适地,选择性磷酸酶抑制剂将增加或延长其底物的磷酸化。在一个实施方案中,选择性抑制剂是在当具有低于10μm,甚至更优选地低于5μm,甚至更优选地低于1μm,以及甚至更优选地低于0.5μm的浓度时,具有结合亲和力或生物活性的抑制剂。
根据本发明的试验的一个实例如图33所示。
在该实例中,所述方法包括以下步骤(图33):
1.在该实例中分离并纯化全磷酸酶(称为a)。
这可通过任何可用的方法来完成,或利用内源性蛋白,或通过在任何合适系统(细菌、昆虫或哺乳动物细胞等)中表达亚基,纯化亚基并重构全磷酸酶。在该实例中,磷酸酶pp1c的催化亚基在体内被生物素酰化,用于在链亲和素spr芯片上进行高亲和力捕集。
2.在芯片上固定全磷酸酶
在该实例中,pp1c的催化亚基首先固定在芯片上,随后将其结合至调节亚基(在该实例中的a或b)。
3.筛选结合至全磷酸酶a(芯片a)的分子/受试化合物
4.在该实例(芯片b)中用称为b的不同的磷酸酶重复步骤1-3
5.利用催化亚基重复步骤1-2以生成芯片c
6.通过测试受试化合物对芯片a、b和c的结合来表征它们的
选择性。
选择性a抑制剂(或活化剂)将优先结合至芯片a而非b或c。选择性b抑制剂(或活化剂)将优先结合至芯片b而非a或c。非选择性抑制剂能够结合至超过一个芯片。
通过这种方法鉴定的受试化合物可测试其单独对催化亚基的活性。调节亚基的选择性结合剂或抑制剂或活化剂对催化亚基无效应。
通过这种方法鉴定的化合物在其它试验(包括酶试验或基于细胞的试验)中验证以展示靶结合。选择性磷酸酶抑制剂将增加或延长其底物的磷酸化。为了验证靶结合,在敲除或敲减靶向磷酸酶的细胞中重复相同试验。在不存在靶的情况下,选择性化合物将在细胞中无效应。
可在生物试验中验证所述化合物。揭示特定靶活性的合适的试验将是本领域技术人员熟悉的方法。
根据本发明的另一方面,提供了一系列试验方法,用于鉴定、筛选、评估、或表征能够抑制ppp1r15b(“r15b”)的候选多肽、多核苷酸、抗体、肽或小分子化合物。
在本发明的其它方面,描述了抑制剂化合物。
虽然之前已经描述了ppp1r15a抑制剂,但尚未报道不同丝氨酸/苏氨酸磷酸酶的选择性抑制剂。因此不知道是否可选择性抑制另一种磷酸酶。申请人研究了是否可能选择性抑制ppp1r15b以及此类选择性抑制是否可为有益的。与看起来正常的ppp1r15a敲除小鼠相反,缺失ppp1r15b的小鼠活不过产后第一天(harding等人,proc.natl.acad.sci.u.s.a.,106,1832-1837,2009)。因此,虽然预测ppp1r15a抑制是安全的,但是预测ppp1r15b抑制是有害的。然而,发明人已经令人惊讶地发现可选择性抑制ppp1r15b并且此类抑制产生治疗有益效果。
ppp1r15b抑制取代ppp1r15a抑制可为有利的,因为预测可经由ppp1r15a抑制剂治疗的治疗适应症的数目受限于其中表达ppp1r15a的疾病以及其中ppp1r15a参与疾病作用方式的疾病。相比之下,ppp1r15b是组成型表达的,并且因此可较广泛地应用于目标疾病。如本文所述,ppp1r15b抑制可用于治疗亨廷顿氏病(huntington’sdisease)。用于本发明的ppp1r15b选择性抑制剂可为蛋白或多肽、多核苷酸、抗体、肽或小分子化合物。另选地,ppp1r15b可通过基因编辑失活。
在一个方面,提供了一种ppp1r115b选择性抑制剂,(e)-2-(2,3-二氯亚苄基)肼-1-甲脒(本文也称为“tst3”):
根据本发明的另一方面,提供了一种用于治疗的ppp1r15b选择性抑制剂。
根据本发明的另一方面,提供了治疗患有通过抑制ppp1r15b而减轻的疾病状态的受试者的方法,其中所述方法包括向受试者施用治疗有效量的ppp1r15b选择性抑制剂。
根据本发明的另一方面,提供了预防受试者通过抑制ppp1r15b而减轻的疾病状态的方法,其中所述方法包括向受试者施用治疗有效量的ppp1r15b选择性抑制剂。
根据本发明的另一方面,提供了用于治疗或预防通过抑制ppp1r15b而减轻的疾病状态的ppp1r15b选择性抑制剂。
根据本发明的另一方面,提供了ppp1r15b选择性抑制剂在制造用于治疗或预防通过抑制ppp1r15b而减轻的疾病状态的药物中的应用。在一个实施方案中,通过抑制ppp1r15b而减轻的疾病状态是与错误折叠蛋白的积聚相关联的障碍或蛋白内稳态障碍。
在另一个实施方案中,上述疾病是亨廷顿氏病(huntington’sdisease)、帕金森氏病(parkinson’sdisease)、tau蛋白病(tauopathy)、蛋白质运输疾病或髓鞘质障碍。
在另一个实施方案中,上述疾病为任何多聚谷氨酰胺障碍。
在另一个实施方案中,上述疾病为远端型遗传性运动神经病,其具有在分子伴侣hsj1中的突变。
根据本发明的另一方面,提供了使用一种化合物或其药学上可接受的盐作为ppp1r15b的选择性抑制剂的应用,其中所述化合物选自以下结构:
附图简述
现在将仅以举例的方式描述本发明的某些实施方案,参照下图,其中:
附图
图1示出实施例1的r15b抑制剂对r15b-pp1选择性结合超过r15a-pp1。
图2示出实施例1的选择性r15b抑制剂在不存在应激的情况下诱导细胞中elf2α的瞬时磷酸化以及诱导细胞中的r15a表达。
图3示出实施例1的选择性r15b抑制剂保护细胞免于应激。
图4示出应激后选择性r15b抑制剂对elf2α磷酸化的效应。实施例1的化合物延长应激后的eif2α磷酸化。
图5示出实施例1的化合物的组织分布,其表现出广泛的组织分布。
图6示出用无毒性的实施例1的化合物(10mg/kg)治疗小鼠。
图7示出用不引起胍那苄的副作用的实施例1的化合物(10mg/kg)治疗小鼠。
图8示出在用实施例1的化合物治疗后,在哺乳动物中诱导r15a。
图9示出实施例1的r15b抑制剂对预防哺乳动物疾病的效果。在图9使用的示例是亨廷顿氏病(huntington’sdisease),其使用小鼠模型hd82gln(schilling等人,hum.mol.genet.,8,387-407,1999)。wt:野生型小鼠。tg:hd82gln。
图10以红色(杆状)示出来自培养的背根神经节(dorsalrootganglia,drg)的髓鞘质节间体并以蓝色(球‘团’状)示出用溶媒或实施例1的化合物治疗的指示基因型的核。pmp22-突变小鼠中的髓鞘质节间体较短。用实施例1的化合物治疗增加突变drg中髓鞘质节间体的长度,这表明它改善髓鞘形成。
图11示出在用实施例1的化合物治疗后肥胖小鼠db/db动物(每种条件n=5)中的血糖水平。
图12示出instantblue(考马斯蓝)-染色的凝胶,显示重组蛋白mbp-r15a325-636-his、mbp-r15b340-698-his。
图13a.示出说明用于测定生物素酰化的胍那苄(bio-gbz)对r15a和r15b的结合亲和力的spr方法的草图。b.结合至固定在spr传感芯片表面的bio-gbz的r15a和r15b的spr传感图。r15a/b浓度=0.0244-12.5μm。
图14示出来自图13b的响应单位对蛋白浓度作图以测定稳态结合常数(kd)。r15a的结合(○,蓝色)和r15b的结合(▲,品红)。r15a对bio-gbz的kd是11μm并且r15b对bio-gbz的kd是123μm。
图15上面板:instantblue-染色的凝胶显示重组bio-pp1(部分纯化)、mbp-r15a325-636-his和mbp-r15b340-698-his(输入)。bap-pp1c,在中和亲和素微珠上纯化,结合r15a和r15b(结合)。bio-pp1c=生物素酰化的pp1。下面板:示出生物素酰化pp1c的免疫印迹。
图16人r15a和r15b的序列匹配。虽然功能上相关,r15a和r15b不同且仅共有23%同一性。
图17示出描述在链亲和素(sa)-spr芯片上的r15全磷酸酶的重构的草图。
图18示出胍那苄结合至固定在spr传感器芯片上的r15a-pp1c全磷酸酶的spr传感图。
图19示出胍那苄结合至固定在spr传感器芯片上的r15b-pp1c全磷酸酶的spr传感图。
图20示出胍那苄结合至固定在spr传感器芯片上的pp1c全磷酸酶的spr传感图。
图21示出gbz对固定在本发明的spr芯片上的r15a-pp1c、r15b-pp1c和pp1c的稳态亲和力。gbz结合至固定在链亲和素传感芯片表面的r15a/pp1c(○)和r15b/pp1c(▲)。将响应单位对化合物浓度作图以测定稳态结合常数(kd)。gbz对r15a的kd是0.1221μm并且未检测到gbz对r15b的结合。
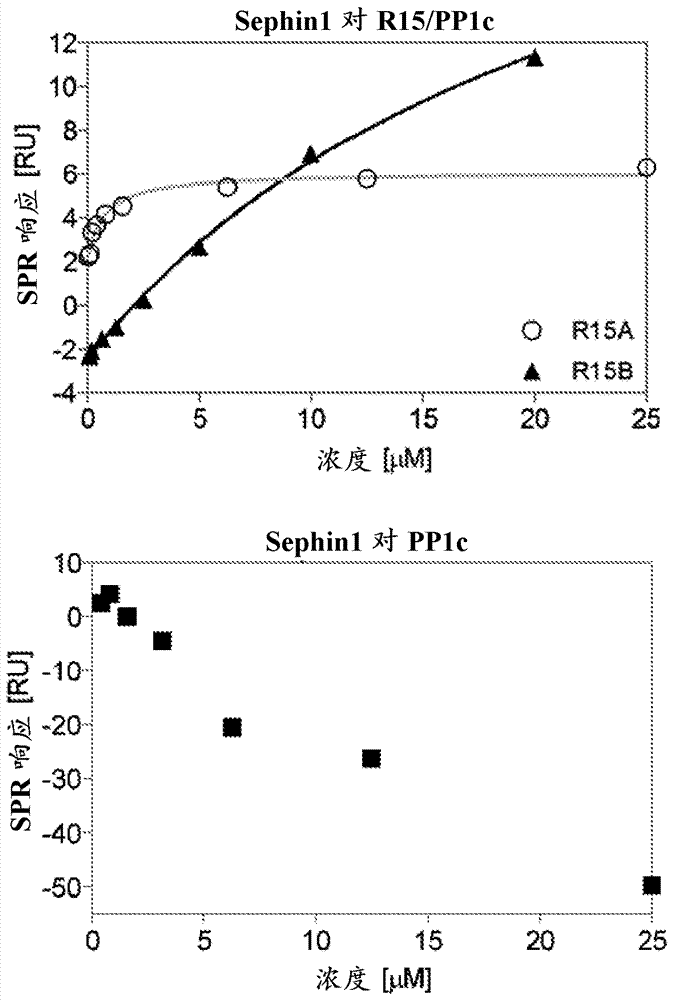
图22示出sephin1对固定在本发明的spr芯片上的r15a-pp1c、r15b-pp1c和pp1c的稳态亲和力。sephin1对r15a的kd是0.786μm并且对r15b的kd是23μm。
图23示出salubrinal对固定在本发明的spr芯片上的r15a-pp1c、r15b-pp1c和pp1c的稳态亲和力。
图24示出tst3对固定在本发明的spr芯片上的r15a-pp1c、r15b-pp1c和pp1c的稳态亲和力。
图25示出不同的化合物对固定在本发明的spr芯片上的r15a-pp1c、r15b-pp1c和pp1c的稳态亲和力。
图表示出gbz、sephin1、sal003和tst3以及它们各自对eif2α全磷酸酶或单独的pp1c的亲和力(kd)。(--):未结合。在各面板中显示至少3个独立实验的代表性结果。数据是平均数±sd,n=3。kd值使用稳态亲和力模型通过biacoret200分析软件(biaevaluation1.0版)计算。
图26与花萼海绵诱癌素a相反,pp1、tst3、类gbz(likegbz)和sephin1的催化抑制剂不抑制pp1c。
图27tst3通过选择性抑制r15b来瞬时诱导eif2α磷酸化。以10μm的tst3处理的海拉细胞溶解产物中的所标明的蛋白的免疫印迹。
图28由于tst3选择性抑制r15b而非r15a,tst3瞬时降低蛋白合成。来自以10μm的tst3处理所标明时间的海拉细胞溶解产物的以35s-甲硫氨酸放射性标记的新合成蛋白的放射自显影图。下面板:instantblue染色。
图29在gbz的存在下,tst3瞬时抑制蛋白合成。来自以10μm的tst3+/-gbz处理所标明时间的海拉细胞溶解产物的以35s-甲硫氨酸放射性标记的新合成蛋白的放射自显影图。下面板:instantblue染色。
图30在gbz的存在下,tst3瞬时诱导eif2α磷酸化。以10μm的tst3+gbz处理的海拉细胞溶解产物中的所标明的蛋白的免疫印迹。
图31tst3活性在r15b敲除细胞中被废除。
以10μm的tst3处理所标明时间的r15amut/mut或r15bmut/mutmefs溶解产物中的所标明蛋白的免疫印迹。
图32tst3对r15b-/-细胞中的蛋白合成无影响。上面板:来自以10μm的tst3处理所标明时间的r15amut/mut或r15bmut/mutmefs溶解产物的以35s-甲硫氨酸放射性标记的新合成蛋白的放射自显影图。
发明详述
eif2α的α亚基的磷酸化是抗多种应激的第一道防线,并且因此是两个部分重叠的信号途径的中心组分:未折叠蛋白反应(unfoldedproteinresponse,upr)和整合应激反应(integratedstressresponse,isr)。为了逆转eif2α磷酸化,哺乳动物细胞具有两种eif2α磷酸酶。eif2α磷酸酶是二聚体全酶,其与200种其它磷酸酶共享催化亚基pp1c,并且结合到两种相关的调节亚基之一上:ppp1r15a(novoa等人,thejournalofcellbiology,153,1345-1355,2001)——一种应激诱导型蛋白,或者组成型表达的ppp1r15b(jousse等人,thejournalofcellbiology,163,767-775,2003)。
ppp1r15a(“r15a”)抑制选择性抑制包含ppp1r15a和pp1的应激诱导型eif2α磷酸酶,而放过高度相关的组成型磷酸酶ppp1r15b-pp1。ppp1r15a抑制延长应激细胞中的eif2α磷酸化并且这导致应激细胞中翻译衰减的延长。因此,应激细胞中分子伴侣的可用性提高,这是因为通常参与辅助新合成蛋白折叠的分子伴侣当翻译衰减后变得可用。这有利于蛋白折叠并且拯救蛋白内稳态缺陷的细胞。因此,原则上ppp1r15a抑制剂能够治疗涉及蛋白错误折叠应激的哺乳动物细胞疾病。哺乳动物中ppp1r15a的抑制具有吸引人的治疗潜力,这是因为预测ppp1r15a的抑制是安全的,因为ppp1r15a/gadd34敲除小鼠很大程度上与野生型小鼠不可区分(marciniak等人,genes&development,18,3066-3077,2004)。然而,预期可经由ppp1r15a抑制剂治疗的治疗适应症的数目受限于其中表达ppp1r15a的疾病以及ppp1r15a参与作用疾病模式的疾病。因此,ppp1r15a的抑制可为强力的且安全的,但是将局限于涉及ppp1r15a的疾病。
无论与ppp1r15a抑制相关联的限制如何,通过对翻译的精细调节提高分子伴侣的可用性,从而恢复蛋白内稳态的方法理论上是强效的、直接的并且可用于治疗涉及错误折叠蛋白的广范围的疾病。如上所述,ppp1r15a抑制剂的使用将最可能受限于表达ppp1r15a的疾病以及ppp1r15a参与疾病作用方式的疾病。
为了扩大可利用选择性pp1抑制的疾病范围,本发明致力于提供一种鉴定选择性和/或非-选择性pp1抑制剂的方法。
如本文所用,术语“ppp1r15a抑制剂”是指选自多肽、多核苷酸、抗体、肽或小分子化合物的选择性抑制剂。术语“ppp1r15a”与术语“r15a”互换使用。合适地,“ppp1r15a抑制剂”是一种抑制剂,其对r15a的选择性超过r15b和/或ppic。本文描述了选择性抑制的试验。
如本文所用,术语“ppp1r15a和ppp1r15b抑制剂”是指选自多肽、多核苷酸、抗体、肽或小分子化合物的选择性抑制剂。合适地,“ppp1r15a抑制剂和ppp1r15b抑制剂”是结合和/或抑制r15a和r15b这二者的抑制剂。本文描述了此类抑制剂的试验。
如本文所用,术语“ppp1r15b抑制剂”是指选自多肽、多核苷酸、抗体、肽或小分子化合物的选择性抑制剂。术语“ppp1r15b”与术语“r15b”互换使用。合适地,“ppp1r15b抑制剂”是一种抑制剂,其对r15b的选择性超过r15a和/或ppic。本文描述了选择性抑制的试验。
在一个实施方案中,“选择性抑制剂”可定义为其中在一种全磷酸酶如r15a或r15b和另一种全磷酸酶之间的kd值差值在3倍范围内以及优选地大于3倍,或者甚至更优选地10或20倍的化合物。
受试化合物
根据本发明实施方案的任何方面用于试验的受试化合物可为蛋白或多肽、多核苷酸、抗体、肽或小分子化合物。在一个实施方案中,试验可涵盖筛选受试化合物库,例如蛋白库、多肽库、多核苷酸库、抗体库、肽库或小分子化合物库。合适的高通量筛选法将是本领域的技术人员已知的。例如,高通量spr可使用阵列进行。
试验
在一个实施方案中,本发明描述对r15b特异性的抑制剂的试验。然而,应当理解,更一般地根据本发明的任何方面或实施方案,本文所述方法同样适用于用于鉴定全磷酸酶的特异性或非特异性抑制剂的试验。
在本文实施例1至4中描述的抑制剂选择性结合至ppp1r15b-pp1复合物,但是不结合至ppp1r15a-pp1复合物或与其的结合显著更少。优选地,ppp1r15b抑制剂表现出1μm以下的对ppp1r15b-pp1复合物的kd并且对ppp1r15a-pp1复合物显示5倍大的结合,优选10倍大,或甚至更优选地至少20倍大。
例如,实施例1化合物对ppp1r15b-pp1具有0.035μm的kd以及对ppp1r15a-pp1具有1μm的kd,并且实施例2的化合物对ppp1r15a-pp1具有5μm的kd以及对ppp1r15b-pp1具有0.143μm的kd。上述实施例2化合物曾被认为是非-选择性抑制剂(wo2014108520)。然而,此前测量kd值是不可能的。通过本发明所述的新试验,本发明人确立了kd值,并揭示了对于实施例2化合物,亲和力的差别超过30倍。因此,认为实施例2是ppp1r15b-pp1的选择性抑制剂。发现实施例3对ppp1r15b-pp1具有0.149μm的以及对ppp1r15a-pp1具有3.93μm的kd,并且发现实施例4对ppp1r15a-pp1具有0.457μm的kd以及对ppp1r15b-pp1a具有0.022μm的kd。
在本发明的一个实施方案中,提供了用于测定选择性抑制ppp1r15b超过ppp1r15a的多肽、多核苷酸、抗体、肽或小分子化合物。在另一个实施方案中,提供了用于测定选择性抑制ppp1r15a超过ppp1r15b的多肽、多核苷酸、抗体、肽或小分子化合物。在另一个实施方案中,提供了用于测定抑制ppp1r15b和ppp1r15a这二者的多肽、多核苷酸、抗体、肽或小分子化合物。
可选择性结合至单独的ppp1r15b或与pp1形成复合物的ppp1r15b。同样地,可选择性结合至单独的ppp1r15a或与pp1形成复合物的ppp1r15a。
在另一个实施方案中,提供了竞争性结合试验,其中所述试验包含将本发明所记载的化合物与ppp1r15b和候选多肽、多核苷酸、抗体或其片段、肽或小分子化合物接触,并检测所述化合物与ppp1r15b之间的相互作用的任何改变。
另选地,上述竞争性结合试验可包含在已知的ppp1r15b底物的存在下,将本发明所记载的化合物与ppp1r15b接触,并检测ppp1r15b和所述已知底物之间的相互作用的任何改变。
任选地,上述试验用作筛选或高通量筛选(hts)。
当结合试验可用于筛选选择性结合至ppp1r15b的候选物时,并不必须通过结合试验预测候选物的性质。因此需要其它试验以评估候选物是否抑制ppp1r15b的功能。
在本发明的另一个实施方案中,提供了一组试验用于测定候选物的ppp1r15b或ppp1r15a的选择性抑制,所述候选物选自多肽、多核苷酸、抗体、肽或小分子化合物,其中所述试验包括以下步骤:i)用所述候选物治疗哺乳动物;
ii)监测随时间推移的eif2α磷酸化;
其中eif2α磷酸化的瞬时诱导指示ppp1r15b或ppp1r15a的选择性抑制。
任选地,该试验用作高通量筛选。例如,eif2α磷酸化可通过适于hts的方法进行检测,例如但不限于eif2α磷酸化的免疫学检测(例如
选择性ppp1r15b抑制剂诱导瞬时elf2α磷酸化,因为elf2α最终被ppp1r15a去磷酸化。因此筛选仅瞬时诱导elf2α磷酸化的化合物将鉴定选择性ppp1r15b抑制剂。另选地,用于直接或间接监测elf2α磷酸化的任何其它方法可用于hts。例如:监测翻译速率将反映elf2α磷酸化;选择性ppp1r15b抑制剂将仅瞬时诱导翻译速率并且这种特性可用于hts以鉴定选择性ppp1r15b抑制剂。因为elf2α磷酸化诱导atf4、ppp1r15a和chop,这些基因或蛋白可在本文所述的elf2α磷酸化仅为瞬时的条件下在鉴定选择性ppp1r15b抑制剂的筛选中用作报道物。
在一个实施方案中,候选化合物通过对实施例1至4中任一项的化合物的常规sar修饰改性而产生。
在另一个实施方案中,ppp1r15b抑制剂能够保护至少20%,更优选地至少30%,甚至更优选地至少40%、至少50%、至少60%,至少70%、至少80%,还更优选地至少90%的细胞免于应激。
例如,实施例1的抑制剂保护细胞免于衣霉素引起的细胞毒性er应激。抗er应激的细胞保护作用可通过任何合适的试验进行测量。例如,可测量海拉细胞中的细胞保护作用,其中通过加入包含衣霉素(一种阻断n-糖基化的药物)的培养基引起er应激,从而阻止蛋白质折叠并诱导未折叠蛋白反应。在一组时间段后,可利用标准细胞活力试剂盒(例如来自dojindo的cellviabilitycountingkit-8),通过测量wst-8还原成甲臜的情况,在存在和不存在ppp1r15b抑制剂的情况下检测细胞活力。er应激的细胞保护作用根据在er应激后存活细胞的百分比增加(相对于对照)进行测量。
通过拓展,实施例1的化合物能够保护细胞免于衣霉素诱导的应激,而且还免于其它类型的应激,例如但不限于由毒胡萝卜素诱导的应激、由蛋白错误折叠、氨基酸类似物(例如氮杂环丁烷、刀豆氨酸)、还原剂(dtt)引起的应激和氧化应激。
应激的细胞保护作用可用于鉴定其它ppp1r15b抑制剂。任选地,该试验用作高通量筛选。例如,hts可用于测量应激下的细胞存活,用于鉴定新的ppp1r15b抑制剂。
在一个实施方案中,提供了对比细胞活力试验以测定ppp1r15b抑制剂的选择性,包含步骤i)以ppp1r15b抑制剂处理ppp1r15a和ppp1r15b敲除细胞,并随后ii)与野生型、ppp1r15a和ppp1r15b敲除细胞的活力进行对比。
该试验类似于用于显示ppp1r15a抑制剂的选择性的试验。缺乏ppp1r15a或ppp1r15b活性的任一者的细胞是有活力的,而缺乏构成性(ppp1r15b-pp1)和应激诱导性(ppp1r15a-pp1)elf2α磷酸酶这二者的细胞是无活力的(harding等人,proc.natl.acad.sci.u.s.a.,106,1832-1837,2009;tsaytler等人,science,332,91-94,2011)。ppp1r15a和ppp1r15b敲除细胞已用于评估ppp1r15a抑制剂的选择性。胍那苄降低缺乏ppp1r15b的细胞的活力,因为缺乏ppp1r15a和ppp1r15b活性这二者是有害的(tsaytler等人,febsjournal,280,766-770,2011)。因此,发明人已推断ppp1r15b抑制剂的选择性可通过在使用ppp1r15b抑制剂处理之后比较野生型、ppp1r15a和ppp1r15b敲除细胞的活力而在细胞中揭示。ppp1r15a和ppp1r15b这二者的失活是致命的(harding等人,proc.natl.acad.sci.u.s.a.,106,1832-1837,2009)。因此,以ppp1r15b抑制剂处理过的缺乏ppp1r15a活性的细胞选择性地降低其活力,这确认了选择性ppp1r15b抑制剂的存在。
该细胞活力试验可用于hts以鉴定其他ppp1r15b抑制剂,所述ppp1r15b抑制剂对缺乏ppp1r15a的细胞或ppp1r15a已被抑制的细胞是选择性毒性的。此类细胞可通过常规基因失活方法(例如基因敲除、crispr/cas9、sirna)产生。另选地,ppp1r15a可用胍那苄或任何其它选择性ppp1r15a抑制剂进行药理抑制。选择性ppp1r15b抑制剂将以比仅用ppp1r15b抑制剂处理的细胞更大的程度减少用ppp1r15a抑制剂处理的细胞的活力。
磷酸酶活性测定法也可用于筛选ppp1r15b抑制剂。
在一个实施方案中,本发明描述用于鉴定选择性磷酸酶抑制剂的方法。
试剂盒和设备
在本发明的另一方面或实施方式中,提供被安排用于根据本发明的筛选方法的试剂盒和/或设备和/或当用于根据本发明的筛选方法时,提供试剂盒和/或设备。合适的试剂盒和/或设备可包含spr芯片或其他固体表面,其被产生以通过接附至芯片或固体表面的表面“显示”第一和/或第二全磷酸酶,例如微珠或微量滴定板。合适的芯片或微珠可以使得如本文所述的筛选方法被实施的方式安排。
因此,在另一方面提供了在根据本发明的实施方式的任一方面中使用的筛选方法。合适地,上述试剂盒可包含捕集至第一表面的第一全磷酸酶和捕集至第二表面的第二全磷酸酶。这样的第一和/或第二表面可以是适用于通过spr的结合反应分析的芯片或微珠。在一个实施方案中,根据本发明的这一方面的试剂盒或设备是在用于如本文所述的筛选方法时的试剂盒或设备。
治疗应用
使用根据本发明的任何方面或实施方式的试验所鉴定的抑制剂包括ppp1r15a和/或ppp1r15b的抑制剂,其在多种疾病和障碍的治疗和预防中具有潜在治疗应用。eif2α的磷酸化的抑制降低翻译,并且作为其结果,增加有助于折叠的分子伴侣的可利用性。
本发明已示出,例如,:
·ppp1r15b抑制剂(以实施例1所记载的化合物例示)具有良好的组织分布;
·ppp1r15b抑制在哺乳动物中是安全的(图5、6、7);
·抑制ppp1r15b在哺乳动物中预防疾病(图9);并且
·抑制ppp1r15b在哺乳动物中减轻代谢疾病(图11)。
本发明的一个方面涉及用于治疗的ppp1r15b抑制剂。
本发明的另一方面涉及治疗患有通过抑制ppp1r15b而减轻的疾病状态的受试者的方法,其中所述方法包括向受试者施用治疗有效量的ppp1r15b抑制剂。
本发明的另一方面涉及在受试者中预防通过抑制ppp1r15b而减轻的疾病状态的方法,其中所述方法包括向受试者施用治疗有效量的ppp1r15b抑制剂。
本发明的另一方面涉及ppp1r15b抑制剂,其用于治疗或预防通过抑制ppp1r15b而减轻的疾病状态。
本发明的另一方面涉及ppp1r15b抑制剂在制造用于治疗或预防通过抑制ppp1r15b而减轻的疾病状态的药物中的应用。
ppp1r15b相关的疾病是可通过抑制ppp1r15b而改善的疾病。这些包括与错误折叠蛋白的积聚或蛋白质内稳态(蛋白内稳态)干扰相关联的障碍,例如亨廷顿氏病(huntington’sdisease)以及其它多聚谷氨酰胺障碍、帕金森氏病(parkinson’sdisease)、阿尔茨海默病(alzheimer’sdisease)、共济失调和其它多聚谷氨酰胺障碍以及视网膜变性、青光眼、肌萎缩性侧索硬化(als)与朊病毒病;与微管相关蛋白tau的聚集相关联的障碍并且包括阿尔茨海默病(alzheimer’sdisease)、肌萎缩性侧索硬化和关岛帕金森-痴呆综合征(parkinsonism-dementiacomplex)、嗜银颗粒病、慢性创伤性脑病、皮质基底节变性、弥漫性神经原纤维缠结伴钙化症(dntc)、唐氏综合征(down’ssyndrome)、家族性英国型痴呆(fbd)、家族性丹麦型痴呆(fdd)、与17号染色体相关的额颞性痴呆及帕金森综合征(ftdp-17)、额颞叶变性(ftld)、杰茨曼-斯脱司勒-史茵克症
在一个优选的实施方案中,ppp1r15b的抑制剂例如但不限于实施例1至4中任一项的化合物,用于治疗与病变upr或isr和/或蛋白质内稳态缺陷相关联的障碍。
在一个实施方案中,ppp1r15b抑制剂具有实施例1至4中任一项的化合物的结构。
在一个实施方案中,ppp1r15b抑制剂具有实施例1的化合物的结构。
在另一个实施方案中,ppp1r15b抑制剂具有实施例2的化合物的结构。
在另一个实施方案中,ppp1r15b抑制剂具有实施例3的化合物的结构。
在另一个实施方案中,ppp1r15b抑制剂具有实施例4的化合物的结构。
如本文所用,术语“方法”是指用于完成给定任务的方式、手段、技术和程序,所述任务包括但不限于,化学、药理、生物学、生物化学和医学领域的从业者已知的那些方式、手段、技术和程序或者容易由化学、药理、生物学、生物化学和医学领域的从业者从已知的方式、手段、技术和程序开发的方式、手段、技术和程序。
术语“治疗有效量”是指所施用的化合物的量将在某种程度上缓解所治疗疾病或障碍的一个或多个症状。
本文术语“治疗”包括消除、基本上抑制、减缓或逆转疾病或障碍的进展、基本上改善疾病或障碍的临床症状或基本上预防疾病或障碍的临床症状的出现。
短语“药物制备”包括除了在筛选程序中用于得到进一步的活性剂外直接使用或用于此类药物制备过程中的任何阶段外,如上所述的化合物直接作为药物。
在它们的作用方式中具有潜在的蛋白或肽错误折叠和/或聚集的疾病引起疾病的蛋白在整个生命周期内表达,但是退行性疾病多数是迟发的。这表明不同的引起疾病的蛋白随时间推移逐渐变得有害。虽然目前确认错误折叠的蛋白引起独特的退行性疾病,但是它们为何积聚很大程度上仍不清楚。细胞通常力图蛋白正确折叠,并且实际上所有细胞具有强力且精密的蛋白控制系统,在几十年里非常高效地处理可能有害的蛋白。然而,蛋白质量控制机制似乎随着衰老逐渐失效,导致错误折叠的蛋白积聚,引起细胞和生物体的灾难性后果。这些错误折叠/聚集的蛋白或肽可存在于细胞内部或外部,并且可见于任何位置。原则上,促进抗错误折叠蛋白的天然细胞防御应代表一种通用方法,其用于减少各种蛋白错误折叠疾病的病变,其中易发生错误折叠/聚集的蛋白存在于所述病变中。本发明描述此种方法并展示它在哺乳动物中的安全性和功效。
神经退行性疾病如阿尔茨海默病(alzheimer’sdisease,ad)、帕金森氏病(parkinson’sdisease,pd)、亨廷顿氏病(huntington’sdisease,hd)、共济失调和其它多聚谷氨酰胺障碍、tau蛋白病以及、视网膜变性、青光眼、肌萎缩性侧索硬化(als)和朊病毒病是破坏性的并且在老龄人群中影响越来越多的个体。这些疾病临床上各异但共有共同的机理。它们由由于异常形状的特定蛋白的积聚导致的大脑选择性区域中的特定神经细胞的进行性功能障碍以及死亡引起。易发生错误折叠并聚集的蛋白包括但不限于:aβ42、α-突触核蛋白、tau、tdp-43、tls/fus、sod1、亨廷顿蛋白(huntingtin)和其它具有多聚谷氨酰胺扩增的蛋白、朊病毒以及c9orf72的翻译产物。
申请人已经证明实施例1的化合物选择性抑制ppp1r15b-pp1,矫正小鼠的蛋白错误折叠疾病。本发明所述的ppp1r15b抑制剂因此具有在涉及错误折叠蛋白、尤其是错误折叠蛋白积聚的多种疾病的治疗中的治疗应用。
例如,申请人已经示出实施例1的化合物改善哺乳动物的亨廷顿氏病(huntington’sdisease)。因此,不受理论的束缚,据信ppp1r15b的抑制剂,例如但不限于实施例1至4中的任何化合物,具有对由错误折叠/聚集的蛋白引起的多种疾病的保护效应,所述疾病例如但不限于阿尔茨海默病(alzheimer’sdisease,ad)、帕金森氏病(parkinson’sdisease,pd)、亨廷顿氏病(huntington’sdisease,hd)、共济失调和其它多聚谷氨酰胺障碍、以及视网膜变性、青光眼、肌萎缩性侧索硬化(als)、tau蛋白病和朊病毒病。
本发明提供多聚谷氨酰胺障碍的疗法。亨廷顿氏病(huntington’sdisease)属于一种较广泛的障碍种类,“多聚谷氨酰胺障碍”,其特征在于在不相关蛋白中以谷氨酰胺翻译的cag密码子的扩增。亨廷顿氏病(huntington’sdisease)由编码亨廷顿蛋白(huntingtin)的基因扩增引起;脊髓延髓肌萎缩症、齿状核红核苍白球路易体萎缩症(dentalorubral-pallidoluysianatrophy)、和脊髓小脑共济失调由分别编码雄激素受体、atrophin1、ataxin1、ataxin2、ataxin3、α-电压依赖性钙通道亚基和tbp的基因扩增引起。cag扩增以多聚谷氨酰胺翻译并引起受影响蛋白的聚集。因此,预防和/或治疗诸如这些的多聚谷氨酰胺障碍也在本发明的范围内。
上述疾病包括错误折叠/聚集涉及目前已知蛋白和上文所述蛋白的任何疾病,但是也将应用于未来的新蛋白和可能的新疾病。
在一个优选的实施方案中,本发明提供蛋白内稳态疾病的疗法。
在另一个实施方案中,ppp1r15b的抑制剂例如但不限于实施例1至4中任一项的化合物,用于治疗其中作用方式涉及错误折叠蛋白的积聚的疾病。
在另一个实施方案中,疾病或障碍为阿尔茨海默病(alzheimer’sdisease,ad)、帕金森氏病(parkinson’sdisease,pd)、亨廷顿氏病(huntington’sdisease,hd)、共济失调或其它多聚谷氨酰胺障碍、视网膜变性、青光眼、肌萎缩性侧索硬化(als)、tau蛋白病或朊病毒病。
在一个具体实施方案中,实施例1至4中任一项的化合物用于治疗亨廷顿氏病(huntington’sdisease)。
在另一个具体实施方案中,实施例1至4中任一项的化合物用于治疗帕金森氏病(parkinson’sdisease)。
在一个实施方案中,疾病或障碍与微管相关蛋白tau的聚集相关联。
申请人已经证明实施例1的化合物选择性抑制ppp1r15b-pp1,矫正小鼠的蛋白错误折叠疾病。ppp1r15b抑制剂也可用于预防或终止由相同机理(错误折叠蛋白的积聚)引起的疾病进展。
此类疾病的示例包括阿尔茨海默病(alzheimer’sdisease)、肌萎缩性侧索硬化、帕金森病和痴呆、嗜银颗粒病、慢性创伤性脑病、皮质基底节变性、弥漫性神经原纤维缠结伴钙化症(dntc)、唐氏综合征(down’ssyndrome)、家族性英国型痴呆(fbd)、家族性丹麦型痴呆(fdd)、与17号染色体相关的额颞性痴呆及帕金森综合征(ftdp-17)(由mapt突变引起)、额颞叶变性(ftld)(一些病例由c9orf72突变引起)、杰茨曼-斯脱司勒-史茵克症
在一个实施方案中,疾病是髓鞘质障碍。
髓鞘质是中枢和外周神经系统的富含蛋白。它由两种细胞类型产生:中枢神经系统中的少突胶质细胞和外周神经系统中的神经膜细胞。髓鞘质形成围绕轴突的鞘以确保电脉冲沿轴突的传导速度,并且用于防止电流从轴突上消散。髓鞘质功能对于神经系统来说是必需的。
髓鞘质障碍在世界范围内影响超过2.5百万人并且定义为与髓鞘质的损伤相关联的任何疾病。髓鞘质障碍表现为各种不同的症状,包括但不限于运动障碍、感官障碍、认知障碍、情绪困扰、和协调障碍。
存在多种脱髓鞘疾病,其中最常见的是多发性硬化症(multiplesclerosis,ms)。多发性硬化症是一种自身免疫性疾病,影响大脑和脊髓,导致大脑脱髓鞘。除ms之外,其它脱髓鞘疾病包括但不限于佩利措伊斯-梅茨巴赫病(pelizaeus-merzbacherdisease)和白质消失病、急性播散性脑脊髓炎、脑室周围白质软化、脑室周围白质损伤、脊髓痨、德维克病(devic’sdisease)、视神经炎、进行性多灶性白质脑病、横贯性脊髓炎、慢性炎症性脱髓鞘性多发性神经病、抗mag外周神经病、肾上腺脑白质营养不良、肾上腺脊髓神经病、弥漫性脑白质损伤、吉兰-巴雷综合征(guillain-barresyndrome)、脑桥中央髓鞘溶解症、诸如脑白质营养不良的遗传性脱髓鞘疾病、以及腓骨肌萎缩症牙病(charcotmarietoothdisease,cmt)。
cmt疾病是一类髓鞘神经病变,其由多个基因的突变引起。在外周髓鞘蛋白pmp22中的突变是cmt最常见的起因。pmp22(trembler-j)中的突变引起pmp22的错误折叠并导致小鼠中的疾病,其类似于人的cmt,这是由于外周神经系统中的髓鞘质缺陷引起。申请人已经证明实施例1的化合物能够改善来自神经病变小鼠的外植体的髓鞘形成。申请人已经证明改善来自神经病变小鼠的外植体的髓鞘形成预示在哺乳动物中的功效(das等人,已接受待发表)。因此实施例1的化合物将用于治疗哺乳动物的cmt和其它髓鞘质障碍,其中已知机理是相似的并且涉及eif2α途径(linandpopko,nat.neurosci.,12,379-385,2009)。
在一个实施方案中,r15b的抑制剂用于治疗髓鞘质障碍。
在另一个实施方案中,ppp1r15b的抑制剂例如但不限于实施例1至4中任一项的化合物,用于治疗腓骨肌萎缩症牙病(charcotmarietoothdisease)。
在另一个实施方案中,本发明的ppp1r15b抑制剂用于治疗中枢神经系统的髓鞘质障碍,例如多发性硬化症。已知cmt和ms的机理相似之处在于髓鞘产生细胞的耗竭(cmt中的神经膜细胞和ms中的少突胶质细胞)并且涉及eif2α-rrr1r15a途径的病理信号转导(linandpopko,nat.neurosci.,12,379-385,2009)。因为申请人已经展示实施例1对髓鞘质病有效并且也已经展示了实施例1的化合物在中枢神经系统和外周神经系统中的生物利用率(图5),预期ppp1r15b抑制剂将可用于治疗多发性硬化症。
在一个实施方案中,上述疾病是起因于蛋白突变,导致其错误折叠和错误定位或运输缺陷的疾病。
申请人已经展示实施例1的化合物能够治疗由一种在内质网(er)中合成的错误折叠蛋白pmp22引起的缺陷。由于作用机制(减少翻译以增加折叠),根据本发明的ppp1r15b抑制剂也将可用于治疗由于在er中制备的任何蛋白(包括跨膜蛋白或分泌蛋白)的错误折叠或运输缺陷引起的疾病。
此类疾病的示例包括:由破坏跨膜蛋白折叠的突变引起的囊性纤维化(cftr);由于激素甲状腺球蛋白的错误折叠和/或运输缺陷引起的先天性甲状腺肿伴甲状腺球蛋白缺乏症;由错误折叠和缺乏循环精氨酸加压素引起的遗传垂体性尿崩症(familialneurohypophysealdiabetes)(这也可包括某些形式的基因遗传的肾性尿崩症);前胶原生物合成障碍,其中所述疾病由无法折叠、装配并合成胶原引起,例如但不限于成骨不全;更一般地,其中蛋白的错误折叠/无法合成或错误定位参与作用方式中的结缔组织的任何遗传疾病,例如与来自细胞外基质的蛋白缺陷相关联的生长板发育不良;高胆固醇血症,其具有由ldl受体中的突变导致无法合成、改变细胞内运输、或功能异常引起的分子缺陷;由于α1抗胰蛋白酶的错误折叠引起的α-1抗胰蛋白酶缺乏症;由于与溶酶体功能相关联的蛋白错误折叠引起的溶酶体疾病如戈谢病(gaucherdisease)和尼曼-皮克病(niemann-pickdisease)以及安德森-法布里病(anderson-fabrydisease);色素性视网膜炎(rp),它是由视紫质蛋白的错误折叠、它们的er驻留以及导致的er应激和细胞凋亡引起的遗传性视网膜变性最常见的形式;和与er应激相关联的炎性肠病。
出于相同原因,根据本发明的ppp1r15b抑制剂可用于治疗与病变upr和/或跨膜蛋白缺陷相关联的以下疾病(linandpopko,nat.neurosci.,12,379-385,2009)。这些疾病包括但不限于与膜蛋白脂质蛋白(plp)基因中的突变相关联的佩利措伊斯-梅茨巴赫病(pelizaeus-merzbacherdisease)、和白质消失(vwm)病、以及多发性硬化症(一种常见的髓鞘质障碍)。
在一个实施方案中,本发明涉及ppp1r15b抑制剂,其用于治疗由导致蛋白错误折叠和错误定位或运输缺陷的蛋白突变引起的疾病。
在另一个实施方案中,由导致蛋白错误折叠和错误定位或运输缺陷的蛋白突变引起的疾病选自囊性纤维化、先天性甲状腺肿、遗传垂体性尿崩症、前胶原生物合成障碍(诸如成骨不全)、高胆固醇血症、α-1抗胰蛋白酶缺乏症、溶酶体疾病(诸如戈谢病(gaucherdisease)、尼曼-皮克病(niemann-pickdisease)和安德森-法布里病(anderson-fabrydisease))、色素性视网膜炎和炎性肠病。
在一个实施方案中,上述疾病是代谢疾病。
已知诸如糖尿病、肥胖症、胰岛素抵抗、血脂过多、脂肪性肝病、和动脉粥样硬化的代谢疾病与病理er应激相关联,并且据信upr的药理调节剂可具有治疗有益效果(cao和kaufman,2012,currbiol,卷22(16))。然而,因为之前无ppp1r15b抑制剂可用并且曾预测ppp1r15b抑制是有毒性的,以及此外因为抑制磷酸酶具有挑战性,不清楚是否ppp1r15b可为代谢疾病的治疗靶点。
发明人已经证明实施例1的化合物能够改善哺乳动物的代谢障碍(图11)。因此,ppp1r15b抑制剂将可用于治疗代谢疾病例如但不限于糖尿病、肥胖症、脂肪性肝病、和动脉粥样硬化。
在一个实施方案中,本文所述的ppp1r15b抑制剂用于治疗代谢障碍。
在一个优选的实施方案中,代谢障碍选自糖尿病、肥胖症、脂肪性肝病、和动脉粥样硬化。
ppp1r15b选择性抑制剂用于治疗其它疾病,包括类风湿性关节炎、糖尿病、沃尔科特-拉里森综合征(wolkottrallisonsyndrome)、炎性肠病和白癜风,它们的作用机理涉及upr(cao和kaufman,2012,currbiol,vol.22(16))。
已经描述了减少蛋白合成以增加寿命(参见例如tavernarakis,n.(2008).(ageingandtheregulationofproteinsynthesis:abalancingact?trendscellbiol,18(5),228–235.http://doi.org/10.1016/j.tcb.2008.02.004.)。根据本发明已经通过抑制r15b表现出减少的蛋白合成的那些化合物因此可用于治疗,从而增加寿命/减轻衰老。
化合物
在本发明的一个实施方案中,提供了实施例1至4的化合物以及它们用作ppp1r15b选择性抑制剂:
相对于本领域化合物如胍那苄,本文所述化合物有利地对肾上腺素α2a受体表现出无活性。这种α-2肾上腺素活性的丧失致使化合物可在治疗上用于对本文所公开的疾病和障碍的治疗。相比之下,具有肾上腺素活性的胍那苄衍生物不能够用于治疗,因为这引起副作用诸如低血压、嗜睡、嗜睡症以及甚至昏迷。(hall等人,anninternmed102,787–788,1985)。缺失α-2肾上腺素活性意味着本发明的化合物可以适于治疗上述疾病的剂量施用,对血压无任何显著效应。
盐和酯
本发明所述的化合物可以盐或酯形式存在,尤其是药学上可接受的盐或酯。
本发明的化合物的药学上可接受的盐包括其合适的酸加成盐或碱盐。合适的药物盐的综述可见于berge等人,jpharmsci,66,1-19(1977)。非药学或兽医学可接受的盐作为中间体仍可为有价值的。
酯用有机酸或醇/氢氧化物形成,这取决于被酯化的官能团。
对映异构体/互变异构体
在本发明之前讨论的所有方面,本发明包括在适用情况下本发明化合物的所有对映异构体、非对映异构体和互变异构体。本领域的技术人员将认识到具有光学性质(一个或多个手性碳原子)或互变异构特征的化合物。对应的对映异构体和/或互变异构体可通过本领域已知的方法分离/制备。对映异构体的特征在于它们手性中心的绝对构型,并通过cahn、ingold和prelog的r-和s-顺序规则描述。此类规则在本领域中是公知的(例如参见‘advancedorganicchemistry’,第3版,march,j.编辑,johnwileyandsons,newyork,1985)。
立体和几何异构体
本发明的一些化合物可存在立体异构和/或几何异构体-例如,它们可具有一个或多个不对称和/或几何中心,并因此可能存在两个或更多个立体异构和/或几何异构形式。本发明考虑使用那些抑制剂的所有单独的立体异构体和几何异构体、以及它们的混合物。在权利要求书中使用的术语包括这些形式,只要所述形式保留适当的功能活性(但不必到相同程度)。
本发明还包括上述药剂或其药学上可接受的盐的所有合适的同位素变体。本发明的试剂或其药学上可接受的盐的同位素变体定义为其中至少一个原子被具有相同原子序数但原子质量与通常在自然界中发现的原子质量不同的原子替代。可掺入到上述试剂及其药学上可接受的盐的同位素的示例包括氢、碳、氮、氧、磷、硫、氟和氯的同位素,例如分别为2h、3h、13c、14c、15n、17o、18o、31p、32p、35s、18f和36cl的同位素。上述试剂及其药学上可接受的盐的某些同位素变体,例如其中掺入放射性同位素如3h或14c的那些,可用于药物和/或底物组织分布研究。氚化,即,3h,和碳-14,即,14c,同位素是特别优选的,因其易于制备和检测。此外,用同位素如氘(即,2h)进行取代可提供由更大的代谢稳定性所带来的某些治疗优势,例如增加体内半衰期或减少剂量要求,并因此在某些情况下优选。例如,本发明包括其中任意的氢原子已被为氘原子取代的实施例1至4的化合物。本发明试剂及其药学上可接受的盐的同位素变体一般可通过使用合适试剂的适当同位素变体,通过常规方法来制备。
前药
本发明还包括前药形式的本发明的化合物,即,共价键合的化合物,其在体内释放根据任何示例性化合物的活性母体药物。此类前药通常是本发明的化合物,其中一个或多个适当基团已被修饰,使得所述修饰可以在施用于人或哺乳动物受试者时逆转。逆转通常由天然存在于这些受试者体内的酶进行,但是此种前药与第二药剂一起施用以在体内进行逆转是可能的。此类修饰的示例包括酯(例如,上述那些中的任一种),其中逆转可以由酯酶等进行。其它此类系统是那些本领域技术人员将公知的。
溶剂化物
本发明还包括本发明化合物的溶剂化物形式。在权利要求书中使用的术语包括这些形式。
多晶型物
本发明还涉及本发明化合物的各种结晶形式、多晶型形式和水合形式。制药工业中已经确认化合物可通过稍微改变纯化和/或分离方法从合成制备此类化合物的溶剂中以任何此类形式分离出来。
抗体
提及“抗体”包括但不限于单克隆抗体、人抗体、人源化抗体、或嵌合抗体。抗体可为包括vh或vl结构域或单链抗体分子(scfv)的抗体片段。在一个实施方案中,抗体是人的。
药物组合物
根据本发明的另一方面,提供了包含ppp1r15b抑制剂的药物组合物。在一个实施方案中,药物组合物与任何药学上可接受的载体、助剂或溶媒(vehicle)组合用于治疗。
术语“药物组合物”在本发明的上下文中是指包含活性剂或其药学上可接受的盐以及附加的一种或多种药学上可接受的赋形剂的组合物。
合适的药学上可接受的赋形剂是本领域已知的,并且一般包括可接受的组合物、材料、载体、稀释剂或溶媒,它们适于施用本发明的ppp1r15b抑制剂于动物。
在一个实施方案中,所述动物是哺乳动物。在另一个实施方案中,所述哺乳动物是人。
药物制剂包括那些适于口服的、局部的(包括皮肤的、口腔的、眼的和舌下的)、直肠的或肠胃外的(包括皮下的、真皮内的、肌肉内的和静脉内的)、经鼻的、眼内的和肺部给药(例如通过吸入)的药物制剂。在合适情况下,制剂可以独立的剂量单位便利地存在,并且可通过制药领域中任何熟知的方法制备。
剂量可根据患者需求、待治疗病症的严重度和待使用活性成分的特性而变化。确定有效剂量是在技术人员的知识范围内,无过度的负担。施用于包括人的哺乳动物的合适剂型通常在至多100mg/kg体重的范围内,或者可为例如0.1mg/kg、10mg/kg、20mg/kg、30mg/kg。
根据本发明的另一方面,提供了用于制备如上所述的药物组合物的方法,该方法包括使活性化合物与载体结合,例如通过掺合剂结合。
一般来讲,通过均匀并紧密地使活性剂与液体载体或细粉碎的固体载体或以上二者结合,并且随后根据需要成形产品来制备所述制剂。本发明扩展至制备药物组合物的方法,该方法包括使本文所公开的化合物与药学上可接受的载体或溶媒结合或结合。所有方法包括使活性化合物与液体载体或细粉碎的固体载体或以上二者结合的步骤,并且随后根据需要将产品成形成所需的制剂。
在一个方面,提供了如本文所述的ppp1r15b抑制剂在制造用于治疗通过选择性抑制ppp1r15b而减轻的疾病或障碍的药物中的应用。
组合
在一个尤其优选的实施方案中,本发明的一种或多种ppp1r15b抑制剂与一种或多种其它活性剂,例如市售的现有药物组合施用。在这种情况下,本发明的抑制剂可以连续、同时或贯序与一种或多种其它活性剂共同施用。
当组合使用时,药物一般是更有效的。具体地,组合疗法是可取的,以避免主要毒性、作用机制和耐药机制的重叠。此外,期望将大部分药物以其最大耐受剂量通过这些剂量之间的最短时间间隔施用。组合药物的主要优点是,它可以通过生物化学相互作用促进额外的或可能的协同效应,并且还可以减少耐药性的出现。
有利的组合可以通过以已知的或推测在特定障碍的治疗中有价值的药剂来测试抑制剂的抑制活性而被提出。此过程也可用于确定药剂的施用顺序,即,在递送前、与递送同时、或在递送后的顺序。这样的时序安排可为所有本文中所鉴定的活性剂的特征。
在另一方面或实施方案中,本发明涉及ppp1r15b选择性抑制剂和筛选ppp1r15b选择性抑制剂的方法。本发明还涉及选择性抑制ppp1r15b的化合物及其在治疗中的使用。
因此,本发明的其它方面和实施方案在以下编号条款中提供,作为本发明的声明:
1.一种用于鉴定和/或测定选择性结合ppp1r15b超过ppp1r15a的多肽、多核苷酸、抗体、肽或小分子化合物的试验方法。
2.根据条款1所述的试验方法,其中所述试验方法是竞争性结合试验方法,包括使ppp1r15b选择性抑制剂接触ppp1r15b和候选多肽、多核苷酸、抗体、肽或小分子化合物,并且检测在ppp1r15b选择性抑制剂和ppp1r15b之间的相互作用的任何变化。
3.根据条款2所述的试验方法,其中所述试验方法用作筛选或高通量筛选。
4.一种用于测定候选物的ppp1r15b选择性抑制的试验方法,所述候选物选自多肽、多核苷酸、抗体、肽或小分子化合物,其中所述试验方法包括以下步骤:
i)用所述候选物处理哺乳动物细胞;
ii)监测随时间推移的eif2α磷酸化;
其中eif2α磷酸化的瞬时诱导指示ppp1r15b的选择性抑制。
5.根据条款4所述的试验方法,其中所述试验方法用作高通量筛选。
6.一种用于测定ppp1r15b抑制剂的选择性的细胞活力试验,所述试验包括以下步骤:
i)用所述ppp1r151b抑制剂处理细胞;
ii)比较所述细胞的活力与野生型、ppp1r151a和ppp1r15b敲除细胞的活力;
其中在所述经处理细胞中的活力降低指示ppp1r15b选择性抑制剂的存在。
7.一种用于测定候选物的ppp1r15b选择性抑制的试验,所述候选物选自多肽、多核苷酸、抗体、肽或小分子化合物,其中所述试验包括以下步骤:
i)用所述候选物治疗哺乳动物细胞或生物体;
ii)随时间推移监测ppp1r15a;
其中ppp1r15a的瞬时诱导指示ppp1r15b的选择性抑制。
8.一种在治疗中应用的选择性ppp1r15b抑制剂。
9.一种选择性ppp1r15b抑制剂,所述抑制剂在通过ppp1r15b的选择性抑制而减轻的疾病或障碍的预防或治疗中应用。
10.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍是蛋白内稳态疾病。
11.一种用于根据条款10所述的应用的选择性ppp1r15b抑制剂,其中所述蛋白内稳态疾病是亨廷顿氏病(huntington’sdisease)、帕金森氏病(parkinson’sdisease)、阿尔茨海默病(alzheimer’sdisease)、tau蛋白病(tauopathy)、共济失调、视网膜变性、青光眼、肌萎缩性侧索硬化(als)或朊病毒病。
12.一种用于根据条款11所述的应用的选择性ppp1r15b抑制剂,其中所述疾病是亨廷顿氏病(huntington’sdisease)。
13.一种用于根据条款11所述的应用的选择性ppp1r15b抑制剂,其中所述疾病是帕金森氏病(parkinson’sdisease)。
14.一种用于根据条款11所述的应用的选择性ppp1r15b抑制剂,其中所述疾病是tau蛋白病。
15.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病是蛋白质运输疾病。
16.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍是髓鞘质障碍。
17.一种用于根据条款16所述的应用的选择性ppp1r15b抑制剂,其中所述髓鞘质障碍是多发性硬化症、佩利措伊斯-梅茨巴赫病(pelizaeus-merzbacherdisease)、白质消失病、急性播散性脑脊髓炎、脑室周围白质软化、脑室周围白质损伤、脊髓痨、德维克病(devic’sdisease)、视神经炎、进行性多灶性白质脑病、横贯性脊髓炎、慢性炎症性脱髓鞘性多发性神经病、抗mag外周神经病、肾上腺脑白质营养不良、肾上腺脊髓神经病、弥漫性脑白质损伤、吉兰-巴雷综合征(guillain-barresyndrome)、脑桥中央髓鞘溶解症、脑白质营养不良、或腓骨肌萎缩症牙病(charcotmarietoothdisease)。
18.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍是囊性纤维化、先天性甲状腺肿、家族性垂体性糖尿病、前胶原生物合成疾病包括成骨不全、高胆固醇血症、α-1抗胰蛋白酶缺乏症、溶酶体疾病、色素性视网膜炎或炎性肠病。
19.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍是代谢疾病。
20.一种用于根据条款19所述的应用的选择性ppp1r15b抑制剂,其中所述代谢疾病是糖尿病、沃尔科特-拉里森综合症(wolcottrallisonsyndrome)、肥胖症、胰岛素抵抗、血脂过多、脂肪性肝病或动脉粥状硬化。
21.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍是类风湿性关节炎、1型糖尿病或白癫风。
22.一种用于根据条款9所述的应用的选择性ppp1r15b抑制剂,其中所述疾病或障碍与微管相关蛋白tau的聚集相关联。
23.治疗患有通过抑制ppp1r15b而减轻的疾病状态的受试者的方法,其中所述方法包括向受试者施用治疗有效量的ppp1r15b抑制剂。
24.根据条款1至4中任一项所述的试验方法、用于根据条款8至22中任一项所述的应用的抑制剂或根据条款23所述的治疗方法,其中所述ppp1r15b选择性抑制剂是选自以下的化合物:
(e)-2-(2,3-二氯亚苄基)肼-1-甲脒;
(e)-2-(2-氯-4-氟亚苄基)肼-1-甲脒;
(e)-2-(3,4,5-三氯亚苄基)肼-1-甲脒;和
(e)-2-(2,4,5-三氯亚苄基)肼-1-甲脒。
25.一种在亨廷顿氏病(huntington’sdisease)的治疗中应用的选择性ppp1r15b抑制剂,其中所述抑制剂是选自以下的化合物:
(e)-2-(2,3-二氯亚苄基)肼-1-甲脒;
(e)-2-(2-氯-4-氟亚苄基)肼-1-甲脒;
(e)-2-(3,4,5-三氯亚苄基)肼-1-甲脒;和
(e)-2-(2,4,5-三氯亚苄基)肼-1-甲脒。
26.一种在帕金森氏病(parkinson’sdisease)的治疗中应用的选择性ppp1r15b抑制剂,其中所述抑制剂是选自以下的化合物:
(e)-2-(2,3-二氯亚苄基)肼-1-甲脒;
(e)-2-(2-氯-4-氟亚苄基)肼-1-甲脒;
(e)-2-(3,4,5-三氯亚苄基)肼-1-甲脒;和
(e)-2-(2,4,5-三氯亚苄基)肼-1-甲脒。
27.选自以下的化合物作为ppp1r15b选择性抑制剂的应用:
(e)-2-(2,3-二氯亚苄基)肼-1-甲脒;
(e)-2-(2-氯-4-氟亚苄基)肼-1-甲脒;
(e)-2-(3,4,5-三氯亚苄基)肼-1-甲脒;和
(e)-2-(2,4,5-三氯亚苄基)肼-1-甲脒。
实施例
实施例a
根据本发明的化合物的制备
根据本发明的化合物可根据以下方法制备:
通用方法a:
在25℃下向苯甲醛(1eq.)在乙醇(300ml)中的溶液依次加入氨基胍盐酸盐(1eq.)和乙酸钠(1eq.)。随后将所得反应混合物在80℃下加热约6小时。在使用二氯甲烷/甲醇(8/2)作为流动相的tlc上监测反应完成。在反应完成后,使反应混合物冷却至25℃并倾倒在nahco3饱和溶液(700ml)中。真空滤出所得沉淀物并用水(100ml)洗涤。所得固体材料与乙醚(2x25ml)一起研磨并真空干燥以得到期望的取代氨基胍衍生物。
根据通用方法a制备以下化合物:
实施例1:(e)-2-(2,3-二氯亚苄基)肼-1-甲脒
按照通用方法a从2,3-二氯苯甲醛,以85%产率制备(考虑单乙酸盐)lc-ms:m/z=231.23(m+h).1h-nmr(dmso-d6):(ppm)11.85(brs,1h);8.35(s,1h);8.19-8.21(dd,1h);7.56-7.59(dd,1h);7.32-7.36(t,1h);7.04(brs,4h);1.84(s,3h);ms(esi+):m/z=231.23[m+h]+
实施例2:(e)-2-(2-氯-4-氟亚苄基)肼-1-甲脒
按照通用方法a从2-氯-4-氟苯甲醛,以67%产率制备。1h-nmr(dmso-d6):δ(ppm)5.80(brs,2h);5.84(brs,2h);7.19-7.34(m,4h);8.16(s,1h);ms(esi+):m/z=215.1[m+h]+
实施例3:(e)-2-(3,4,5-三氯亚苄基)肼-1-甲脒
按照通用方法a从3,4,5-三氯苯甲醛,以70.88%产率制备。1h-nmr(dmso-d6):(ppm)7.96(s,2h);7.89(s,1h);6.20(brs,2h);5.69(brs,2h);ms(esi+):m/z=265.1[m+h]+
实施例4:(e)-2-(2,4,5-三氯亚苄基)肼-1-甲脒
按照通用方法a从2,4,5-三氯苯甲醛,以78.76%产率制备。1h-nmr(dmso-d6):(ppm)8.43(s,1h);8.12(s,1h);7.77(s,1h);6.33(brs,2h);5.83(brs,2h);ms(esi+):m/z=265.17[m+h]+
蛋白表达、纯化和通过表面等离子共振分析
蛋白表达和纯化
如下表达并纯化ppp1r15a325-636和ppp1r15b340-698:将编码ppp1r15a的氨基酸325-636和ppp1r15b的氨基酸340-698的cdna加his标记,并克隆进pmal-c5x。r15a和r15b的氨基酸序列在图16中示出。重组ppp1r15a/b在bl21-gold细胞中表达并通过亲和色谱,在histraphp柱(gehealthcare)以及随后mbptraphp柱(gehealthcare)上纯化。将编码人pp1γ(pp1c)的cdna克隆进杆状病毒转移载体pdw464以添加生物素受体肽(bap)。该载体也编码大肠杆菌生物素全酶合成酶(bira),以使bap-标记的蛋白可在草地贪夜蛾(spodopterefrugiperda)(sf9)昆虫细胞中进行体内生物素化(duffy等人,anal.biochem.,262,122-128,1998)。bac-to-bac杆状病毒表达系统(lifetechnologies)用于产生重组杆粒dna,并且sf9昆虫细胞用于扩增病毒原种。培养物通过在1,200g下离心15分钟收集,细胞沉淀物重悬在裂解缓冲液(50mmtrisph7.4,150mmnacl,0.2%triton,5%甘油,1pic片(roche)/50ml以及0.2mmpmsf)中并随后进行轻柔超声处理。蛋白质首先在5mlhitrapqhp柱(gehealthcare)上纯化,随后通过hiload16/600superdex200柱(gehealthcare)纯化。合并通过sds-page和蛋白质印迹确认的阳性级分,浓缩至~1μm并存储在-80℃。
在sa传感器芯片上捕集生物素–pp1
biacoret200(gehealthcare)系统用于所有实验,并且生物素化的pp1使用传感器芯片sa(gehealthcare,目录号br-1005-31)捕集。链亲和素涂覆的表面通过用50mmnaoh和1mnacl的溶液注射1分钟来活化。生物素–pp1在运行缓冲液(50mmtrisph7.5,100mmnacl,0.1mmegta,1mmmncl2,0.05%tween20)中稀释并以大约300nm的浓度直接注射到链亲和素涂覆的表面上,持续100秒,或者达到对应于~7000ru的生物素–pp1固定水平。对一个sa传感器芯片表面进行空白固定,用作参考。
使用bio-pp1表面测定小分子与eif2α全磷酸酶复合物的稳态结合常数
在所有结合实验中使用仅有微小偏差的相同程序和条件。小分子以在100%dmso中的50mm原液形式储存。在测定结合常数前,在96-孔板中在运行缓冲液中制备连续稀释的12个或8个浓度的化合物。在每个化合物稀释系列之前,在运行缓冲液中将调节亚基r15a或r15b稀释至15μm,并在生物素-pp1表面上捕集,从而在传感器芯片表面上形成全磷酸酶复合物。随后,不再生表面,将化合物稀释系列注射到芯片表面上。使用biacoret200评估软件分析传感图和基于稳态模型测定结合常数。使用不同浓度的化合物进行动力学实验,并测定其相应平衡结合水平。这些平衡响应水平(req)对浓度作图并使用全局拟合进行拟合,其能够测定稳态亲和常数,即,在50%饱和度下的浓度为kd(frostell-karlsson等人,j.med.chem.,43,1986-1992,2000)。
哺乳动物细胞培养
在分别含有5%和10%胎牛血清(fbs)并补充有青霉素、链霉素的达尔伯克改良伊格尔培养基(dulbecco’smodifiedeagle’smedia,dmem)中培养海拉细胞。mef细胞在补充有青霉素、链霉素、谷氨酰胺、55μmβ-巯基乙醇、1x非必需氨基酸(sigma-adrich)和10%fbs的dmem中培养。根据指示,细胞用2.5μg/ml衣霉素、1mmdtt(sigma-adrich)和/或指示浓度的指示化合物进行处理。
通过免疫印迹进行蛋白质分析
对于免疫印迹,在每个实验前24小时将海拉细胞(80,000个细胞/ml)铺于12-孔板中。紧接指示的处理后,细胞在75μllaemmlibuffer中裂解,在95℃下煮沸5分钟并用超声波处理。分离蛋白并按所述(tsaytler等人,science,332,91-94,2011)用以下抗体分析:phospho-eif2α[ps52]和ppp1r15a/gadd34(10449-1-ap;proteintechgroup,1/1000稀释)。
评估细胞成活力
在处理前24小时将细胞铺于24-孔板中,密度为15,000(hela)或12,000个细胞/ml(mefs)。通过加入包含2.5μg/ml衣霉素(sigma-aldrich)的新鲜培养基引发er应激。实施例1的化合物溶解在dmso中并如所指出的那样加入。dmso用作模拟处理。利用cellviabilitycountingkit-8(dojindo),根据供应商的推荐,在衣霉素处理后48小时通过测量wst-8[2-(2-甲氧基-4-硝基苯基)-3-(4-硝基苯基)-5-(2,4-二磺基苯基)-2h-四唑鎓]还原成甲臜的情况,评估细胞成活力。
动物研究
所有动物护理和程序符合关于研究动物使用的法规(ukanimalsscientificproceduresactof1986)而进行,获得当地伦理委员会的批准。
为了研究实施例1的化合物对体重的影响,c3h/b6小鼠每日一次口服强饲实施例1的化合物并且每日记录小鼠体重,持续2周。
为了评估实施例1的化合物在改善疾病表型中的功效,28-日龄的转基因小鼠或同窝对照小鼠每日口服实施例1的化合物(2mg/kg)或溶媒,持续4周。通过在处理期间给小鼠称重并且通过在处理4周后评估它们的运动能力,评估疾病进展。
为了评估实施例1的化合物是否具有胍那苄的副作用,小鼠(n>3)口服强饲10mg/kg的化合物或胍那苄。在给药后30分钟监测它们的活动。由于胍那苄的降血压活性,胍那苄处理的小鼠在给药后30分钟不运动,与用实施例1的化合物处理的小鼠(与未处理小鼠一样活跃)相反。
八周龄的hd-n171-82q小鼠和它们的野生型同窝小鼠首先在静止转子上适应1分钟并在恒定速度(4rpm)下适应1分钟。重复适应过程。测试阶段由四个试验组成,之间有15分钟间隔。对于每个试验,将5只小鼠置于加速转子(4至40rpm)上并记录跌落的等待时间,个体动物的最大限制设为300秒。
为了治疗代谢障碍,db/db动物(每种条件n=5)用1mg/kg的实施例1的化合物每日治疗一次,持续三周。在9和10am间用血糖仪(dsi)测量血糖水平。数据为平均值+/-s.e.m。
定量rt-pcr
在trizol(lifetechnologies)中从大脑提取rna。使用nanodrop1000分光光度计(thermofisherscientific)测量rna浓度,并且使用superscript逆转录酶(lifetechnologies)将1μg逆转录成cdna。定量pcr利用引物gapdh(f):accacagtccatgccatcac,gapdh(r):tccaccaccctgttgctgta,ppp1r15a(f):cctcctgaaacttggggact;和ppp1r15a(r):gctgtgatgtgggataagcg,使用
drg培养
从在13.5或发育(e13.5)的野生型或pmp22tr-j(pmp22突变体)(henry等人,neuropathol.exp.neurol.,42,688-706,1983)胚胎中切出的背根神经节(drg)在胶原涂敷的盖玻片上的neurobasal培养基中培养7天,所述培养基补充有4g/l葡萄糖,2mml-谷氨酰胺,2%b27补充剂和50ng/ml神经生长因子(ngf)。为了分化神经膜细胞并诱导髓鞘形成,随后将培养的drg保持在c-培养基(mem培养基,补充有4g/l葡萄糖,2mml-谷氨酰胺,10%fcs,50ng/mlngf)中。每隔一天用新添加的50μg/ml抗坏血酸±5nm实施例1的化合物更换c-培养基,并且培养14天以使许旺细胞形成髓鞘。培养的drg随后在4%多聚甲醛中固定并用mbp(大鼠髓鞘碱性蛋白,1/250稀释,ab73498)免疫染色。
小鼠的参考是pubmedid:631386。
生物化学测定
测定1:选择性ppp1r15b抑制剂选择性地结合ppp1r15b-pp1(图1)
表面等离子共振(spr)用于测量化合物与ppp1r15a/b-pp1磷酸酶复合物的结合亲和力。生物素受体肽(bap)融合在pp1γ的n-末端上,这使bap-标记的蛋白能够在sf9昆虫细胞中进行生物素化。在纯化后,bap-pp1γ蛋白在链亲和素传感器芯片(sa-芯片,gehealthcare)上捕集至~5.000ru的响应水平。使用受控生物素化能够在传感器芯片表面上定向并均匀固定。随后使用pp1γ以在链亲和素芯片表面上捕集ppp1r15a/b并形成全磷酸酶复合物。这种复合物随后能够用于测试化合物的结合。10μmppp1r15a/b蛋白浓度用于在80秒注射期间形成全磷酸酶复合物。在已经捕集了ppp1r15a/b后,将一系列浓度的化合物注射在芯片表面,测量化合物与全磷酸酶的结合。在完成浓度系列(8或12个浓度)后,用3mnacl再生表面,并且能够再次捕集r15a/b以形成新的全磷酸酶复合物,用于测量另一个化合物浓度系列的结合。分析作为浓度函数的平衡结合水平得到相互作用亲和力或稳态结合亲和力(kd)。
图1示出实施例1的化合物的kd值。ppp1r15b-pp1的0.035μm和ppp1r15a-pp1的1μm的kd表明实施例1的化合物选择性结合pp1r15b-pp1复合物,但是与ppp1r15a-pp1复合物的结合显著更低。
测定2:在无应激的情况下选择性ppp1r15b抑制剂诱导细胞中eif2α的瞬时磷酸化(图2a和b)
利用与重组蛋白的体外结合测定揭示实施例1的化合物的选择性。然而,虽然结合测定可用于筛选结合ppp1r15b的选择性化合物,但是通过结合测定未必预测出化合物的特性。因此,需要其它测定以评估化合物是否抑制ppp1r15b的功能。
人类细胞用ppp1r15b抑制剂处理,并且监测随时间推移的eif2α磷酸化。发明人发现在无应激的情况下(在其中细胞不表达ppp1r15a的条件下),用实施例1的化合物处理细胞诱导eif2α磷酸化。这在加入实施例1的化合物后1小时和7.5小时之间出现。然而,在加入实施例1的化合物后10小时,eif2α磷酸化恢复至基线水平。这表明在这个时间点存在活性eif2α磷酸酶。实际上,发明人注意到在加入实施例1的化合物后的后期时间点时诱导ppp1r15a(参见测定3)。eif2α磷酸化的瞬时诱导表明该化合物是细胞中的ppp1r15b的选择性抑制剂。此外,这确立了实施例1的化合物提供ppp1r15a。这一测定可用于鉴定其它选择性ppp1r15b抑制剂。
测定3:选择性ppp1r15b抑制剂诱导细胞中ppp1r15a的表达(图2a和b)
细胞和生物体通常具有缺陷补偿机制。因此发明人考虑细胞是否可通过诱导ppp1r15a来补偿ppp1r15b抑制。以前已经报道了ppp1r15b敲除小鼠的肝脏中的ppp1r15a水平提高(harding等人,proc.natl.acad.sci.u.s.a.,106,1832-1837,2009)。尚不清楚这种补偿响应是否是肝脏特异性的,或者它是否可发生在细胞或其它组织中。此外,在这一研究之前,不知道ppp1r15a诱导是否可在ppp1r15b的药理抑制时观察到,因为它们在这一研究之前不是ppp1r15b的选择性抑制剂。
图2b展示发现用实施例1的化合物处理的细胞诱导ppp1r15a。诱导ppp1r15a的这一特性可用作筛选ppp1r15b抑制剂的方法,因为诱导细胞中的ppp1r15a表达的化合物将具有ppp1r15b抑制特性。例如,可在hts筛选中设计并开发利用融合到报告基因的ppp1r15a基因或启动子的测定,用于鉴定诱导ppp1r15a的化合物。
测定4:选择性ppp1r15b抑制剂保护细胞免于应激(图3)
图3展示选择性ppp1r15b抑制剂保护细胞免于应激。使用衣霉素(2.5ug/ml),在存在0.2-5μm实施例1的化合物的情况下应激细胞。在处理后3天测量细胞成活力。
实施例1的抑制剂保护细胞免于衣霉素引起的细胞毒性应激。抗er应激的细胞保护作用可通过合适的测定进行测量。在此情况下,测量海拉细胞中的细胞保护作用,其中通过加入包含衣霉素(一种阻断n-糖基化的药物)的培养基引起er应激,从而阻止蛋白质折叠并诱导未折叠蛋白反应。随后在一组时间段后,利用来自dojindo的标准细胞成活力试剂盒cellviabilitycountingkit-8,通过测量wst-8还原成甲臜的情况,在存在和不存在实施例1的化合物的情况下检测细胞成活力。er应激的细胞保护作用根据在er应激后存活细胞的百分比增加(相对于对照)进行测量。
测定5:选择性ppp1r15b抑制剂在应激恢复期间延长eif2a磷酸化(图4)
发明人推断ppp1r15b抑制剂将在应激后延长eif2α磷酸化。为了揭示这种活性,寻找其中不表达ppp1r15a的条件以避免混杂效应是至关重要的。发明人利用dtt的应激诱导的快速动力学和可逆性(bertolotti等人,nat.cell.biol.,2,326-332,2000;jousse等人,2003)并且在用1mmdtt处理30分钟并洗脱后监测细胞中的eif2α磷酸化。发明人发现通常发生在dtt洗脱后的eif2α磷酸化的下降延迟了,并且这发生在任何显著的ppp1r15a诱导之前。因此,在应激恢复示例(如本文所述的应激恢复)的早期对eif2α去磷酸化动力学的仔细监测可用于鉴定其它ppp1r15b抑制剂。
小鼠中实施例1的化合物(图5)具有良好的组织分布
在口服强饲实施例1的化合物后的不同时间分析小鼠组织(血浆、脑、脊髓、胰腺、肝脏)揭示ppp1r15b抑制剂具有广泛的组织分布,并且因此展示在治疗影响不同器官的各种疾病和障碍中的应用。
用实施例1的化合物处理小鼠对小鼠无毒性(图6)
用实施例1处理小鼠并密切监测以检测任何临床征象。发现用多达10mg/mg实施例1的化合物每天处理一次,持续2周的小鼠与用安慰剂处理的小鼠无法区分,并且小鼠体重正常增加(图6)。这确定ppp1r15b抑制无毒性。这是令人惊讶的且未预料到的,因为在这一研究之前推测ppp1r15b抑制剂将是有毒性的,使得它们将不具有治疗潜力。
用实施例1的化合物处理小鼠不引起由胍那苄引起的副作用(图7)
在人中,胍那苄的肾上腺素能激动剂活性具有副作用,包括在高剂量下的嗜睡和昏迷(a.h.hall,anninternmed102;787–788;1985)。由于这些副作用,胍那苄不再用于人。预测胍那苄衍生物具有胍那苄的副作用,其与α-2肾上腺素能活性相关联。虽然胍那苄与α-2肾上腺素能受体的结构活性关系不可用,发明人发现本文实施例1无胍那苄的副作用,尽管结构上非常相似。
测定6:在用实施例1的化合物处理后,在哺乳动物中诱导ppp1r15a(图8)
通过qpcr,对从用指示剂量的实施例1的化合物处理过的小鼠脑中提取的总mrna评估ppp1r15a诱导。
类似于已在细胞中观察到的,发现在用实施例1的化合物处理后小鼠诱导ppp1r15a,并且这种诱导是剂量依赖性的。这解释了为什么小鼠耐受选择性ppp1r15b抑制剂:ppp1r15a诱导将eif2α去磷酸化,确保由实施例1的化合物引起的ppp1r15b抑制导致的eif2α磷酸化仅仅是瞬时的。这是重要的,因为eif2α的持续磷酸化是有害的。ppp1r15b抑制剂的体内ppp1r15a诱导是一种药效动力学参数,其可用于在临床前研究或临床研究中评估哺乳动物中的ppp1r15b抑制剂的功效和效能。
实施例1的化合物预防哺乳动物中的疾病(图9)
通过抑制ppp1r15b增加折叠具有有益于非常广泛的人类病理的潜力。为了测试这个观点,发明人研究了亨廷顿氏病(huntington’sdisease,hd),一种蛋白内稳态疾病,其由错误折叠蛋白(突变亨廷顿蛋白)的积聚引起。有一些报道指出突变亨廷顿蛋白诱导upr(duennwald和lindquist,gene&development,22,3308-3319,2008;nishitoh等人,genes&development,16,1345-1355,2002)。然而,发明人未能在亨廷顿氏病模型中检测到ppp1r15a,表明ppp1r15a不是hd的治疗靶点。因为hd迄今无治愈方法,发明人测试是否hd可通过ppp1r15b抑制进行预防。发明人发现用2mg/kg实施例1的化合物处理hd小鼠预防运动能力损害(图9)。这证明ppp1r15b是有效的治疗靶点,并且因此ppp1r15b抑制可用于治疗并预防疾病。
如本文所示,为了测定是否一种疾病能够通过ppp1r15b抑制进行预防或改善,小鼠模型或人类可用耐受剂量的抑制剂进行治疗。为了证明体内的靶点抑制,可监测ppp1r15b途径的标记物并将其用作药效动力学标记物。此类标记物可为如本文所示的ppp1r15a(图8)或任何其它途径上的靶点,例如upr或isr标记物(包括但不限于eif2α磷酸化、chop、atf4)。如本文用实施例1的化合物所示,只要它是安全的,ppp1r15b抑制剂可用于治疗,并且这通过化合物对ppp1r15b的选择性进行测定。
在神经病变小鼠的外植体中的髓鞘形成(图10)
cmt是一类髓鞘神经病变,其由多个基因的突变引起。在外周髓鞘蛋白pmp22中的突变是cmt最常见的起因。pmp22(trembler-j)中的突变引起pmp22的错误折叠以及小鼠中的疾病,其类似于人的cmt,这是由于外周神经系统中的髓鞘质缺陷引起。来自pmp22突变小鼠的外植体重现了人类疾病中观察到的严重的髓鞘形成减少。发明人发现来自pmp22突变小鼠的背根神经节培养物(drg)的治疗改善髓鞘形成。以前已经发现来自突变小鼠的drg培养物是可用于预测化合物的治疗功效的模型。因此,此处提供的数据表明实施例1的化合物可用于治疗由pmp22的突变或过度产生引起的疾病,例如cmt疾病。实施例1的化合物也可用于治疗其它髓鞘障碍。
评估对代谢疾病的ppp1r15b功效(图11)
已知代谢疾病如糖尿病、肥胖症、脂肪性肝病和动脉粥样硬化与病理er应激相关联,并且据信upr的药理调节剂可具有治疗益处。因为在这一研究之前不存在可用的ppp1r15b抑制剂,不清楚是否ppp1r15b可为代谢疾病中的治疗靶点。发明人测试了这种可能性并且发现用实施例1的化合物治疗肥胖小鼠减少了这些哺乳动物中的病理高血糖(图11)。这表明用实施例1的化合物进行治疗能够改善代谢障碍。
在一个疾病模型中已经示出用实施例1的化合物进行治疗是有益的,明显的是本发明的化合物将有益于其它哺乳动物代谢障碍,如糖尿病、肥胖症、脂肪性肝病和动脉粥样硬化。
实施例b
可逆磷酸化控制大多数蛋白的活性。因为仅有一些偶然发现的丝氨酸/苏氨酸磷酸酶抑制剂,仍旧认为酶的这个大家族是无药可靶向的。这里使用表面等离子共振设计一种方法,其能够理性发现tst3(如实施例1所提出的化合物),一种ppp1r15b(蛋白磷酸酶1的调节亚基)的选择性抑制剂。ppp1r15b的选择性抑制引起其磷酸化底物快速且瞬时的积聚,该底物是翻译起始因子2的α亚基(eif2α)。这导致快速且瞬时的蛋白合成减少,这是一种治疗学上用以安全预防典型的蛋白错误折叠疾病亨廷顿氏病的小鼠模型中的行为和分子缺陷的特性。这确定丝氨酸/苏氨酸磷酸酶固有无序的调节亚基是有效且易利用的药物靶点,并且提供用于鉴定它们的选择性抑制剂的通用方法。
为了生存,细胞通过磷酸化在丝氨酸51上的真核细胞翻译起始因子2的α亚基eif2α以减少蛋白合成,对严酷条件产生响应,从而调动资源以应对挑战(1-3)。eif2α磷酸化的动态微调是至关重要的,并且eif2α磷酸化过度或不足都是有害的(4)。为了防止eif2α的持续磷酸化,哺乳动物已经进化出两种选择性eif2α磷酸酶,其由结合催化亚基pp1c的一个或两个调节亚基(诱导型ppp1r15a(r15a)或组成型ppp1r15b(r15b))构成(5,6)。已经偶然鉴定了r15a抑制剂并且提供了以下概念验证:丝氨酸-苏氨酸磷酸酶可通过靶向调节亚基而被选择性抑制(7,8)。虽然理论上可利用相同模式以选择性抑制任何其它pp1全磷酸酶,磷酸酶的固有无序调节亚基的选择性抑制剂的理性发现是一个未解决的挑战。
这里提出开发一种通用策略以鉴定新的选择性磷酸酶抑制剂。首先,表达并纯化r15a和r15b(图12)并利用表面等离子共振(spr)测量已知r15a抑制剂对它们的靶点的结合亲和力。尝试将r15固定在spr芯片上,但是这种方法产生不一致的结果,这可能是因为天然非结构化的蛋白沉积在芯片上。因此使用生物素化的胍那苄(gbz)(7),将其固定在芯片上并测试蛋白与固定化合物的结合(图13a和13b)。发现已知r15a抑制剂gbz与重组r15a片段的结合的亲和力是与r15b结合的十倍(图13和14),证实它对r15a的选择性(7)。然而,gbz对r15a的11μm亲和力与细胞中gbz的亚微摩尔效力不相符(7),指示此处使用的测定法未重现细胞条件,这可能因为分离的调节亚基是固有无序的(9)。
因此设计了另一种试验以避免用分离的调节亚基遇到的问题。
在细胞中,磷酸酶的调节亚基在结合pp1c(9)时折叠,表明可能需要全磷酸酶以设计相关测定法。使用体内生物素化的pp1c和已知结合gbz(7)和sephin1(8)的大r15a片段(氨基酸325-636)重构了重组r15a-pp1c。通过在中和亲和素树脂上的亲和捕获纯化r15a-pp1c复合物(图15)。同样地,纯化了平行同源的全磷酸酶r15b-pp1c(图15)。注意,r15a和r15b是功能相关的,但是具有差异很大的序列(图16)。r15-pp1c全磷酸酶随后通过两步固定在spr链亲和素传感器芯片上(图17)。spr实验显示gbz和sephin1强结合r15a-pp1c,但是不结合或弱结合r15b-pp1c(图18-22),并且不单独结合pp1c(图18-22),证实它们对r15a的选择性。测得的gbz和sephin1对r15a-pp1c的稳态亲和力分别为0.122μm和0.786μm,与在基于细胞的测定法(7)和体内(8)的抑制剂亚微摩尔效力相符。因此,用重组全磷酸酶进行的spr实验提供定量方法以测量已知抑制剂对r15a的相关结合亲和力。
接下来使用本文建立的方法寻找具有新特性的选择性磷酸酶抑制剂。合成gbz衍生物并鉴定tst3(全磷酸酶的理性抑制剂),它是一种强且选择性结合r15b(kd=0.033μm)的化合物(图24)。
也测量salubrinal(sal003)的结合亲和力,它是一种已知的r15a和r15b抑制剂,并且发现它结合r15a、r15b以及pp1(图23),亲和力>20μm(图25)。
随后在酶测定法中确认tst3不抑制pp1(图26),然后在细胞中表征。在基础条件下,gbz不如预期的那样影响eif2α磷酸化或翻译速率,因为ppp1r15a在无应激的情况下不表达(5,7)。与gbz相比,tst3快速并瞬时增加eif2α磷酸化(图27)。翻译速率平行于eif2α磷酸化,并且tst3快速且瞬时地减少翻译(图28)。编码atf4和r15a的转录物不发生由于eif2α磷酸化导致的一般翻译减少(10,11)。tst3诱导atf4和r15a表达(图27)。值得注意的是,r15a表达与在加入tst3后10小时观察到的翻译恢复一致(图27,28)。这表明r15a介导tst3处理细胞中的eif2α去磷酸化和翻译恢复,说明tst3是一种选择性r15b-pp1c抑制剂。
如果这样,在不存在r15a的情况下tst3应导致eif2α的持续磷酸化和蛋白合成的持续抑制。实际上,在存在r15a抑制剂gbz的情况下或在r15a基因失活时,持续导致tst3-诱导的eif2α磷酸化和翻译的减少。重要的是,tst3对eif2α磷酸化和翻译的所有可测量的效应在r15b-/-细胞中不存在(图31-32)。这证明tst3是r15b的选择性抑制剂。r15b的选择性抑制引起eif2α的瞬时磷酸化和蛋白合成的瞬时减少。
本文所述的测定法的组合限定了r15抑制剂的活性。如上文所示(7),选择性r15a抑制剂在非应激细胞中不影响翻译或eif2a磷酸化。相比之下,本文显示选择性r15b抑制剂在无应激的情况下瞬时诱导eif2a磷酸化。这是因为r15a受到选择性r15b抑制剂的诱导。r15a和r15b抑制剂的组合限定r15a/b抑制剂的活性:r15a/b抑制剂诱导细胞中蛋白合成的持续抑制。它也诱导atf4,证实它的中靶效应。
这里已经描述了一种能够发现tst3的方法,它是一种组成型eif2α磷酸酶r15b的选择性抑制剂,并且因此证明理性的药物发现可应用于磷酸酶固有无序的调节亚基。r15b的选择性抑制导致蛋白合成的瞬时减少,这是一种治疗学上用以安全预防小鼠hd的特性。选择性r15b抑制剂如tst3可用于治疗由蛋白错误折叠导致的各种疾病。此外,本文提供的方法在原则上可推广到其它磷酸酶以及固有无序的蛋白,为发现药物创造了新且广泛的机会。所述方法概述于卡通图33中。
材料和方法
蛋白表达和纯化
如前文所述表达并纯化mbp-r15a325-636-his和mbp-r15b340-698-his(das等人,(2015)science348,239–242)。将编码人pp1γ的cdna克隆进杆状病毒转移载体pdw464以添加n-末端生物素受体肽(bap)。该载体也编码大肠杆菌生物素全酶合成酶(bira),以使bap-标记的蛋白可在草地贪夜蛾(sf9)昆虫细胞中,进行体内生物素化(bio-pp1c)(duffy等人,(1998)anal.biochem.262,122–128)。bac-to-bac杆状病毒表达系统(thermofisherscientific)用于产生重组杆粒dna,并且sf9昆虫细胞用于扩增病毒原种。使用sf9昆虫细胞在insect-xpress培养基(lonza)中产生蛋白。bio-pp1通过阴离子交换色谱,在hitrapqhp柱(gehealthcare)上进行纯化,随后通过凝胶过滤(hiload16/600superdex200柱,gehealthcare)纯化。所述蛋白在用instantblue(expedeon)染色的boltsds-page4-12%bis-tris凝胶(thermofisherscientific)上分析,并且通过利用pierc高敏感链亲和素-hrp抗体(thermofisherscientific)的蛋白质印迹确认生物素化的pp1的存在。这产生部分纯化的蛋白,由于生物素对链亲和素的高亲和力和特异性(在spr芯片上),完全纯化在后期实现。
r15与bio-pp1c的结合
部分纯化的bio-pp1c(100μl)在ip缓冲液(50mmtrisph7.5,100mmnacl,0.1mmegta,0.05%tween20,0.1%np40)中,在中和亲和素琼脂糖小珠(thermofisherscientific)上振荡孵育2小时,温度为4℃。小珠随后用ip缓冲液洗涤三次,并且在存在或不存在10μmr15(a或b)的情况下,在ip缓冲液中振荡孵育过夜,温度为4℃。小珠随后用ip缓冲液洗涤三次,并且通过在60μllaemmli缓冲液中煮沸来洗脱结合的蛋白。结合蛋白随后在用instantblue(expedeon)染色的boltsds-page4-12%bis-tris凝胶(thermofisherscientific)上分析。通过利用pierc高敏感链亲和素-hrp抗体(thermofisherscientific)的蛋白质印迹确认生物素化的pp1c的存在。
表面等离子共振(spr)
在sa传感器芯片上捕集bio-gbz或bio–pp1c
biacoret200(gehealthcare)系统用于所有实验,并且生物素化的gbz(bio-gbz)(tsaylter2011)或bio-pp1在传感器芯片sa(gehealthcare)上捕集。链亲和素涂覆的表面通过用50mmnaoh和1mnacl的溶液以10μl/min的流速注射1分钟,重复三次进行活化。bio-gbz或bio–pp1c在运行缓冲液(50mmtrisph7.5,100mmnacl,0.1mmegta,0.05%tween20,0.1%dmso)中稀释并以10μl/min的流速直接注射到链亲和素涂覆的表面,浓度大约300nm,达到分别对应于~200和6000ru的bio-gbz或bio–pp1c固定水平。对一个sa传感器芯片表面进行空白固定,用作参考。
使用bio-pp1c表面测定小分子与r15全磷酸酶复合物的稳态结合常数
在所有结合实验中使用仅有微小偏差的相同程序和条件。小分子以在100%dmso中的50mm原液形式储存。在测定结合常数前,在96-孔板中在运行缓冲液中制备连续稀释的12个或8个浓度的化合物。在每个化合物稀释系列之前,在运行缓冲液中将调节亚基mbp-r15a325-636-his或mbp-r15b340-698-his稀释至10μm,并以30μl/min的流速在bio-pp1c表面上捕集1分钟,从而在传感器芯片表面上形成全磷酸酶复合物。此后进行1分钟的稳定以洗脱任何非特异性的结合。随后,不再生表面,以30μl/min的流速将化合物稀释系列注射到芯片表面上,持续1分钟,随后进行2分钟的解离。在每个稀释系列后,使用3mnacl再生表面90秒。在再生后,spr响应通常回到基线水平,并且bio-pp1c表面为下一个化合物稀释系列准备就绪。为了能修正样品间dmso浓度的微小差异,每50个循环注入范围为0.06至8%的dmso的八个溶剂样品。流动细胞温度为10℃。
数据分析
使用biacoret200评估软件分析传感图,和基于稳态模型测定结合常数。使用不同浓度的化合物进行动力学实验,并测定其相应平衡结合水平。这些平衡响应水平(req)对浓度作图并使用全局拟合进行拟合,其能够测定稳态亲和常数,即,在50%饱和度下的浓度为kd(如上文的frostell-karlsson(2000))。
pp1c催化活性测定
纯化的pp1c(30nm)在具有指示浓度的calyculina、gbz、sal003、sephin1和tst3的50mmtrisph7,1.5mmegta,3mmmncl2,0.01%brij-35,0.15%β-巯基乙醇中孵育30分钟,温度为4℃。然后使用enzchekphosphataseassaykit(thermofisherscientific),根据供应商的说明书测量pp1c的残留活性。
哺乳动物细胞培养
在补充有青霉素、链霉素、谷氨酰胺和10%胎牛血清(fbs)的达尔伯克改良伊格尔培养基(dulbecco’smodifiedeagle’smedia,dmem)中培养海拉细胞。ppp1r15a-/-和ppp1r15b-/-mef细胞在补充有青霉素、链霉素、谷氨酰胺、55μmβ-巯基乙醇、1x非必需氨基酸(sigma)和10%fbs的dmem中培养。
蛋白免疫印迹分析
将细胞(90,000个细胞/ml)铺于24-孔板中并按照指示处理。在处理结束时,在150μllaemmli缓冲液中裂解细胞。溶胞产物在95℃下煮沸5分钟,用超声波处理并在4-12%boltbis-trisplusgels(thermofisherscientific)上分离。利用iblot2系统(thermofisherscientific)将蛋白转移到硝化纤维素膜上,并且使用以下抗体进行分析:e-if2α-p(44-728g,thermofisherscientific,1:1000)、e-if2α(ab5369,abcam,1:1000)、微管蛋白(t5168,sigma-aldrich,1:4000)、bip(610978,bdbiosciencespharmingen,1:1000)、atf4(sc-200,santacruzbiotechnology,1:500)、ppp1r15a(10449-1-ap,proteintech,1:1000)和ppp1r15b(14634-1-ap,proteintech,1:1000)。使用eclprime(gehealthcare)可视化蛋白。
评估翻译速率
将细胞(90,000个细胞/ml)铺于12-孔板中,根据指示处理,用100μci/ml35s-甲硫氨酸(hartmannanalytic)在37℃下标记10分钟,用冰冷的pbs洗涤并在120μllaemmli缓冲液中裂解。溶胞产物在95℃下煮沸5分钟,用超声波处理并在4-12%boltbis-trisplusgels(thermofisherscientific)上分离。凝胶随后用instantblue(expedeon)染色并通过磷光成像进行分析。
动物
所有动物护理和程序符合研究动物使用的法规(ukanimalsscientificproceduresactof1986,以及eudirective2010/63/eu)进行,并获得当地伦理委员会的批准。
c57bl/6j雄性小鼠购自thejacksonlaboratory或charlesriver。hd-n171-82q(hd)转基因小鼠购自thejacksonlaboratory并在混合背景下保持(c3h/b6)。
所有小鼠分组饲养(每笼2-3只)在单独通风的笼中,自由给食和饮水,并且保持12小时光/暗循环(7am-7pm)。
药物治疗
tst3或gbz的乙酸盐溶解在水中,并且超声处理10分钟。将溶液等分并保存在-20℃下直至使用。一旦解冻,将管保持在4℃并在24小时内使用。
tst3或gbz通过口服强饲给药,剂量为2mg/kg(除非另外指明)。小鼠单剂量给药或者长期治疗–每天一次。
为了产生试验组,hd-n171-82q转基因雄性小鼠与c3h/b6f1野生型雌性小鼠杂交。4周龄的转基因雄性小鼠和它们的野生型同窝对照雄性小鼠在不同组中随机化,并且用tst3处理4周。
药代动力学研究
药代动力学研究通过xenogesis进行。口服给药tst3于c57bl/6j雄性小鼠。通过用包含甲醇的内部标准沉淀蛋白来制备血浆样品。组织称重并通过均化(与磷酸盐缓冲液1:3)制备,并且用包含甲醇的内部标准沉淀蛋白。在加入甲醇后,血浆和组织样品置于-20℃下≥1小时(或过夜),使蛋白沉淀。随后样品在4℃下,以2,500xg(3,400rpm)下离心20分钟。上清液通过lc-ms/ms分析。
转杆测试
hd-n171-82q转基因雄性小鼠和它们的野生型同窝对照雄性小鼠的tst3处理在4周龄时开始,并且在测试前继续处理4周。在适应阶段,将小鼠置于静止杆上1分钟,随后以固定速度4rpm培训1分钟。重复适应阶段。在三次试验中进行转杆测试。在每次试验中,允许小鼠在加速杆(4至40rpm)上奔跑至多300秒并计算跌落的等待时间。给出三次试验的平均值。
在急性给药tst3后监测运动能力
为了评估处理的gbz-样的副作用(由于肾上腺素能活性),在单次给药tst3后监测小鼠的运动能力。为此小鼠用tst3处理并留在笼中60分钟。每15分钟监测小鼠行为。用gbz类似处理的小鼠用作对照。
统计分析
使用studentt-检验或双因素方差分析(anova)进行比较。在对应的图中指示显著差异。
化合物合成
合成程序:
在25℃下,向2,3-二氯苯甲醛(22.00g,0.12570摩尔)和氨基胍碳酸氢盐(17.1g,0.12570摩尔)在甲醇(220ml)中的悬浮液加入乙酸(22ml)。随后将所得反应混合物在70℃下加热~30分钟。在加热时,悬浮液变得澄清。在使用二氯甲烷/甲醇(8/2)作为流动相的tlc上监测反应完全。在反应完全后,使反应混合物冷却至25℃并在真空下浓缩。所得残余悬浮在乙醚(100ml)中,并且通过过滤收集所得产物。重复这一过程3次。在上述过程结束时,能够得到期望的(e)-2-(2,3-二氯亚苄基)肼-1-甲脒(“tst3)。lc-ms:m/z=231.23(m+h)。所得产物也通过1h-nmr、13c-nmr、电位滴定、hplc和chn分析进行分析。
参考文献
boens,s.,szekér,k.,vaneynde,a.和bollen,m.(2013).interactor-guideddephosphorylationbyproteinphosphatase-1.methodsmol.biol.1053,271–281.
bollen,m.,peti,w.,ragusa,m.j.和beullens,m.(2010).theextendedpp1toolkit:designedtocreatespecificity.trendsbiochem.sci.35,450–458.
boyce,m.,bryant,k.f.,jousse,c.,long,k.,harding,h.p.,scheuner,d.,kaufman,r.j.,ma,d.,coen,d.m.,ron,d.等人(2005).aselectiveinhibitorofeif2alphadephosphorylationprotectscellsfromerstress.science307,935–939.
chen,r.,rato,c.,yan,y.,crespillo-casado,a.,clarke,h.j.,harding,h.p.,marciniak,s.j.,read,r.j.,ron,d.和nelson,w.j.(2015).g-actinprovidessubstrate-specificitytoeukaryoticinitiationfactor2αholophosphatases.science4,e04871.
choy,m.s.,page,r.和peti,w.(2012a).regulationofproteinphosphatase1byintrinsicallydisorderedproteins.biochem.soc.trans.40,969–974.
choy,m.s.,page,r.和peti,w.(2012b).regulationofproteinphosphatase1byintrinsicallydisorderedproteins.biochem.soc.trans.40,969–974.
choy,m.s.,hieke,m.,kumar,g.s.,lewis,g.r.,gonzalez-dewhitt,k.r.,kessler,r.p.,stein,b.j.,hessenberger,m.,nairn,a.c.,peti,w.等人(2014).understandingtheantagonismofretinoblastomaproteindephosphorylationbypnutsprovidesinsightsintothepp1regulatorycode.proceedingsofthenationalacademyofsciences111,4097–4102.
choy,m.s.,yusoff,p.,lee,i.c.,newton,j.c.,goh,c.w.,page,r.,shenolikar,s.和peti,w.(2015).structuralandfunctionalanalysisofthegadd34:pp1eif2αphosphatase.cellreports.
das,i.,krzyzosiak,a.,schneider,k.,wrabetz,l.,d’antonio,m.,barry,n.,sigurdardottir,a.和bertolotti,a.(2015).preventingproteostasisdiseasesbyselectiveinhibitionofaphosphataseregulatorysubunit.science348,239–242.
gilmartin,a.g.,faitg,t.h.,richter,m.,groy,a.,seefeld,m.a.,darcy,m.g.,peng,x.,federowicz,k.,yang,j.,zhang,s.-y.等人(2014).allostericwip1phosphataseinhibitionthroughflap-subdomaininteraction.natchembiol1–10.
harding,h.p.,novoa,i.,zhang,y.,zeng,h.,schapira,m.和ron,d.(2000).regulatedtranslationinitiationcontrolsstress-inducedgeneexpressioninmammaliancells.mol.cell6,1099–1108.
heroes,e.,lesage,b.,
jousse,c.,oyadomari,s.,novoa,i.,lu,p.,zhang,y.,harding,h.p.和ron,d.(2003).inhibitionofaconstitutivetranslationinitiationfactor2alphaphosphatase,crep,promotessurvivalofstressedcells.thejournalofcellbiology163,767–775.
lee,y.y.,cevallos,r.c.和jan,e.(2009).anupstreamopenreadingframeregulatestranslationofgadd34duringcellularstressesthatinduceeif2alphaphosphorylation.j.biol.chem.284,6661–6673.
novoa,i.,zeng,h.,harding,h.p.和ron,d.(2001).feedbackinhibitionoftheunfoldedproteinresponsebygadd34-mediateddephosphorylationofeif2alpha.thejournalofcellbiology153,1011–22.
robert,f.,kapp,l.d.,khan,s.n.,acker,m.g.,kolitz,s.,kazemi,s.,kaufman,r.j.,merrick,w.c.,koromilas,a.e.,lorsch,j.r.等人(2006).initiationofproteinsynthesisbyhepatitiscvirusisrefractorytoreducedeif2.gtp.met-trna(i)(met)ternarycomplexavailability.molecularbiologyofthecell17,4632–4644.
tsaytler,p.和bertolotti,a.(2013).exploitingtheselectivityofproteinphosphatase1forpharmacologicalintervention.febsj.280,766–770.
tsaytler,p.,harding,h.p.,ron,d.和bertolotti,a.(2011).selectiveinhibitionofaregulatorysubunitofproteinphosphatase1restoresproteostasis.science332,91–94.
virshup,d.m.和shenolikar,s.(2009).frompromiscuitytoprecision:proteinphosphatasesgetamakeover.mol.cell33,537–545.
实施例b的参考文献
1.h.p.harding,y.zhang,a.bertolotti,h.q.zeng,d.ron,perkisessentialfortranslationalregulationandcellsurvivalduringtheunfoldedproteinresponse.mol.cell.5,897–904(2000).
2.d.scheuner等人,translationalcontrolisrequiredfortheunfoldedproteinresponseandinvivoglucosehomeostasis.mol.cell.7,1165–1176(2001).
3.h.p.harding等人,anintegratedstressresponseregulatesaminoacidmetabolismandresistancetooxidativestress.mol.cell.11,619–633(2003).
4.g.d.pavitt,d.ron,newinsightsintotranslationalregulationintheendoplasmicreticulumunfoldedproteinresponse.coldspringharborperspectivesinbiology.4,a012278–a012278(2012).
5.i.novoa,h.zeng,h.p.harding,d.ron,feedbackinhibitionoftheunfoldedproteinresponsebygadd34-mediateddephosphorylationofeif2alpha.thejournalofcellbiology.153,1011–22.(2001).
6.c.jousse等人,inhibitionofaconstitutivetranslationinitiationfactor2alphaphosphatase,crep,promotessurvivalofstressedcells.thejournalofcellbiology.163,767–775(2003).
7.p.tsaytler,h.p.harding,d.ron,a.bertolotti,selectiveinhibitionofaregulatorysubunitofproteinphosphatase1restoresproteostasis.science.332,91–94(2011).
8.i.das等人,preventingproteostasisdiseasesbyselectiveinhibitionofaphosphataseregulatorysubunit.science.348,239–242(2015).
9.s.boens,k.szekér,a.vaneynde,m.bollen,interactor-guideddephosphorylationbyproteinphosphatase-1.methodsmol.biol.1053,271–281(2013).
10.h.p.harding等人,regulatedtranslationinitiationcontrolsstress-inducedgeneexpressioninmammaliancells.mol.cell.6,1099–1108(2000).
11.y.y.lee,r.c.cevallos,e.jan,anupstreamopenreadingframeregulatestranslationofgadd34duringcellularstressesthatinduceeif2alphaphosphorylation.j.biol.chem.284,6661–6673(2009).
12.h.p.harding等人,ppp1r15geneknockoutrevealsanessentialrolefortranslationinitiationfactor2alpha(eif2alpha)dephosphorylationinmammaliandevelopment.proc.natl.acad.sci.u.s.a.106,1832–1837(2009).
13.b.abdulkarim等人,amissensemutationinppp1r15bcausesasyndromeincludingdiabetes,shortstatureandmicrocephaly.diabetes,db150477(2015).
14.s.jazcilevich,
15.m.costa-mattioli等人,eif2alphaphosphorylationbidirectionallyregulatestheswitchfromshort-tolong-termsynapticplasticityandmemory.cell.129,195–206(2007).
16.e.t.powers,r.i.morimoto,a.dillin,j.w.kelly,w.e.balch,biologicalandchemicalapproachestodiseasesofproteostasisdeficiency.annu.rev.biochem.78,959–991(2009).
17.g.schilling等人,intranuclearinclusionsandneuriticaggregatesintransgenicmiceexpressingamutantn-terminalfragmentofhuntingtin.hum.mol.genet.8,397–407(1999).
- 还没有人留言评论。精彩留言会获得点赞!