一种用于调节白光LED的荧光化合物及其制备方法和应用与流程
本发明属于荧光材料领域,具体涉及一种在紫外光激发下具有红光发射的荧光化合物、制备方法及其应用。
背景技术:
当前能源紧张,节能环保成为了各国关心的大事,一些国家逐渐禁止使用和逐渐淘汰白炽灯,推广节能环保的荧光灯。近十年来,铕、钐、镨、铽等稀土掺杂氮化物、氮氧化物、硅酸盐、铝酸盐等、四价锰离子参杂铝酸盐等的LED发光荧光粉被相继报道。氮氧化物、氮化物的制备条件通常比较苛刻,需要高温,高压等特殊条件,这些条件对设备的要求很高,从而提高了荧光粉的价格。所以对植被简单易行的红色荧光粉的研究具有重要意义。
目前商用的二基色白光LED主要是采用蓝光InGaN芯片激发Y3AlO12:Ce3+(YAG:Ce3+)黄色荧光粉。由于缺少红色荧光粉使其在红色光谱区发光较弱,从而导致其色温偏高,显色指数偏低。为了解决这个局限,二基色中加入可在蓝光激发的红色荧光粉,从而形成三基色的白光LED。
技术实现要素:
发明目的:为了克服现有技术中存在的不足,本发明提供了一种简易且价格合理的用于调节白光LED的荧光化合物及其制备方法和应用,该荧光化合物在紫外光激发下具有红光发射的特性,通过有机小分子与过渡金属盐的结合,以制备可以作荧光材料使用的化合物,使得制备工艺简单、易操作。
技术方案:为实现上述目的,本发明采用以下技术方案:
一种用于调节白光LED的荧光化合物,所述荧光化合物的化学式为C8H18N2Br3Mn0.5。
进一步地,所述荧光化合物在296K温度下,晶体属于三方晶系,Pa-3空间群。
本发明进一步提出了上述荧光化合物的制备方法,包括如下步骤:在常温下,将含Mn2+的可溶性盐与三乙烯二胺衍生物分别放入反应器中,以10-15ml/min的速率加入蒸馏水搅拌溶解,然后再将两反应器中的溶液相互融合,搅拌均匀后,室温下静置若干天,优选地,静置7天,即得到化合物C8H18N2Br3Mn0.5,整个反应中反应物的摩尔比与蒸馏水的用量对化合物的合成有一定的影响,控制反应物的摩尔比,可以提高产物的纯度;控制蒸馏水的用量,可以提高反应的速率。
具体地,所述含Mn2+的可溶性盐为溴化锰过渡金属盐。
所述三乙烯二胺衍生物为二溴1,4-二甲基-1,4-二氮杂二环[2.2.2]辛烷。
优选地,所述含Mn2+的可溶性盐与三乙烯二胺衍生物的摩尔比为1~3∶1。
更为优选地,所述含Mn2+的可溶性盐与三乙烯二胺衍生物的物质的量的比为1∶1,蒸馏水的用量为每1mol含Mn2+的可溶性盐加入1~1.5mL蒸馏水。
本发明还提出了所述的红色荧光化合物在白光LED灯,彩色灯等中的应用。
有益效果:与现有技术相比,本发明具有以下优点:
(1)本发明的红色荧光化合物,属于分子离子基范畴,热分解温度点相对较高,晶体颗粒均匀;
(2)本发明提供的制备方法是在室温条件下,通过溶液自然挥发溶剂自组装合成,材料结构稳定性较高,且本化合物的结构可控性较强、产率高以及重复性好,制备方法简单,易操作,所采用的原料来源充足、生产成本低;
(3)本发明提出的荧光化合物,在调配白光LED灯,彩色灯等中有着许多的应用。
附图说明
图1为本发明荧光化合物C8H18N2Br3Mn0.5的合成路线图;
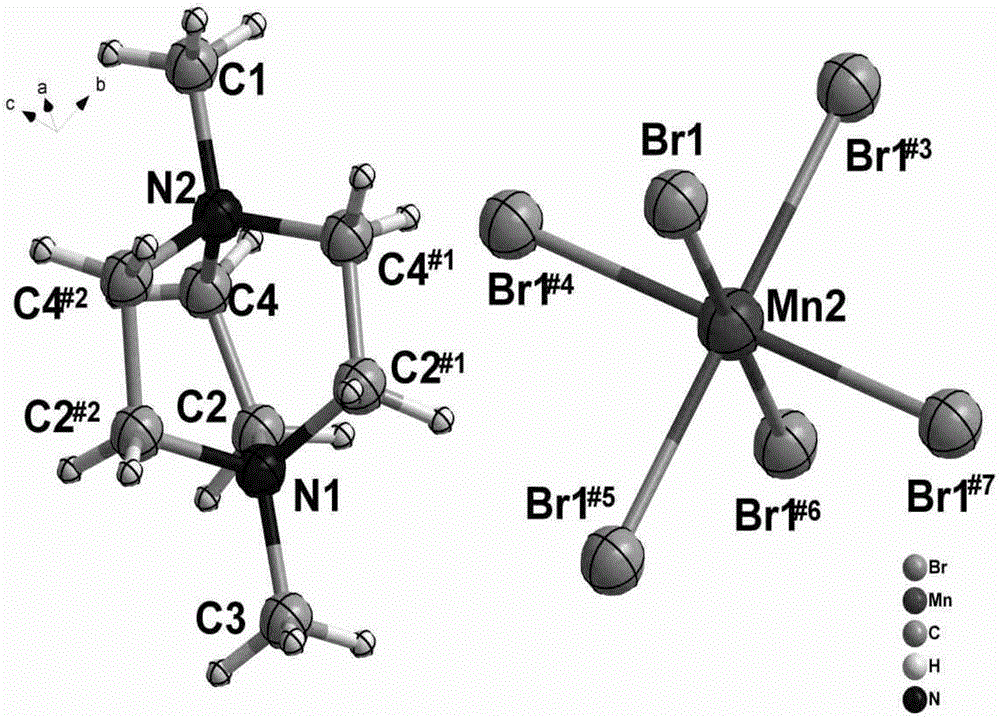
图2为实施例1中荧光化合物C8H18N2Br3Mn0.5在296K温度下的晶胞图;
图3为实施例1中荧光化合物C8H18N2Br3Mn0.5的红外谱图;
图4为实施例1中荧光化合物C8H18N2Br3Mn0.5的粉末PXRD衍射图;
图5为实施例1中荧光化合物C8H18N2Br3Mn0.5的热重TGA分析图;
图6为实施例1中荧光化合物C8H18N2Br3Mn0.5的荧光发射图;
图7为实施例1中荧光化合物C8H18N2Br3Mn0.5的荧光寿命图。
具体实施方式
下面结合附图和实施例对本发明进一步解释说明。
图1为本发明化合物C8H18N2Br3Mn0.5的合成路线图。实施例1-4依据此合成路线制备该荧光化合物。
实施例1
在常温下,分别将10mmol溴化锰与10mmol二溴1,4-二甲基-1,4-二氮杂二环[2.2.2]辛烷放入烧杯中,以10ml/min的速率缓慢加入蒸馏水搅拌溶解,蒸馏水的体积分别为10mL,然后再将两烧杯溶液相互融合,搅拌均匀后,室温下静置7天,即得到所述具有荧光性质的化合物C8H18N2Br3Mn0.5。
实施例2
在常温下,分别将20mmol溴化锰与10mmol二溴1,4-二甲基-1,4-二氮杂二环[2.2.2]辛烷放入烧杯中,以15ml/min的速率缓慢加入蒸馏水搅拌溶解,蒸馏水的体积分别为10mL,然后再将两烧杯溶液相互融合,搅拌均匀后,室温下静置7天,即得到所述具有荧光性质的化合物C8H18N2Br3Mn0.5。
实施例3
在常温下,分别将30mmol溴化锰与10mmol二溴1,4-二甲基-1,4-二氮杂二环[2.2.2]辛烷放入烧杯中,缓慢加入蒸馏水搅拌溶解,蒸馏水的体积分别为10mL,然后再将两烧杯溶液相互融合,搅拌均匀后,室温下静置一段时间,即得到所述具有荧光性质的化合物C8H18N2Br3Mn0.5。
实施例4
在常温下,分别将10mmol溴化锰与10mmol二溴1,4-二甲基-1,4-二氮杂二环[2.2.2]辛烷放入烧杯中,以15ml/min的速率缓慢加入蒸馏水搅拌溶解,蒸馏水的体积分别为15mL,然后再将两烧杯溶液相互融合,搅拌均匀后,室温下静置一段时间,即得到所述具有荧光性质的化合物C8H18N2Br3Mn0.5。
对实施例1所制备的荧光化合物晶体进行分析,在显微镜下选取合适大小的单晶,室温时用经石墨单色化的Mo Kα射线在Bruker Apex II CCD衍射仪上测定单晶的X射线衍射结构,该荧光化合物的晶体学参数结果见表1。用SADABS方法进行半经验吸收校正,晶胞参数用最小二乘法确定,数据还原和结构解析分别使用SAINT和SHELXL程序包完成,所有非氢原子用全矩阵最小二乘法进行各向异性精修,化合物的单胞图如图2所示。在296K条件下(图2),Mn原子处于扭曲的八面体环境中,分别与六个溴原子配位;修饰后的三乙烯二胺环处于扭曲的状态。其中,对称码为:#11+x,y,z-1;#2x,1+y,z-1;#3x+1/2,3/2-y,1-z;#41+x,1/2-y,z-1/2,#51/2-x,1/2+y,z-1;#6-x,1-y,2-z;#71-x,y-1/2,3/2-z.
表1 化合物的晶体学数据
对实施例1中的化合物的红外光谱表征,如图3所示。在3384cm-1处,有一个强烈的吸收峰,是三乙烯二胺衍生物上C-H单键的伸缩振动吸收峰;在3022cm-1有一个强烈的吸收峰,是-CH3吸收峰。
图4为对实施例1中的化合物的PXRD分析表征,从粉末PXRD衍射图可以看出,模拟衍射峰与实际实验测得衍射峰对比的很好,说明了该化合物有着很高的相纯度。
图5为对实施例1中的化合物的热重分析表征,从热重分析中可以看出,化合物有着很高的稳定性。从图5中可以看出,在200℃左右,化合物中金属八面体配位模式发生分解;在300℃左右,化合物中有机骨架开始分解;在400℃之后,化合物中坍塌完毕剩下质量为金属的氧化物。
采用Spectrofluorometer FS5荧光测试仪对实施例1中的化合物进行荧光性能研究。这种化合物的荧光发射光谱图如图6所示。从图6中发现,在激发波长为378mm,发射波长为670mm,发光范围在红光范围内。
实施例1中制备的荧光化合物的荧光衰减曲线如图7所示,监测波长为670mm,激发波长为378mm。通过计算得出,衰减时间t1=0.36ns,x2=1.305.
以上描述是用于实施本发明的一些最佳模式和其他实施方式,只是对本发明的技术构思起到说明示例作用,并不能以此限制本发明的保护范围,本领域技术人员在不脱离本发明技术方案的精神和范围内,进行修改和等同替换,均应落在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!
- 化合物及使用其的有机电激发光组件的制作方法与工艺
- 一种烟草中倍半萜类化合物的测定方法与流程
- 对有机含磷化合物有毒气体具有荧光响应的一维有机半导体纳米线/带及其制备方法和应用与流程
- 一种用于调节白光LED的荧光化合物及其制备方法和应用与流程
- 联咔唑化合物、光固化性组合物、其固化物、用于塑料透镜的固化性组合物和塑料透镜的制作方法与工艺
- 联咔唑化合物、光固化性组合物、其固化物、用于塑料透镜的固化性组合物和塑料透镜的制作方法与工艺
- 一种基于π‑π堆积化合物的荧光材料及其制备方法与流程
- 一种有机电致荧光化合物及其在电致发光器件中的应用的制作方法与工艺
- 一种有机电致荧光化合物及其在电致发光器件中的应用的制作方法与工艺
- 一种有机荧光化合物及其应用的制作方法与工艺