膜制造方法与流程
本发明涉及膜制造方法。具体地,其涉及水过滤膜制造方法。
背景技术:
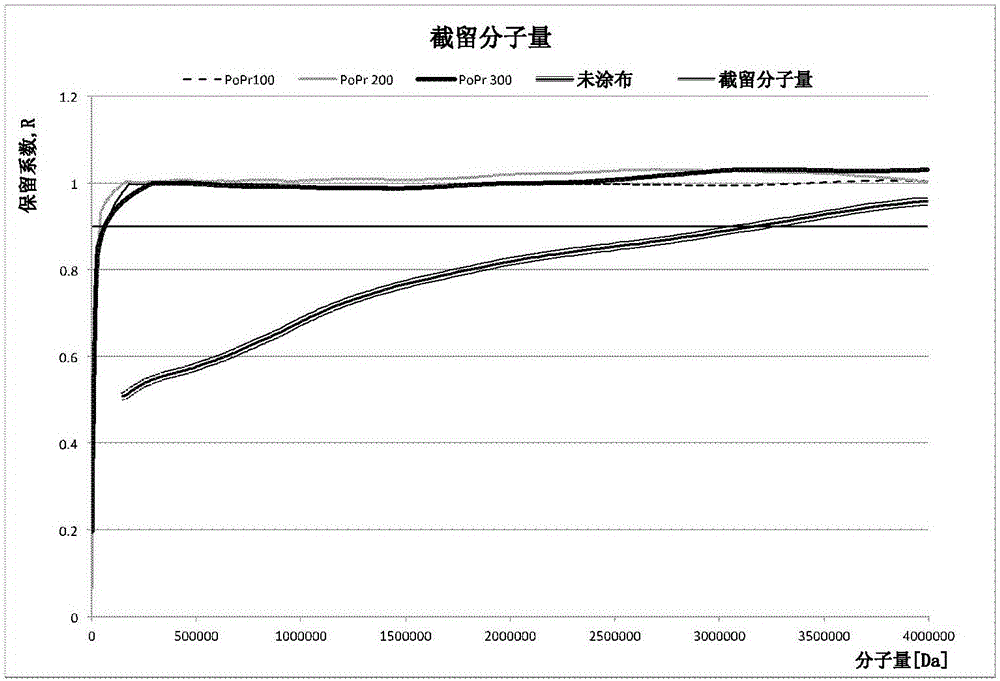
:传统的纳米过滤或反渗透水过滤膜已知晓数十年。典型地,其通过以下方法制造:浇铸载体膜(常为聚砜或聚醚砜);将产生的浇铸物浸入在二胺水溶液中;从膜表面除去过量的水溶液;将膜浸入在三官能酰基卤有机溶液中;和使产生的产品固化,产生聚酰胺层。然后,如果必要,进行洗涤和二次涂覆。由WO01/32146已知,膜蛋白可以并入到由两亲性ABA嵌段共聚物制成的囊泡的壁中。该文献包括大量聚合物性质的讨论,并公开道聚合物可以在两个链端处均具有可聚合基团。这些可聚合基团可以在形成自组装囊泡之后聚合,聚合仅发生在囊泡内。WO2004/011600公开道,水通道蛋白可以并入到三嵌段共聚物中,以形成仅通过水、排除所有污染物的膜。由于这些公开,进行了大量工作来开发商业上可行的并入跨膜蛋白的膜,特别是基于水通道蛋白的水过滤膜。挑战之处在于产生物理上足够结实到承受必需条件的工作膜。WO2009/076174描述了一种制备基于嵌段共聚物和水通道蛋白的基本上平的膜的方法。在Dong等人的J.Mem.Sci.2012,409-410,34-43中生成并入有水通道蛋白的嵌段共聚物囊泡,但然后使用囊泡破裂方法破坏囊泡,将聚合物平面单层沉积在载体表面上。WO2010/146365描述了悬浮在油相中以形成液体膜的其中可能嵌有水通道蛋白的囊泡。根据Zhao等人J.MembraneSci.2012,422-428,各种提出的制造水通道蛋白膜的方法包括栓有聚合物的生物层、生物膜孔划分阵列、经由囊泡融合的膜支撑的脂双层和悬浮在膜孔之上的囊泡,但是这些大部分不能承受所要求的高液体静压力。Zhao自己对该问题的解决方案实际上是使用通过向二胺水溶液中加入负载水通道蛋白的脂质囊泡(即脂质体)改良的上述常规膜制备法。结果提供嵌在聚酰胺层中的脂质体。尽管Zhao正面报道了得到的结果,但是从提供的数据很明显发现,尽管得到的水通量有小的增加(图4(a)),但与常规膜相比较,该膜排斥溶质的能力没有提高(图5)。据信这是因为负载水通道蛋白的脂质体变得完全被聚酰胺包围,因此通过膜的主要水通量是经由聚酰胺(即,经由基膜的常规路径),仅仅部分地通过水通道蛋白通道。同样来自Zhao等人的WO2013/043118描述了相同的技术,并且还公开道嵌段共聚物可以用于形成嵌入到聚酰胺层中的含有或不含有水通道蛋白的囊泡。再次,结果清楚地显示获得的水通量经由聚酰胺层,并非专一地经由水通道蛋白通道。Xie等人J.Mater.ChemA,2013,1,7592和WO2013/180659描述了包括以下步骤的方法:(i)将水通道蛋白并入到基于主要(95%)具有甲基丙烯酸酯端基、但另外还有一些(3%)羧酸端基的自组装聚合物囊泡中;(ii)使用UV光使甲基丙烯酸酯端基交联;(iii)将交联的囊泡以分离的囊泡在载体表面上彼此位置隔开的浓度沉积并共价固定化在载体上;和(iv)通过称作“表面印迹”的方法在单个囊泡之间产生聚合物薄层。在该方法中,重要的是,固定化的囊泡的大小使得它们大于印迹聚合物层的厚度,以防止水通道蛋白水通道的堵塞。据称该方法在水过滤过程中表现出高的机械强度和稳定性,但也陈述道,最关键的问题在于,印迹聚合物层不足以致密到防止所有的溶质和水分子渗透。而且,通过这样的系统仅可得到非常有限的流速。因此,对于得到物理上结实且并入跨膜蛋白的膜、特别是使用水通道蛋白有效地作用于水过滤的膜的方法仍有需求。技术实现要素:本发明提供一种过滤膜,其包括多孔载体和在其表面上共价结合的层,该层包括多个并入有跨膜蛋白的囊泡,所述囊泡由两亲性嵌段共聚物形成,其特征在于在所述层内,囊泡共价连接在一起,形成连续体(coherentmass)。层的厚度将大于囊泡的平均直径。按绝对值计,层的厚度适当地为至少0.04微米。本发明进一步提供制备根据本发明的过滤膜的方法,其包括:提供并入有跨膜蛋白的囊泡的含水悬浮液,所述囊泡由具有反应性端基的两亲性嵌段共聚物形成;将所述囊泡悬浮液沉积在多孔载体的表面;和提供反应条件,使得在不同的囊泡之间以及囊泡与所述表面之间形成共价键。优选地,过滤膜是水过滤膜,优选地,跨膜蛋白是水通道蛋白。在本说明书和权利要求书通篇,除非上下文另外要求,任何提及过滤膜应当理解成包括具体提及水过滤膜,任何提及跨膜蛋白应当理解成包括具体提及水通道蛋白。发明详述与上述Xie的方法完全相反,本发明的基本特征在于,载体负载其中多个囊泡紧密堆积在一起的层。层中的堆积可以是例如六方密堆积。载体表面上存在的囊泡层比囊泡的平均直径厚,即,其厚度大于单层囊泡可以提供的厚度。优选地,层的厚度应当等于囊泡平均直径的至少2倍,例如,至少10倍,优选至少50倍,更优选至少150倍,最优选至少200倍。优选地,层不多于囊泡平均直径的500倍,例如,不多于300倍。因此,例如,层的厚度可以是囊泡平均直径的2-500倍,例如,50-300倍,特别是200-300倍。就绝对值而言,囊泡层的厚度优选为至少0.01微米,例如,至少0.04微米,例如,至少0.1微米,例如,至少0.2微米,例如,至少2微米,优选至少10微米,更优选至少30微米,最优选至少40微米。没有特别优选的层最大厚度。例如,层的厚度可以是至多100微米,例如,至多60微米。因此,例如,层的厚度可以是0.01-100微米,例如,0.04-100微米,例如,0.2-100微米,优选10-60微米,特别是40-60微米。为了增加结实性,制成的膜的囊泡层优选地具有保护性顶涂层,或者在载体层的对侧上具有第二载体层。例如,该顶涂层可以在轧制过程中提供额外的针对机械损伤的保护。例如,其可以包括亲水性聚合物,例如聚乙烯醇。本发明的方法可以若干种不同的方式进行。在第一优选实施方式中,提供一种制备根据本发明的膜的方法,其包括:(a)提供并入有跨膜蛋白的囊泡的含水悬浮液,所述囊泡由具有反应性端基X的两亲性嵌段共聚物形成;(b)提供多官能性连接剂,该多官能性连接剂具有至少两种与聚合物端基X具有反应性的反应性基团Y;(c)将所述囊泡悬浮液和所述多官能性连接剂沉积在载体上,该载体具有与聚合物端基X或反应性基团Y具有反应性的表面;和(d)引发端基X与基团Y以及端基X或基团Y与载体表面的反应。在第二优选实施方式中,提供一种制备根据本发明的膜的方法,其包括:(a)提供并入有跨膜蛋白的囊泡的第一含水悬浮液,所述囊泡由具有反应性端基X的两亲性嵌段共聚物形成;(b)提供并入有跨膜蛋白的囊泡的第二含水悬浮液,所述囊泡由具有反应性端基X的两亲性嵌段共聚物形成,该反应性端基X与聚合物端基Y具有反应性;(c)将所述囊泡悬浮液沉积在载体上,该载体具有与聚合物端基X或Y具有反应性的表面;和(d)引发端基X与端基Y以及端基X或端基Y与载体表面的反应。本发明的方法得到物理上结实的、任选地经由连接剂彼此连接并且也与载体表面连接的聚合物囊泡层。本发明中使用的所有嵌段共聚物分子并非必需均具有反应性端基。具有反应性端基的嵌段共聚物分子的比例并非关键,其条件在于有足够多的基团与囊泡第二群体中或多官能性连接剂中的反应性基团反应,以形成连续体。通常,用于形成囊泡的嵌段共聚物分子的至少10%,例如至少20%,例如至少30%,例如至少40%,例如至多60%,或者至多100%将会具有官能性端基X或Y。类似地,不要求仅存在一种类型的端基X或Y。例如,合意的是,可以使用嵌段共聚物的掺合物,一种含有一反应性端基X(1),例如包括-NH2基团的端基,第二种含有不同的反应性端基X(2)。任何具体聚合物分子上的端基可以彼此相同,或者它们可以不同,但优选它们是相同的。例如,一种端基可以是反应性端基X,而另一端基可以是非反应性基团。基团的确切性质当然将会取决于方法的性质,也取决于载体表面的性质。合适的反应性基团包括胺基(例如与羧酸、活化羧酸和/或叠氮基具有反应性)、羧酸、活化羧酸和/或叠氮基(与例如胺基Y具有反应性)和“点击化学”基团(例如叠氮基或炔基,其分别与炔基和叠氮基Y具有反应性)。特别优选使用胺基。许多种基于胺的端基是可用的,这些可以含有–NH2和/或NH基团。已经发现,当提供具有这类端基的两亲性嵌段共聚物时,嵌段共聚物自组装成囊泡的能力提高:这是令人惊异的,因为通常预期最影响囊泡形成的两亲性嵌段共聚物的特性是(i)嵌段的大小和性质;和(ii)聚合物的多分散性。当使用多官能性连接剂时,该试剂中存在的反应性基团可以彼此相同,或者它们可以是不同的。它们必须使得与囊泡中存在的互补性反应性基团和/或与载体表面反应。合适的基团如上文所述。当使用多官能性试剂时,例如,试剂可以含有3或4个反应性基团,但优选地其含有2个反应性基团,并且在本文中任何提及多官能性试剂应当理解成包括具体提及双官能性试剂。在本发明的优选实施方式中,囊泡含有包括胺基的反应性基团;并且提供有互补性反应性基团,其为活化羧酸基团或叠氮基,例如,苯基叠氮基。在本发明一实施方式中,载体表面可以在一个或多个步骤中进行官能化,以引入特定的能够与互补性反应基团X和/或Y反应的反应性基团Z。合适的基团包括胺基(例如与羧酸或活化羧酸基团X和/或Y具有反应性);羧酸或活化羧酸基团(例如与胺基X和/或Y具有反应性);和“点击化学”基团(例如与炔基或叠氮基X和/或Y具有反应性的叠氮基或炔基)。表面多步官能化的一个例子是使用酸例如盐酸水解聚丙烯腈表面,以引入表面羧酸基团,随后可以使用1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(EDC)和N-羟基琥珀酰亚胺(NHS)将其活化,然后使用例如炔丙胺转化成炔基,或者使用例如氨基-三乙二醇-叠氮化物转化成叠氮基。但是,在本发明另一实施方式中,可以没有必要对载体表面进行官能化,因为X和/或Y可以与形成载体的材料中已经存在的基团具有反应性。例如,Y可以是叠氮基:这些基团一经使用UV光激活则具有高度反应性,能够与载体材料中存在的许多聚合物中的C-H键反应。具体地,叠氮基,特别是苯基叠氮基,能够与下文讨论的作为用于本发明的优选载体材料的聚砜共价结合。当提及活化的羧酸基团时,其应当理解成包括任何常规的活化羧酸基团,例如,活化酯,例如N-羟基琥珀酰亚胺酯或酰基卤。这些活化技术是本领域公知的。在优选的实施方式中,活化羧酸端基通过羧酸基团与EDC和NHS的反应产生。这是在蛋白质缀合和固定化领域常用的公知技术。羧基与EDC和NHS的反应导致形成胺反应性NHS酯。当使用多官能性连接剂时,其确切性质并不重要,其条件在于它能够有效反应,导致囊泡通过X和Y基团的反应连接在一起。合适的多官能性连接剂包括同双官能交联剂,即,在两端具有相同官能性的交联剂。能够与胺基结合的例子包括:(i)NHS酯。典型的酯包括:二琥珀酰亚胺戊二酸酯:双(琥珀酰亚胺基)聚乙二醇:例如双(琥珀酰亚胺基五(乙二醇);乙二醇双(磺基琥珀酰亚胺基琥珀酸盐):3,3'-二硫代双(磺基琥珀酰亚胺丙酸酯):双(磺基琥珀酰亚胺基)辛二酸酯:二琥珀酰亚胺酒石酸酯:该类型的试剂在弱碱性条件下与伯胺反应,例如,在pH7.2-8.5下,例如,pH7.2-8.0,并生成稳定的酰胺键。反应温度典型地在0-30℃范围内,例如,4-25℃。反应产生N-羟基琥珀酰亚胺,其可以经由渗析或脱盐除去。例如,反应可以在PBS缓冲液中在pH7.2-8.0下在室温或4℃进行0.5-4小时。磺基NHS酯在NSH环上含有-SO3基团。这对于反应化学没有影响,但这类试剂倾向于水溶性增加。(ii)亚氨酸酯。典型的亚氨酸酯包括以下(常作为二盐酸盐获得):己二酰亚胺二甲酯:3,3'-二硫代二丙酰亚胺二甲酯:辛二亚氨酸二甲酯:庚二亚氨酸二甲酯:己二亚氨酸二甲酯:亚氨酸酯与伯胺反应,形成脒键。为了保证对于伯胺的特异性,反应典型地在不含胺的碱性条件下(pH9-11,例如pH10)以硼酸盐缓冲液进行。(iii)京尼平(genipin),其具有下式:(iv)环氧化物,例如三环氧丙基胺:三环氧丙基胺(v)二醛化合物,例如HOC.(CH2)x.CHO,其中x是1-6。典型的二醛包括戊二醛、丁二醛、乙二醛、丙二醛和苯二醛。(vi)COOH-PEG-COOH。该试剂是水溶性的,如果需要,可以用EDC/NHS活化,以提供与胺的反应性。合适的多官能性连接剂还包括杂双官能性交联剂,即,在两端具有不同官能性的交联剂。例子包括:1-乙基-3-(3-二甲基氨基丙基)碳二亚胺(通常以盐酸盐的形式获得):卡必醇:环氧化物,例如,三环氧丙基胺;COOH-PEG-NH2;磺基琥珀酰亚胺6-(4'-叠氮基-2'-硝基苯基氨基)己酸酯;聚(2-羟乙基-co-2-甲基丙烯酰氧基乙基天冬酰胺);N,N’-二琥珀酰亚胺碳酸酯:对叠氮基苯甲酰肼:本发明的方法可以使用“点击化学”,例如,其可以利用叠氮化物与炔的反应。例如,炔基可以通过伯胺与NHS酯的反应作为基团X或Y引入。许多叠氮基-PEG-叠氮基连接剂是市售的。优选地,多官能性连接剂包括(CH2)m链,其中m是2-20,优选3-10,特别是3-9。特别优选的双官能性连接剂是市售产品N-磺基琥珀酰亚胺基-6-(4'-叠氮基-2'-硝基苯基氨基)己酸酯。该产品具有下式:磺基琥珀酰亚胺基团是反应性基团Y,其是活化的羧酸酯,能够自发地与胺基反应。苯基叠氮基是基团Y,其在无光条件下是惰性的,但在使用UV光活化时变得反应性很高,很容易与胺基反应。在不存在胺基的情况下,活化的基团也能够与反应性较低的基团反应,甚至在某些情形中与C-H键反应;具体地,它能够与聚砜中的芳香性C-H基团反应。上述进行本发明方法的步骤(d)的条件将取决于各种反应性基团的性质,该步骤(d)即发生互补性反应性基团X和Y的反应以及X或Y与载体表面的反应。在一些实施方式中,反应性基团一旦在合适的条件下彼此接触就将自发地互相反应。在其他实施方式中,可以存在可光活化的基团,在该情形中反应物可以彼此接触,随后进行光辐照,以引发反应。本发明方法的优选实施方式中,通过使用具有在与端基X接触时反应的第一基团Y和在用UV光辐照时与端基X且与载体表面反应的第二基团Y的多官能性试剂,可以将两种机制结合起来。因此,本发明方法的一实施方式的步骤可以进行如下:(a)提供并入有跨膜蛋白的囊泡的含水悬浮液,所述囊泡由具有反应性端基X的两亲性嵌段共聚物形成;(b)提供多官能性、优选双官能连接剂,其具有至少两种与聚合物端基X具有反应性的反应性基团Y,包括能够在第一组反应条件下与聚合物端基X反应的第一反应性基团Y(1),以及在所述第一组反应条件下与聚合物端基X不反应、但在第二组反应条件下与聚合物端基X反应的第二反应性基团Y(2);(b')将所述囊泡水溶液与所述多官能性连接剂在所述第一组反应条件下混合,使得反应性基团Y(1)与聚合物端基(X)反应;(c)将产生的溶液以足以产生所需的囊泡层的量沉积在与第二反应性基团Y(2)具有反应性的载体上;和(d)通过应用所述第二组反应条件,引发端基X与所述第二反应性基团Y(2)以及第二反应性端基Y(2)与载体表面的反应。可以使用任何合适的区分两个反应步骤的反应条件。例如,第一组反应条件可以涉及在第一温度下反应的基团X和Y(1),而第二组反应条件可以涉及在更高的第二温度下反应的基团X和Y(2)。但是,在优选实施方式中,X和Y(1)使得它们在接触时或者如果需要的话在加热时自发反应,而X和Y(2)使得它们仅仅通过光辐照被活化时反应。因此,特别优选的方法包括:(a)提供并入有跨膜蛋白的囊泡的水溶液,所述囊泡由具有反应性端基X的两亲性嵌段共聚物形成;(b)提供多官能性、优选双官能连接剂,其具有至少两种与聚合物端基X具有反应性的反应性基团Y,包括能够在接触时与聚合物端基X反应的第一反应性基团Y(1),以及能够在光辐照时与聚合物端基X反应的第二反应性基团Y(2);(b')将所述囊泡水溶液与所述多官能性连接剂在使得反应性基团Y(2)与聚合物端基X反应的条件下混合;(c)将产生的溶液以足以产生所需的囊泡层的量沉积在与第二反应性基团Y(2)具有反应性的载体上;和(d)通过施加光辐照,引发端基X与所述第二反应性基团Y(2)以及第二反应性端基Y(2)与载体表面的反应。在特别优选的实施方式中,本发明提供一种方法,其包括:(a)提供并入有跨膜蛋白的囊泡的水溶液,所述囊泡由具有末端胺基的两亲性嵌段共聚物形成;(b)将所述囊泡水溶液与N-磺基琥珀酰亚胺基-6-(4'-叠氮基-2'-硝基苯基氨基)己酸酯在使得所述己酸酯的琥珀酰亚胺基团与所述聚合物末端胺基反应的条件下混合;(c)将产生的溶液沉积在载体上;和(d)用UV光辐照所述沉积物,引发所述己酸酯的叠氮基与聚合物末端胺基以及与载体表面的反应。在该实施方式中,优选地嵌段共聚物是下文提及的优选聚合物中的一种,特别是胺封端的[(聚)2-甲基-2-噁唑啉][(聚)二甲基硅氧烷][(聚)2-甲基-2-噁唑啉]。在所有上述实施方式中,步骤(c)中沉积的悬浮液的量足以为载体表面提供囊泡连续层。通常,在进行步骤(d)之后,该层将会是连续体的形式,其厚度大于囊泡的平均直径;或者,按绝对值计,厚度为至少0.04微米。可以使用范围很宽的反应条件,以进行本发明的方法。在一实施方式中,当使用多官能性连接剂时,使用的多官能性连接剂的量将使得存在的反应性基团Y的总量过量于存在的聚合物端基X的总量,以保证充分交联。对pH、温度和其他反应条件的控制是常规的,并且在技术人员的常规做法以内。两亲性嵌段共聚物适当地是具有亲水性和疏水性嵌段的双嵌段共聚物AB,或者优选地,具有亲水性端部嵌段和疏水性内部嵌段的三嵌段共聚物ABA。这些共聚物在囊泡形成中的使用是公知的,可以使用范围很宽的亲水性聚合物和疏水性聚合物形成嵌段A和B。疏水性聚合物包括例如聚硅氧烷,例如聚二甲基硅氧烷或聚二苯基硅氧烷、全氟聚醚、聚苯乙烯、聚氧丙烯、聚乙烯基乙酸酯、聚氧丁烯、聚异戊二烯、聚丁二烯、聚氯乙烯、聚丙烯酸烷基酯、聚甲基丙烯酸烷基酯、聚丙烯腈、聚丙烯、聚四氢呋喃、聚甲基丙烯酸酯、聚丙烯酸酯、聚砜、聚乙烯基醚和聚(环氧丙烷)及其共聚物。疏水性链段优选地含有主要量的疏水性单体。疏水性单体是通常形成不溶于水、并可以吸收小于10重量%水的均聚物的单体。合适的疏水性单体是二甲基硅氧烷、C1-C18烷基和C3-C18环烷基丙烯酸酯和甲基丙烯酸酯、C3-C18烷基丙烯酰胺和-甲基丙烯酰胺、丙烯腈、甲基丙烯腈、乙烯基Cl-C18烷酸酯、C2-C18烯烃、C2-C18卤代烯烃、苯乙烯、(低级烷基)苯乙烯、C4-C12烷基乙烯基醚、C2-C10全氟烷基丙烯酸酯和甲基丙烯酸酯和相应地部分氟化的丙烯酸酯和甲基丙烯酸酯、C3-C12全氟烷基乙基硫代羰基氨基乙基丙烯酸酯和甲基丙烯酸酯、丙烯酰氧基-和甲基丙烯酰氧基烷基硅氧烷、N-乙烯基咔唑、马来酸、富马酸、衣康酸、中康酸的Cl-C12烷基酯、乙酸乙烯酯、丙酸乙烯酯、丁酸乙烯酯、戊酸乙烯酯、氯丁二烯、氯乙烯、偏氯乙烯、乙烯基甲苯、乙烯基乙基醚、全氟己基乙基硫代羰基氨基乙基甲基丙烯酸酯、甲基丙烯酸异冰片烯酯、甲基丙烯酸三氟乙基酯、甲基丙烯酸六氟异丙酯、甲基丙烯酸六氟丁酯、三三甲基甲硅烷氧基甲硅烷基丙基甲基丙烯酸酯和3-甲基丙烯酰氧基丙基五甲基二硅氧烷。疏水性聚合物可以包括单一类型的聚合物或者多于一种类型的聚合物,例如两种或更多种上文所述的聚合物。优选的疏水性聚合物是聚硅氧烷,特别是(聚)二甲基硅氧烷。一个链段B的平均分子量(g/mol)优选在大约500至大约50,000的范围内,优选在大约800至大约15,000的范围内,更优选在大约1,000至12,000的范围内,特别优选在大约5,000至大约12,000的范围内。除疏水性链段B以外,两亲性共聚物还包括至少一个、优选两个链段A,其包括至少一种亲水性聚合物,例如,聚噁唑啉、聚乙二醇、聚环氧乙烷、聚乙烯醇、聚乙烯基吡咯烷酮、聚丙烯酰胺、聚(甲基)丙烯酸、聚环氧乙烷-co-聚环氧丙烷嵌段共聚物、聚(乙烯基醚)、聚(N,N-二甲基丙烯酰胺)、聚丙烯酸、聚酰基亚烷基亚胺、聚羟基烷基丙烯酸酯例如甲基丙烯酸羟乙酯、丙烯酸羟乙酯、丙烯酸羟丙酯,和多元醇及其共聚物。亲水性链段优选地含有主要量的亲水性单体。亲水性共聚单体典型地是形成可溶于水或者可以吸收至少10重量%水的均聚物的单体。合适的亲水性单体包括羟基1-取代低级烷基丙烯酸酯和甲基丙烯酸酯、丙烯酰胺、甲基丙烯酰胺、(低级烷基)丙烯酰胺和甲基丙烯酰胺、N,N-二烷基-丙烯酰胺、乙氧基化丙烯酸酯和甲基丙烯酸酯、聚乙二醇-单甲基丙烯酸酯和聚乙二醇单甲基醚甲基丙烯酸酯、羟基取代的(低级烷基)丙烯酰胺和甲基丙烯酰胺、羟基取代的低级烷基乙烯基醚、乙烯基磺酸钠、苯乙烯磺酸钠、2-丙烯酰胺-2-甲基丙磺酸、N-乙烯基吡咯、N-乙烯基-2-吡咯烷酮、2-乙烯基噁唑啉、2-乙烯基-4,4'-二烷基噁唑啉-5-酮、2-和4-乙烯基吡啶、具有共计3-5个碳原子的烯键(vinylically)不饱和羧酸、氨基(低级烷基)-(其中术语氨基还包括季铵盐)、单(低级烷基氨基)(低级烷基)和二(低级烷基氨基)(低级烷基)丙烯酸酯和甲基丙烯酸酯、烯丙醇、3-三甲基铵2-羟丙基甲基丙烯酸酯氯化物(Blemer,QA,例如,来自NipponOil)、甲基丙烯酸二甲基氨基乙酯(DMAEMA)、二甲基氨基乙基甲基丙烯酰胺、甲基丙烯酸甘油酯和N-(l,l-二甲基-3-氧代丁基)丙烯酰胺。可以由其制造这些聚合物的亲水性单体的具体例子为环状亚氨基醚、乙烯基醚、包括环氧化物、环状不饱和醚的环醚、N-取代的氮丙啶、β-内酯和β-内酰胺。其他合适的单体包括烯酮缩醛、乙烯醇缩醛和正膦。合适的环状亚氨基醚包括2-噁唑啉。如果使用在2位上具有烯基的2-噁唑啉作为亲水性单体,则在两亲性多嵌段共聚物的链段A(在侧链中)提供可聚合的不饱和基团,用作最终聚合得到聚合产物所必需的可聚合不饱和基团,或者作为在聚合物制备中提供直接交联可能性的额外的可聚合不饱和基团。最优选的环状亚氨基醚是2-C1-3烷基噁唑啉,特别是2-甲基噁唑啉。最优选的乙烯基醚是甲基乙烯基醚、乙基乙烯基醚和甲氧基乙基乙烯基醚。优选的亲水性聚合物嵌段是(聚)2-C1-3烷基-2-噁唑啉,特别是(聚)2-甲基-2-噁唑啉。一个链段A的平均分子量(g/mol)适当地在大约200至大约50,000的范围内,优选在大约800至大约15,000的范围内,更优选在大约1,000至12,000的范围内,特别优选在大约5,000至大约12,000的范围内。通过聚合来合成嵌段共聚物是公知的,要在起始链段上共聚的一个或多个链段的长度可以很容易地通过控制共聚加入的单体(亲水性或疏水性)的量和/或通过加入合适的链终止封端剂来控制。通过该方式,链段的大小及其比例可以很容易地加以控制。本领域公知的是,亲水性和疏水性嵌段的绝对和相对长度在决定形成囊泡的共聚物的适合性中非常重要(所谓的聚合物疏水比)。而且,嵌段的长度应该使得囊泡壁的厚度与跨膜蛋白的长度大致相当,使得蛋白质可以容易地在通道不变得阻塞的情况下并入到囊泡壁中。例如,囊泡壁的厚度可以在1nm至50nm的范围内。疏水性嵌段B的长度不是特别重要,其应当优选地不大于150个重复单元。用于本发明的特别优选的嵌段共聚物为PAOXA-a-PDMS-b-PAOXA-a,特别是PMOXA-a-PDMS-b-PMOXA-a,其中PAOXA是(聚)2-C1-3烷基-2-噁唑啉,PMOXA是(聚)2-甲基-2-噁唑啉,PDMS是(聚)二甲基硅氧烷。优选地,每个a独立地为5-100的数,优选10-100,b是5-150的数,优选20-150。各种PAOXA-PDMS-PAOXA聚合物是市售的,其他可以很容易通过已知方法合成。反应性端基X可以在共聚物的初始合成之后存在,或者它们可以在共聚物合成之后引入。例如,在使用特定单体例如诸如聚丁二烯或聚异戊二烯的二烯聚合物时,或者如果用于制造亲水性链段的单体包括不饱和侧链例如2-烯丙基-噁唑啉,共聚物可以已经含有合适的端基。另外可选地,当已通过使用合适的封端剂停止聚合时,聚合物可以已经含有反应性端基。如果在初始合成之后不存在,可以通过相关嵌段端部的合适的反应引入反应性基团。出于该目的,增长中的链段的聚合可以在达到合适的链长之后终止,链端存在的引发剂基团封端,例如,通过使用特定的试剂例如羟基苯乙烯、烯丙醇、甲基丙烯酸羟乙基酯、炔丙醇、烯丙基胺和炔丙基胺,或者通过使用KOH/EtOH或伯胺,在增长中的链段端部留下-OH或-NH-基团或不饱和基团。还可以通过在共聚中使用合适的共聚单体例如2-羟基-烷基噁唑啉,将羟基引入到共聚物中。然后可以使羟基或-NH-基团与例如带有可聚合不饱和基团的异氰酸酯反应。这类双官能化合物的优选的例子是异氰酸乙烯酯、烯丙基异氰酸酯、烯丙酰异氰酸酯、苯乙烯异氰酸酯、乙烯基苄基异氰酸酯和炔丙基异氰酸酯。其他反应性基团可以通过本领域技术人员已知的技术引入。在特别优选的实施方式中,本发明使用的聚合物具有胺基端基。最优选地,聚合物是端胺基PAOXA-a-PDMS-b-PAOXA-a,例如,上文所述的PAOXA-PDMS-PAOXA聚合物之一,带有胺基端基。胺基端基可以含有-NH2基团或-NH-基团或者含有二者。在本发明特别优选的实施方式中,两亲性嵌段共聚物通过具有式-NHR的端基X封端,其中R表示烷基,其可以是直链或支链的,具有1-6个碳原子,被至少1个例如1、2或3个-NH2基团取代。优选地,这样的端基X具有式-NH-CH-(NH2)2,或者优选-NH-(CH2)n-NH2,其中n是2-6的整数,优选2-4,特别是2。这样的端基可以通过使具有-OH端基的聚合物与合适的反应性胺NH2R反应来引入,例如,二胺,例如H2N-(CH2)n-NH2,特别是H2N-(CH2)2-NH2,或者三胺,例如N.([CH2]nNH2)3或CH.([CH2]nNH2)3,例如CH(NH2)3或三(3-氨基丙基)胺。也可以使用支链的低聚亚胺。PAOXA-a-PDMS-b-PAOXA-a型两亲性嵌段共聚物是新颖的,其中PAOXA是(聚)2-C1-3烷基-2-噁唑啉,PDMS是(聚)二甲基硅氧烷,其含有包括-NH2基团或-NH-基团二者的端基,即,含有伯胺和仲胺基团,特别是-NH-CH-(NH2)2或-NH-(CH2)n-NH2,其在我们共同未决(conpending)的申请第22883WO号中要求保护。由这些聚合物形成并且并入有跨膜蛋白的囊泡也是新颖的,并在我们共同未决的申请中要求保护。嵌段共聚物可以通过本领域公知的方法制备成囊泡的形式。通常,这些方法涉及溶剂置换或无溶剂再水化。在溶剂置换方法中,在与水混合之前,将嵌段共聚物溶解在有机溶剂中。混合并任选地除去有机溶剂之后,发生自发的囊泡自组装。在无溶剂再水化中,使干的嵌段共聚物与含水介质接触,于是水化导致自发的囊泡自组装。在无溶剂再水化的特定情形薄膜再水化方法中,将嵌段共聚物溶解在有机溶剂中,然后将有机溶剂在使得形成薄膜的条件下除去。然后通过与水接触使该膜水化。通过已知方法可以得到具有所需大小和低多分散性的囊泡,例如,通过经孔径已知的一个或多个膜挤出大的单层或多层多分散囊泡。径迹蚀刻(tracketched)聚碳酸酯膜例如可获自Millipore的Isopore(商标)膜对于该目的来说是合适的。适当地,本发明中使用的囊泡的平均直径在30-10,000nm、优选50-1000nm、更优选100-400nm、特别是150-250nm范围内。已知的PAOXA-a-PDMS-b-PAOXA-a聚合物形成囊泡而不是其他自组装结构例如胶束的倾向主要取决于嵌段的绝对和相对大小。因此,当聚合物用-OH基团封端时,以及当嵌段具有相对高的分子量例如在PAOXA14PDMS55PAOXA14中或更高时,倾向于形成胶束,这意味着如果要求囊泡,需要使用分子量较低的聚合物。出人意料地,存在包括-NH2和-NH-基团二者的端基产生重要的差异,使用PAMOXA-a-PDMS-b-PAOXA-a,例如PAOXA14PDMS55PAOXA14,特别是具有这些端基的PMOXA14PDMS55PMOXA14,例如:H2N-(CH2)n-NH-PAOXA14PDMS55PAOXA14-NH-(CH2)n-NH2特别是H2N-(CH2)n-NH-PMOXA14PDMS55PMOXA14-NH-(CH2)n-NH2,已经证实对于制备囊泡特别有价值。总之,与制备工作过滤膜的已知方法相比较,将官能团封端的聚合物特别是胺封端聚合物与互补性多官能性连接剂一起使用具有重大的优势。尽管形成囊泡,但囊泡形成过程可以在跨膜蛋白特别是水通道蛋白的存在下进行,从而跨膜蛋白变得并入到囊泡壁中。通常,该过程在洗涤剂的存在下进行,其有助于保持蛋白质的完整性和生物功能。因此,上述再水化步骤可以使用优选地还包括洗涤剂的跨膜蛋白水溶液进行。优选使用水通道蛋白,水通道蛋白在范围很宽的处理条件下均稳定。水通道蛋白是生物细胞跨膜蛋白,其功能是选择性地运输水,不运输其他分子;蛋白质的运输通道是双向通道,水可以通过其沿任一方向流动。它们由许多人细胞类型表达,也由细菌和植物细胞表达。本发明中可以使用水通道蛋白蛋白质家族的任何不同成员。合适的水通道蛋白包括Aqp4、Aqp1和尤其是AqpZ。水通道蛋白可以单体、二聚、四聚和更高级的低聚形式存在,以及以一级序列的突变、缀合和截短的版本存在。只要水通道蛋白的生物功能即选择性运输水得以保持,本发明中可以使用其任意种类。在本发明中可以使用任何其他具有所需运输特性的跨膜蛋白。可以使用这些跨膜蛋白的变体,包括天然或非天然变体以及这些蛋白质的直系同源物或横向同源物。这些蛋白质包括,例如:·单元分布体(Monotopic)膜蛋白o环氧酶■Ram前列腺素H2合成酶-1(环氧酶-1orCOX-1):绵羊(Ovisaries)■Ram前列腺素H2合成酶-1(COX-1)R120Q/天然杂二聚体:绵羊■阿司匹林乙酰化COX-1■环氧酶-2:小鼠(MusMusculus)o鲨烯-藿烯环化酶■鲨烯-藿烯环化酶:酸热脂环酸芽孢杆菌(Alicyclobacillusacidocaldarius)o一元胺氧化酶·一元胺氧化酶B:人线粒体外膜·一元胺氧化酶A:大鼠线粒体外膜·一元胺氧化酶A:人线粒体外膜·G110A突变体o水解酶·脂肪酸酰胺水解酶:褐家鼠(Rattusnorvegicus)o氧化还原酶(单元分布体)·硫化物:与癸基泛醌复合的醌氧化还原酶:风产液菌(Aquifexaeolicus)·电子转运黄素蛋白-泛醌氧化还原酶(ETF-QO):野猪(Susscrofa)o肽聚糖糖基转移酶·肽聚糖糖基转移酶:金黄色葡萄球菌(Staphylococccusaureus)·肽聚糖糖基转移酶青霉素结合蛋白质1a(PBP1a):风产液菌·肽聚糖糖基转移酶青霉素结合蛋白质1b(PBP1b):大肠埃希氏菌(Escherichiacoli)o肽酶■信号肽酶(SPase):大肠埃希氏菌■信号肽酶(SppA),天然蛋白质:大肠埃希氏菌o脱氢酶■甘油-3-磷酸酯脱氢酶(GlpD,天然):大肠埃希氏菌o二氢乳清酸脱氢酶(DHODH,2类)■二氢乳清酸脱氢酶:大肠埃希氏菌■二氢乳清酸脱氢酶:黑鼠(Rattusrattus)■二氢乳清酸脱氢酶,脱辅形式:智人(Homosapiens)■二氢乳清酸脱氢酶:恶性疟原虫(Plasmodiumfalciparum)3d7o聚合酶■TagF磷壁酸聚合酶:表皮葡萄球菌(Staphylococcusepidermidis)oADP-核糖基化因子■ADP-核糖基化因子(ARF1),十四烷基化:啤酒糖酵母(Saccharomycescerevisiae)■ADP-核糖基化因子(ARF1*GTP),十四烷基化:啤酒糖酵母o异构酶■RPE65视觉循环类视黄醇异构酶:牛(BosTaurus)·膜蛋白:β-桶oβ-桶膜蛋白:多聚■孔蛋白:荚膜红细菌(Rhodobactercapsulatus)■孔蛋白:生芽红假单胞菌(Rhodopeudomonasblastica)·OmpK36osmoporin:肺炎克雷伯氏菌(Klebsiellapneumonia)■Omp32阴离子选择性孔蛋白:食酸丛毛单胞菌(Comamonasacidovorans)■Omp32阴离子选择性孔蛋白:食酸代尔夫特菌(Delftiaacidovorans)■OmpFMatrix孔蛋白:大肠埃希氏菌■OmpCOsmoporin:大肠埃希氏菌■OmpG*单体*孔蛋白:大肠埃希氏菌■PhoE:大肠埃希氏菌■LamB麦芽糖孔蛋白:鼠伤寒沙门氏菌(Salmonellatyphimurium)■LamB麦芽糖孔蛋白:大肠埃希氏菌■LamB麦芽糖孔蛋白:大肠埃希氏菌■ScrY蔗糖特异性孔蛋白:鼠伤寒沙门氏菌■MspA分枝杆菌孔蛋白:耻垢分枝杆菌(Mycobacteriumsmegmatis)■OprP磷酸盐特异性转运蛋白:铜绿假单胞菌(Pseudomonasaeruginosa)■OprD碱性氨基酸吸收通道:铜绿假单胞菌■OpdK烃转运蛋白:铜绿假单胞菌■PorB外膜蛋白,天然结构:脑膜炎奈瑟氏球菌(Neisseriameningitidis)oβ-桶膜蛋白:单聚/二聚■TolC外膜蛋白:大肠埃希氏菌■TolC外膜蛋白,配体阻断:大肠埃希氏菌■TolC外膜蛋白(Y362F,R367E):大肠埃希氏菌·C2形式·P2:2:2形式■VceC外膜蛋白:霍乱弧菌(Vibriocholera)■OprM药物释放外膜蛋白:铜绿假单胞菌■CusC重金属释放外膜蛋白:大肠埃希氏菌■CusBA重金属外排复合外膜蛋白:大肠埃希氏菌■BenF样孔蛋白(假定):荧光假单胞菌(Pseudomonasfluorescens)■OprM药物释放外膜蛋白:铜绿假单胞菌■脱辅BtuB钴胺素转运蛋白:大肠埃希氏菌■BtuB:大肠埃希氏菌■脱辅BtuB,通过内消旋结晶:大肠埃希氏菌■大肠杆菌素I受体:大肠埃希氏菌■OmpA:大肠埃希氏菌,■OmpA,具有4个缩短的回环:大肠埃希氏菌·所谓的β-桶平台(BBP)■OmpT外膜蛋白酶:大肠埃希氏菌■Pla纤溶酶原激活物(天然1):鼠疫耶尔森氏菌(Yersiniapestis)■OmpW外膜蛋白:大肠埃希氏菌·斜方晶系形式·三方晶系形式■OprG外膜蛋白:铜绿假单胞菌■OmpX:大肠埃希氏菌■TtoA外膜蛋白(OMP):嗜热栖热菌(Thermusthermophilus)HB27■OmpLA(PldA)外膜磷脂酶A单体:大肠埃希氏菌■OmpLA(PldA)活性位点突变体(N156A):大肠埃希氏菌■OpcA粘附素蛋白质:脑膜炎奈瑟氏球菌■NspA表面蛋白质:脑膜炎奈瑟氏球菌■NalP自转运蛋白转位因子结构域:脑膜炎奈瑟氏球菌■NanC孔蛋白,KdgM孔蛋白家族模型:大肠埃希氏菌■Hia1022-1098三聚自转运蛋白:流感嗜血杆菌(Haemophilusinfluenza)·Hia992-1098■EspP自转运蛋白,切割后状态:大肠埃希氏菌■EstA自转运蛋白,全长:铜绿假单胞菌■PagP外膜棕榈酰基转移酶:大肠埃希氏菌■FadL长链脂肪酸转运蛋白:大肠埃希氏菌■FadL长链脂肪酸转运蛋白A77E/S100R突变体:大肠埃希氏菌·ΔS3扭折·P34A突变体·N33A突变体·ΔNPA突变体·G212E突变体■FadL同源长链脂肪酸转运蛋白:铜绿假单胞菌■FauAalcaligin外膜转运蛋白:百日咳博德特氏菌(Bordetellapertusssis)■TodX烃转运蛋白:恶臭假单胞菌(Pseudomonasputida)■TbuX烃转运蛋白:皮氏拉斯通氏菌(Ralstoniapickettii)■Tsx核苷转运蛋白(脱辅基蛋白):大肠埃希氏菌■FhuA,高铁色素-铁受体:大肠埃希氏菌■FepA,铁肠杆菌素受体:大肠埃希氏菌■FecA,铁载体转运蛋白:大肠埃希氏菌■HasR血红素吸收受体:粘质沙雷氏菌(Serratiamarcescens)·Ile671Gly突变体■FptA,铜绿假单胞菌螯铁蛋白外膜受体:铜绿假单胞菌■FpvA,荧光铁载体(Pyoverdine)受体:铜绿假单胞菌■FpvA,荧光铁载体受体(脱辅形式):铜绿假单胞菌■P菌毛引座子(usher)易位结构域,PapC130-640:大肠埃希氏菌oβ-桶膜蛋白:线粒体外膜■VDAC-1电压依赖型阴离子通道:人(Human)■VDAC-1电压依赖型阴离子通道:鼠(Murine)oOmp85-TpsB外膜转运蛋白超家族■FhaC丝状血凝素转运蛋白:百日咳博德特氏菌■TeOmp85-NPOTRA结构域:ThermosynechococcusanaOmp85-N鱼腥藻属(Anabaenasp.)PCC7120■BamA:大肠埃希氏菌■BamE:大肠埃希氏菌o非组成型.β-折叠孔形成毒素■α-溶血素:金黄色葡萄球菌■LukF:金黄色葡萄球菌■产气荚膜梭菌溶素(Perfringolysin)O(PFO)原聚体:产气荚膜梭菌(Clostridiumperfringens)■炭疽保护性抗原(PA)和致死因子(LF)通道前复合物:炭疽芽孢杆菌(Bacillusanthraciss)■淋巴细胞穿孔素单体:小鼠(Musmusculus)·跨膜蛋白:α-螺旋o非组成型.α-螺旋孔形成毒素■溶细胞素A(ClyA,akaHlyE):大肠埃希氏菌■来自海葵的FraC真核孔形成毒素:Actiniafragaceao外膜蛋白质■荚膜多糖Wza易位子:大肠埃希氏菌■孔蛋白B蛋白:谷氨酸棒杆菌(Corynebacteriumglutamicum)■IV型外膜分泌复合物:大肠埃希氏菌■细菌视紫红质(BR):盐沼盐杆菌(Halobacteriumsalinarium)■嗜盐菌视紫红质(HR):盐沼盐杆菌■嗜盐菌视紫红质(HR):法老嗜盐碱单胞菌(Natronomonaspharaonis)■感觉视紫红质I(SRI):鱼腥藻(念珠藻属)(Anabaena(Nostoc)sp.)PCC7120■感觉视紫红质II(SRII):法老嗜盐碱单胞菌■古紫质-1(aR-1):盐红菌(Halorubrumsp.)aus-1■古紫质-2(aR-2):盐红菌aus-2■Xanthorhodopsin:SalinibacterruberoG蛋白耦合受体(GPCR)■视紫红质:牛视网膜感光细胞外节膜盘(RodOuterSegment)牛(BosTaurus)■视紫红质:鱿鱼(太平洋褶柔鱼(Todarodespacificus))■β1肾上腺素能受体(改造的):Meleagrisgallopavo(火鸡)■β2肾上腺素能受体:智人■甲基化β2肾上腺素能受体:智人■A2A腺苷受体:智人■CXCR4趋化因子受体:智人·多巴胺D3受体:智人o自主折叠“膜蛋白”(不依赖于Sec)·Mistic膜整合蛋白:枯草芽孢杆菌(Bacillussubtilis)o糖蛋白·血型糖蛋白A跨膜结构域二聚体:智人oSNARE蛋白质家族■突触融合蛋白1A/SNAP-25/小突触泡蛋白-2复合物:大鼠(ratusratus)o整合素粘附受体■人整合素αIIbβ3跨膜-细胞质杂二聚体:智人o组氨酸激酶受体■ArcB(1-115)需氧呼吸控制传感膜结构域:大肠埃希氏菌■QseC(1-185)传感蛋白膜结构域:大肠埃希氏菌■KdpD(397-502)传感蛋白膜结构域:大肠埃希氏菌o免疫受体·TCR-CD3复合物的跨膜ζ-ζ二聚体:智人·DAP12二聚:智人o通道:钾和钠离子选择性·KcsA钾通道,H+门:变铅青链霉素(Streptomyceslividans)·KcsA钾通道E71H-F103A失活态突变体(闭合状态):变铅青链霉素·KcsA钾通道E71I模态门控突变体:变铅青链霉素·KvAP电压门控钾通道:敏捷气热菌(Aeropyrumpernix)·Kv1.2电压门控钾通道:褐家鼠·Kv1.2/Kv2.1电压门控钾通道嵌合体:褐家鼠·F233W突变体■MthK钾通道,Ca++门:热自养甲烷嗜热杆菌(Methanothermobacterthermautotrophicus)■人BK通道Ca2+-激活装置:智人·Kir3.1-原核Kir嵌合体:小鼠(Musmusculus)&Burkholderiaxenovornas■Kir2.2内向整流钾通道:原鸡(Gallusgallus)■KirBac1.1内向整流钾通道:类鼻疽伯克氏菌(Burkholderiapseudomallei)■MlotiK1环状核苷酸调节K+-通道:百脉根中间根瘤菌(Mesorhizobiumloti)■mGIRK1G-蛋白门控内向整流钾受体:小鼠■NaK通道(Na+复合物):蜡样芽孢杆菌(Bacilluscereus)·D66/S70E突变体·D66N突变体·D66E突变体·CNG-模拟NaK通道突变体:蜡样芽孢杆菌·NaK通道;K+选择性突变体:蜡样芽孢杆菌o通道:其他离子通道■GluA2谷氨酸受体(AMPA-亚型):褐家鼠■M2质子通道:甲型流感病毒(InfluenzaA)■M2质子通道:乙型流感病毒(InfluenzaB)■ASIC1酸传感离子通道:原鸡■ATP-门控P2X4离子通道(脱辅蛋白质):Daniorerio(斑马鱼)■烟碱乙酰胆碱受体孔:石纹电鳐(Torpedomarmorata)■原核五聚配体门控离子通道(pLGIC):菊欧文氏菌(Erwiniachrysanthemi)■原核五聚配体门控离子通道(GLIC):Gloebacterviolaceus·E221A突变体■原核五聚配体门控离子通道(GLIC),野生型-TBSb复合物:Gloebacterviolaceus·野生型-TEAs复合物·E221D-TEAs复合物·野生型-TMAs复合物·野生型-溴-利多卡因复合物·野生型-Cd2+复合物·野生型-Zn2+复合物·野生型-Cs+复合物■MscL力敏感通道:结核分枝杆菌(Mycobacteriumtuberculosis)■MscS电压调节的力敏感通道:大肠埃希氏菌■CorAMg2+转运蛋白:海栖热袍菌(Thermotogamaritime)■MgtEMg2+转运蛋白:嗜热栖热菌(Thermusthermophilus)■SLAC1阴离子通道,TehA同源物(野生型):流感嗜血杆菌(Haemophilusinfluenzae)·F262A突变体·F262L突变体·F262V突变体·G15D突变体o通道:蛋白质-传导■SecYEβ蛋白质-传导通道:詹氏甲烷球菌(Methanococcusjannaschii)o通道:水通道蛋白和甘油孔蛋白(Glyceroporins)■AQP0水通道蛋白水通道:牛晶状体(Bovinelens)■AQP1水通道蛋白水通道:人红血球■AQP1水通道蛋白水通道:牛红血球■AQP4水通道蛋白水通道:大鼠神经胶质细胞·S180D突变体■AQP4水通道蛋白水通道:人■AQP5水通道蛋白水通道(HsAQP5):人■AqpM水通道蛋白水通道:马堡甲烷嗜热杆菌(Methanothermobactermarburgensis)■AqpZ水通道蛋白水通道:大肠埃希氏菌■AqpZ水通道蛋白(C9S/C20S),T183C突变体:大肠埃希氏菌·L170C突变体■AqpZ水通道蛋白突变体F43W:大肠埃希氏菌·H17G/T183F突变体·F43WH174G/T183F突变体■SoPIP2;1植物水通道蛋白:菠菜(Spinaciaoleracea)■GlpF甘油易化蛋白通道:大肠埃希氏菌■GlpF甘油易化蛋白通道,W84F/F200T-突变体:大肠埃希氏菌■PfAQP水甘油通道蛋白(aquaglyceroporin):恶性疟原虫(Plasmodiumfalciparum)■Aqy1酵母水通道蛋白(pH3.5):巴斯德毕赤氏酵母(Pischiapastoris)o通道:甲酸硝酸盐转运蛋白(FNT)家族■FocA,五聚水通道蛋白样甲酸转运蛋白:大肠埃希氏菌■FocA无甲酸的甲酸转运蛋白:霍乱弧菌■FocA甲酸转运蛋白:鼠伤寒沙门氏菌(Salmonelatyphimurium)o通道:尿素转运蛋白■尿素转运蛋白:普通脱硫弧菌(Desulfovibriovulgaris)■连接蛋白26(Cx26;GJB2)缝隙连接:人o通道:Amt/Rh蛋白质■AmtB氨通道(突变体):大肠埃希氏菌■AmtB氨通道(野生型):大肠埃希氏菌·H168E突变体·H168A突变体·H168F突变体·H318A突变体·H318突变体·H318F突变体·H168A/H318A突变体■Amt-1铵通道:闪烁古生球菌(Archaeoglobusfulgidus)■Rh蛋白质,可能的氨或CO2通道:欧洲亚硝化单胞菌(Nitrosomonaseuropaea)■人RhC糖蛋白氨转运蛋白:智人o膜内蛋白酶■GlpG扁菱形-家族膜内蛋白酶:大肠埃希氏菌·W136A突变体·S201T活性位点突变体■GlpG扁菱形-家族膜内肽酶:流感嗜血杆菌■位点-2蛋白酶(S2P).膜内金属蛋白酶:詹氏甲烷球菌■信号肽肽酶(SppA),天然蛋白质:大肠埃希氏菌o膜结合金属蛋白酶■脱辅-FtsHATP-依赖型金属蛋白酶:海栖热袍菌oH+/Cl-交换转运蛋白■H+/Cl-交换转运蛋白:鼠伤寒沙门氏菌■H+/Cl-交换转运蛋白:大肠埃希氏菌·E148A突变体·E148Q突变体·S107A/E148Q/445A突变体■单体H+/Cl-交换转运蛋白:大肠埃希氏菌■+/Cl-真核交换转运蛋白:Cyanidioschyzonmerolae■H+/Cl-真核交换转运蛋白:集胞藻属(Synechocystissp.)pcc6803o细菌汞解毒蛋白质■MerFHg(II)转运蛋白:摩氏摩根氏菌o多药外排转运蛋白■AcrB细菌多药外排转运蛋白:大肠埃希氏菌■AcrB细菌多药外排转运蛋白,脱辅蛋白质,N109A突变体:大肠埃希氏菌■AcrB细菌多药外排转运蛋白D407A突变体:大肠埃希氏菌■MexB细菌多药外排转运蛋白:铜绿假单胞菌■CusA金属离子外排泵:大肠埃希氏菌■EmrE细菌多药外排转运蛋白:大肠埃希氏菌■NorM多药和毒素化合物挤出(MATE)转运蛋白(脱辅形式):霍乱弧菌o类二十烷酸和谷胱甘肽代谢中的膜相关蛋白(MAPEG)■微粒体前列腺素E合成酶1:人■5-脂氧合酶-激活蛋白质(FLAP),具有结合的MK-591抑制剂:人■白三烯LTC4合成酶:人o主要易化子(facilitator)超家族(MFS)转运蛋白■LacY乳糖通透酶转运蛋白(C154G突变体):大肠埃希氏菌■具有TDG的LacY乳糖通透酶(野生型):大肠埃希氏菌■向外的构象的FucP海藻糖转运蛋白:大肠埃希氏菌·N162A突变体■GlpT甘油-3-磷酸转运蛋白:大肠埃希氏菌■EmrD多药转运蛋白:大肠埃希氏菌■PepTSo寡肽-质子共转运蛋白(symporter):奥奈达湖希瓦氏菌(Shewanellaoneidensis)o溶质钠共转运蛋白(SSS)家族■vSGLT钠半乳糖转运蛋白:副溶血弧菌(Vibrioparahaemolyticus)·K294A突变体o核碱基-阳离子-共转运-1(NCS1)家族■Mhp1苄基-乙内酰脲转运蛋白:液化微杆菌(Microbacteriumliquefaciens)o甜菜碱/胆碱/肉毒碱转运蛋白(BCCT)家族■BetP甘氨酸甜菜碱转运蛋白:谷氨酸棒杆菌(Corynebacteriumglutamicum)■CaiT肉毒碱转运蛋白:大肠埃希氏菌■CaiT肉毒碱转运蛋白:奇异变形杆菌(Proteusmirabilis)o氨基酸/多元胺/有机阳离子(APC)超家族■AdiC精氨酸:胍基丁胺反向转运体(Antiporter):大肠埃希氏菌·N22A、L123W突变体·N101A突变体■脱辅ApcT不依赖于Na+的氨基酸转运蛋白:詹氏甲烷球菌o氨基酸次级转运蛋白■LeuTAa亮氨酸转运蛋白:风产液菌(Aquifexaeolicus)■野生型LeuT转运蛋白:风产液菌·E290S突变体■具有硝基氧自旋标记(F177R1)的突变LeuT转运蛋白:风产液菌·I204R1突变体■谷氨酸转运蛋白同源物(GltPh):堀越氏热球菌(Pyrococcushorikoshii)■天冬氨酸转运蛋白Li+-结合态(GltPh):堀越氏热球菌o阳离子扩散易化子(CDF)家族■YiiP锌转运蛋白:大肠埃希氏菌o反向转运体■NhaANa+/H+反向转运体:大肠埃希氏菌■线粒体ADP/ATP载体:牛心脏线粒体o能量耦合因子(ECF)转运蛋白■RibU,核黄素转运蛋白的S组分:金黄色葡萄球菌oATP结合盒(ABC)转运蛋白■BtuCD维生素B12转运蛋白:大肠埃希氏菌■Sav1866多药转运蛋白:金黄色葡萄球菌■钼酸盐转运蛋白ModB2C2:闪烁古生球菌■ModBC钼酸盐ABC转运蛋白:噬菌乙酸甲烷八叠球菌(Methanosarcinaacetivorans)■HI1470/1假定金属螯合型ABC转运蛋白:流感嗜血杆菌■结合有AMPPNP的MsbA脂类“翻转酶”:鼠伤寒沙门氏菌■P-糖蛋白:Musmusculus(小鼠)■MalFGK2-MBP麦芽糖吸收转运蛋白复合物:大肠埃希氏菌■MetNI甲硫氨酸吸收转运蛋白复合物:大肠埃希氏菌■FbpC三价铁吸收转运蛋白核苷酸结合结构域:淋病奈瑟氏球菌(Neisseriagonorrhoeae)oK+转运蛋白超家族(SKT蛋白)■TrkH钾离子转运蛋白:副溶血弧菌■钙ATP酶:兔肌浆网■Na,K-ATP酶:猪肾脏■Na,K-ATP酶:鲨鱼■Na,K-ATP酶调节蛋白质FXYD1:人■受磷蛋白同五聚体:人肌浆网■质膜H+-ATP酶:拟南芥(Arabidopsisthaliana)oV-型ATP酶■V-型Na+-ATP酶转子:海氏肠球菌(Enterococcushirae)■V1-ATP酶复合物:Thermusthermophiles■V1-ATP酶A3B3复合物:嗜热栖热菌oF-型ATP酶■来自牛心脏线粒体的F1-ATP酶:牛(BosTaurus)■ATP合成酶(F1c10):啤酒糖酵母■F1ATP酶:啤酒糖酵母■Na+-依赖性F-ATP合成酶转子(c11):酒石酸泥杆菌(Ilyobactertartaricus)■菠菜叶绿体的H+-依赖性F-ATP合成酶转子(c14):菠菜■嗜碱蓝细菌H+-依赖性F-ATP合成酶转子(c15):钝顶螺旋藻(Spirulinaplatensis)■H+-依赖性F-ATP合成酶转子(c13):假坚强芽孢杆菌(Bacilluspseudofirmus)■H+-依赖型F-ATP合成酶外周杆:嗜热栖热菌o磷酸转移酶■甘油二酯激酶(DAGK):大肠埃希氏菌o水解酶■雌酮硫酸酯酶:人胎盘o加氧酶■颗粒状甲烷单加氧酶(pMMO):荚膜甲基球菌(Methylococcuscapsulatus)■颗粒状甲烷单加氧酶(pMMO):发孢甲基弯菌(Methylosinustrichosporium)OB3bo氧化还原酶■硫化物:醌氧化还原酶:风产液菌■电子转移黄素蛋白-泛醌氧化还原酶(ETF-QO):野猪(Susscrofa)■甘油-3-磷酸酯脱氢酶(GlpD,天然):大肠埃希氏菌■NarGHI硝酸盐还原酶A:大肠埃希氏菌·K86A突变体·H66Y突变体■NrfH细胞色素C醌醇脱氢酶:普通脱硫弧菌■DsbB-DsbA周质氧化酶复合物:大肠埃希氏菌■DsbB-Fab复合物:大肠埃希氏菌■wtDsbB-DsbA(Cys133A)-Q8复合物:大肠埃希氏菌■维生素K环氧化物还原酶:聚球藻属(Synechococcussp.)oMo/Wbis-MGD氧化还原酶■聚硫化物还原酶PsrABC(天然):Thermusthermophileso电子传递链复合物:复合物I■复合物I膜结构域:大肠埃希氏菌■复合物I完整:Thermusthermophileso电子传递链复合物:复合物II■天然富马酸还原酶复合物:大肠埃希氏菌■富马酸还原酶复合物:产琥珀酸沃林氏菌(Wolinellasuccinogenes)■甲酸脱氢酶-N:大肠埃希氏菌■琥珀酸脱氢酶(复合物II):大肠埃希氏菌■琥珀酸:泛醌氧化还原酶(SQR,复合物II):猪心线粒体■琥珀酸:泛醌氧化还原酶(SQR,复合物II):鸡心线粒体o电子传递链复合物:复合物III(细胞色素bc1)■细胞色素bc1:牛■细胞色素bc1:原鸡■细胞色素bc1:Sarcomycescerevisiae■细胞色素bc1:类球红细菌(RhodobacterSphaeroides)o电子传递链复合物:生氧光合作用细胞色素b6f■细胞色素b6f复合物:层理鞭枝藻(Mastigocladuslaminosus)■细胞色素b6f复合物:莱茵衣藻(Chlamydomonasreinhardtii)■细胞色素b6f复合物:念珠藻属(Nostocsp.)PCC7120o电子传递链复合物:复合物IV(细胞色素C氧化酶)■细胞色素C氧化还原酶aa3:Bostaurus(牛)心线粒体■细胞色素C氧化还原酶aa3:脱氮副球菌(Paracoccusdenitrificans)·N131D变体■细胞色素氧化酶cbb3:施氏假单胞菌(Pseudomonasstutzeri)·细胞色素ba3:嗜热栖热菌■细胞色素C氧化酶野生型:类球红细菌■泛醌氧化酶,细胞色素bo3:大肠埃希氏菌o一氧化氮还原酶■一氧化氮还原酶:铜绿假单胞菌o光合系统■光合系统I:Thermosynechococcuselongates■光合系统(植物)I:豌豆(Psiumsativum)■光合系统II:Thermosynechococcuselongates■光合系统II:Thermocynechococcusvulcanuso捕光复合物■捕光复合物:嗜酸红假单胞菌(Rhodopseudomonasacidophila)■捕光复合物:莫氏红螺菌(Rhodospirillummolischianum)■捕光复合物LHC-II,菠菜光合系统II:菠菜■捕光复合物CP29,菠菜光合系统II:菠菜■捕光复合物LHC-II,豌豆光合系统II:豌豆o光合反应中心■光合反应中心:绿色绿芽菌(Blastochlorisviridis)■光合反应中心:类球红细菌■光合反应中心:Thermochromatiumtepidum载体可以由任何适当的微孔材料制成。例如,其可以基于常规的膜载体,如反向渗透膜或超滤膜中所使用的那样。例如,这些载体可以由聚烯烃、纤维素、再生纤维素、醋酸纤维素、聚丙烯腈、聚醚砜或聚砜制成。在本发明的优选实施方式中,载体由聚砜制成。载体膜的化学官能性可以按照其可为低分子量或聚合的添加剂的形式递送至浇铸掺杂物,或者是载体表面的官能化,例如,通过化学处理、接枝聚合或等离子聚合。通过这些方式,例如,可以实现载体的以下化学转化:将胺基转化成羧酸基团,或者反之;将醛转化成胺;以及将羟基转化成羧酸基团。所有这些反应都是本领域公知的。例如,多孔超滤膜可以通过例如以下方式制备:空气浇铸,其中溶解的聚合物溶液在一系列以非常慢的方式控制溶剂蒸发的气流管下通过;溶剂或浮出(emersion)浇铸,其中将溶解的聚合物铺展在移动的带上,并经过液体浴,浴液中的液体与漆(lacquer)中的溶剂交换,并导致孔的形成;热浇铸,其中使用热来促进指定溶剂系统中聚合物的溶解度。然后将漆浇铸到正在被冷却的移动的带上。使漆中的热骤冷,导致开始沉淀,并形成孔。该方法中通常使用的材料包括但不限于再生纤维素、硝酸纤维素、醋酸纤维素、聚酰胺、聚砜、聚(醚砜)、聚碳酸酯、聚(醚酰亚胺)、聚(2,6-二甲基-1,4-氧化亚苯)、聚酰亚胺、聚(偏氟乙烯)、聚四氟乙烯、聚丙烯、聚丙烯腈、聚甲基丙烯酸甲酯、聚乙烯醇和聚二甲基硅氧烷。浇铸物的形态通过最终模件的结构调节。例如,其可以包括用于螺旋缠绕元件的平板;用于中空-纤维元件的中空纤维;或者其可以是管状的。通过控制应用于载体的囊泡溶液中存在的囊泡的浓度和/或沉积在载体上的溶液的体积,可以实现具有包括囊泡连续体的层的膜的制备,所述层具有确定的厚度。Xie等人J.Mater.ChemA,2013,1,7592公开了在聚合物囊泡制备过程中涉及交联的方法,但该交联不改变聚合物囊泡的结构或大小(第7596页第2栏最上一段),始终是与本发明的基团X对应的可交联端基之间的内部交联。类似地WO01/32146中公开的交联始终是内部交联。取决于存在的各种基团的性质,内部交联当然可以在本发明的囊泡中发生,但本发明的基本特征是也发生外部交联,优选地通过多官能性连接剂。本发明相对于Xie等人以及Zhao等人J.MembraneSci.2012,422-428和WO2013/043118公开的方法的优势在于,通过嵌入聚合物囊泡壁中的跨膜蛋白以外的任何可能的通过膜的路径得以最小化,同时在载体膜单位表面积上提供大量可能的跨膜蛋白,从而使通过膜的流量最大化。该方法在技术上简单,产生的膜在物理上结实。附图说明图1显示了实施例1的步骤1中制备的聚合物的NMR谱图。图2显示了实施例2的步骤4的截留分子量实验的结果。图3显示了实施例1的步骤5的流动测试实验的结果。图4和图5是实施例1中制备的膜的扫描电子显微镜图像。图6显示了实施例2的动态光散射测量的结果。图7A和图7B显示了实施例4中制备的囊泡的LSM成像显微图像。图8显示了如实施例4所述将水通道蛋白Z蛋白并入到囊泡中的效果。图9是实施例4的膜的显微图像。图10显示了实施例4的膜中聚丁二烯内部交联的效果。以下的实施例说明了本发明。实施例1材料:·2-甲基-2-噁唑啉,Sigma·三乙胺,Sigma·己烷,无水,Sigma·乙二胺,Sigma·三氟甲磺酸,Sigma·乙酸乙酯,Sigma·水通道蛋白-Z原液,在1%辛基葡糖苷和100mMNaMPOS缓冲液pH7.5中,1mg/ml·100mMNaMPOS缓冲液pH7.5·氯仿(Puriss)·辛基葡糖苷(Anatrace)·胺官能性聚合物囊泡,在Na.MOPS中10mg/mL·PoPR(聚合物与蛋白质的比例,质量)·N-磺基琥珀酰亚胺基-6-(4'-叠氮基-2'-硝基苯基氨基)己酸酯,磺基-SANPAH(Pierce;产品编号22589)·葡聚糖(AmericanPolymerStandardsCorporation)·365nmUV灯(EntelaUVP)·47mm膜模冲片(stamp)·25mm膜模冲片·聚砜膜;孔径150nm(截留超过1000kDa)1)聚合物制备—伯/仲胺封端的聚-2-甲基噁唑啉-聚-二甲基-硅氧烷-聚-2-甲基噁唑啉(PMOXA-PDMS-PMOXA)步骤a)α,ω-羟基-丁基-聚-二甲基-硅氧烷(PDMS)合成:以分子量4000g/mol为目标,将93.03g(0.34mol)八甲基环四硅氧烷和6.97g(0.0025mol)1,3-双(羟基丁基)-四甲基二硅氧烷装入到具有氩气入口、温度计和冷凝管的三口圆底Pyrex反应器中。加入三氟乙酸6.55g(0.05755mol)。将反应混合物在60℃加热48小时。该时间之后,将过量三氟乙酸用蒸馏水萃取,直至水相提取物为中性。然后将反应混合物在高真空下抽提,以除去环状副产物。通过在THF和等体积的5%碳酸钠水溶液中在40-45℃进行48小时弱碱催化的水解,将酯基进一步转化成醇。分离出有机相和水相。通过THF的蒸发回收83.72克产品。通过质子NMR评价产物分子量,在氯仿中通过GPC评价分子量分布。步骤b)伯/仲胺封端的PMOXA-PDMS-PMOXA合成如上述步骤a合成的羟基封端的PDMS用于合成聚PMOXA-PDMS-PMOXA两亲性嵌段共聚物。在三口圆底烧瓶中,将50克(0.012mol)PDMS在高度真空下保持24小时。在下一步中,将反应瓶充以干燥氩气,将聚合物溶解在干燥己烷(200ml)中,并经由隔膜加入到三口烧瓶中。然后,通过在2.45g(0.024mol)三乙胺的存在下逐滴加入6.62g(0.02346mol)三氟甲磺酸酐,并使其补充反应3小时,将冷却的(0-5℃)PDMS活化。将活化的PDMS进一步在氩气下过滤,减压除去己烷。加入250ml干燥乙酸乙酯,以再溶解活化的聚合物,一经在40℃加入23.5g(0.27mol)干燥的2-甲基噁唑啉,开始2-甲基噁唑啉的开环聚合。在氩气下反应12小时之后,加入3倍过量的4.14g(0.069mol)丁基二胺作为终止剂。在高度真空下回收产物,并通过质子NMR评价分子量(示于图1),在氯仿中通过GPC评价分子量分布。产物100%可溶于乙醇,99.5%不溶于己烷。如质子NMR所示,剩余0.5%是未反应的PDMS。2)聚合物囊泡/蛋白-囊泡制备在圆底烧瓶(Pyrex100ml)中将50mgABA嵌段共聚物溶解在2ml氯仿中。然后在高度真空下除去氯仿,形成聚合物薄膜。将该膜用5ml缓冲液(对照)或5ml水通道蛋白-Z含水原液进行水化,并搅拌过夜。在这些样品中,所加入蛋白质的量从聚合物与蛋白质比例1:1变化至1:1200。随后通过在NaMOPS缓冲液中在30kDa渗析膜中通过渗析除去洗涤剂。然后将产生的产物通过径迹蚀刻膜挤出至均匀的200nm大小。3)涂布在该步骤中,沉积的囊泡的浓度保持恒定,并通过将动态光散射(MalvernZetasizerNano)中的计数率(250kcps)与静态衰减器匹配来监测。在不存在光的情况下使磺基-SANPAH(SS)溶液(100mMNaMOPS中10mM,pH7.5)与步骤(1)中制备的囊泡反应(250μL囊泡溶液与50μLSS组合15分钟)。将一组47mm聚砜膜(NanoH2OInc,150nm)通过冲压机切割,并置于特氟隆(Teflon)膜夹具中,用去离子水漂洗。通过压缩空气除去过量水,将300μL(各个)SS-活化的囊泡/蛋白-囊泡溶液置于聚砜载体膜上。然后将膜夹具置于UV光下距光源大约5cm,用箔覆盖保护30分钟。然后使用1ml移液管在不触碰膜表面的情况下从膜表面除去过量反应物。上述步骤重复3次,之后将膜从夹具上取下,使用冲压机从涂布的区域切割25mm直径的膜样品。然后在测试之前将这些样品在振动台上在过量的100mMNaMOPSpH7.5中漂洗。4)截留分子量实验通过测量其截留(cut-off)分子量,即至少90%指定分子量的分子得以被膜保留的点,来测试步骤(2)的25mm样品保留高分子量的能力。将磷酸盐缓冲液(0.03MNa2HPO4+0.03MKH2PO4)使用0.2um膜预过滤,在用于制备溶液之前将pH调节至7.2。将葡聚糖(DXT)标准物溶解在磷酸盐缓冲液中(DXT165kDa、325kDa、548kDa、1300kDa和5000kDa,DXT0.505kDa、4kDa、6kDa、11kDa、20kDa和28kDa)。所有葡聚糖溶液用磷酸盐缓冲液稀释至0.5mg/ml,并在使用之前用0.2umPES膜预过滤。所有过滤实验在10mlAmicon搅拌超滤池(Model8010,MilliporeCorp.)中进行。所有样品根据下述方案评价:·在20psi下过滤10ml体积去离子水,以润湿孔结构和整个系统。·将具有葡聚糖溶液进料的进料线连接至数字蠕动泵(ThermalFisherScienceInc.),将池再加压至20psi,将滤液流量设为5μm/s。·过滤用于平衡的2,000μL水并洗出膜下游的死体积之后,得到800μL滤液溶液样品。·过滤之后由池直接得到1ml透过样品。·用去离子水清洗和漂洗整个系统。·搅拌速度保持在600rpm,所有实验均在室温(22±3℃)进行。透过物进一步使用高压液相色谱(HPLC柱PL1149-6840,MW10,000至200,000,PL1120-6830,MW100至30,000,PL1149-6860,MW200,000至>10,000,000)评价。进料与透过物色谱图的比较使得可以计算保留系数和膜截留分子量。结果如图2所示,显示根据本发明的所有膜保留了所有分子量较高的分子,而对照膜表现出相对较差的性能,截留分子量超过3,000kDa。5)流动测试使用搅拌测试池(Amicon10ml,Model8010,MilliporeCorp.)测试步骤(2)的25mm膜传输纯水的能力,其中进料是纯水。将系统闭合,并设定成在测试之前搅拌至少5分钟。随后,将压力逐渐从1巴增加至5巴,以1巴的间隔收集代表1分钟内经过膜表面的纯水的体积的数据点(在每个压力下独立地收集透过物)。实验还包括了目前市场上最好的市售水过滤膜——来自Millipore的Biomax30kDa用于比较。结果显示于图3,其中LMH/巴是升/m2/小时/巴纯水,即,是压力校正的流速,PoPr代表聚合物:蛋白质比例(注意PoPr越高,水通道蛋白蛋白质的含量越低)。步骤2中制备的具有囊泡涂布但没有水通道蛋白蛋白质的对照膜在所有测试的膜中流速最低。根据本发明的所有膜均表现得明显更好,水通道蛋白含量越高,导致流量越高,水通道蛋白含量最高的膜显著地优于市售的膜。图4和图5显示了根据本发明的膜的SEM。在图4中(放大倍数1000),具有海绵样外观的底层是聚砜载体,其由于浇铸方法而具有大孔隙。上层是包括含有水通道蛋白的囊泡的连续体的连续涂层。在图5中(放大倍数20,000),具有纹理外观的SEM下部是聚砜载体,而最上面的薄层是包括含有水通道蛋白的囊泡的连续体的连续涂层。这两层之间的边界处的亮线是边界层,其中囊泡层与聚砜共价结合。实施例2和3进行模型实验,以确认各种聚合物端基对于制备囊泡和囊泡彼此共价连接的适合性。另外可选的聚合物制备如下。(a)羧基封端的聚-2-甲基噁唑啉-聚-二甲基-硅氧烷-聚-2-甲基噁唑啉(PMOXA-PDMS-PMOXA)将如实施例1的步骤(a)中合成的羟基封端的聚合物Mn=4262g/mol(PDMS)用于合成聚PMOXA-PDMS-PMOXA两亲性嵌段共聚物。在三口圆底烧瓶中,将50克(0.01173mol)PDMS在高度真空下保持24小时。在下一步反应中,将烧瓶充以干燥氩气,将聚合物溶解在经由隔膜加入到三口烧瓶中的干燥己烷(200ml)中。然后,通过在2.45g(0.024mol)三乙胺的存在下逐滴加入6.62g(0.02346mol)三氟甲磺酸酐,并使其补充反应3小时,将冷却的(0-5℃)PDMS活化。然后将活化的PDMS进一步在氩气下过滤,减压除去己烷。加入250ml干燥乙酸乙酯,以使活化的聚合物再溶解,一经在40℃加入23.5g(0.27mol)干燥的2-甲基噁唑啉,则开始2-甲基噁唑啉的开环聚合。在氩气下反应12小时之后,在3.05g(0.030mol)三乙胺的存在下,加入1.3x过量的去质子化丙二酸作为终止剂3.12g(0.030mol)。在高度真空下回收产物,并通过质子NMR评价分子量,在氯仿中通过GPC评价分子量分布。(b)羟基封端的聚-2-甲基噁唑啉-聚-二甲基-硅氧烷-聚-2-甲基噁唑啉(PMOXA-PDMS-PMOXA)将如实施例1的步骤(a)中合成的羟基封端的硅Mn=4262g/mol(PDMS)用于合成聚PMOXA-PDMS-PMOXA两亲性嵌段共聚物。在三口圆底烧瓶中,将50克(0.01173mol)PDMS在高度真空下保持24小时。在下一步中,将反应瓶充以干燥氩气,将聚合物溶解在经由隔膜加入到三口烧瓶中的干燥己烷(200ml)中。然后,通过在2.45g(0.024mol)三乙胺的存在下逐滴加入6.62g(0.02346mol)三氟甲磺酸酐,并使其补充反应3小时,将冷却的(0-5℃)PDMS活化。然后将活化的PDMS进一步在氩气下过滤,减压除去己烷。加入250ml干燥乙酸乙酯,以使活化的聚合物再溶解,一经在40℃加入23.5g(0.27mol)干燥的2-甲基噁唑啉,则开始2-甲基噁唑啉的开环聚合。在氩气下反应12小时之后,加入1.3x过量的氢氧化钾作为终止剂(1.68g(0.030mol),50ml甲醇中)。在高度真空下回收产物,并通过质子NMR评价分子量,在氯仿中通过GPC评价分子量分布。实施例2将250μL实施例1中制备的由胺基封端的聚合物制成的囊泡置于64mL清洁的小玻璃瓶中,并通过将小瓶用铝箔包裹保护其免受光照。加入变化量(0、1、5、10、25和50μl)的双官能性连接剂磺基-SANPAH(100mMNa.MOPS中10mMSulfo-SANPAH,pH7.5),并通过轻轻振动进行搅拌。使反应发生15分钟,之后将100μL溶液置于比色皿中用于动态光散射(DLS)测量,DLS是用于测量溶液中颗粒大小的技术。将样品置于UV灯下大约5cm处,取下盖子和箔,打开灯,将整体用箔帐覆盖。在所有情形中,衰减器固定在6。在UV下15分钟之后,在与磺基-SANPAH反应之前,DLS显示囊泡的直径为200nm。UV辐照导致与磺基-SANPAH反应之后,肉眼可以看出形成大的聚集体。DLS结果如图6所示。这些聚集体在超声下是稳定的,说明存在共价键。作为比较,使用预期与磺基-SANPAH不反应的羟基封端的聚合物进行类似实验。如所预期,不发生交联,因此不发生DLS测得的直径增加。实施例3使用由具有活化羧酸基作为端基的聚合物制成的囊泡进行实验。材料·EDC,Pierce(产品编号22980)·NHS,Pierce(产品编号24500)·MalvernZetasizerNANODLS·超声浴·具有微探头的pH计·如上所述制备的羧基封端的聚合物囊泡·如上所述制备的胺基封端的聚合物囊泡实验根据上述薄膜水化方案使用去离子水制备囊泡。使用DLS显示产生的聚合物囊泡的平均直径为大约200nm。通过向1ml羧基囊泡中加入950μgEDC和570μgofNHS,制备用EDC和NHS活化的羧基囊泡。然后使用HCl将溶液调节至pH5,使其在室温下反应30分钟,产生EDC-NHS活化的囊泡。使(对照)羧基囊泡(1ml)和EDC-NHS活化的囊泡(1ml)溶液与等量胺官能性囊泡(1ml)反应。随后,将所有溶液的pH用去离子水的NaOH稀溶液调节至大约7.5,使其反应至少90分钟。使用静态衰减器设定为5的DLS对100μL产生的样品进行测试。测试之后,将比色皿超声1分钟,然后再测试。经发现,等量胺和羧基囊泡的反应导致形成大的聚集体(通过DLS测量大约2000nm)。但是,当超声时,这些聚集体分散,表明结合是离子的,而不是共价的。相反,等量胺和EDC-NHS活化羧基囊泡的反应导致形成大的聚集体(通过DLS测量大约3600),其在超声时不分散,表明将聚集体保持在一起的力是共价的。实施例4使用二嵌段共聚物聚丁二烯-PMOXA进行一组实验。步骤(a):PB合成按照Hillmyer,M.A.;Bates,F.S.1996,9297,6994-7002的方案加以一些修改,合成聚丁二烯。使用仲丁基丁基锂作为引发剂,在-60至-50℃在THF中进行丁二烯的阴离子聚合。将干燥的两口烧瓶在烘箱中干燥过夜,一口连接有具有彼此隔膜的管线。将烧瓶火焰干燥,加入搅拌子。使用套管向两口烧瓶中加入30ml干燥SolvTHF。在冷凝瓶中冷凝11ml丁二烯(0.13mol)。首先使用液氮冷凝聚丁二烯,然后使用干冰-丙酮浴熔化。使用套管将其转移至两口烧瓶中。迅速加入7ml(0.0098mol)1.4M叔丁基锂引发剂。聚合进行3小时。通过在-60℃加入2ml(0.051mol)环氧乙烷,一经丁二烯完全转化,则完成封端。然后使用酸性甲醇(5mlHCl:50ml甲醇),释放聚丁二烯醇,其通过蒸发溶剂而分离。通过用蒸馏水萃取聚合物环己烷溶液,除去无机盐。将聚合物置于高真空下,以除去水。通过在索氏提取器中使用分子筛在干燥己烷中回流聚合物,进行进一步干燥。步骤(b):PB-PMOXA合成在氩气中在-10℃在2.63g(0.0260M)三乙胺(SigmaAldrichT0886)的存在下将20g(0.0260M)聚丁二烯(Mn769g/mol)用7.33g(0.0260M)三氟甲磺酸酐(SigmaAldrich176176-5G)官能化。将有机盐进一步滤出。三氟甲磺酸盐官能化的PB用作2-甲基-2-噁唑啉(SigmaAldrich137448)阳离子开环聚合的大分子引发剂。聚合在40℃在无水乙酸乙酯(SigmaAldrich270989)中进行12小时。反应用乙二胺0.4g(SigmaAldrich03550)终止。这提供了伯胺和仲胺封端的PB-PMOXA聚合物。聚合物表征:PB12-OHNMR5.45ppm–CH=CH2(重复单元),4.94ppm–CH=CH2(重复单元),2.12ppmCH(重复单元-骨架),1.27ppmCH2(重复单元-骨架),CH2和CH33.65ppm0.82ppm–端基。聚合物溶剂MnMwPDIPB12CHCl35266021.14PB12PMOXA5CHCl36327381.19PB12-PMOXA5-NH-(CH2)-NH2NMRPB:5.45ppm–CH=CH2(重复单元),4.94ppm–CH=CH2(重复单元),2.12ppmCH(重复单元-骨架),1.27ppmCH2(重复单元-骨架),CH2和CH33.65ppm0.82ppm–端基。PMOXA:3.45ppm(-CH2-CH2-N-),2.11ppm(-N-CO-CH3)步骤(c)囊泡制备在圆底烧瓶(Pyrex200ml)中将PB12-PMOXA5-NH-(CH2)2-NH2聚合物(50mg)溶解在1ml氯仿中。在减压下在旋转蒸发仪中将溶剂蒸发,产生聚合物薄膜。随后进行3小时高真空处理,除去痕量氯仿。进一步加入5ml水,并在600rpm下搅拌。通过该方式制备10mg/ml囊泡悬浮液。在取样用于表征(LSM,截流(Stopped-Flow),DLS)时,将悬浮液通过1μm、800nm、400nm、200nm聚碳酸酯径迹蚀刻过滤器(Millipore)连续挤出。每次挤出时,对悬浮液进行取样用于表征。囊泡表征如下。使用低温透射电子显微镜(cryo-TEM)用于颗粒成像,表面官能化使用LSM成像考察。对于cryo-TEM,显微镜是FEITecnaiG2,TF20。使用玻璃化冷冻机器人VitrobotTMFEI对样品进行玻璃化。使用的放大率为25000x(校准31625x)=标尺200μm。对于LSM成像,使上述制备的囊泡表面上存在的胺基端基与四甲基异硫氰酸罗丹明荧光染料(摩尔比1:1000)反应,并相对于去离子水进行渗析。渗析进行至渗析物不显示荧光迹象,然后再改变DI水,以消除非特异性结合。囊泡使用具有Apochromat63x/1.4OilDICM27物镜和561nm激光线的ZeissLSM710倒置共焦显微镜可视化。针孔从50um至70um变化。这使得共焦平面“看穿”囊泡,因此呈现为悬浮物中的光边缘(共焦点中心的囊泡的中心)或者光的盘(共焦点中囊泡顶部),其中囊泡动态地漂浮出入焦点。图7A和图7B显示了清楚地显示囊泡的两张样品显微照片。步骤(d)将蛋白质插入到囊泡中通过水通道膜蛋白——水通道蛋白Z的重构提高聚合物囊泡的水渗透性。对膜水化过程进行改变,以适应在PoPr400下加入蛋白质。简言之:在PoPr400下向水化囊泡蛋白质溶液中加入。接下来的步骤遵照标准囊泡形成方案。在圆底烧瓶(Pyrex200ml)中将PB12-PMOXA5-NH-(CH2)2-NH2聚合物(50mg)溶解在1ml氯仿中。在减压下在旋转蒸发仪中将溶剂蒸发,产生聚合物薄膜。随后进行3小时高真空处理,除去痕量氯仿。进一步加入5ml含有0.1245mg水通道蛋白Z(AppliedBiomimetic)和0.5%辛基葡糖苷(O311–正辛基-β-D-吡喃葡糖苷,Anagrade,Anatrace)的100mMNa-MOPS缓冲液,并在600rpm下搅拌。将10mg/ml蛋白囊泡悬浮液通过200nm聚碳酸酯径迹蚀刻过滤器(Millipore)挤出。渗透性测量使用截流分光计进行。使用截流分光计评价蛋白质插入。测量其为,用水通道蛋白水通道重构的囊泡的水渗透性的增加。所加入蛋白质的量小至400PoPR(聚合物与蛋白质的比例),水渗透性相对于对照囊泡的增加测量为46倍。结果示于图8。步骤(e):膜制备在该实施例中,沉积的囊泡的浓度保持恒定,并通过将动态光散射(MalvernZetasizerNano)中的计数率(250kcps)与静态衰减器匹配来监测。在不存在光的情况下使磺基-SANPAH(SS)溶液(100mMNaMOPS中10mM,pH7.5)与之前制备的PB-PMOXA-NH-(CH2)2-NH2囊泡反应(250μL囊泡溶液与50μLSS组合15分钟)。将一组47mm聚砜膜(手工浇铸)通过冲压机切割,并置于膜夹具中,用去离子水漂洗。通过压缩空气除去过量水,将300μL(各个)SS-活化的囊泡悬浮液置于聚砜载体膜上。然后将膜夹具置于UV光下距光源大约5cm,用箔覆盖保护30分钟。然后使用1ml移液管在不触碰膜表面的情况下从膜表面除去过量反应物。上述步骤重复3次,之后将膜从夹具上取下,使用冲压机从涂布的区域切割25mm直径的膜样品。然后在测试之前将这些样品在振动台上在过量100mMNaMOPSpH7.5中漂洗。图9是产生的膜的纤维照片,表明连续体包括多个在载体膜表面上交联的囊泡。对上述步骤中制备的膜用10或150μL由以下组成的自由基引发溶液进行处理:25mM七水合硫酸亚铁(II),25mM偏亚硫酸氢钠,25mM过硫酸钾。处理导致PB疏水核心的交联。使用标准截留分子量分析技术对产生的膜样品进行孔径分布测试。通过测量其截留分子量,即至少90%指定分子量的分子被膜保留的点,对前述步骤中制备的25mm样品进行其保留高分子量物质的能力的测试。将磷酸盐缓冲液(0.03MNa2HPO4+0.03MKH2PO4)使用0.2um膜预过滤,在用于制备溶液之前将pH调节至7.2。将葡聚糖(DXT)标准物溶解在磷酸盐缓冲液中(DXT165kDa、325kDa、548kDa、1300kDa和5000kDa,DXT0.505kDa、4kDa、6kDa、11kDa、20kDa和28kDa)。所有葡聚糖溶液用磷酸盐缓冲液稀释至0.5mg/ml,并在使用之前用0.2um聚醚砜膜预过滤。所有过滤实验在10mlAmicon搅拌超滤池(Model8010,MilliporeCorp.)中进行。所有样品根据下述方案评价。在20psi下过滤10ml体积去离子水,以润湿孔结构和整个系统。将具有葡聚糖溶液进料的进料线连接至数字蠕动泵(ThermalFisherScienceInc.),将池再加压至20psi,将滤液流量设为5μm/s。过滤用于平衡的2,000μL水并洗出膜下游的死体积之后,得到800μL滤液溶液样品。过滤之后由池直接得到1ml透过样品。用去离子水清洗和漂洗整个系统。搅拌速度保持在600rpm,所有实验均在室温下(22±3℃)进行。透过物进一步使用高压液相色谱(HPLC柱PL1149-6840,MW10,000至200,000,PL1120-6830,MW100至30,000,PL1149-6860,MW200,000至>10,000,000)评价。进料与透过物色谱图的比较使得可以计算保留系数和膜截留分子量。结果如图10所示,其显示当用囊泡涂布时,对照膜的截留分子量降低至一半。使用引发剂使聚丁二烯核交联时,囊泡涂布膜的截留分子量降低至4000Ka。截留分子量的降低显示出依赖于所用交联剂的量。当前第1页1 2 3
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1