一种核壳型复合分子筛及其分离二氧化碳的用途的制作方法
本发明涉及一种结构可调控的核壳型复合分子筛材料,对二氧化碳具有吸附选择性。
背景技术:
二氧化碳是产生影响气候变化的主要的温室气体,工业废气和汽车尾气等排放的大量二氧化碳将会带来严重的环境问题。二氧化碳既是一种温室气体,也是一种重要的碳资源,在农业,轻工、机械、化工以及其它行业中都有广泛应用,所以二氧化碳的捕集和利用已引起广泛关注。如2016年6月王保登申请的《一种高性能羰基二氧化碳吸附材料的制备方法及其应用》(cn105554850a)通过引入强金属阳离子掺杂碳材料,获得在低压下对二氧化碳具有良好吸附性能的吸附材料。2016年10月赵灵智申请的《二氧化碳吸附材料的制备》(cn106040191a)制备了一种无毒,热稳定性良好,耐常规化学腐蚀,对二氧化碳气体小分子具有良好吸附效果的吸附剂。目前沸石分子筛例如13x和5a等是性能较为优异的商用二氧化碳吸附剂,然而在实际应用中由于它们对其他气体如氮气和水也有高吸附容量,导致对二氧化碳的吸附选择性低,并成为吸附技术推广应用的瓶颈。
技术实现要素:
本发明基于二氧化碳和氮气的分子动力学直径的差异,在现有低成本商用沸石分子筛表面构筑具有选择性透过二氧化碳而阻隔其他气体的多孔材料,形成核壳型结构的复合分子筛材料。通过构筑不同壳层厚度的核壳型复合分子筛材料,并通过离子交换调节壳层分子筛孔径,在保持原有沸石分子筛优异吸附容量的同时,提高二氧化碳的吸附选择性。
本发明所述核壳型复合分子筛,选用商用分子筛,如13x、β、zsm-5、5a等分子筛为核体材料,naa、sba-15、mcm-41分子筛为壳层材料,经离子交换后得到n@ms复合型分子筛,其中n为核体材料,m为交换离子,s为壳体材料,如13x@naka、13x@ksba-15、β@kmcm-41、β@ksba-15、zsm-5@kmcm-41、zsm-5@ksba-15、5a@ksba-15复合分子筛材料。
本发明中系列核壳复合分子筛材料不同晶化时间和不同程度的离子交换,其处理方法和原理相似。因此,为节约篇幅,本说明书主要提供晶化时间为30,60和120分钟,钾离子交换程度为8%,18%和30%的典型13x@naka核壳复合分子筛材料的合成及其对二氧化碳的选择性吸附
本发明所采用的技术方案包括:通过采用不同晶化时间进行合成,调控13x@naa复合分子筛材料的壳层厚度;采用不同氯化钾溶液浓度和时间进行离子交换,调控13x@naka复合分子筛材料的壳层孔径。
本发明合成13x@naa复合分子筛所采用的晶化时间为30-120分钟,分别在室温条件下进行钾离子交换2-3次,控制时间在20-40分钟,得到钾离子交换程度为8-30%的13x@naka复合分子筛材料。
本发明获得的13x@naka复合分子筛材料可有效地调控气体的扩散途径和透过性能,从而实现壳层分子筛对二氧化碳的高选择性,核层分子筛对二氧化碳的高吸附容量。
本发明获得的13x@naka复合分子筛材料的二氧化碳的最高选择性为422.3,二氧化碳的最高吸附容量为4.07mmol/g。
对于不同壳层厚度的核壳型复合分子筛材料,可以通过不同程度的离子交换,控制壳层孔径大小,实现二氧化碳可调控的选择性吸附分离,可广泛应用于现实生产生活中汽车尾气,烟道气等区域的多组分气体的吸附分离,实现环境的净化以及能源的捕集利用。
附图说明
图1为晶化时间分别为30,60和120分钟所得到的13x@naa核壳复合分子筛材料与纯13x分子筛的扫描电镜图对比。
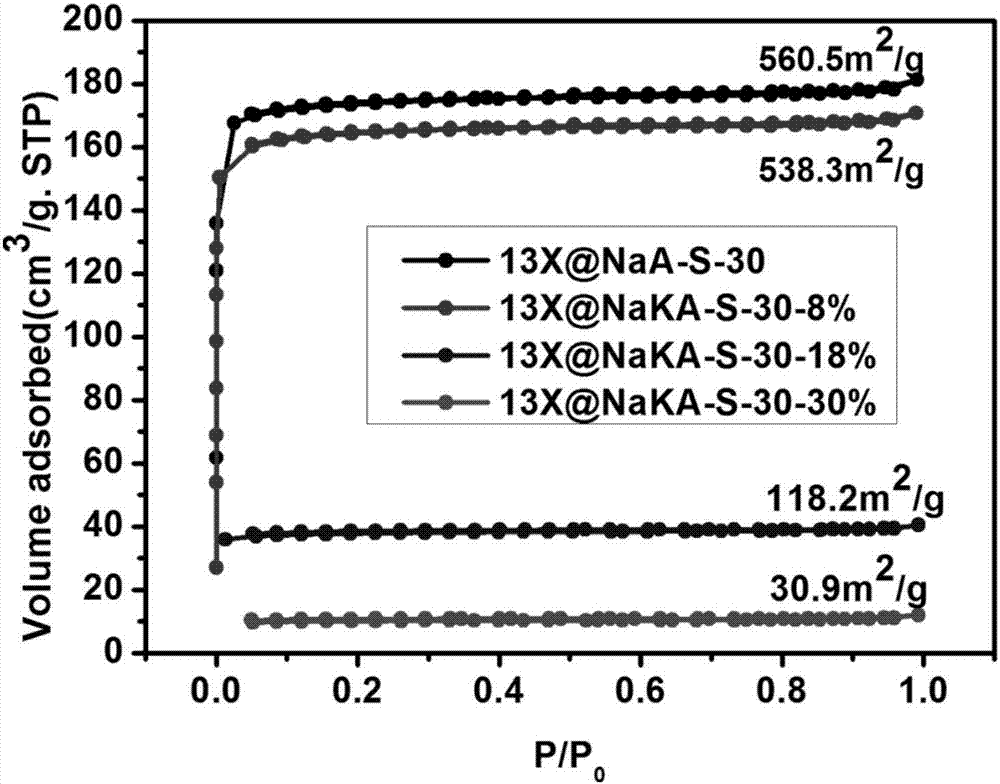
图2为晶化30分钟,不同钾离子交换所得系列13x@naka核壳复合分子筛材料在77k下氮气的吸附等温曲线和比表面积。
图3为晶化30分钟,未经过钾离子交换的13x@naa核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图4为晶化30分钟,进行8%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图5为晶化30分钟,进行18%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图6为晶化30分钟,进行30%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图7为晶化120分钟,进行8%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图8为晶化120分钟,进行18%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
图9为晶化120分钟,进行30%钾离子交换所得13x@naka核壳复合分子筛材料在298k下二氧化碳和氮气的吸附曲线。
具体实施方案
以下结合具体实施例,对本发明做进一步说明。
本发明中系列核壳复合分子筛材料不同晶化时间和不同程度的离子交换,其处理方法和原理相似。因此,本说明书主要提供晶化时间为30,60和120分钟,钾离子交换程度为8%,18%和30%的典型13x@naka核壳复合分子筛材料的合成及其对二氧化碳的选择性吸附。二氧化碳和氮气吸附性测定采用静态吸附的方法。
实施例1、晶化时间30分钟合成13x@naa核壳复合分子筛
13x在使用前通过在500℃加热1小时,采用低温等离子体表面处理10分钟使其活化,将1g活化的13x粉末分散在一定量的naa前体凝胶(1.9naoh/1.5naalo2/3.5nasio3·9h2o/43h2o)中。在333k下搅拌混合均匀,将混合物浆液转移到高压釜中并在373k下晶化30分钟。然后将样品过滤,并用蒸馏水洗涤3次,在383k下干燥,所得材料记为13x@naa-30。
如图1所示,其扫描电镜图片表明已生成了稳定的核壳结构13x@naa-30
实施例2、晶化时间60分钟合成13x@naa核壳复合分子筛
13x在使用前通过在500℃加热1小时,采用低温等离子体表面处理10分钟使其活化,将1g活化的13x粉末分散在一定量的naa前体凝胶(1.9naoh/1.5naalo2/3.5nasio3·9h2o/43h2o)中。在333k下搅拌混合均匀,将混合物浆液转移到高压釜中并在373k下晶化60分钟。然后将样品过滤,并用蒸馏水洗涤3次,在383k下干燥,所得材料记为13x@naa-60。
如图1所示,其扫描电镜图片表明已生成了稳定的核壳结构13x@naa-60
实施例3、晶化时间120分钟合成13x@naa核壳复合分子筛
13x在使用前通过在500℃加热1小时,采用低温等离子体表面处理10分钟使其活化,将1g活化的13x粉末分散在一定量的naa前体凝胶(1.9naoh/1.5naalo2/3.5nasio3·9h2o/43h2o)中。在333k下搅拌混合均匀,将混合物浆液转移到高压釜中并在373k下晶化120分钟。然后将样品过滤,并用蒸馏水洗涤3次,在383k下干燥,所得材料记为13x@naa-120。
如图1所示,其扫描电镜图片表明已生成了稳定的核壳结构13x@naa-120
实施例4、晶化30分钟,未经钾离子交换的13x@naa核壳复合分子筛及其二氧化碳的吸附性能
其氮气吸附等温线和比表面积如图2所示,交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到4.28mmol/g,氮气的吸附量达到0.27mmol/g,二氧化碳的选择性达到73.3。
实施例5、晶化30分钟,进行8%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化30分钟的核壳复合分子筛材料13x@naa-30放入烧杯中,加入5mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到8%钾离子交换的复合材料,记为13x@naka-30-8%。其氮气吸附等温线和比表面积如图2所示。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到4.07mmol/g,氮气的吸附量达到0.20mmol/g,二氧化碳的选择性达到81.9。
实施例6、晶化30分钟,进行18%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化30分钟的核壳复合分子筛材料13x@naa-30放入烧杯中,加入10mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到18%钾离子交换的复合材料,记为13x@naka-30-18%。其氮气吸附等温线和比表面积如图2所示。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到3.41mmol/g,氮气的吸附量达到0.11mmol/g,二氧化碳的选择性达到172.6。
实施例7、晶化30分钟,进行30%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化30分钟的核壳复合分子筛材料13x@naa-30放入烧杯中,加入20mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到30%钾离子交换的复合材料,记为13x@naka-30-30%。其氮气吸附等温线和比表面积如图2所示。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到2.60mmol/g,氮气的吸附量达到0.03mmol/g,二氧化碳的选择性达到357.4。
实施例8、晶化120分钟,进行8%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化120分钟的核壳复合分子筛材料13x@naa-120放入烧杯中,加入10mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到8%钾离子交换的复合材料,记为13x@naka-120-8%。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到3.30mmol/g,氮气的吸附量达到0.18mmol/g,二氧化碳的选择性达到128.8。
实施例9、晶化120分钟,进行18%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化120分钟的核壳复合分子筛材料13x@naa-120放入烧杯中,加入20mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到18%钾离子交换的复合材料,记为13x@naka-120-18%。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到2.89mmol/g,氮气的吸附量达到0.04mmol/g,二氧化碳的选择性达到318.2。
实施例10、晶化120分钟,进行30%钾离子交换合成13x@naka核壳复合分子筛及其二氧化碳的吸附性能
将1g晶化120分钟的核壳复合分子筛材料13x@naa-120放入烧杯中,加入40mmol/l的氯化钾溶液,在298.15k下搅拌30分钟。然后用蒸馏水洗涤样品并在383.15k下干燥,得到30%钾离子交换的复合材料,记为13x@naka-120-30%。
交换后的气体吸附曲线图,分析结果表明,二氧化碳的吸附量达到1.84mmol/g,氮气的吸附量达到0.02mmol/g,二氧化碳的选择性达到422.3。
- 还没有人留言评论。精彩留言会获得点赞!