包括离散氧化铝纳米材料的正电极以及形成氧化铝纳米材料的方法与流程
二次或可充电锂离子电池通常被用于许多固定和便携装置中,例如在客户电子设备、汽车和航空工业中遇到的那些装置。锂类型的电池由于如下各种原因已经得到普及:包括相对高的能量密度、与其他种类的可充电电池相比一般不显示出任何的记忆效应、相对低的内阻、以及不使用时低的自放电速率。在锂电池的有效寿命期间锂电池经受重复电力循环的能力使得它们成为有吸引力并且可靠的电源。
技术实现要素:
在本文中公开的方法的示例中,通过将氧化铝前驱体和酸混合来形成溶液。将碳材料加入到溶液中,以形成其中具有碳材料的含水混合物。使用所述含水混合物进行水热合成,从而在碳材料上生长前驱体纳米结构。对碳材料上的前驱体纳米结构进行退火以便去除碳材料并形成氧化铝纳米材料。
氧化铝纳米材料的示例可以用作锂离子电池的正电极中的添加剂。正电极的示例包括锂基活性材料、粘结剂、导电填料和离散氧化铝纳米材料。在整个正电极中,氧化铝纳米材料作为添加剂与锂基活性材料、粘结剂以及导电填料混合。
附图说明
通过参考下面详细的描述和附图,本公开内容的示例的特征将变得清楚,其中相同的附图标记对应相似(尽管可能不相同)的部件。为了简洁,具有在先已描述的功能的附图标记或特征在结合其出现的其他附图时可以描述或可以不描述。
图1A-1D是一起示出了用于形成本文所公开的氧化铝纳米材料的示例的方法的几个示例的示意图和部分截面图;
图2是电流收集器上的正电极的示例的截面图;
图3是锂离子电池的示例(包括本文所公开的正电极的示例)的透视示意图;
图4是由本文所公开的方法的示例形成的氧化铝纳米材料的示例的扫描电子显微镜(“SEM”)图片,使用标尺为4.29μm;
图5是由本文所公开的方法的示例形成的氧化铝纳米材料的示例的透射电子显微镜(“TEM”)图片,使用标尺为2μm;
图6是从氧化铝纳米材料中心径向并向外延伸的纳米结构之一的示例的TEM图片,使用标尺为50nm;
图7是由比较方法形成的氧化铝纳米棒的示例的SEM图片,使用标尺为300nm;
图8是示出对于由比较方法形成的氧化铝纳米棒的示例和对于由本文所公开的方法的示例形成的氧化铝纳米材料的示例的表面积(m2/g,左边Y轴)相对于酸碱度(PH)值(X轴)的图;以及
图9是示出对于包括具有作为添加剂的离散氧化铝纳米材料的正电极的示例性硬币状电池的放电容量(mAh/g,左边Y轴)相对于循环数(X轴)的图。
具体实施方式
锂离子电池通常通过在负电极(有时称阳极)与正电极(有时称阴极)之间可逆地传递锂离子来运作。负电极和正电极位于用电解质溶液浸泡的多孔聚合物隔膜的相对侧上,所述电解质溶液适合于传导锂离子。在充电期间,锂离子注入(例如添加、合金等)到负电极,而在放电期间,锂离子从负电极逸出。每个电极也都与各自的电流收集器相关联,其通过允许电流在负电极与正电极之间穿过的可中断的外部电路连接。
在锂离子电池中,在电解质中残留的水污染物可与诸如六氟磷酸锂(LiPF6)的锂盐反应,产生氢氟酸(HF)。HF可与电池的有源部件和无源部件两者都起反应,这会限制电池的循环寿命。HF生成的减少有助于创造具有长循环寿命的锂离子电池。铝氧化物可以通过用作HF清除剂来减少HF的生成。根据下面的反应(I),铝氧化物可以清除HF:
Al2O3+6HF→2AlF3+3H2O(I)
其中氧化铝可以与HF反应生成氟化铝(AlF3)和水。认为AlF3产物也可有助于形成的固体电解质界面(SEI)的稳定性。
在本文所公开的正电极中,离散氧化铝纳米材料作为添加剂加入。如在本文中使用的,“离散”表示纳米材料为独特结构,其并不被嵌入在活性材料、粘结剂、导电填料或其他氧化铝纳米材料内或不被涂覆在其上。遍及正电极,将添加剂与活性材料、粘结剂和导电填料混合。离散氧化铝纳米材料可以至少部分地通过用作HF清除剂来改善锂离子电池的循环寿命。通过清除HF,离散氧化铝纳米材料可减少阴极/正电极过渡金属(例如锰、镍和钴)溶解,这抑制了活性材料的损耗。此外,迁移到阳极/负电极的还原量的溶解的过渡金属离子可在阳极处被还原成纯金属纳米颗粒。纯金属纳米颗粒可对在阳极处的固体电解质界面(SEI)的形成起到催化作用。
本文所公开的氧化铝纳米材料可包括从中心径向并向外延伸的多个纳米结构,使得它们像海胆。纳米结构可在中心处或中心附近彼此连接。每个纳米结构可以沿着纳米结构的长度远离中心直径减小。在组合体中小的空间(即,间隙)可使一个纳米结构与另一个纳米结构间隔开。
现在参考图1A-1D,将讨论用于形成氧化铝纳米材料的方法的示例。在示例中,该方法部分地涉及水热合成以形成氧化铝纳米材料。
转到图1A,含水混合物16通过在容器18中混合去离子水、Al2O3前驱体12、酸14和碳材料19来形成。Al2O3前驱体12可以是氯化铝(AlCl3)或异丙醇铝(Al(O-i-Pr)3)。在示例中,约12g的Al2O3前驱体12可被添加用于约60mL的含水混合物16。在Al2O3前驱体12被添加到容器18中的去离子水中之后,可通过搅拌使Al2O3前驱体12完全溶解。可以使用磁性搅拌棒、手动搅拌棒或本领域技术人员已知的任何其他合适的方法来混合组分。例如,含水混合物16可以被混合持续从约5分钟至约2小时范围内的时间。在示例中,含水混合物16被混合持续约30分钟。
酸14可以是盐酸(HCl)(例如,1M HCl)、H2SO4、HNO3、H2PO4或任何其他合适的酸。酸14被添加到含水混合物16中,直到混合物16获得期望的pH值。在酸14已经被添加之后混合物16的pH值的范围可以为从约1至约3。
碳材料19可以悬浮或分散到去离子水中。可以使用能为Al2O3提供异质成核点并在水热合成期间为惰性的任意碳材料19。在示例中,碳材料19容易分散在含水混合物16中,具有用作异质成核点的许多缺陷的大比表面积,并在水热合成之后容易被去除(例如,通过热氧化被去除)。在示例中,碳材料19是中空碳或石墨。中空碳可通过热氧化炭黑来制备。合适的可商购获得的炭黑颗粒的一些示例包括XC72(卡博特公司)、(阿克苏诺贝尔)、以及Black Pearl(BP2000)(卡博特公司)。在示例中,被包括在含水混合物16中每1克的Al2O3前驱体12可以添加从约0.8mg至约2.5mg的碳材料19。
在含水混合物16的水热合成期间,碳材料19提供异质成核点,并因此促进Al2O3前驱体纳米结构24的晶核形成和生长过程(参见图1C)。通过在水热合成期间提供异质成核点,认为碳材料19提供了Al2O3前驱体纳米结构24能够从其生长的中心结构。这些Al2O3前驱体纳米结构24从中心径向并向外生长。如此,碳材料19能够使得最终形成的氧化铝纳米材料26(参见图1D)具有类似于海胆的结构,即,从中心径向并向外延伸的单个纳米结构。此外,认为碳材料19增大了Al2O3前驱体纳米结构24的产量,并且因此最终增大了氧化铝纳米材料26的产量。碳材料19的边缘和/或腔为Al2O3前驱体纳米结构24的生长提供了成核点。
现在转到图1B,在将含水混合物16混合之后,可以将含水混合物16添加到封闭系统20。在示例中,封闭系统20为高压釜。高压釜的一些示例包括聚四氟乙烯内衬(例如,内衬)或铜内衬不锈钢高压釜。内衬高压釜在低于200℃的温度下使用。铜内衬高压釜在200℃或以上的温度下使用。
如图1B所示,在封闭系统20中执行水热合成。更特别地,在封闭系统20内,含水混合物16经受加热和蒸汽压力持续特定量的时间。加热的温度范围从约150℃至约200℃。蒸汽压力范围从约700psi至约1380psi。加热和蒸汽压力施加的时间范围从约24小时至约48小时。在示例中,封闭系统20可升温至约200℃并持续约24小时。认为在封闭系统20中的蒸汽压力可以在1000psi左右。
如上指出,经受水热合成的含水混合物16其中具有水溶性Al2O3前驱体12。在封闭系统20中应用加热和蒸汽压力由水溶性Al2O3前驱体12形成Al2O3前驱体纳米结构24。在示例中,Al2O3前驱体纳米结构24是附接到碳材料19的AlOOH瓣或钉。若干Al2O3前驱体纳米结构24附接到碳材料19,且连同Al2O3前驱体纳米结构24一起形成类似海胆的纳米材料。这种类似海胆的纳米材料具有从碳材料19的成核点径向并向外生长的许多固态Al2O3前驱体纳米结构24。
如图1C中所示,在水热合成之后,若干Al2O3前驱体纳米结构24生长在碳材料19的单个颗粒上。认为在水热合成期间形成的至少一些Al2O3前驱体纳米结构24附接到中空碳19,如图1C中所示。若干Al2O3前驱体纳米结构24甚至可以从相同优选的点生长,并且因此可以附接至其他Al2O3前驱体纳米结构24。在这些示例中,当Al2O3前驱体纳米结构24生长时,Al2O3前驱体纳米结构24保持附接至碳材料19表面。Al2O3前驱体纳米结构24继续生长成类似海胆的氧化铝纳米材料26(图1D中所示)。
在该方法的一个特定示例中,Al2O3前驱体12为AlCl3,并且酸14为HCl。AlCl3和1M HCl被添加到去离子水中,以形成水溶液(未示出)。在这个示例中,添加1M HCl,直到溶液具有1.5的pH值。在这个示例中,还添加了中空碳到溶液中,如碳材料19,从而形成含水混合物16。碳材料19可以在添加Al2O3前驱体12和/或酸14之前或之后添加,或者与其同时添加。应当理解,由于中空碳19并不与Al2O3前驱体12或酸14反应,因此可以在形成含水混合物16期间的任何时候添加其他组分。由于Al2O3前驱体12和酸14将溶解在去离子水中,因此可以在添加碳材料19和形成含水混合物16之前形成溶液。在先前所述的特定示例中,一旦AlCl3溶解后,则该溶液具有1.5的pH,且添加中空碳以形成含水混合物16,将含水混合物16置于封闭系统20(例如高压釜)中。加热和蒸汽压力应用于封闭系统20,以引起如先前所述的类似海胆的Al2O3前驱体纳米结构24的形成。在这个示例中,AlOOH为形成的Al2O3前驱体纳米结构24。
在水热合成之后,应该理解的是含水混合物16已经被改变(在图1C中由附图标记16’表示),并至少包括Al2O3前驱体纳米结构24,其如先前描述的形成类似海胆的形态。在含水混合物16’中存在至少一些去离子水。在一些情况下,其他离子(如Cl-)也可以以不影响Al2O3前驱体纳米结构24的量而存在。
在水热合成之后,然后可使用任何合适的分离技术从含水混合物16’中去除Al2O3前驱体纳米结构24。例如,可通过真空过滤、离心力或任何其他合适的方法去除Al2O3前驱体纳米结构24。在从含水混合物16’分离Al2O3前驱体纳米结构24期间和/或之后可用去离子水对Al2O3前驱体纳米结构24进行多次洗涤。可以期望的是在退火过程中使用Al2O3前驱体纳米结构24之前用去离子水洗涤Al2O3前驱体纳米结构24。
在Al2O3前驱体纳米结构24从含水混合物16’分离并洗涤之后,Al2O3前驱体纳米结构24可在从约60℃至约80℃的温度范围内干燥从约12小时至约24小时的时间。
然后干燥后的Al2O3前驱体纳米结构24可进行不同示例的热处理,以形成氧化铝纳米材料26。在示例中,热处理是在空气或另一含氧环境中执行的退火过程(即,加热之后缓慢地炉冷却)。热处理可在从约400℃至约800℃的温度下实施从约3小时至约8小时的时间。在示例中,热处理在550℃下实施约5小时。在热处理期间,形成氧化铝纳米材料26。特别地,空气用作Al2O3前驱体纳米结构24的氧化环境,并因此形成氧化铝纳米材料26。此外,在热处理期间,碳材料19被燃烧掉,以类似海胆结构/形态留下氧化铝纳米材料26(参见图4和图5)。
在示例中,在热处理期间,在中空碳19与Al2O3前驱体纳米结构24之间发生下述反应(II、III),以形成氧化铝纳米材料26:
2γ-AlOOH→γ-Al2O3+H2O(II)
C+(来自空气的)O2→CO2↑ (III)
Al2O3前驱体纳米结构24可被氧化以形成Al2O3(反应I)。中空碳燃烧掉,如反应(II)中所示。
最终的氧化铝纳米材料26的形态的示例在图4和图5中示出。这些纳米材料如何形成的描述在示例部分中阐述。
图1D示意性并分别示出了一个氧化铝纳米材料26。从中心径向并向外延伸的每个纳米结构具有从约10nm至约200nm范围内的直径。每个纳米结构的长度在从约80nm至约3微米的范围内。纳米结构的直径可以沿着其长度减小,使得纳米结构末端为点,或具有钉状结构。与金属氧化物纳米颗粒(其可以被看作是零维的,这是因为它基本上是点)或金属氧化物纳米棒(其可以被看作是一维的,这是因为它基本上是线)相比,氧化铝纳米材料26具有较大的表面。在示例中,每个氧化铝纳米材料26的表面积至少约150m2/g。相比之下,纳米颗粒一般具有从大于0m2/g至约100m2/g范围内的表面积,以及纳米棒一般具有从约115m2/g至约150m2/g范围内的表面积。氧化铝纳米材料26的较大的表面积提高了它们减少HF形成的能力。氧化铝纳米材料26可物理或化学吸收HF。氧化铝纳米材料26的较大的表面积提供给氧化铝纳米材料26更多的吸收点,并因此实现电解质中的HF更好地减少。
在获得氧化铝纳米材料26后,氧化铝纳米材料26可以作为添加剂添加到锂离子电池的正电极组合物中。在示例中,将离散氧化铝纳米材料26添加到正电极组合物中。在另一示例中,将氧化铝纳米材料26与纳米材料26’一起添加到正电极组合物中,纳米材料26’通过断开(有意地或者在正电极组合物形成期间)从纳米材料26的中心径向并向外延伸的一些纳米结构来制备。所断开的纳米结构26’倾向于侧向下铺设并且大体上均匀地分散于整个电极组合物。正电极组合物包括至少活性材料。这将参照图2进行进一步详细描述。
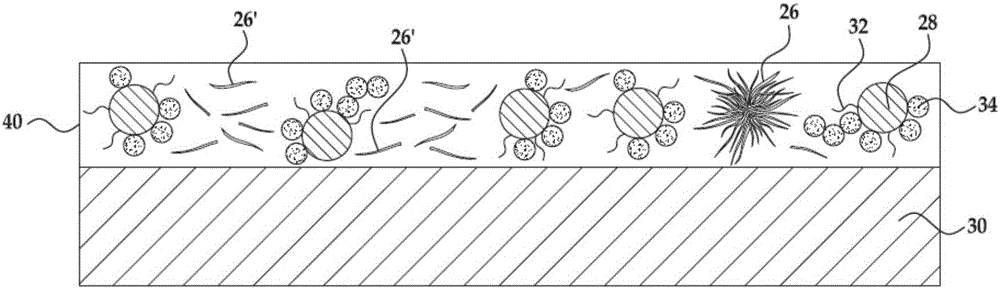
现在将参照图2讨论用于制备锂离子电池300的正电极40的方法的示例(参见图3)。图2示出了载体30上的正电极40的示例,所述正电极40包括锂基活性材料28、粘结剂32、导电填料34、以及作为添加剂的离散氧化铝纳米材料26。
在制备正电极40的示例中,氧化铝纳米材料26与锂基活性材料28以及导电填料34干混合。在一些情况下,粘结剂32还与其他组分26、28、34干混合。然后可以添加溶剂。在其他情况下,粘结剂32与溶剂混合在一起,并且然后添加到干混合组分26、28、34中。如以下将进行的更详细的讨论,取决于选择粘结剂32来形成分散体或混合物,溶剂可以是去离子水或有机溶剂。
锂基活性材料28可以包括如下的任何锂基活性材料:其能够充分地经历锂嵌入和脱嵌入,同时铝或另一合适的电流收集器30用作锂离子电池300的正极端(参见图3)。适用于本示例正电极40的一类常见的已知锂基活性材料包括层状锂过渡金属氧化物。例如,锂基活性材料28可以是尖晶石氧化锰锂(LiMn2O4)、氧化锂钴(LiCoO2)、锰-镍氧化物尖晶石[Li(Li(Mn1.5Ni0.5)O2]、或者层状镍锰钴氧化物(通式为xLi2MnO3·(1-x)LiMO2或者M由任意比例的Ni、Mn和/或Co构成)。特定示例的层状镍-锰-钴氧化物包括(xLi2MnO3·(1-x)Li(Ni1/3Mn1/3Co1/3)O2)。其他合适的锂基活性材料包括Li(Ni1/3Mn1/3Co1/3)O2,Lix+yMn2-yO4(LMO,0<x<1和0<y<0.1)、或者锂铁聚阴离子氧化物,例如锂铁磷酸盐(LiFePO4)或锂铁氟磷酸盐(Li2FePO4F)、或富锂层状结构。也可以利用其他锂基活性材料,例如,LiNi1-xCo1-yMx+yO2或者LiMn1.5-xNi0.5-yMx+yO4(M由任意比例的Al、Ti、Cr、和/或Mg构成)、稳定的氧化锂锰尖晶石(LixMn2-yMyO4,其中M由任意比例的Al、Ti、Cr、和/或Mg构成)、氧化锂镍钴铝(例如,LiNi0.8Co0.15Al0.05O2或NCA)、铝稳定的锂锰氧化物尖晶石(例如,LixAl0.05Mn0.95O2)、氧化锂钒(LiV2O5)、Li2MSiO4(其中M由任意比例的Co、Fe、和/或Mn构成)、以及任何其他高能镍-锰-钴材料(HE-NMC、NMC或LiNiMnCoO2)。通过“任意比例”表示任何元素都可以以任意量存在。因此,在一些示例中,M可以是有或者没有Cr、Ti、和/或Mg的Al,或者所列元素的任何其他组合。在另一示例中,阴离子置换可以在任一示例的锂过渡金属基活性材料的晶格中进行来稳定晶体结构。例如,任意O原子可被F原子取代。
正电极40的锂基活性材料28可以与粘结剂32、导电填料34、以及氧化铝纳米材料26混合。粘结剂32将锂基活性材料28与导电填料34结构上保持在一起。适合的粘结剂32的一些示例包括聚偏氟乙烯(PVdF)、聚环氧乙烷(PEO)、乙烯丙烯二烯单体(EPDM)橡胶、羧甲基纤维素(CMC)、丁苯橡胶(SBR)、丁苯橡胶-羧甲基纤维素(SBR-CMC)、聚丙烯酸(PAA)、交联的聚丙烯酸-聚氮丙啶、聚酰亚胺、或者任何其他合适的粘结剂材料。其他适合的粘结剂的示例包括聚乙烯醇(PVA)、藻酸钠、或者其他水溶性粘结剂。
导电填料34可以为导电碳材料。导电碳34可以为高表面积碳,例如,乙炔黑或另一碳材料(例如Super P)。适合的导电填料34的其他示例包括石墨烯、石墨、碳纳米管和/或碳纳米纤维。导电填料34确保正极侧电流收集器30与正电极40中的锂基活性材料28之间的电子导电。
如上所述,氧化铝纳米材料26为从中心径向并向外延伸的纳米结构,使得它们类似海胆。除了氧化铝纳米材料26之外,正电极40中的添加剂还可以包括断开海胆结构26的纳米材料26’。氧化铝纳米材料26和纳米材料26’没有嵌入其他正电极组分中,或者涂覆在其他正电极组分上。在一些示例中,氧化铝纳米材料26具有至少150m2/g的表面积。在示例中,按正电极40的总重量百分比计,氧化铝纳米材料26的含量的范围为从大于0重量%至约10重量%。
在制造正电极40的方法的示例中,氧化铝纳米材料26与粘结剂32、导电填料34、以及锂基活性材料28混合。所有这些组分都可以通过干研磨手动混合。在所有这些组分被一起研磨之后,研磨组分与水或有机溶剂(取决于所使用的粘结剂32)结合以形成分散体/混合物。在示例中,溶剂为极性非质子溶剂。适合的极性非质子溶剂的示例包括二甲基乙酰胺(DMAc)、N-甲基-2-吡咯烷酮(NMP)、二甲基甲酰胺(DMF)、二甲基亚砜(DMSO)、或另外的路易斯碱,或者它们的组合。当使用水溶性粘结剂(例如藻酸钠)时,溶剂可以为水。
分散体/混合物可以通过研磨来混合。研磨有助于将分散体/混合物转换成可涂覆的浆。低剪切研磨或者高剪切研磨可以用来混合分散体/混合物。分散体/混合物的研磨时间范围为从约10分钟到约20小时,这取决于研磨剪切速率。在示例中,使用旋转混合器约20分钟以约2000rmp来研磨分散体/混合物。
在分散体/混合物的一个示例中,锂基活性材料28的量范围为从约50重量%到约95重量%(基于分散体/混合物的总固体重量%),导电填料34的量范围为从约5重量%到约20重量%(基于分散体/混合物的总固体重量%),粘结剂32的量范围为从约5重量%到约20重量%(基于分散体/混合物的总固体重量%),以及氧化铝纳米材料26的量范围为从大于0重量%高至约10重量%(基于分散体/混合物的总固体重量%)。
然后将浆沉积到载体30上。在示例中,载体30为正极侧电流收集器。应当理解的是载体30可以由铝或本领域技术人员已知的任何其他合适的导电材料来形成。所选的载体30应当能够从与其连接的外部电路收集自由电子,并且将自由电子移动到与其连接的外部电路。
浆可以使用任何适合的技术来沉积。作为示例,浆可以浇铸在载体30的表面上,或可以散布在载体30的表面上,或者可以使用槽模涂布机涂覆在载体30的表面上。
为了除去任何残留的溶剂和/或水,所沉积的浆可以经受干燥处理。可以使用任何适合的技术来完成干燥。例如,在环境条件(即,在室温下,约18℃至22℃,并且1个大气压)下实施干燥。干燥可以在从约60℃到约150℃的较高温度范围内进行。在一些示例中,真空也可以用来加速干燥处理。作为干燥处理的一个示例,所沉积的浆可以在约120℃下经受真空约12小时到24小时。
干燥处理导致正电极40的形成。在示例中,已干燥的浆(即,正电极40)的厚度范围为从约5μm到约200μm。在另一示例中,已干燥的浆(即,正电极40)的厚度范围为从约10μm到约100μm。
在形成正电极40期间,水和/或有机溶剂被去除,并因此所得到的正电极40包括从约50重量%至约95重量%(基于正电极40的总重量%)的活性材料28、从约5重量%高至20重量%(基于正电极40的总重量%)的导电填料34、从约5重量%高至20重量%(基于正电极40的总重量%)的粘结剂32、以及从大于0重量%高至约10重量%(基于正电极40的总重量%)的氧化铝纳米材料26。
现在参照图3,示出了锂离子电池300。图3中所示的锂离子电池300包括具有作为添加剂的离散氧化铝纳米材料26的正电极40。
如图3所示,除了正电极40与正极侧电流收集器30之外,锂离子电池300包括负电极38、负极侧电流收集器36、以及位于正电极40与负电极38之间的多孔隔膜42。
在图3中,正电极40可由任何合适的锂基活性材料28形成,如先前参照图2所述。如上所述,锂基活性材料28可与粘结剂32、导电填料34、以及离散氧化铝纳米材料26混合。
正极侧电流收集器30可由铝或本领域技术人员已知的任何其他适当的导电材料来形成。
图3中的多孔隔膜42(可作为电绝缘体和机械支撑件两者)被夹在负电极38与正电极40之间,以防止两个电极38、40之间的物理接触和发生短路。除了在两个电极38、40之间提供物理屏障之外,通过电解质溶液填充其孔,多孔隔膜42确保了锂离子(图3中由黑点和由具有(+)电荷的空心圆标识)和相关阴离子(图3中由具有(-)电荷的空心圆标识)的通路。这有助于确保锂离子电池300正常工作。
多孔隔膜42可以是聚烯烃膜。聚烯烃可以是均聚物(由单个单体成分所衍生)或杂聚物(由多于一个的单体成分所衍生),并且可是直链或支链的。如果使用了由两种单体成分所衍生的杂聚物,则聚烯烃可假定任何共聚物链结构,包括那些嵌段共聚物或无规共聚物。如果聚烯烃是由多于两个的单体成分所衍生的杂聚物,也是如此。作为示例,聚烯烃膜可由聚乙烯(PE)、聚丙烯(PP)、PE和PP的共混物、或者PE和/或PP的多层结构的多孔膜形成。
在其他示例中,多孔隔膜42可由选自如下的另一聚合物形成:聚对苯二甲酸乙酯(PET)、聚偏二氟乙烯(PVdF)、聚酰胺(尼龙)、聚氨酯、聚碳酸酯、聚酯、聚醚醚酮(PEEK)、聚醚砜(PES)、聚酰亚胺(PI)、聚酰胺-酰亚胺、聚醚、聚甲醛(例如,乙缩醛)、聚对苯二甲酸丁二酯、聚环烷酸乙二醇脂、聚丁烯、丙烯腈-丁二烯-苯乙烯共聚物(ABS)、聚苯乙烯共聚物、聚甲基丙烯酸甲酯(PMMA)、聚氯乙烯(PVC)、聚硅氧烷聚合物(如,聚二甲基硅氧烷(PDMS))、聚苯并咪唑(PBI)、聚苯并恶唑(PBO)、聚亚苯基(例如,PARMAXTM(密西西比州贝圣路易斯的密西西比聚合物技术公司(Mississippi Polymer Technologies,Inc.)))、聚亚芳基醚酮、聚全氟环丁烷、聚四氟乙烯(PTFE)、聚偏二氟乙烯共聚物和三元共聚物、聚偏二氯乙烯、聚氟乙烯、液晶聚合物(例如,VECTRANTM(德国的赫斯特公司)、(特拉华州威尔明顿的杜邦)、聚(对羟基苯甲酸)、聚芳酰胺、聚苯醚,和/或其组合。在又一示例中,多孔隔膜42可选自聚烯烃(如,PE和/或PP)与上面列出的聚合物中的一种或多种的组合。
多孔隔膜42可包含由干法或湿法工艺制造的单层或多层层压件。例如,单层聚烯烃和/或其他所列出的聚合物可完全构成多孔隔膜42。然而,作为另一示例,类似或不同的聚烯烃和/或聚合物的多个离散层可被组装成多孔隔膜42。在一个示例中,将一种或多种聚合物的离散层涂覆于聚烯烃的离散层上,以形成多孔隔膜42。此外,聚烯烃(和/或其他聚合物)层和任何其他任选的聚合物层可进一步被包括在多孔隔膜42中作为纤维层,以帮助提供具有适当结构和多孔特性的多孔隔膜42。还有其他适合的多孔隔膜42包括具有粘附至其的陶瓷层的那些,以及聚合物基质(即,有机-无机组合物基质)中具有陶瓷填料的那些。
可以在负电极38与正电极40之间传导锂离子的任何合适的电解质溶液可用于锂离子电池300。在一个示例中,电解质溶液可以是包括溶解在有机溶剂或有机溶剂混合物中的锂盐的非水液体电解质溶液。本领域技术人员知道可用于锂离子电池300的非水液体电解质溶液以及如何制造或购买到这些非水液体电解质溶液。可溶解于有机溶剂以形成非水液体电解质溶液的锂盐的示例包括LiClO4、LiAlCl4、LiI、LiBr、LiSCN、LiBF4、LiB(C6H5)4、LiCF3SO3、LiN(FSO2)2(LIFSI)、LiN(CF3SO2)2(LITFSI)、LiAsF6、LiPF6、LiB(C2O4)2(LiBOB)、LiBF2(C2O4)(LiODFB)、LiPF4(C2O4)(LiFOP)、LiNO3、以及它们的混合物。这些和其他类似的锂盐可溶解于各种有机溶剂,例如,环碳酸酯(碳酸亚乙酯、碳酸丙烯酯、碳酸丁烯酯、碳酸氟代)、直链碳酸酯(碳酸二甲酯、碳酸二乙酯、碳酸甲乙酯)、脂肪族羧酸酯(甲酸甲酯、乙酸甲酯、丙酸甲酯)、γ-内酯(γ丁内酯、γ戊内酯)、链状结构醚(1,2-二甲氧基乙烷、1-2二乙氧基乙烷、乙氧基甲氧基乙烷、四甘醇二甲醚)、环醚(四氢呋喃、2-甲基四氢呋喃、1,3-二氧戊环)、以及它们的混合物。
如图3中所示,锂离子电池300还包括连接负电极38与正电极40的可中断的外部电路46。锂离子电池300还可以支撑可以有效连接到外部电路46的负载装置44。当锂离子电池300放电时,负载装置44接收来自穿过外部电路46的电流的电能进给。尽管负载装置44可以是任意数目已知的电源装置,但是功率消耗负载装置44的一些特定示例包括用于混合动力汽车或所有电动汽车的电动机、便携式计算机、移动电话和无绳电动工具。然而,负载装置44还可是为了存储能量的目的对锂离子电池300充电的电功率生成装置。例如,风车和太阳能电池板可变和/或间歇发电的倾向通常产生存储过剩能量以备后用的需要。
锂离子电池300还可包括虽然本文没有描述但是本领域技术人员已知的宽范围的其他组件。例如,锂离子电池300可包括套管、垫圈、端子、极耳、以及可以为了性能有关或其他实践目的而位于负电极38与正电极40之间或周围的任何其他所期望的组件或材料。此外,锂离子电池300的尺寸和形状以及其主要组件的设计和化学组成可根据为了其而设计的特定应用而变化。例如,电池供电式汽车和手持式消费电子装置是其中锂离子电池300很有可能设计成不同的尺寸、容量和功率-输出规格的两个实例。如果负载装置44如此需要,则锂离子电池300也可以以串联和/或并联的方式与其他类似的锂离子电池连接以产生更大的电压输出和电流(如果并联布置)或电压(如果串联布置)。
锂离子电池300通常通过在负电极38与正电极40之间可逆地传递锂离子来运作。在完全充电状态下,电池400的电压处于最大值(通常在2.0V至5.0V的范围内);而在完全放电状态下,电池300的电压处于最小值(通常在0V至2.0V的范围内)。本质上,正电极40和负电极38中的活性材料的费米能级在电池运作期间变化,并且因此两者之间的差称为电池电压。随着费米能级彼此越来越接近,电池电压在放电期间降低。在充电期间,逆过程发生,当费米能级被驱动分离时,电池电压增加。在电池放电期间,外负载装置44能够使电子电流在外部电路46中沿使得费米能级(以及,对应的电池电压)之间的差减小的方向流动。在电池充电期间发生相反的情况:电池充电器迫使电子电流在外部电路46中沿使得费米能级(以及,对应的电池电压)之间的差增大的方向流动。
在放电开始时,锂离子电池300的负电极38含有高浓度的插入的锂,而正电极40相对耗尽。当负电极38包含足够较高的相对量的插入的锂时,锂离子电池300可以通过在外部电路46闭合以连接负电极38与正电极40时产生的可逆电化学反应来生成有益电流。在这种条件下建立闭合外部电路46导致从负电极38提取插入的锂。当提取的锂原子离开负电极-电解质界面处的插入宿主时,提取的锂原子被分解为锂离子(由黑点以及由具有(+)电荷的空心圆来标识)和电子(e-)。
正电极40与负电极38之间的化学势差(在约2.0V到约5.0V的范围内,这取决于电极38、40确切的化学构成)驱动通过在负电极38处插入的锂氧化产生的电子(e-)穿过外部电路46朝向正电极40。锂离子被电解质溶液同时携带穿过多孔隔膜42朝向正电极40。流经外部电路46的电子(e-)和在电解质溶液中迁移跨过多孔隔膜42的锂离子最终在正电极40处结合并形成插入的锂。通过外部电路46的电流可以被利用并且引导通过负载装置44直到负电极38中插入的锂的水平下降至低于工作水平或停止对电能的需要。
锂离子电池300可以在其可用容量部分或全部放电后被再充电。对锂离子电池300充电时,外部电池充电器连接到正电极40和负电极38以驱动电池放电电化学反应的逆转。在再充电期间,电子(e-)通过外部电路46流回到负电极38,且电解质携带的锂离子穿过多孔隔膜42回到负电极38。电子(e-)和锂离子在负电极38处再次结合,因而在下次电池放电循环期间用插入的锂补充消耗。
可用来对锂离子电池300充电的外部电池充电器可以根据锂离子电池300的尺寸、结构并且特别是最终用途而变化。一些合适的外部电池充电器包括插入到AC壁装电源插座的电池充电器和机动车辆交流发电机。
氧化铝纳米材料26的大的表面积(如,至少150m2/g)和独特结构(如,具有从中空中心径向且向外延伸的多个纳米结构,每个纳米结构具有从约10nm到约200nm的直径以及约80nm到约3微米的长度)使它们适合于在各种另外的应用中使用。在示例中,氧化铝纳米材料26可用于水净化。氧化铝纳米材料26可以从水中去除离子(如,铅(II)和汞(II))。氧化铝纳米材料26的大的表面积和独特结构可以为从水中去除离子提供更大数目的吸收点。在另一示例中,氧化铝纳米材料26也可适合于用作药物输送的载体材料。
为了进一步示出本公开内容,本文中给出多个示例。应当理解,这些示例被提供用于说明的目的,并且不被解释为限制本公开内容的范围。
示例
示例1
制备了氧化铝纳米材料的六种样品。样品1-4根据比较方法来制备。样品5和6根据本文中所公开的方法的示例来制备。
样品1通过向去离子水中添加5.4克AlCl3粉末(即,12克AlCl3·9H2O)和1M HCl制备。AlCl3粉末溶解在去离子水中。1M NaOH作为pH调节剂被滴加到溶液中直到形成白色沉积物并达到期望的pH。该混合物的pH为约11。将该混合物放入到衬里的不锈钢高压釜中。用于水热合成的处理参数包括将含水混合物暴露在200℃的温度下持续约24小时到48小时的时间段。认为在水热合成期间高压釜内的压力为约1400psi。水热合成反应结束时,反应产物从高压釜中除去,用去离子水洗涤,真空过滤,并将其在真空中在约80℃下干燥约12小时到约24小时。
包括纳米管的反应产物经受在空气中在550℃下退火约5小时。在热处理期间,纳米管烧结以形成纳米棒,并且水作为副产物产生并汽化,在纳米棒中形成三维互联孔隙。在退火期间的反应可能是:-AlOOH→γ-Al2O3+H2O↑。样品1中制备的多孔γ-Al2O3纳米棒具有约120m2/g的平均表面积。
样品2根据与制备样品1相同的方法来制备,制备具有下列变化。在将pH调节剂加到混合物中后,pH为约9。样品2中制备的多孔γ-Al2O3纳米棒具有约130m2/g的平均表面积。
样品3根据与制备样品1相同的方法来制备,制备具有下列变化。在将pH调节剂加到混合物中后,pH为约5。样品3中制备的多孔γ-Al2O3纳米棒具有约140m2/g的平均表面积。
样品4根据与制备样品1相同的方法来制备,制备具有下列变化。Al(O-i-Pr)3被用作代替AlCl3的前驱体。该混合物的pH为约11。样品4中制备的多孔γ-Al2O3纳米棒具有约120m2/g的平均表面积。样品1至样品4示出AlCl3粉末和Al(O-i-Pr)3在所形成的最终γ-Al2O3纳米棒的表面积方面十分相似。
获取了样品1中制备的多孔γ-Al2O3纳米棒的TEM图像。这显示在图7中,图7清晰地示出了一维维度。
样品5根据本文中所公开的方法的示例来制备。含水混合物通过向60mL去离子水添加12g AlCl3、1M HCl和10-30mg中空碳来制备。该含水混合物的pH为1.5。
将该含水混合物放入到衬里的不锈钢高压釜中。用于水热合成的处理参数包括使含水混合物在200℃的温度下经受约24小时到36小时的时间段。认为在水热合成期间高压釜中的压力约1400psi。在水热合成结束时,将反应产物从高压釜中除去。
在水热合成之后,将反应产物过滤、洗涤并干燥以获得前驱体纳米结构。前驱体纳米结构包括诸如海胆状纳米结构的共同组装在中空碳复合材料上的AlOOH瓣/钉,其中每个AlOOH瓣具有从80nm到约3μm范围内的平均长度,以及从约20nm到约200nm范围内的平均直径。
然后,具有中空碳复合材料的海胆状纳米结构在空气中在550℃下经受退火约5小时。在热处理期间,中空碳复合材料被烧掉,并且纳米结构烧结形成具有海胆状结构的氧化铝纳米材料,并且水作为副产物产生并汽化。在退火期间的反应可能是:2γ-AlOOH→γ-Al2O3+H2O↑。在样品5中制备的铝氧化物纳米材料具有约240m2/g的平均表面积。
样品6根据与制备样品5相同的方法来制备,制备方法具有下面的变化。石墨被用作碳材料。在样品6中制备的氧化铝纳米材料具有约195m2/g的平均表面积。
比较样品5和样品6,中空碳导致更高表面积的纳米材料,并且在后期水热处理期间更容易被烧掉。然而,应指出,使用石墨形成的纳米材料具有比样品1-4中任何一个更高的表面积。
获取了在样品5中制备的氧化铝纳米材料的SEM图像。这显示在图4中。还获取了在样品5中制备的氧化铝纳米材料的TEM图像。这显示在图5中。图4和图5清楚地示出了氧化铝纳米材料的海胆状结构。获取了从氧化铝纳米材料的中心径向并向外延伸的纳米结构中之一的TEM图像。这显示在图6中,图6清楚地显示了每个纳米结构沿着纳米结构的长度远离中心会如何减小直径。图8是示出了对于样品1-6的表面积(m2/g,左Y轴)相对于pH值变化的图。
示例2
样品5的氧化铝纳米材料作为添加剂被并入到两个示例性正电极(A、A’)中。示例性正电极包括约78%的Li(Li0.2Mn0.54Ni0.13Co0.13)O2材料作为活性材料、约10%的粘结剂(PVdF)、约10%的导电填料(炭黑)、以及约2重量%的氧化铝纳米材料。在混合之后,从中心径向并向外延伸的大多数纳米结构从氧化铝纳米材料断开。断开的纳米结构侧向铺设并大体上均匀地分散在电极中。
比较正电极(B)包括与示例性正电极相同的所有组件,除了氧化铝纳米材料之外。该比较正电极不包括氧化铝纳米材料。
为了形成正示例性电极,Li(Li0.2Mn0.54Ni0.13Co0.13)O2活性材料、炭黑、和氧化铝纳米材料在混合器中干混合。将PVdF和溶剂(NMP)添加到干混合物中。为了形成比较电极,Li(Li0.2Mn0.54Ni0.13Co0.13)O2活性材料和炭黑在混合器中干混合。将PVdF和溶剂(NMP)添加到干混合物中。将混合物进行混合直到形成两种相对均匀的可涂覆的浆。将浆浇注到各自的铝电流收集器上。电极涂层和比较电极涂层在室温下在空气中干燥,然后在烘箱中在约80℃下干燥约24小时,并且然后在真空中在约100℃下干燥约24小时。
比较正电极和示例性正电极中的每一个与锂箔负电极一起使用以构建半电池。硬币状电池(2032硬件)在充Ar的手套箱内组装。微孔三层聚丙烯(PP)和聚乙烯(PE)聚合物膜(CELGARD 2032,可从卡尔格德公司购得)被用作隔膜。电解质由在溶剂的混合物(例如,以1:2体积比的碳酸乙烯酯(EC)和碳酸二乙酯(DEC))中的1M LiPF6组成。
硬币状电池被保持在45℃下以进行恒电流循环测试。循环测试在C/3的速率下进行,并且在2.0V至4.6V的电压窗口内循环至少100个周期。
图9示出了硬币状电池的放电容量(mAh/g,Y轴)相对于周期数(X轴)的变化,该硬币状电池包括比较示例性正电极(B)和具有氧化铝纳米材料添加剂的示例性正电极(A、A’)。随着周期数增加到30或更多,与比较示例性正电极的放电容量(实心正方形B)相比,示例性正电极的放电容量(实心圆A’,和空心圆A)更大。
如图9中所示,当正电极包括在本文中所公开的氧化铝纳米材料时,改善了在放电期间的循环稳定性。
在整个说明书中,提及“一个示例”、“另一个示例”、“示例”等等,表示结合示例描述的特定要素(例如,特征、结构和/或特性)被包含在本文中所描述的至少一个示例中,并可以存在于或可以不存在于其他示例中。此外,应当理解的是,除非上下文以另外的方式明确说明,对于任何示例所描述的要素可以以任何适当的方式在各个示例中结合。
应当理解的是,在本文中所提供的范围包括所描述的范围和所描述范围内的任何值或子范围。例如,从大于0重量%高至约10重量%的范围应解释为不仅包括从大于0重量%高至约10重量%的明确叙述的限制,也包括单个的值(如3.5重量%、6重量%、2重量%等)和子范围(如从约0.5重量%至约8重量%等)。此外,当“约”被用来描述值时,这表示涵盖从所描述的值的小的变化(高至+/-10%)。
除非上下文以另外的方式明确说明,在描述和要求保护在本文中公开的示例时,单数形式包括复数参照对象。
虽然已详细描述了若干示例,但是应当理解的是,可以修改所公开的示例。因此,以上描述将被视为非限制性的。
- 还没有人留言评论。精彩留言会获得点赞!
- 酸敏感可控释放单线态氧纳米材料及其制备方法与应用与流程
- 一种层状复合纳米材料M‑LDHs@Si02微球的制备方法与流程
- 复合纳米材料和微米材料、它们的膜和其制备方法及用途与流程
- 复合纳米材料和微米材料、它们的膜和其制备方法及用途与流程
- 包括离散氧化铝纳米材料的正电极以及形成氧化铝纳米材料的方法与流程
- 一种基于TiO2介晶纳米材料的双响应夹心型免疫传感器的制备方法及应用与流程
- 一种基于核酸和铂纳米材料的自组装体系检测核酸浓度的方法与流程
- 一种高容量蜂窝结构的ZnCo2S4纳米材料及其制备和应用的制作方法与工艺
- 一种银纳米棒/聚合物/银纳米片核壳纳米材料及其制备方法和应用与流程
- 一种WC‑SiO2‑Mn‑Fe纳米材料及其制备方法与流程