具有质子电子混合导电的铁基单相阴极材料体系及制备方法与流程
本发明涉及一种铁基单相阴极材料体系及制备方法,特别是一种具有质子电子混合导电的铁基单相阴极材料体系及制备方法。
背景技术:
固体氧化燃料电池(SOFC)一种能够把燃料中的化学能直接转变成为电能的能量转化装置。目前,SOFC商业化进程所遇到最大的瓶颈就是成本问题和使用可靠性问题。从传统的1000℃左右的高温范围降低至中低温范围(400-800℃),较低成本的金属合金连接材料和相应的高稳定性的电极材料都能够得到使用,同时降低了电池组元间的侵蚀,从而SOFC的材料成本和电池的维护成本都大大降低,并且也没有影响SOFC的发电效率。然而,随着操作温度的降低,电池的阴极极化损失急剧增加,远远大于电解质欧姆损失的增加幅度,这就需要寻找和研制在中低温范围比经典的La1-xSrxMnO3(LSM)阴极更具有良好性能和稳定性的新型阴极材料。
无论是氧离子传导型O-SOFC还是质子传导型H-SOFC的阴极过程主要是氧气吸附解离并与电子相结合形成氧离子的活性区,并在阴极与电解质的三相界面处发生氧离子的电化学反应及迁移。这些主要涉及氧气的气相扩散、解离吸附、得电子成为氧离子的电化学反应、氧离子在电极中的体扩散和表面扩散,不同的是对于O-SOFC型是氧离子穿越三相界面进入电解质内部传输,而对于H-SOFC型是氧离子与从电解质内部传输过来的质子发生在三相界面处发生电化学反应。但是对于H-SOFC的阴极材料来说,大部分的阴极材料体系的选择还是直接把O-SOFC的阴极材料体系直接拿过来使用,考虑到H-SOFC特殊的阴极过程,使用氧离子导体和质子导体混合形成质子氧离子复合阴极可以有效的降低阴极极化电阻,增加电池的性能。但是复合阴极中经常出现化学相容性差,在长期工作过程中易产生第二相,降低电池是实际使用;其次复合阴极的复杂的制备过程进一步增加电池的制造成本,制约了SOFC商业化。
技术实现要素:
本发明的目的是要提供一种具有质子电子混合导电的铁基单相阴极材料体系及制备方法,获得在中低温范围内具备高的化学稳定性和催化活性的铁基单相阴极材料体系及制备方法。
本发明的目的是这样实现的:本发明的具有质子电子混合导电的铁基单相阴极材料包括铁基阴极材料体系及制备方法;
所述的铁基单相阴极材料体系:选择质子导体BaZrO3,掺杂三价阳离子Y3+,增加材料的质子电导率,再引入过渡金属离子Fe改变材料的能带结构,降低带隙,产生电子电导,获得具有质子电子混合导电的单相阴极材料。
所述的铁基单相阴极材料体系的制备方法:按照Ba:Zr:Y:Fe=1:0.8-x:0.2:x的摩尔比例称量每个元素所对应的化学原料,加入柠檬酸,EDTA两种络合剂,通过硝酸,氨水溶解,调节PH=6-7,烧成初级粉,再预烧1250℃-5h成粉,得到所制备阴极材料。
制备方法步骤为:
(1)首先将阴极材料式子中的元素,按比例找取相对应的化学药品,C4H6BaO4、Zr(NO3)4·3H2O、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,根据成分中所含元素比例,称量所需质量;所述的式子为BaZr0.8-xFexY0.2O3-δ其中x=0.2,0.4,0.6;
(2)先往干净的烧杯中加入Zr(NO3)4·3H2O,在加入10-15ml硝酸,50-100ml蒸馏水,放在电炉上加热,搅拌至澄清;
(3)再向烧杯中加入称取好的C4H6BaO4、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,然后再加入络合剂柠檬酸和乙二胺四乙酸(EDTA),所述柠檬酸和EDTA的质量按:按总金属离子数:柠檬酸:EDTA=1:1:0.8加入烧杯中;
(4)最后加入氨水,氨水量为20~60ml,搅拌溶液变至澄清,测pH6-7;再放入陶瓷锅中在电炉上加热、搅拌,至溶液水分完全蒸发;溶液变得粘稠随后发生起火,等锅中粉体冷却下来即为所得阴极初级粉体;
(5)将收集的初级粉体放入耐高温陶瓷锅中,再放入箱式炉中加热1250℃-5h,待降到室温后取出,所得到的阴极材料。
有益效果,由于采用了上述方案,通过在拥有很好的化学稳定性和良好的质子电导率的钙钛矿结构BaZrO3中,掺杂Y3+能够提高质子电导率,再掺杂过渡金属Fe,可以产生电子电导,由此获得一种具有质子电子混合导电单相极材料。BaZr0.2Fe0.6Y0.2O3-δ的最大电子电导率达到1.46×10-1S/cm,烧结1250℃-5h后750℃的极化阻抗为0.88Ωcm2,具有混合质子电子混合导电的阴极材料BaZr0.2Fe0.6Y0.2O3-δ的电极极化损失Rp的电导活化能只有120.83kJmol-1。
附图说明
图1为实施例1-3BaZr0.8-xFexY0.2O3-δ(x=0.2,0.4,0.6)预处理后粉体的XRD图。
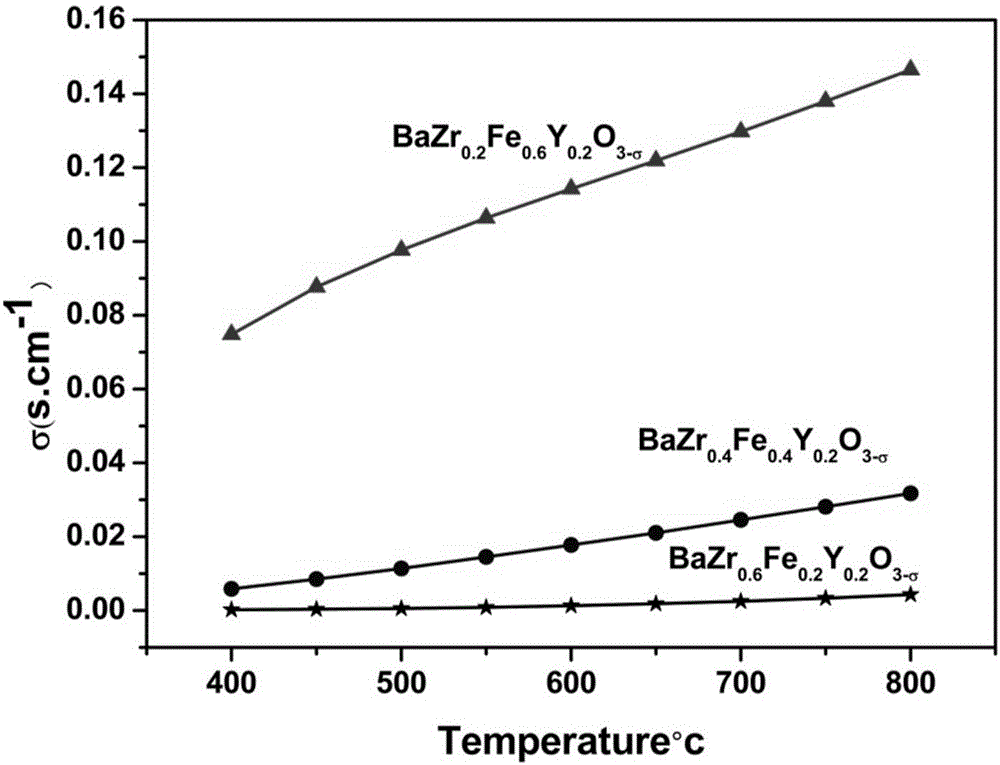
图2为实施例1-3BaZr0.8-xFexY0.2O3-δ(x=0.2,0.4,0.6)三种阴极粉体电导率与温度的关系图。
图3为实施例3BaZr0.2Fe0.6Y0.2O3-δ烧结1250℃-5h,在不同温度下的阻抗谱图。
图4为实施例3BaZr0.2Fe0.6Y0.2O3-δ的电极极化损失Rp随温度的变化关系图。
具体实施方式
本发明的具有质子电子混合导电的铁基单相阴极材料包括铁基阴极材料体系及制备方法;
所述的铁基单相阴极材料体系:选择质子导体BaZrO3,掺杂三价阳离子Y3+,增加材料的质子电导率,再引入过渡金属离子Fe改变材料的能带结构,降低带隙,产生电子电导,获得具有质子电子混合导电的单相阴极材料。
所述的铁基单相阴极材料体系的制备方法:按照Ba:Zr:Y:Fe=1:0.8-x:0.2:x的摩尔比例称量每个元素所对应的化学原料,加入柠檬酸,EDTA两种络合剂,通过硝酸,氨水溶解,调节PH=6-7,烧成初级粉,再预烧1250℃-5h成粉,得到所制备阴极材料。
制备方法步骤为:
(1)首先将阴极材料式子中的元素,按比例找取相对应的化学药品,C4H6BaO4、Zr(NO3)4·3H2O、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,根据成分中所含元素比例,称量所需质量;所述的式子为BaZr0.8-xFexY0.2O3-δ其中x=0.2,0.4,0.6;
(2)先往干净的烧杯中加入Zr(NO3)4·3H2O,在加入10-15ml硝酸,50-100ml蒸馏水,放在电炉上加热,搅拌至澄清;
(3)再向烧杯中加入称取好的C4H6BaO4、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,然后再加入络合剂柠檬酸和乙二胺四乙酸(EDTA),所述柠檬酸和EDTA的质量按:按总金属离子数:柠檬酸:EDTA=1:1:0.8加入烧杯中;
(4)最后加入氨水,氨水量为20~60ml,搅拌溶液变至澄清,测pH6-7;再放入陶瓷锅中在电炉上加热、搅拌,至溶液水分完全蒸发;溶液变得粘稠随后发生起火,等锅中粉体冷却下来即为所得阴极初级粉体;
(5)将收集的初级粉体放入耐高温陶瓷锅中,再放入箱式炉中加热1250℃-5h,待降到室温后取出,所得到的阴极材料。
实施例1:
Ⅰ.制备0.05mol粉体,当阴极材料成分为BaZr0.6Fe0.2Y0.2O3-δ时,首先计算出Zr(NO3)4·3H2O所需的质量11.7992g,加入一个洗干净的烧杯中,倒入50-100ml蒸馏水,再加入10-15ml硝酸,放在万用电阻炉上加热,搅拌加热直至变成澄清溶液。
Ⅱ.再加入式子中剩下几种元素所对应的化学原料,C4H6BaO4、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,所需质量和Ⅰ的Zr(NO3)4·3H2O质量计算方法一样,再按照金属离子:柠檬酸:EDTA=1:1:0.8,加入柠檬酸和乙二胺四乙酸(EDTA),注意称量时有吸水的原料,要用蒸馏水冲掉称量纸上的残留物,减小称量误差。
Ⅲ.逐渐加入氨水,加入的同时搅拌溶液,氨水量大概40-50ml,使溶液澄清没有沉淀,PH6-7。
Ⅳ.将澄清的溶液倒入洗干净的陶瓷锅中,放在电子万用炉上加热自然燃烧,待降温后所收集粉体为初级粉体。
Ⅴ.将初级粉体放入型号KSL-1400X的箱式炉中加热1250℃-5h,得到所发明阴极材料。
实施例2:
Ⅰ.制备0.05mol粉体,当阴极材料成分为BaZr0.4Fe0.4Y0.2O3-δ时,首先计算出Zr(NO3)4·3H2O所需的质量7.8662g,加入一个洗干净的烧杯中,倒入50-100ml蒸馏水,再加入10-15ml硝酸,放在万用电阻炉上加热,搅拌加热直至变成澄清溶液。
Ⅱ.再加入式子中剩下几种元素所对应的化学原料,C4H6BaO4、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,所需质量和Ⅰ的Zr(NO3)4·3H2O质量计算方法一样,再按照金属离子:柠檬酸:EDTA=1:1:0.8,加入柠檬酸和乙二胺四乙酸(EDTA),注意称量时有吸水的原料,要用蒸馏水冲掉称量纸上的残留物,减小称量误差。
Ⅲ.逐渐加入氨水,加入的同时搅拌溶液,氨水量大概40-50ml,使溶液澄清没有沉淀,PH6-7。
Ⅳ.将澄清的溶液倒入洗干净的陶瓷锅中,放在电子万用炉上加热自然燃烧,待降温后所收集粉体为初级粉体。
Ⅴ.将初级粉体放入型号KSL-1400X的箱式炉中加热1250℃-5h,得到所发明阴极材料。
实施例3:
Ⅰ.制备0.05mol粉体,当阴极材料成分为BaZr0.2Fe0.6Y0.2O3-δ时,首先计算出Zr(NO3)4·3H2O所需的质量3.9331g,加入一个洗干净的烧杯中,倒入50-100ml蒸馏水,再加入10-15ml硝酸,放在万用电阻炉上加热,搅拌加热直至变成澄清溶液。
Ⅱ.再加入式子中剩下几种元素所对应的化学原料,C4H6BaO4、Y(NO3)3·6H2O、Fe(NO3)3·9H2O,所需质量和Ⅰ的Zr(NO3)4·3H2O质量计算方法一样,再按照金属离子:柠檬酸:EDTA=1:1:0.8,加入柠檬酸和乙二胺四乙酸(EDTA),注意称量时有吸水的原料,要用蒸馏水冲掉称量纸上的残留物,减小称量误差。
Ⅲ.逐渐加入氨水,加入的同时搅拌溶液,氨水量大概40-50ml,使溶液澄清没有沉淀,PH6-7。
Ⅳ.将澄清的溶液倒入洗干净的陶瓷锅中,放在电子万用炉上加热自然燃烧,待降温后所收集粉体为初级粉体。
Ⅴ.将初级粉体放入型号KSL-1400X的箱式炉中加热1250℃-5h,得到所发明阴极材料。
- 还没有人留言评论。精彩留言会获得点赞!