一种肿瘤细胞内pH触发式释药的多级靶向聚合物胶束及其制备方法与流程
本发明属于高分子材料及药物制剂技术领域,涉及一种肿瘤细胞内pH触发式释药的多级靶向聚合物胶束及其制备方法。
技术背景
化疗是目前临床上治疗肿瘤的有效方法,但肿瘤细胞对抗癌药产生的多药耐药性是导致化疗失败的重要原因。经典的肿瘤耐药机制是高度表达的耐药蛋白,主要是P-糖蛋白,将细胞内的抗癌药“泵”到细胞外,导致胞内药物水平下降,产生耐药性。因此,利用载药体系靶向传递药物进入肿瘤细胞内,避免P-糖蛋白外排,是逆转多药耐药,提高药物肿瘤治疗功效函待解决的关键问题。
疏水化修饰具有细胞因子CD44受体靶向作用的靶向性多糖—透明质酸(hyaluronic acid,HA),制得的聚合物胶束具有良好的生物相容性,载药能力强,良好的体内外稳定性和长循环等特点。HA胶束系统能够通过高通透性与滞留(EPR)效应介导的被动靶向实现肿瘤组织的蓄积,携带药物借助CD44受体介导的胞吞进入细胞,实现了其在肿瘤组织、肿瘤细胞的有效蓄积与摄取。
针对肿瘤细胞内涵体低pH值特点,构筑具有触发释药机制的pH敏感胶束输送抗癌药,在逆转多药耐药方面取得了突破性进展。该智能型递药系统可响应内涵体酸性pH触发释药,并释放药物到细胞质中,有效提高胞质中的药物浓度,饱和肿瘤细胞的耐药机制,克服多药耐药。因此,受体介导的靶向递药和pH敏感靶向释药策略联合应用于胶束系统,表现出良好的协同靶向递药作用,提高抗癌药的治疗效率并减少其毒副作用,为癌症的靶向治疗提供新的途径。
技术实现要素:
鉴于疏水化修饰多糖聚合物胶束表现出优良的被动靶向,载药能力和长循环特性;主动靶向策略的肿瘤靶向能力,以及物理化学靶向策略的定位释药功能,本发明联合被动靶向、主动靶向和物理化学靶向机制,提供一种肿瘤细胞内涵体pH触发式释药的多级靶向聚合物胶束,以实现EPR效应介导的肿瘤组织靶向蓄积、CD44受体介导的主动靶向摄取入胞和内涵体pH触发释药,联合逆转肿瘤耐药,提高药物的抗肿瘤功效。
本发明的另一个目的是提供上述肿瘤细胞内涵体pH触发式释药的多级靶向聚合物胶束的制备方法。
为实现上述发明目的,本发明采用以下技术方案予以实现:
一种肿瘤细胞内pH触发式释药的多级靶向聚合物胶束,其特征在于该胶束包括具有内涵体pH敏感特性的疏水化修饰多糖聚合物,该聚合物在水介质中自组装形成。
所述聚合物具有亲水链段和疏水链段,其中亲水链段为具有CD44受体靶向特性的透明质酸(HA);疏水链段选自脱氧胆酸(deoxycholic acid,DOCA),并在其末端连接内涵体pH敏感单元。
所述疏水链段的取代度为5%~30%。
所述pH敏感单元为组氨酸(histidine,His)或其结构类似物。
所述组氨酸或其结构类似物的分子结构中含有咪唑环,其pH响应范围介于5.0~7.4之间。
所述透明质酸的分子量为1×103~1×107 Da。
所述聚合物按照如下工艺步骤制备:
1)脱氧胆酸-组氨酸或其结构类似物(Trt)的合成
将脱氧胆酸(DOCA)溶于反应溶剂中,以1-乙基-(3-二甲基氨基丙基)碳二亚胺(EDC)和羟基琥珀酰亚胺(NHS)为活化剂,室温下活化2~24 h;
将组氨酸或其结构类似物(Trt)溶于反应溶剂中,加入三乙胺,然后缓慢滴加到上述脱氧胆酸混合液中,于30~50℃温度条件下搅拌反应12~48 h,收集产物,减压干燥,得到脱氧胆酸-组氨酸或其结构类似物(Trt);
2)透明质酸-脱氧胆酸-组氨酸或其结构类似物(Trt)的合成
将透明质酸溶于反应溶剂中,在40~60℃温度条件下搅拌溶解,冷却至室温;然后加入1-乙基-(3-二甲基氨基丙基)碳二亚胺和羟基琥珀酰亚胺,冰浴下活化2~5 h;
将步骤1)得到的脱氧胆酸-组氨酸或其结构类似物(Trt)溶于反应溶剂中,然后缓慢滴加到上述透明质酸混合液中,于40~70℃温度条件下搅拌反应6~12 h,于室温下继续搅拌反应24~48 h,收集产物,产物经透析纯化、冷冻干燥,得到透明质酸-脱氧胆酸-组氨酸或其结构类似物(Trt);
3)透明质酸-脱氧胆酸-组氨酸或其结构类似物的合成
将步骤2)所得透明质酸-脱氧胆酸-组氨酸或其结构类似物(Trt)溶于三氟乙酸,加入苯甲硫醚,室温下搅拌2~12 h,收集产物,产物经透析纯化、冷冻干燥,得到透明质酸-脱氧胆酸-组氨酸或其结构类似物。
所述反应溶剂为N,N- 二甲基甲酰胺、甲酰胺、乙醇水溶液和N,N- 二甲基甲酰胺水溶液中的一种或多种组合。
步骤1)中,所述脱氧胆酸与组氨酸或其结构类似物的摩尔比为1:1~2;
脱氧胆酸、1-乙基-(3-二甲基氨基丙基)碳二亚胺和羟基琥珀酰亚胺的摩尔比为1:1~2:1~2;
组氨酸或其结构类似物(Trt)与三乙胺的摩尔比为1:1~2;
步骤2)中,所述透明质酸与脱氧胆酸-组氨酸或其结构类似物(Trt)中间体的摩尔比为1:2~5,
透明质酸与1-乙基-(3-二甲基氨基丙基)碳二亚胺、羟基琥珀酰亚胺的摩尔比为1:1~5:1~5,
步骤3)中,透明质酸-脱氧胆酸-组氨酸或其结构类似物(Trt)与三氟乙酸、苯甲硫醚的摩尔比为1:1~5:1~5。
上述肿瘤细胞内pH触发式释药的多级靶向聚合物胶束的制备方法,其特征在于:将具有内涵体pH敏感特性的疏水化修饰多糖聚合物采用超声法、透析法或溶剂挥发法制备聚合物胶束,包载难溶性抗肿瘤药物。
所述超声法的具体步骤为:
1)将所述具有内涵体pH敏感特性的疏水化修饰多糖聚合物按1~5 mg/mL的浓度溶于pH 7.4的磷酸盐缓冲液(phosphate buffer solution,PBS)中;
2)将难溶性抗肿瘤药物用有机溶剂溶解后,滴入上述过程1)所得的聚合物PBS中,经超声处理,制得粒径为10~1000 nm的载药胶束。
所述透析法的具体过程为:将所述具有内涵体pH敏感特性的疏水化修饰多糖聚合物和难溶性抗肿瘤药物共溶于有机溶剂,置于截留分子量为3500的透析袋内,浸入pH 7.4的PBS中,透析除去有机溶剂和游离药物,袋内液体即为制得的粒径为10~1000 nm的载药胶束。
所述溶剂挥发法的具体过程为:将所述具有内涵体pH敏感特性的疏水化修饰透明质酸聚合物和难溶性抗肿瘤药物共溶于有机溶剂,加入pH 7.4的PBS,搅拌至有机溶剂挥去,制得粒径为10~1000 nm的载药胶束。
所述难溶性抗肿瘤药物为紫杉醇、阿霉素、喜树碱、羟基喜树碱、拓扑替康、达沙替尼、5-氟尿嘧啶、长春新碱和顺铂中的一种或者两种以上。
所述有机溶剂为乙醇、四氢呋喃、二甲基亚砜、N,N- 二甲基甲酰胺中的一种或多种组合。
通过以上技术方案,本发明的有益效果是:该胶束可用于制备治疗肿瘤疾病药物的用途,经静脉注射给药,在生理环境(pH 7.4)和肿瘤细胞外液(pH 6.5~7.2),胶束结构完整,不释放或低释放药物,可通过EPR效应介导的肿瘤血管靶向蓄积于肿瘤组织,并进一步借助HA的CD44受体主动靶向机制摄取进入肿瘤细胞;最终在内涵体(pH 5.0~6.0)中胶束解聚,触发释药,同时内涵体膜破裂,释放药物到达细胞质,提高胞内药物浓度,饱和耐药机制,克服肿瘤多药耐药,提高药物抗肿瘤功效。
综上所述,本发明采用透明质酸-脱氧胆酸-组氨酸聚合物为载体,通过超声法、透析法或溶剂挥发法制备肿瘤主动靶向的内涵体pH敏感型聚合物胶束,包载难溶性抗肿瘤药物。本发明利用EPR介导的被动靶向、CD44受体主动靶向和pH敏感靶向策略协同机制,从血液长循环、肿瘤组织蓄积、细胞摄取和胞内释药这四个药物输送关键阶段进行“全程靶向”引导,实现多级靶向递药,为提高难溶性抗肿瘤药物的抗肿瘤疗效提供一种新型的载体和制剂策略。
附图说明
图1为HA-DOCA-His聚合物的合成路线图;
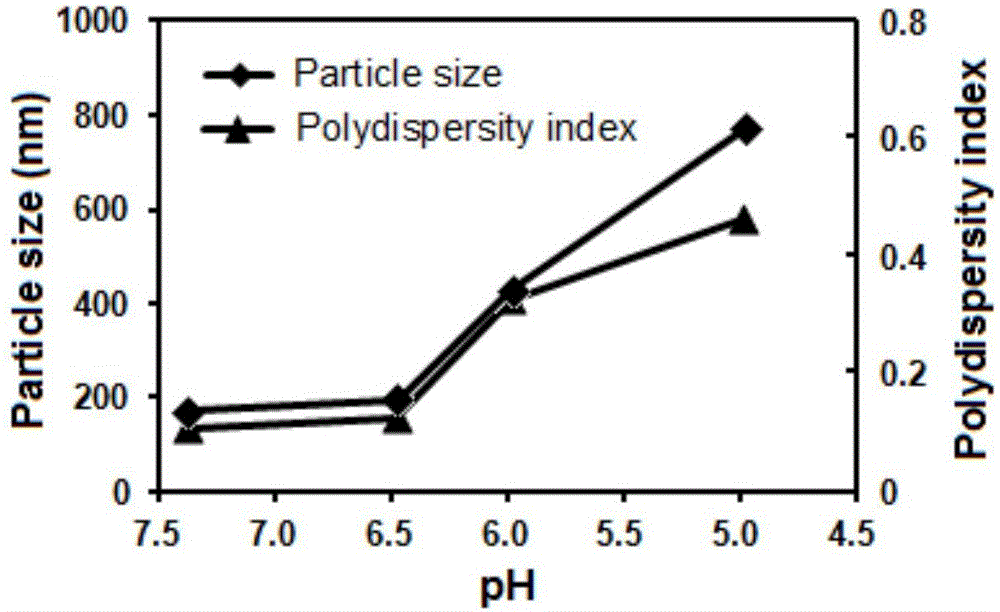
图2为HA-DOCA-His胶束在不同pH值下的粒径分布图;
图3为载紫杉醇的HA-DOCA-His胶束在不同pH释放介质中的释放曲线;
图4为HA-DOCA-His载药胶束自组装,靶向至肿瘤组织蓄积、肿瘤细胞摄取及细胞内内涵体酸敏解聚触发释药示意图。
具体实施方式
为更好的说明本发明的目的、技术方案和优点,下面将结合附图和具体实施例对本发明作进一步说明,但本发明的保护范围并不仅限于此。
实例1:HA-DOCA-His聚合物的合成
0.5 g DOCA溶于5 mL N,N-二甲基甲酰胺,加入0.29 g EDC和0.18 g NHS,室温搅拌2 h。0.37 g 三苯甲基组氨酸甲酯盐酸盐(H-His (Trt)-OMe·HCl)溶于20 mL DMF中,加入50 µL三乙胺,缓慢滴加到DOCA混合液中,混合液于35℃水浴搅拌24 h。反应混合液中加入NaHCO3溶液(pH 9~10),抽滤得沉淀,减压干燥得DOCA-His (Trt)。
0.1 g HA溶于5 mL无水甲酰胺,50℃加热溶解,冷却至室温。加入96 mg EDC和58 mg NHS,冰浴磁力搅拌2 h。0.4 g DOCA-His(Trt)溶于5 mL无水DMF中,缓慢滴加到HA混合液中,50 ℃水浴搅拌6 h后,于室温继续搅拌24 h。 反应混合液于蒸馏水中透析2~3天(透析袋截留分子量:3500),过滤除去不溶性杂质,冷冻干燥,得HA-DOCA-His (Trt)白色粉末。
0.1 g HA-DOCA-His (Trt)溶于0.5 mL DMSO,加入0.5 mL三氟乙酸和25 µL苯甲硫醚,室温搅拌2 h,反应混合液于碱水(pH 9~10)中透析2 d(透析袋截留分子量:3500),蒸馏水中透析2天,过滤除去不溶性杂质,冷冻干燥,得HA-DOCA-His白色粉末。反应路线如图1所示。
实例2:HA-DOCA-His聚合物的合成
0.5 g DOCA溶于5 mL N,N-二甲基甲酰胺,加入0.29 g EDC和0.18 g NHS,室温搅拌24 h。0.37 g三苯甲基组氨酸甲酯盐酸盐(H-His (Trt)-OMe·HCl)溶于20 mL DMF中,缓慢滴加到DOCA混合液中,混合液于35 ℃水浴搅拌24 h。反应混合液旋蒸除去有机溶剂,柱分离,得DOCA-His (Trt)。
0.1 g HA溶于5 mL无水甲酰胺,50 ℃加热溶解,冷却至室温。加入96 mg EDC和58 mg NHS,冰浴磁力搅拌2 h。0.4 g DOCA-His(Trt)溶于5 mL无水DMF中,缓慢滴加到HA混合液中,50 ℃水浴搅拌6 h后,于室温继续搅拌24 h。 反应混合液于蒸馏水中透析2~3天(透析袋截留分子量:3500),过滤除去不溶性杂质,冷冻干燥,得HA-DOCA-His (Trt)白色粉末。
0.1 g HA-DOCA-His (Trt)溶于0.5 mL DMSO,加入0.5 mL三氟乙酸和25 µL苯甲硫醚,室温搅拌2 h,反应混合液于蒸馏水中透析2 d(透析袋截留分子量:3500),蒸馏水中透析2天,过滤除去不溶性杂质,冷冻干燥,得HA-DOCA-His白色粉末。
实例3:HA-DOCA-His聚合物的合成
0.5 g DOCA溶于5 mL N,N-二甲基甲酰胺,加入0.29 g EDC和0.18 g NHS,室温搅拌24 h。0.37 g 三苯甲基组氨酸甲酯(H-His(Trt)-OH)溶于20 mL DMF中,缓慢滴加到DOCA混合液中,混合液于35 ℃水浴搅拌24 h。反应混合液旋蒸除去有机溶剂,柱分离,得DOCA-His (Trt)。
0.1 g HA溶于5 mL无水甲酰胺,60 ℃加热溶解,冷却至室温。加入192 mg EDC和116 mg NHS,冰浴磁力搅拌5 h。0.8 g DOCA-His(Trt)溶于5 mL无水DMF中,缓慢滴加到HA混合液中,室温搅拌48 h。 反应混合液中加入乙醇沉淀除杂,得HA-DOCA-His (Trt)白色粉末。
0.1 g HA-DOCA-His (Trt)溶于0.5 mL DMSO,加入0.5 mL三氟乙酸和50 µL苯甲硫醚,室温搅拌12 h,反应混合液于蒸馏水中透析2天(透析袋截留分子量:3500),蒸馏水中透析2天,过滤除去不溶性杂质,冷冻干燥,得HA-DOCA-His白色粉末。
HA-DOCA-His的1HNMR图谱如图2所示,HA的NHCOCH3上-CH3的化学位移在 1.95 ppm,2、3、4和5 位碳上氢的化学位移在 3.0~4.0 ppm,而6位碳上氢的化学位移在4.35~4.45 ppm,0.8~2.0 ppm处归属于DOCA中-CH3和-CH2-的特征峰,7.45 ppm和8.82 ppm处归属于His中-N=CH-和-N=CH=C-的特征峰,证实DOCA-His成功合成到了HA上。
实例4:超声法制备载紫杉醇的HA-DOCA-His胶束
HA-DOCA-His溶解于pH 7.4的PBS,浓度为1~5 mg/mL,磁力搅拌至完全溶解,将溶解于无水乙醇(甲醇、四氢呋喃)的紫杉醇(HA-DOCA-His加入量的10%、20%和30%)缓慢滴加入上述聚合物溶液中,磁力搅拌24~48 h后,冰浴超声(超声功率 100~400 W、工作2 s、间歇3 s)2~20 min,胶束溶液经0.45 µm滤膜过滤,制得载药胶束,冻干可得载药胶束粉末。
实例5:透析法制备载阿霉素的HA-DOCA-His胶束
称取5 mg阿霉素盐酸盐分散于1 mL DMSO(四氢呋喃)中,加入7 µL三乙胺,搅拌至阿霉素溶解,制得阿霉素DMSO(四氢呋喃)溶液(5 mg/mL)。HA-DOCA-His溶于DMSO(10 mg/mL)中,加入阿霉素(HA-DOCA-His加入量的10%、20%和30%)DMSO(四氢呋喃)溶液,室温下磁力搅拌使其混匀,置于透析袋(截留分子量:3500)内,浸入pH7.4的PBS中透析3天,透析袋内液体经0.45 µm滤膜过滤,制得载药胶束,冻干可得载药胶束粉末。
实例6:溶剂挥发法制备载阿霉素的HA-DOCA-His胶束
称取5 mg阿霉素盐酸盐分散于1 mL 甲醇中,加入7 µL三乙胺,搅拌至阿霉素溶解,制得阿霉素甲醇溶液(5 mg/mL)。HA-DOCA-His溶于四氢呋喃(10 mg/mL)中,加入阿霉素(HA-DOCA-His加入量的10%、20%和30%)甲醇溶液,磁力搅拌使其混匀,滴入pH7.4的PBS,磁力搅拌24~48 h,胶束溶液经0.45 µm滤膜过滤,制得载药胶束,冻干可得载药胶束粉末。
实例7:HA-DOCA-His胶束pH敏感性测定
HA-DOCA-His聚合物溶于pH7.4的PBS,浓度为1 mg/mL。采用粒径分析仪测定胶束的平均粒径和PI,用0.01 mol/L的HCl溶液,依次调节pH为6.5、6.0、5.0,每调节一个pH值,样品溶液磁力搅拌30 min,静置10 min,测定粒径,重复三次,观察粒径变化情况。结果见图3, 胶束在pH 7.4和6.5时粒径变化不明显,pH 6.0和pH 5.0时粒径和PI急剧增大,表明HA-DOCA-His胶束具有内涵体pH(5.0~6.0)敏感性。
实例8:载紫杉醇的HA-DOCA-His胶束的体外释放
采用透析法考察实例4中制得的载药胶束的体外释药。精密量取3 mL载紫杉醇的HA-DOCA-His胶束,置于透析袋(截留分子量:3500)内,浸入80 mL含2% Cremophor EL(w/v),pH分别为7.4、6.5、6.0、5.0的PBS中,于37℃,100 r/min振摇,分别于1、2、4、6、8、12、16、24、36 h和48 h取样3 mL,同时补充相同pH值、体积和温度的新鲜介质。样品经0.45 µm滤膜过滤,弃去初滤液,HPLC法测定紫杉醇含量,并计算累积释药百分数,结果见图4。载紫杉醇的HA-DOCA-His胶束在pH为7.4、6.5、6.0、5.0的释放介质中,6 h的累积释药量分别为12.2%、13.8%、29.9%和55.3%,表明HA-DOCA-His胶束在生理环境(pH 7.4)和肿瘤细胞外液(>pH 6.5)中均稳定,进入肿瘤细胞内涵体的酸性环境(pH 5.0~6.0)能够实现触发释药。
- 还没有人留言评论。精彩留言会获得点赞!