一种miR‑214纳米基因复合物及其制备方法、应用与流程
本发明涉及基因治疗技术领域,具体是一种miR-214纳米基因复合物及其制备方法、应用。
背景技术:
结直肠癌是人类最常见的恶性肿瘤之一,且发病率逐年上升。超过60%的结直肠癌患者都会出现肝转移,其中约10%~25%的患者首诊时就已经存在肝转移(同时性肝转移),可见肝转移是结直肠癌主要的死亡原因之一。为了能够有效治疗结直肠癌、降低肝转移发生的机率,基因治疗已经成为越来越受到重视的治疗方法。
miRNA是小分子非编码RNA家族的重要成员,许多研究表明,miRNA表达谱在恶性肿瘤中会发生改变。如果能够通过基因治疗的方法,改变肿瘤中miR-214的基因的表达,这将为结直肠癌的治疗提供新的思路。
技术实现要素:
本发明公开一种miR-214纳米基因复合物及其制备方法和应用,以通过基因治疗降低结直肠癌肝转移的发生。
第一方面,本发明公开一种miR-214纳米基因复合物,所述miR-214纳米基因复合物是聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇-DNA纳米基因聚合物,其中DNA是嵌有miR-214的DNA。
在本发明中,miR-214是miRNA-214,嵌有miR-214的DNA可通过商业购买得到,也可通过本领域常规技术手段制得,例如通过基因修饰技术将miR-214嵌入到DNA中。嵌有miR-214的DNA材料属于现有技术,在本发明中不作进一步描述。
进一步地,所述miR-214纳米基因复合物是通过将聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物与嵌有miR-214的DNA进行孵育得到的。
进一步地,所述聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物是以聚乙烯咪唑为大分子引发剂,通过开环聚合反应合成聚天冬氨酸主体化合物,通过化学连接将胆固醇分子引入所述主体化合物末端,再通过氨解反应及化学链接将胱胺和R8多肽引入所述主体化合物主体的侧链形成的。
其中,R8多肽是指具有八个精氨酸的多肽结构,可以通过商业购买获得,例如R8多肽可购自于上海吉尔生化有限公司。
第二方面,本发明公开一种上述miR-214纳米基因复合物的制备方法,包括以下步骤:
制备聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液;
将所述聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液与嵌有miR-214的DNA溶液进行孵育,通过静电作用力形成所述纳米基因复合物。
进一步地,在所述纳米基因复合物的制备方法中,制备聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液的步骤为:将所述聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶解在二甲基亚砜中,得到浓度为5mg/mL的母液,再用pH为5.2、浓度为25mM的乙酸钠缓冲液稀释,得到浓度为1mg/mL的所述聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液;所述聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液与所述DNA溶液的孵育时间为30min。
第三方面,本发明公开一种上述miR-214纳米基因复合物的应用,所述miR-214纳米基因复合物用于制备预防癌症和/或治疗癌症的药物。
进一步地,所述癌症是结直肠癌和/或结直肠癌的肝转移。
第四方面,本发明公开一种具有预防结直肠癌肝转移和/或治疗结直肠癌肝转移功能的药物,所述药物包含上述的miR-214纳米基因复合物。
与现有技术相比,本发明具备以下有益效果:
第一,本发明中的miR-214纳米基因复合物能够改变结直肠癌中miR-214基因的表达,通过上调miR-214的表达来抑制细胞的增殖,转移,侵袭以及体内肿瘤的生长和向肝脏的转移,可有效减少结直肠癌的肝转移的发生。
第二,本发明的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物具有较高的自组装能力及稳定性,其自组装形成的纳米基因载体具有较强的跨细胞膜转运能力,能够提高DNA分子的核靶向能力,使得纳米基因载体具有高效的体内外基因转染效率。
本发明的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物分子结构中末端具有胆固醇基团没能够增强该高分子聚合物的自组装能力及稳定性。该高分子聚合物自组装形成纳米基因载体后,由于纳米基因载体的聚乙烯咪唑片段中具有咪唑环基团,其不仅可以提高该纳米基因载体的质子缓冲作用,还可以实现其表面电位在肿瘤部位由负向正的翻转,从而增强了该纳米基因复合物的跨细胞膜转运能力。这主要是由于咪唑环基团的pKa值为6.5,具有在弱酸性环境中质子化的特性。这一特性一方面可以使纳米基因载体在进入溶酶体后,通过质子缓冲作用逃离溶酶体,避免核酸分子在溶酶体中被降解;另一方面,咪唑环的质子化作用可使纳米基因载体在弱酸性的肿瘤微环境中实现表面电位由负向正的翻转,从而增强了纳米载体与细胞膜的相互作用及其跨膜转运能力。
R8多肽通过二硫键连接在聚合物的侧链,可使纳米基因载体在溶酶体中经谷胱甘肽(GSH)还原后快速释放出DNA分子,而被释放的DNA分子可继续与R8多肽结合,并通过R8多肽与核定位信号蛋白的结合能力,提高DNA分子的核靶向能力,从而最终使该纳米基因载体具有高效的体内外基因转染效率。
附图说明
为了更清楚地说明本发明实施例中的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他的附图。
图1是本发明制备例中聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物的氢核磁谱图。
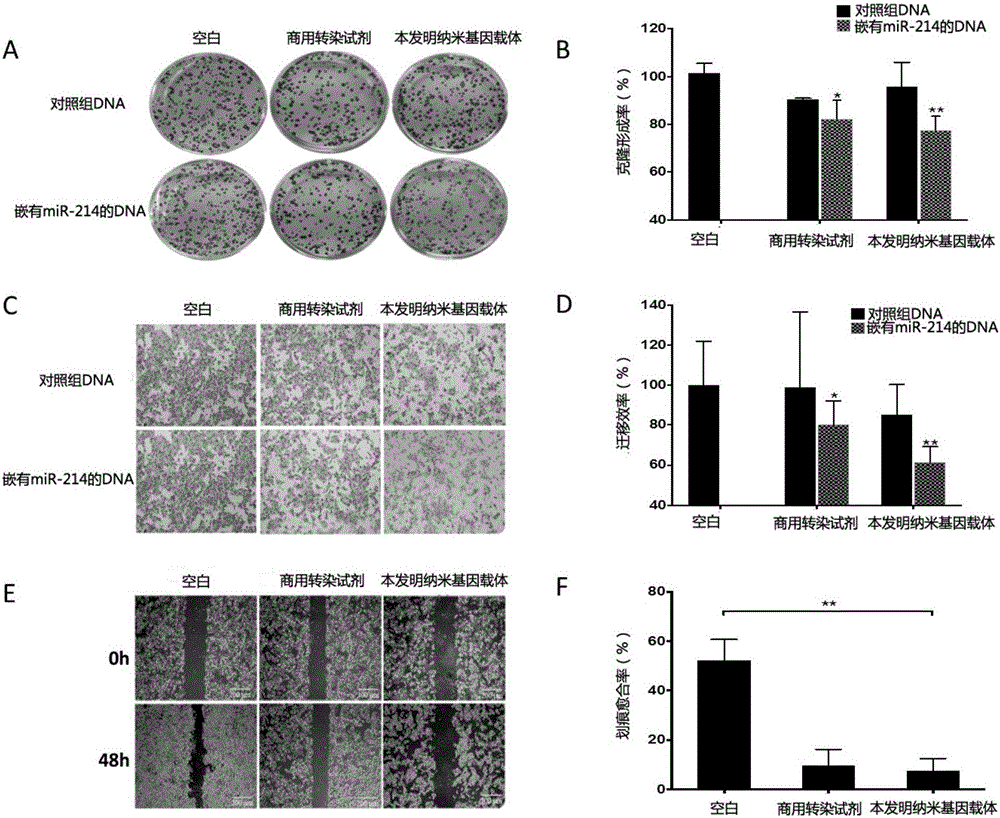
图2是本发明实施例miR-214纳米基因复合物对肿瘤细胞克隆形成、侵袭和转移能力的影响。
图3是本发明实施例miR-214纳米基因复合物用于治疗结直肠癌肝转移的效果。
具体实施方式
下面将结合本发明实施例中的附图,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
除非特别说明,以下实施例所述试剂和材料均为市购。
本发明实施例公开了一种miR-214纳米基因复合物及其制备方法、应用,能够降低结直肠癌肝转移的发生。以下进行结合附图进行详细描述。
制备例
本制备例提供一种高分子聚合物,该高分子聚合物为聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物,其制备方法包括如下步骤:
合成聚乙烯咪唑(PVIm):以偶氮二异丁腈为引发剂,半胱胺为链转移引发剂,乙烯基咪唑为单体,通过自由基聚合合成理论分子量为5000的聚乙烯咪唑。
合成N-羧基-L-天冬氨酸-苄脂-环内酸酐(BLA-NCA):采用Fuchs-Farthing法进行N-羧基-L-天冬氨酸-苄脂-环内酸酐的合成。具体步骤如下:称取摩尔比为1:2.5的L-天冬氨酸-苄脂和三光气溶于无水四氢呋喃以形成反应液,在50摄氏度、氮气保护下搅拌0.5-1h。当反应液澄清透亮时,滴加入无水正己烷,直至反应液中出现白色沉淀并迅速消失。将反应液置于-20摄氏度冰箱静置过夜,通过重结晶得到N-羧基-L-天冬氨酸-苄脂-环内酸酐的粗产物。将粗产物溶于无水乙酸乙酯,过滤,将滤液滴加入无水正己烷中进行重沉淀,重复2次后真空干燥得到N-羧基-L-天冬氨酸-苄脂-环内酸酐。
合成聚乙烯咪唑-聚L-天冬氨酸-苄脂(PVIm-PBLA):以聚乙烯咪唑为大分子引发剂,以N-羧基-L-天冬氨酸-苄脂-环内酸酐为单体,通过开环聚合反应合成聚乙烯咪唑-聚L-天冬氨酸-苄脂。
合成聚乙烯咪唑-聚L-天冬氨酸-苄脂-胆固醇(PVIm-PBLA-Cholesteryl):将合成好的聚乙烯咪唑-聚L-天冬氨酸-苄脂溶于无水四氢呋喃与无水二甲基亚砜的混合溶剂中,形成第一混合溶液,其中无水四氢呋喃与无水二甲基亚砜的体积比为1:1;将胆固醇甲酰氯溶于无水四氢呋喃中,并加入三乙胺,形成第二混合溶液,且聚乙烯咪唑-聚L-天冬氨酸-苄脂与所述胆固醇甲酰氯的摩尔比为1:5;将第二混合溶液缓慢滴加至第一混合溶液中,先在冰上反应30min,再在室温下反应24h,得到所述聚乙烯咪唑-聚L-天冬氨酸-苄脂-胆固醇。
合成聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物(PPCRC):以胱胺为胺解试剂,通过胺解反应使合成的聚乙烯咪唑-聚L-天冬氨酸-苄脂-胆固醇中的苄脂基团被胱胺取代;再通过化学连接将R8多肽连接在胱胺末端的氨基上,形成聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物。
具体的胺解反应包括以下步骤:将胱胺溶于无水二甲基亚砜并加入三乙胺进行脱质子化反应15min,其中胱胺的用量为聚乙烯咪唑-聚L-天冬氨酸-苄脂-胆固醇中苄脂基团摩尔数的50倍;将脱质子化反应后的溶液滴加至聚乙烯咪唑-聚L-天冬氨酸-苄脂-胆固醇 的二甲基亚砜溶液中,在40摄氏度、氮气保护下反应24h;将反应后的液体滴加至冷的盐酸水溶液中,再将其置于至5000Da的透析袋中,分别在0.01M的盐酸水溶液及超纯水中进行透析,之后冷冻干燥得到聚乙烯咪唑-(聚天冬氨酸-胱胺)-胆固醇(PPCC)。
具体的化学连接包括以下步骤:称取R8多肽和聚乙烯咪唑-(聚天冬氨酸-胱胺)-胆固醇(PPCC)溶解至无水二甲基亚砜,并加入EDC和NHS,且EDC和NHS的摩尔数是R8多肽的2倍,在室温、氮气保护下反应24h。反应结束后,将反应液转移至3500Da的透析袋中,分别在二甲基亚砜及超纯水中进行透析,并通过冷冻干燥得到产物聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇(PPCRC)聚合物。
本实施例制备的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物的化学结构式为:
其中,x为正整数,y为正整数,z为正整数。
采用氢核磁共振谱仪对聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物的分子结构进行表征。具体氢核磁谱图如图1所示。
实施例
本实施例提供一种miR-214纳米基因复合物,其制备方法包括以下步骤:将制备例中制备的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶解在二甲基亚砜中,得到浓度为5mg/mL的母液,再用pH为5.2、浓度为25mM的乙酸钠缓冲液稀释,得到浓度为1mg/mL的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液;
根据不同的聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物与DNA的质量比,将聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇聚合物溶液与DNA溶液在室温下孵育30min,通过静电作用力形成聚乙烯咪唑-(聚天冬氨酸-胱胺-R8多肽)-胆固醇-DNA纳米基因复合物(以下简称PPCRC/DNA纳米基因复合物)。其中,DNA是嵌有miR-214的DNA,可通过商业购买得到。
将制备好的PPCRC/DNA纳米基因复合物稀释在1mL的超纯水中,并采用纳米激光粒度分析仪,在25摄氏度条件下对PPCRC/DNA纳米基因复合物的粒径及Zeta电位进行检测。结果如下表1所示:
表1:PPCRC/DNA纳米基因复合物的粒径电位表
通过表1可知,PPCRC/DNA纳米基因复合物的平均粒径分布在160nm-230nm,Zeta电位则随着聚合物/DNA质量比的增加而增加,并主要分布在19mV~34mV。
测试例一miR-214纳米基因复合物对体外细胞功能学的影响
1、miR-214的转染
培养低表达miR-214的结肠癌细胞株HCT116,取对数生长期的细胞铺六孔板,并在含10%FBS(v/v)的RPIM-1640培养基中孵育,使其贴壁生长,当细胞生长至30%-40%,吸去培养基,在无血清培养基条件下用商用转染试剂(脂质体lipofactamine 2000)、本发明制备例自组装形成的纳米基因载体(以下简称本发明纳米基因载体)分别转染嵌有miR-214的DNA,6小时后换成正常的培养基,继续培养24小时后,收集细胞。
2、细胞平板克隆形成实验
将转染后的细胞用胰酶消化成单细胞,将300-500个细胞加入到六孔板中,培养1-2周待肉眼可见克隆时中止培养,染色固定,结果如图2中的A图和B图所示。
通过图2中的A图和B图可知:采用商用转染试剂转染嵌有miR-214的DNA可抑制HCT116单细胞克隆形成,而采用本发明的纳米基因载体转染嵌有miR-214的DNA后对HCT116单细胞克隆形成抑制更为明显,说明本发明的纳米基因载体转染嵌有miR-214的DNA后对HCT116的克隆形成的抑制作用要优于商用转染试剂。
此外,对照组DNA采用商用转染试剂转染的克隆形成率要低于本发明的纳米基因载体转染组,说明本发明的纳米基因载体的毒性要低于商用转染试剂载体的毒性。
3、Transwell实验检测侵袭和转移能力
转染后继续培养12-24小时,将细胞用胰酶消化成单细胞,加入Transwell板中,12-18小时后终止培养,用棉签擦去未转移的细胞,并染色固定。结果如图2中的C图和D图所示,其中C图是镜下未转染以及不同载体转染对照组DNA和嵌有miR-214的DNA后结肠癌细胞HCT116的侵袭转移的结果,D图为相应的每个视野中侵袭转移的细胞数。
结合图2中的C图和D图可知:本发明的纳米基因载体转染嵌有miR-214的DNA后的细胞的转移能力下降了59%,而商用转染试剂转染嵌有miR-214的DNA后的细胞的转移能力下降了78%,说明本发明的纳米基因载体转染嵌有miR-214的DNA后对细胞侵袭和转移能力的抑制作用要明显优于商用转染试剂。
4、划痕实验检测细胞的迁移能力变化
将转染后的细胞用胰酶消化后加入6孔板培养,待细胞长至80%密度时划痕,每6小时用显微镜记录细胞的变化。结果如图2中的E图和F图所示。
通过图2中的E图和F图可知:未转染的细胞划痕48小时后,划痕已近弥合,而两种载体转染嵌有miR-214的DNA后,细胞的迁移运动均被明显抑制,比较起来采用本发明纳米基因载体转染嵌有miR-214的DNA对细胞迁移运动的抑制较商用转染试剂更为明显。同时也可观察到本发明的纳米基因载体转染嵌有miR-214的DNA后细胞的增殖也被明显抑制。
通过本测试例可以得出结论,当本发明制备例的高分子聚合物自组装形成纳米基因载体后,其负载嵌有miR-214的DNA形成的纳米基因复合物能显著抑制结肠癌细胞的增殖、迁移、侵袭和转移能力,其转染效率要优于商用转染试剂。
测试例二:miR-214纳米基因复合物对体内肿瘤转移治疗作用
1、建立裸鼠荷结肠癌细胞肝转移模型:将结肠癌细胞注射入裸鼠脾脏,10天后癌细胞将转移至肝脏,以用于肝转移作用的研究。
2、采用负载有miR-214的纳米基因复合物对裸鼠荷结肠癌细胞肝转移模型进行治疗。分别于肿瘤接种后10、13、16、19、21、25天尾静脉给予负载miR-214的纳米基因复合物或空载的纳米基因载体治疗,第28天处死裸鼠,观察脾脏和肝脏转移瘤情况,计数转移瘤数目。实验结果如图3所示。
根据图3可以看出,治疗组的肝转移数目明显少于对照组,表明负载有miR-214的纳米基因载体能够显著抑制结直肠癌的肝转移,对结直肠癌肝转移具有显著的疗效,可用于制备治疗结直肠癌肝转移的药物。
以上对本发明实施例公开的一种miR-214纳米基因复合物及其制备方法、应用进行了详细介绍,本文中应用了具体个例对本发明的原理及实施方式进行了阐述,以上实施例的说明只是用于帮助理解本发明的方法及其核心思想;同时,对于本领域的一般技术人员,依据本发明的思想,在具体实施方式及应用范围上均会有改变之处,综上所述,本说明书内容不应理解为对本发明的限制。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种基于生物功能化纳米银装载紫杉醇或其类似物的靶向递送系统的制作方法与工艺
- 一种Al‑Zn‑Si纳米复合物速凝早强剂及其制备方法与流程
- 一种载纳米银的PNIPAM/PVA复合温敏凝胶的制备及其应用的制作方法与工艺
- 一种利用蓝莓叶提取液生物合成的纳米银抑菌剂及其制备工艺的制作方法与工艺
- 金属‑有机配合物与银纳米线复合物及其制备方法与应用与流程
- 一种TiO2/SnO2/Carbon纳米复合物及其制备方法与流程
- 一种含纳米NaY分子筛的复合物及其制备方法与流程
- 基于CdTe‑Ag2Se纳米复合物的皮质酮电化学发光传感器的制备方法和应用与流程
- 一种以纳米银茶叶渣生物碳为主滤料的车载式空气净化器的制作方法与工艺
- PLGA纳米复合物及其制备方法与流程
- 一种TaC@洋葱状碳/无定形碳纳米复合物及其制备方法和应用与制造工艺
- 一种W2C@洋葱状碳/无定形碳纳米复合物及其制备方法和应用与制造工艺
- 五氧化二矾及其碳纳米复合物规模化制备与锂电池应用的制造方法与工艺
- 一种ZnPc‑UCNP‑PEG‑G纳米复合物的制备方法与制造工艺
- 蒙脱土增强固体丙烯酸酯树脂及其制备方法与制造工艺
- 一种Fe(Ⅲ)和Cu(Ⅱ)掺杂的聚苯胺纳米复合物及其应用
- 一种Sn@C@g?C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法
- 一种Co@C@g?C<sub>3</sub>N<sub>4</sub>纳米复合物及其制备方法和应用
- 基于超支化纳米复合物的双酚a增敏型免疫层析金标试纸条的制备方法
- 一种的强韧性石墨烯纳米改性橡胶及其制备工艺的制作方法
- 一种四氧化三铁/石墨复合纳米材料及其制备方法与在锂离子电池中的应用与流程
- 一种Al‑Zn‑Si纳米复合物速凝早强剂及其制备方法与流程
- 一种耐老化四氧化三钴纳米线碳气凝胶复合超级电容器正极材料及其制备方法与流程
- 一种TiO2/SnO2/Carbon纳米复合物及其制备方法与流程
- 一种超级电容器用二氧化钌/碳复合纳米材料及其制备方法与流程
- 复合电极材料三氧化二钒/碳、超级电容器及其制备方法与流程
- 一种含纳米NaY分子筛的复合物及其制备方法与流程
- 基于CdTe‑Ag2Se纳米复合物的皮质酮电化学发光传感器的制备方法和应用与流程
- 四氧化三钴复合α型氧化铁蠕虫状纳米结构阵列光阳极及其制备方法和应用与流程
- PLGA纳米复合物及其制备方法与流程