一种肝素修饰的阳离子脂质体及其制备方法与流程
本发明涉及药物制剂领域,具体涉及一种肝素修饰的阳离子脂质体,本发明还公开了这种肝素修饰的阳离子脂质体的制备方法。
背景技术:
阳离子脂质体具有无免疫原性、可生物降解、可重复转染等特性,一直受到相关研究者的重视,至今已有数十种阳离子脂质体被研制出来。但研究表明,单独使用阳离子脂质体具有一定的风险。实验动物静脉注射给予阳离子脂质体后,倾向于与血浆蛋白或血细胞聚合,并通过静电作用附着于血管内皮细胞上,因此导致其从血液中快速消除或定位于肺部,增加肺栓塞的危险。阳离子脂质体的另一个毒性表现为免疫反应,Zelphati等的试验结果显示阳离子脂质可以激活血清中的补体系统,补体系统激活后可以促进补体成分与脂质体的结合,因而会被肺部或肝脏补体成分受体所识别,导致阳离子脂质体快速地从血流中清除而被肺或肝脏所摄取。采用亲水性的材料结合阳离子脂质体,对阳离子脂质体实施保护,可以大大降低阳离子脂质体引起的体内安全性风险。
肝素是一种酸性的粘多糖,极易溶于水。肝素作为理想的阳离子脂质体修饰材料的优势主要集中体现在两个方面:首先,肝素可以代替PEG作为药物载体的亲水性修饰材料,用于构建胶束、脂质体等。亲水性材料PEG常用于载体修饰,以达到长循环的目的。但是,PEG修饰的载体在体内中也存有诸多弊端和一些不能忽视的问题,如静脉重复注射PEG化脂质体可加速血液清除,从而大大限制了其临床应用。肝素作为修饰材料,具有类PEG化的作用,修饰后的载体表现出更为出色的稳定性、安全性。其次,有研究表明肝素或肝素类似物可以通过成纤维细胞生长因子受体内吞进入肿瘤和肿瘤内皮细胞。因此,肝素修饰的阳离子载药脂质体可赋予药物载体一定的肿瘤血管内皮细胞和肿瘤细胞靶向性,提高治疗效果。
本发明是在构建阳离子脂质体的基础上,通过共价键连接的方式结合肝素,得到肝素修饰的阳离子脂质体。本发明的肝素修饰的阳离子脂质体,体外稳定性实验证明,肝素修饰的阳离子脂质体能显著提高阳离子脂质体的稳定性。载体溶血性实验证明,修饰肝素后,阳离子脂质体的安全性得到提高。
技术实现要素:
本发明的肝素修饰的阳离子脂质体,含下列组分及重量比:
本发明的肝素修饰的阳离子脂质体的制备方法包括:将蛋黄卵磷脂、胆固醇、阳离子材料、药物溶于有机溶剂,减压蒸发去除有机溶剂;活化剂活化肝素,备用;将活化后的肝素溶液加入制备的阳离子脂质体中室温反应过夜;超滤除去游离的肝素,即得肝素修饰的阳离子脂质体混悬液;制备成冻干粉针剂时,将冻干保护剂溶解于脂质体混悬液中,冷冻干燥即可。
上述阳离子材料选自氯化三甲基-2,3-二油烯氧基丙基铵、溴化三甲基-2,3-二油酰氧基丙基铵、三氟乙酸二甲基-2,3-二油烯氧基丙基-2-(2-精胺甲酰氨基)乙基铵、溴化三甲基十二烷基铵、溴化三甲基十四烷基铵、溴化三甲基十六烷基铵、溴化二甲基双十八烷基铵、N-(2-精胺甲酰基)-N’,N’-双十八烷基甘氨酰胺、1,2-二油酰-3-琥珀酰-sn-甘油胆碱酯、3β-[N-(N’,N’-二甲基胺乙基)胺基甲酰基]胆固醇、脂质多聚-L-赖氨酸、硬脂胺中的一种或几种。
上述冻干保护剂选自蔗糖、乳糖、葡萄糖、甘露醇中的一种或几种。
上述药物可以是姜黄素及其衍生物的一种或几种的混合物。
上述有机溶剂选自氯仿、二氯甲烷、乙醚、乙醇、丙酮中的一种或几种,优选二氯甲烷、氯仿。
上述活化剂选自1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐与N-羟基硫代琥珀酰亚胺的混合物,两者比例为1∶2-1∶6。
上述肝素选自普通肝素、达肝素钠、依诺肝素、纳肝素钙、帕肝素钠、汀肝素钠中的一种或几种。
本发明所涉及的比例均为重量比。
当胆固醇取一个固定值,蛋黄卵磷脂取不同的重量时,肝素修饰的阳离子脂质体混悬液的平均粒径和包封率也不同。结果见表1。
表1:药物和蛋黄卵磷脂的比例对脂质体粒径和包封率的影响(n=3)
从表中可以看出,当药物和蛋黄卵磷脂重量比小于1∶5时,粒径较大,包封率很低;当药物:磷脂重量比大于1∶35时,脂质体溶液的透光性下降,粒径逐渐增大,放置越久越不稳定;当药物和大豆卵磷脂重量比在1∶5~35范围内,包封率较高,粒径符合要求,因此本发明中药物/蛋黄卵磷脂的比例为1∶5~35。
当蛋黄卵磷脂取一个固定值,胆固醇取不同的重量时,肝素修饰的阳离子脂质体混悬液的平均粒径和包封率也不同。结果见表2。
表2:药物和胆固醇的比例对脂质体粒径和包封率的影响(n=3)
从表中可以看出,药物和胆固醇的重量比小于1∶0.5时,粒径较大,包封率很低;当药物和胆固醇的重量比大于1∶7时,包封率较低,且放置片刻即絮凝,当药物和胆固醇的重量比例在1∶0.5~7范围内,粒径和包封率均较好,因此本发明中药物/胆固醇的比例在1∶0.5~7。
上述方法制备的肝素修饰的阳离子脂质体混悬液电位在2-5mV。
本发明的突出优点在于:肝素修饰阳离子脂质体后,显著提高阳离子脂质体的血浆稳定性,降低阳离子脂质体的溶血率,提高载体安全性,可以作为抗肿瘤药的有效载体,具有靶向到肿瘤及肿瘤新生血管的功能,提高药物疗效。
附图说明
图1是本发明的肝素修饰的阳离子脂质体血清稳定性结果
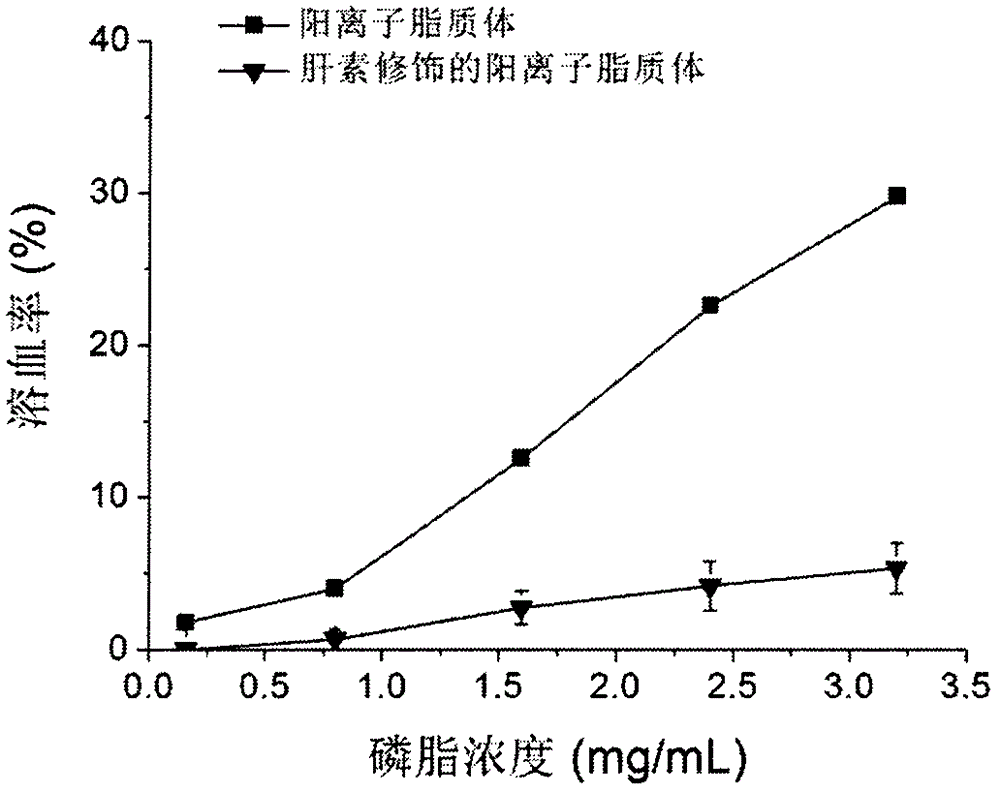
图2是本发明的肝素修饰的阳离子脂质体溶血率结果
具体实施方式
下面结合实施例对本发明作进一步详细描述。但是本发明不限于所给出的例子。下述实施例中的试验方法,如无特殊说明,均为常规方法;试剂和材料,如无特殊说明,均可通过商业途径获得。
实施例1肝素修饰的阳离子脂质体
分别称取处方量的蛋黄卵磷脂10mg、胆固醇1mg、双十八烷基二甲基溴化铵1mg、姜黄素1mg置于茄形瓶中,加入适量二氯甲烷,超声使之完全溶解;旋转减压蒸发除去有机溶剂,在瓶壁上形成干燥均匀的脂质薄膜;加入蒸馏水溶液1mL洗膜,37℃下水合1h,形成脂质体初乳液;探头超声(200W,100次),即得空白脂质体;加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐与N-羟基硫代琥珀酰亚胺至依诺肝素溶液中,比例为1∶3,活化依诺肝素;取阳离子脂质体溶液与等体积的活化后依诺肝素溶液(4mg/mL)室温搅拌过夜;超滤法去除游离的肝素,即得肝素修饰的阳离子脂质体溶液;再将上述溶液中加入适量蔗糖,无菌过滤后(膜滤器孔径0.2μm),将续滤液分装于西林瓶中,冷冻干燥即可。
成品性状:本品为疏松不塌陷粘连的固态。
复水分散性:本品在注射用溶剂如生理盐水中轻微震荡,10s内即可迅速形成均一、稳定、透光性好的混悬液。
粒径测定:取本品适量用采用激光粒度分析仪测定粒径,平均粒径为140.9nm,多分散系数为0.265。
电位测定:取本品适量用采用激光粒度分析仪测定电位,平均电位为3.4mV,多分散系数为0.743。
实施例2肝素修饰的阳离子脂质体
分别称取处方量的蛋黄卵磷脂15mg、胆固醇2mg、硬脂胺1mg、一脱甲氧基姜黄素1mg,置于茄形瓶中,加入适量氯仿,超声使之完全溶解;旋转减压蒸发除去有机溶剂,在瓶壁上形成干燥均匀的脂质薄膜;加入蒸馏水溶液1mL洗膜,37℃下水合1h,形成脂质体初乳液,探头超声(200W,100次),即得空白脂质体。取上述空白脂质体加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐与N-羟基硫代琥珀酰亚胺至普通肝素溶液中,比例为1∶2,活化普通肝素;取阳离子脂质体溶液与等体积的活化后普通肝素溶液(4mg/mL)室温搅拌过夜;超滤法去除游离的肝素,即得肝素修饰的阳离子脂质体溶液;再将上述溶液中加入适量葡萄糖,无菌过滤后(膜滤器孔径0.2μm),将续滤液分装于西林瓶中,冷冻干燥即可。
将冻干脂质体在4℃环境贮存3个月后,粒径为152.4nm,电位为4.7mV。
实施例3肝素修饰的阳离子脂质体
分别称取处方量的蛋黄卵磷脂20mg、胆固醇1.5mg、溴化三甲基十六烷基铵1mg双脱甲氧基姜黄素1mg置于茄形瓶中,加入适量甲醇,超声使之完全溶解;旋转减压蒸发除去有机溶剂,在瓶壁上形成干燥均匀的脂质薄膜;加入蒸馏水溶液1mL洗膜,37℃下水合1h,形成脂质体初乳液,探头超声(200W,100次),即得空白脂质体;取上述空白脂质体加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐与N-羟基硫代琥珀酰亚胺至达肝素溶液中,比例为1∶4,取阳离子脂质体溶液与等体积的达肝素钠溶液(4mg/mL)孵育30min,25℃;超滤法去除游离的肝素,即得肝素修饰的阳离子脂质体溶液;再将上述溶液中加入适量乳糖,无菌过滤后(膜滤器孔径0.2μm),将续滤液分装于西林瓶中,冷冻干燥即可。
将冻干脂质体在4℃环境贮存3个月后,粒径为156.9nm,电位为2.1mV。
实施例4阳离子脂质体血清稳定性考察
取阳离子脂质体溶液和肝素修饰的阳离子脂质体溶液,各500μL置于2mL离心管中与1mL的胎牛血清混合;水浴37℃放置1、6、12、24小时,每个时间点拿出,使用Zetaplus电位及激光粒度分析仪进行粒径检测,直至24小时。
实施例5阳离子脂质体体外溶血率考察
取新鲜的家兔抗凝全血(内部涂肝素钠溶液)5mL,搅拌去除纤维蛋白凝块,加0.9%氯化钠注射用生理盐水,充分混匀后分装于5mL离心管内,1500r/min离心4min,弃去上清液,重复前述操作5次,直至上清液基本无色;剩余的血红细胞用生理盐水配成2%(v/v)的血红细胞悬液,4℃保存,现配现用。取阳离子脂质体溶液和肝素修饰的阳离子脂质体溶液,置于2.5mL离心管中,加入等体积的2%(v/v)血红细胞悬液混匀,于37℃下振荡中孵育20h;另取2%(v/v)的血红细胞悬液2.5mL,分别加入等体积的去离子水和生理盐水混匀,作为阳性对照和阴性对照;将孵育后样品以1500r/min离心10min,取上清液,用紫外-可见光分光光度计于λ=540nm测定吸光度,计算溶血率。
- 还没有人留言评论。精彩留言会获得点赞!