一种脂质体冻干粉制备配方及制备工艺的制作方法
本发明涉及脂质体技术领域,具体为一种脂质体冻干粉制备配方及制备工艺。
背景技术:
自然科学进入21世纪的高速发展以来,人们发现了越来越多药物对人类健康具有巨大帮助,而药学领域,也遇到了这样那样的问题,其中药物的溶解性、稳定性、透皮性,是当前制剂技术的重点和难点之一。这样应运而生的载体技术就成为了一个重要的课题,其中脂质体技术是载体技术的典型代表,脂质体技术的优点:1、将难溶性药物包裹承载,变成易溶于水的包裹物;2、将不稳定成分包裹后,进行很好的保护,提高被包裹物的稳定性;3、脂质体的磷脂双分子层,具有很好的仿生效应,与细胞膜的磷脂双分子层,如出一辙,具有很好的兼容性,能够大大提高其透皮效果,成为一个透皮载体,将药物输送到目标位置;液体状态下的脂质体缺点也非常明确,它只是相对稳定的结构,长期存放,有诸多不稳定因素和现象,例如:受温度、温差、光照、外力等因素的影响,相互融合导致的粒径变大,进而导致失去脂质体结构,释放出被包裹药物等;通过干燥技术获得的前脂质体,成为了解决这一难题的重要方法。而脂质体为保护不稳定成分而存在的意义,让我们更青睐于通过冻干技术来获得前脂质体。
冻干技术,是20世纪以来,应用比较深入的制剂干燥技术,它的原理是,通过一个低温的过程,将含有一定量赋形剂的药物水溶液,冻成冰,确保每个水分子都是以冰的状态存在;然后通过抽真空并给热的方式,改变药物的三相线,让冰始终通过升华的方式变成气态的水分子,被冷井捕捉,从而达到干燥的目的;整个干燥过程,在低温环境下进行,有效保护了热敏感药物及磷脂双分子层。然而脂质体的冻干制剂也存在很多难点,比如由于冰水体积的变化,所导致的磷脂双分子层被破坏,导致冻干后不能形成前脂质体,复水后,无法形成脂质体,或形成较大粒径的脂质体,并伴随着被包裹物包覆率大幅度下降,透皮效果严重受损等问题。
本发明,从处方和工艺等方面的创新上,解决了上述脂质体冻干中遇到的问题,制备出了,复水后脂质体粒径接近冻干前粒径,包覆率基本保持不变,透皮效果显著的脂质体冻干制剂。
技术实现要素:
本发明所解决的技术问题在于提供一种脂质体冻干粉制备配方及制备工艺,以解决上述背景技术中的问题。
本发明所解决的技术问题采用以下技术方案来实现:一种脂质体冻干粉制备配方,包括:脂质体、赋形剂、水;具体配方由以下百分比的原料制成:脂质体50%、赋形剂5-15%、其余为水;所述脂质体的组成为:磷脂1-20%、胆固醇0.1-10%、吐温0.2-2%、海藻糖5-10%、活性物0.2-20%、无水乙醇2-30%和其余为水。
优选地,所述赋形剂包括海藻糖及甘露醇、蔗糖、鼠李糖、葡萄胺中的一种或多种。
优选地,所述吐温为吐温20、吐温60、吐温80中的一种或多种。
优选地,所述活性物为寡肽、白藜芦醇、抗坏血酸钠、传明酸、光甘草定、积雪草苷、甘草亭酸、熊果苷等中的一种或几种。
一种脂质体冻干粉制备工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取活性物、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、活性物、吐温溶解在水中构成水相;
步骤2:在80-95℃条件下,将乙醇相以0.5-5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30-90转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在1000-10000pa、80-95℃的条件下,减压蒸馏除去乙醇,然后高压均质,均匀压力800-1200mpa,控制粒径60-150nm,得脂质体;
步骤4:按照脂质体冻干制剂的原料百分比,取步骤3所制取的脂质体、赋形剂、水,混合均匀得冻干母液;
步骤5:将冻干母液分装在冻干用包材中,以1-5℃/分钟的速率,快速降到-30℃至-40℃,保温30分钟,以1-3℃/分钟的速度,将温度回升到-15℃至-20℃,保温5-10分钟,再以0.5-2℃/分钟的速率,将温度降低到-40℃至-50℃,保温30分钟,将箱内压力控制在5-250pa的真空条件下,升温升华,直至干燥。
优选地,所述步骤4中的包材为西林瓶、冻干安瓶、冻干泡罩等。
本发明的脂质体冻干粉的用法如下:
脂质体冻干粉可以添加到护肤各类外用制剂中,添加两0.1%-10%,起到相应的活性功效,或者直接用溶媒溶解后,涂抹在皮肤上使用。
与已公开技术相比,本发明存在以下优点:本发明的脂质体,由吐温的存在,大大提高了脂质体的柔性,在外力的作用下,可以使脂质体任意变形,增加韧性;本发明的脂质体,由海藻糖的参与构成,在冻干过程中,具有对水分子补位的效果,能够使脂质体在干燥过程中,得到最大的保护;冻干后的前脂质体,在复水之后粒径变化在可控范围之内;生产的脂质体冻干粉可直接加溶媒使用。
附图说明
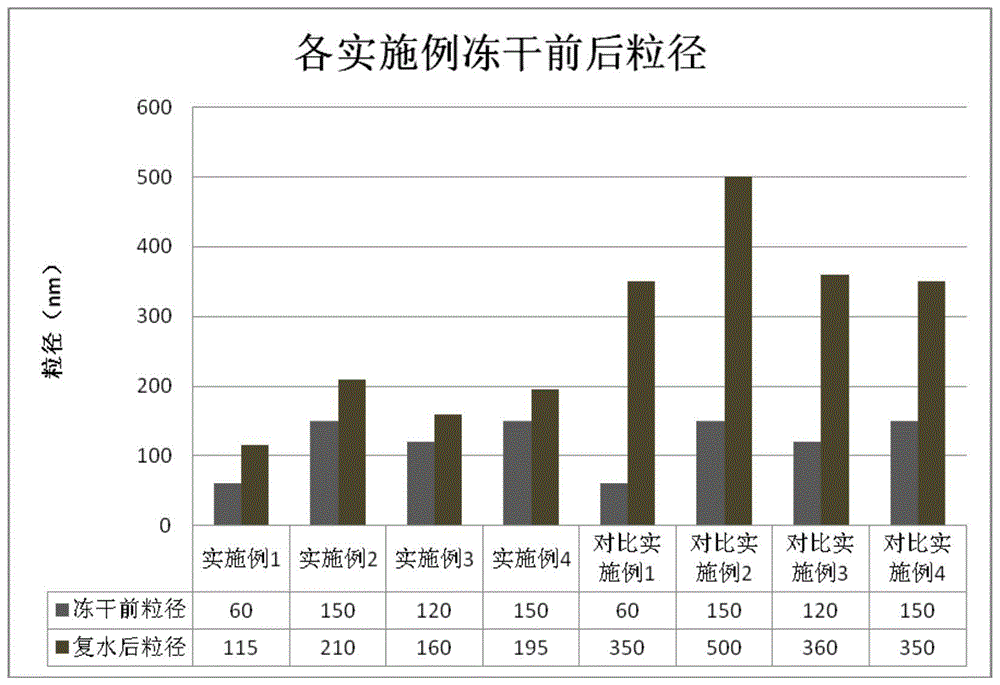
图1为本发明实施例所得冻干前后脂质体粒径数据对比图;
图2为本发明实施例所得冻干粉复水后粒径增加值对比图;
图3为为本发明实施例所得冻干后复水的透皮测试数据对比图。
具体实施方式
为了使本发明的技术手段、创作特征、工作流程、使用方法达成目的与功效易于明白了解,下面将结合本发明实施例,对本发明实施例中的技术方案进行清楚、完整地描述,显然,所描述的实施例仅仅是本发明一部分实施例,而不是全部的实施例。基于本发明中的实施例,本领域普通技术人员在没有做出创造性劳动前提下所获得的所有其他实施例,都属于本发明保护的范围。
实施例1
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用甘露醇;具体配方由以下百分比的原料制成:甘露醇5%、脂质体50%、其余为水;其中脂质体的组成为:磷脂20%、胆固醇10%、吐温20为2%、海藻糖5%、视黄醇7.8%、光甘草定0.2%、抗坏血酸10%、传明酸2%、无水乙醇30%和加水至100%。
一种脂质体冻干粉制备工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取视黄醇、光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、传明酸、抗坏血酸、吐温20溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在1000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力1200mpa,控制粒径60nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3制得的脂质体、甘露醇、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以1℃/分钟的速率,快速降到-30℃,保温30分钟,以1℃/分钟的速度,将温度回升到-15℃,保温10分钟,再以0.5℃/分钟的速率,将温度降低到-40℃,保温30分钟,将箱内压力控制在5pa的真空条件下,升温升华,直至干燥。
实施例2
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用海藻糖;具体配方由以下百分比的原料制成:海藻糖10%、脂质体50%、其余为水;其中脂质体组成:磷脂1%、胆固醇0.5%、吐温60为0.2%、海藻糖10%、光甘草定0.2%、无水乙醇2%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、吐温60溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在10000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力800mpa,控制粒径150nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、海藻糖、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以1℃/分钟的速率,快速降到-40℃,保温30分钟,以3℃/分钟的速度,将温度回升到-20℃,保温5分钟,再以1℃/分钟的速率,将温度降低到-50℃,保温30分钟,将箱内压力控制在250pa的真空条件下,升温升华,直至干燥。
实施例3
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用赤藓糖醇;具体配方由以下百分比的原料制成:赤藓糖醇15%、脂质体50%、其余为水;其中脂质体组成:磷脂10%、胆固醇5%、吐温80为1%、海藻糖7.5%、寡肽0.2%、白藜芦醇1%、光甘草定0.2%、维生素e0.5%、无水乙醇20%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取白藜芦醇、神经酰胺、光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取寡肽、海藻糖、吐温80溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在10000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力800mpa,控制粒径120nm,然后加入甘露醇得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、赤藓糖醇、鼠李糖、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以3℃/分钟的速率,快速降到-35℃,保温30分钟,以2℃/分钟的速度,将温度回升到-18℃,保温8分钟,再以0.75℃/分钟的速率,将温度降低到-45℃,保温30分钟,将箱内压力控制在150pa的真空条件下,升温升华,直至干燥。
实施例4
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用赋形剂选用葡糖胺与鼠李糖,质量比为1:1;具体配方由以下百分比的原料制成:赋形剂10%、脂质体50%、其余为水;其中脂质体组成:磷脂10%、胆固醇5%、吐温80为1%、海藻糖7.5%、神经酰胺0.2%、光甘草定0.2%、维生素e0.5%、无水乙醇20%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取光甘草定、神经酰胺、维生素e、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、吐温80溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在10000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力800mpa,控制粒径150nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、葡萄胺、鼠李糖、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以3℃/分钟的速率,快速降到-35℃,保温30分钟,以2℃/分钟的速度,将温度回升到-18℃,保温8分钟,再以0.75℃/分钟的速率,将温度降低到-45℃,保温30分钟,将箱内压力控制在150pa的真空条件下,升温升华,直至干燥。
对比实施例1
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用甘露醇;具体配方由以下百分比的原料制成:赋形剂5%、脂质体50%、其余为水;其中脂质体组成:磷脂20%、胆固醇10%、海藻糖5%、视黄醇7.8%、光甘草定0.2%、抗坏血酸10%、传明酸2%、无水乙醇30%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取视黄醇、光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、传明酸、抗坏血酸溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在1000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力1200mpa,控制粒径60nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、甘露醇、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以1℃/分钟的速率,快速降到-30℃,保温30分钟,以1℃/分钟的速度,将温度回升到-15℃,保温10分钟,再以0.5℃/分钟的速率,将温度降低到-40℃,保温30分钟,将箱内压力控制在5pa的真空条件下,升温升华,直至干燥。
对比实施例2
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用海藻糖;具体配方由以下百分比的原料制成:赋形剂15%、脂质体50%、其余为水;其中脂质体组成:磷脂1%、胆固醇0.5%、吐温60为0.2%、光甘草定0.2%、无水乙醇2%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取吐温60溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在10000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力800mpa,控制粒径150nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、海藻糖、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以1℃/分钟的速率,快速降到-40℃,保温30分钟,以3℃/分钟的速度,将温度回升到-20℃,保温5分钟,再以1℃/分钟的速率,将温度降低到-50℃,保温30分钟,将箱内压力控制在250pa的真空条件下,升温升华,直至干燥。
对比实施例3
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用赤藓糖醇;具体配方由以下百分比的原料制成:赋形剂15%、脂质体50%、其余为水;其中脂质体组成:磷脂10%、胆固醇5%、吐温80为1%、海藻糖7.5%、寡肽0.2%、白藜芦醇1%、光甘草定0.2%、维生素e0.5%、无水乙醇20%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取白藜芦醇、神经酰胺、光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取寡肽、海藻糖、吐温80溶解在水中构成水相;
步骤2:在80℃条件下,将乙醇相以0.5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度30转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在10000pa、80℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力800mpa,控制粒径120nm,然后加入甘露醇得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、赤藓糖醇、鼠李糖、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以3℃/分钟的速率,快速降到-35℃,保温30分钟,将温度降低到-45℃,保温30分钟,将箱内压力控制在150pa的真空条件下,升温升华,直至干燥。
对比实施例4
一种脂质体冻干制剂的配方包括:脂质体、赋形剂、水,所述赋形剂选用鼠李糖;具体配方由以下百分比的原料制成:赋形剂12%、脂质体50%、其余为水;其中脂质体组成:磷脂4%、胆固醇2%、吐温80为0.2%、海藻糖6%、积雪草苷0.5%、甘草亭酸0.2%、光甘草定0.2%、水杨酸2%、无水乙醇25%和加水至100%。
一种脂质体冻干制剂的工艺,具体包括以下步骤:
步骤1:按照脂质体冻干制剂中脂质体配方的原料百分比,取积雪草苷、甘草亭酸、水杨酸、光甘草定、磷脂、胆固醇溶解在无水乙醇中构成乙醇相;取海藻糖、吐温80溶解在水中构成水相;
步骤2:在95℃条件下,将乙醇相以5升/分钟的速度注入水相中,边注入边搅拌,搅拌速度90转/分钟;
步骤3:将步骤2中获得混合均匀的溶液,在8000pa、85℃的条件下,蒸馏除去乙醇;然后高压均质,均质压力1000mpa,控制粒径60nm,得脂质体;
步骤4、按照脂质体冻干制剂的原料百分比,取步骤3的脂质体、赋形剂、水,混合均匀得冻干母液;
步骤5:冻干母液分装在冻干用包材中,包材为西林瓶、或冻干安瓶、或冻干泡罩,以0.5℃/分钟的速率,降到-35℃,保温30分钟,以0.5℃/分钟的速度,将温度回升到-18℃,保温8分钟,再以2℃/分钟的速率,将温度降低到-45℃,保温30分钟,将箱内压力控制在150pa的真空条件下,升温升华,直至干燥。
效果实施例1:脂质体冻干制剂复水后粒径的变化
一、实验方法
使用ms2000马尔文粒度仪对各实施例及对比实施例的样品,冻干前后进行粒径测试。
操作步骤
1、仪器开机
(1)先打开与ms2000马尔文粒度仪相连的计算机,进入windows操作环境。
(2)打开粒度仪主机开关,粒度仪分散器电源开关。
(3)打开mastersizer2000操作软件,仪器进入主工作程序,开机预热30min。
2、参数设置
(1)设定泵的转速,如有必要则设定超声的强度和时间,在烧杯中加入600ml左右的分散介质(通常是蒸馏水),然后打开循环泵,让分散介质循环。
(2)新建一个文件,单击“测量”菜单中的“手动”按钮,进入测量窗口。然后进入“选项”菜单。
(3)单击“物质”按钮,根据折射率选择“样品物质”和“分散剂”,单击“模型”选择“通用模式”进行未知样品的测量;单击“高级”,选择结果转换为“数量”。
(4)单击“测量”按钮,输入“样品测量时间”和“背景测量时间”。在高级选项中单击“测量”,输入遮光度界限“下限”及“上限”。
(5)单击“测量循环”,选择测量循环次数及测量之间延迟时间,并创建平均值。
(6)单击“文档”输入样品名称后“确定”。
3、样品测量
(1)点击“开始”按钮,系统自动对光,测量背景。
(2)当背景测量完成以后并提示“加入样品”后,开始加入样品到所设定的遮光度界限内,然后单击“开始”,仪器会进行测量样品。
(3)结果分析
单击检查样品名称,进入结果分析界面,红色d(0.5)即样品粒径大小。
二、实验结果:
结果如图1、图2;
三、结果分析:
根据图1、图2可以看出,冻干后复水,脂质体粒径都有所增加,其中,实施例增加幅度远不如对比实施例粒径增加幅度大,说明实施例的处方与工艺,对脂质体冻干制剂有很好的稳定作用。
效果实施例2:脂质体冻干制剂复水后透皮吸收的比较
一、实验方法:
1、实验分组及处理
选取实施例1、实施例2、实施例3、实施例4、对比实施例1、对比实施例2,对比实施例3、对比实施例4前脂质体冻干制剂,用水分别复溶,配制含光甘草定500ppm的脂质体,用于透皮测试,500ppm的光甘草定混悬液作为对照。
2、离体鼠皮的制备
将昆明种合格小鼠用10%na2s脱去背部皮毛,脱颈椎处死后,立即剥取背部皮肤,除去皮下脂肪层,用蒸馏水洗净,浸于蒸馏水中备用。
3、透皮吸收实验
采用franz实验装置,将皮肤固定于扩散池的给药室与接受室之间,两池有效接触面积为2.06cm2,真皮一侧与接受液接触,注意结合紧密,勿有气泡,接受液为5ml生理盐水。供给池内加1ml各实施例复水后的脂质(光甘草定500ppm),磁力搅拌速度为100r/min,水浴温度为37±1℃,在5h后取接受池样品,破坏样品脂质结构后测试接受室中光甘草定含量。
二、实验结果:
结果如图3;
三、结果分析:
从图3,我们可以看出,各实施例、对比实施例脂质体冻干制剂复水后,其透皮效果都比光甘草定混悬液效果好,说明包裹有利于难溶性物质的透皮吸收;各实施例比对比实施例冻干制剂复水后的透皮效果,要显著提高,说明本发明技术冻干制剂复水后在透皮效果上有明显的提高。
以上显示和描述了本发明的基本原理、主要特征及本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的只是说明本发明的原理,在不脱离本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明的要求保护范围由所附的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!