一种聚乙二醇修饰的钆‑二硫化钼纳米花的一步制备法的制作方法
本发明涉及一种多功能纳米花的制备方法,具体涉及一种聚乙二醇修饰的钆-二硫化钼纳米花的一步制备法。
背景技术:
二维纳米材料因其优越性能而在各类研究中发挥作用,石墨烯及其衍生物氧化石墨烯(GO)作为其中的典型代表已广泛用于生物传感、癌症治疗试剂、生物成像探针以及组织工程支架等(F. Li, J. Chao, Z. Li, S. Xing, S. Su, X. Li, S. Song, X. Zuo, C. Fan, B. Liu, W. Huang, L. Wang, L. Wang. Anal. Chem.2015, 87 , 3877-3883. H. Zhang, H. Wu, J. Wang, Y. Yang, D. Wu, Y. Zhang, Z. Zhou, S. Yang. Biomaterials2015, 42 , 66-77. S. Shi, K. Yang, H. Hong, F. Chen, H. F. Valdovinos, S. Goel, T. E. Barnhart, Z. Liu, W. Cai. Biomaterials 2015, 39, 39-46. K. Yang, L. Hu, X. Ma, S. Ye, L. Cheng, X. Shi, C. Li, Y. Li, Z. Liu. Adv. Mater.2012, 24 , 1868-1872.)。作为纳米载体,石墨烯及其衍生物具有超大的比表面可以提高载药率、易在肿瘤部位富集等优点而用于蛋白药物、基因、小分子药物的靶向递送。随着人们对纳米载体要求的不断提高,纳米载体也逐渐由传统的单一功能向多功能转变。
二硫化钼(MoS2)作为典型的过渡金属二硫族化合物成为近年来备受关注的二维量子功能材料之一,它们有着与石墨烯类似的结构,但相邻的晶格点位被不同原子交替占据,具有强烈的自旋-轨道耦合,展现出一系列新奇的性能。MoS2良好的电性能使其用于FET传感器(D. Sarkar, W. Liu, X. Xie, A. C. Anselmo, S. Mitragotri, K. Banerjee. ACS Nano 2014, 8 , 3992-4003. B. Cho, M. G. Hahm, M. Choi, J. Yoon, A. R. Kim, Y.-J. Lee, S.-G. Park, J.-D. Kwon, C. S. Kim, M. Song, Y. Jeong, K.-S. Nam, S. Lee, T. J. Yoo, C. G. Kang, B. H. Lee, H. C. Ko, P. M. Ajayan, D.-H. Kim. Sci. Rep.2015, 5 , 8052-8057.),良好的荧光猝灭功能可用于DNA检测和光电化学传感(C. Zhu, Z. Zeng, H. Li, F. Li, C. Fan, H. Zhang. J. Am. Chem. Soc. 2013, 135 , 5998-6001. Y. Huang, Y. Shi, H. Y. Yang, Y. Ai. Nanoscale 2015, 7 , 2245-2249.),2D结构提供的大比表面积可用于气体吸附(M. Donarelli, S. Prezioso, F. Perrozzi, F. Bisti, M. Nardone, L. Giancaterini, C. Cantalini, L. Ottaviano. Sens. Actuators B2015, 207 , 602-613.)和药物装载(T. Liu, C. Wang, X. Gu, H. Gong, L. Cheng, X. Z. Shi, L. Z. Feng, B. Q. Sun, Z. Liu. Adv. Mater.2014, 26 , 3433-3440.)。作为纳米载体MoS2具有其特有的优势。与GO相比,MoS2的表面功能化更简单,MoS2表面自由暴露的硫原子很容易与其他含硫基团结合形成双硫键,此类双硫键对肿瘤微环境敏感,可用于药物递送系统的构建及传感(S. Son, R. Namgung, J. Kim, K. Singha, W. J. Kim. Acc. Chem. Res.2012, 45 , 1100-1112.)。此外,Mo具有很强的X射线减弱能力,可将近红外光转化为热能,用于CT、光声成像引导下的光热治疗、化学治疗和多模态成像(S. S. Chou, B. Kaehr, J. Kim, B. M. Foley, M. De, P. E. Hopkins, J. Huang, C. J. Brinker, V. P. Dravid. Angew. Chem. Int. Ed.2013, 52, 4160-4164. T. Liu, S. Shi, C. Liang, S. Shen, L. Cheng, C. Wang, X. Song, S. Goel, T. E. Barnhart, W. Cai, Z. Liu. ACS Nano 2015, 9 , 950-960. L. Cheng, J. Liu, X. Gu, H. Gong, X. Shi, T. Liu, C. Wang, X. Wang, G. Liu, H. Xing, W. Bu, B. Sun, Z. Liu. Adv. Mater.2014, 26 , 1886-1893.)。
在结构上,MoS2单层包含三个共价结合的六边形原子层(S-Mo-S),在邻近MoS2单层间存在弱的范德瓦耳斯相互作用(V. Nicolosi, M. Chhowalla, M. G. Kanatzidis, M. S. Strano, J. N. Coleman. Science 2013, 340 , 1421-1439.)。不同于石墨烯,单层MoS2的三个原子层纳米片使其没有明显的褶皱形貌,取而代之的是更光滑的形貌。但是如何对MoS2进行缺陷的引导、层数的控制、有效、低耗、简单易操作的制备方法仍然需要,对于MoS2及其相关纳米复合物质量和结构的优化、功能的开发仍然需要开展大量工作。
技术实现要素:
针对上述现有技术存在的问题,本发明提供一种聚乙二醇修饰的钆-二硫化钼纳米花的一步制备法,聚乙二醇即PEG,钆-二硫化钼即Gd-MoS2,制备方法步骤简单,对制备条件要求相对宽松,制备的PEG功能化Gd-MoS2纳米花具备Gd的磁共振成像对比增强能力和MoS2光热转化能力。
为了实现上述目的,本发明采用的技术方案是:一种聚乙二醇修饰的钆-二硫化钼纳米花的一步制备法,包括以下步骤,
A.钼酸铵与聚乙二醇分散于水中,搅拌均匀;
B.随后加入2mmol硫代乙酰胺搅拌形成均一透明溶液;
C.最后加入六水合硝酸钆搅拌均匀后转入高压反应釜中加热;
D.得到的产物离心后乙醇、水洗各三遍,产物再经过冷冻干燥得到的黑色粉末状样品即为成品。
进一步的,所述步骤A中钼酸铵的质量为0.1-0.2g,聚乙二醇的质量为0.3-0.8g,水的容积为5-40mL。
进一步的,所述步骤B中硫代乙酰胺的容积为2-20mL。
进一步的,所述步骤C中六水合硝酸钆的质量为0.02-0.04g,在高压反应釜中加热的温度为150-200度,加热的时间为15-20小时。
进一步的,所述聚乙二醇的分子量为400。
与现有技术相比,本发明对制备聚乙二醇修饰的钆-二硫化钼纳米花条件要求相对宽松,步骤简单,采用聚乙二醇作为表面活性剂,一步法制备聚乙二醇修饰的钆-二硫化钼纳米花粒径大小均一、分散性好、稳定,而且表面修饰的聚乙二醇减少纳米粒子的非特异性吸附,且制备的钆-二硫化钼纳米花具有良好的生物相容性,在磁共振成像时有助于增强T1信号,具有光热转化能力。
附图说明
图1A为本发明所制备PEG修饰Gd-MoS2纳米花的透射电镜图;
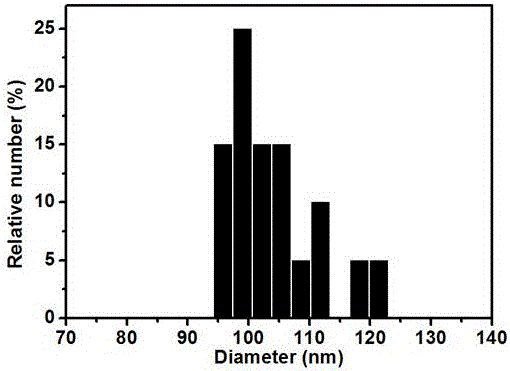
图1B为本发明所制备PEG修饰Gd-MoS2纳米花粒径大小分布图;
图1C为本发明所制备PEG修饰Gd-MoS2纳米花的扫描电镜图;
图1D为本发明所制备PEG修饰Gd-MoS2纳米花的EDS元素分布图;
图2A为本发明所制备PEG修饰Gd-MoS2纳米花MRI弛豫率测定曲线图;
图2B为不同浓度水溶性PEG修饰Gd-MoS2纳米花的MRI图像和T1 map图;
图3为本发明所制备PEG修饰Gd-MoS2纳米花的光热转化;
图4为本发明所制备PEG修饰Gd-MoS2纳米花的傅立叶变换红外吸收光谱;
图5为本发明所制备PEG修饰Gd-MoS2纳米花的XRD光谱;
图6A为本发明所制备PEG修饰Gd-MoS2纳米花的X射线光电子能谱分析(XPS)图谱;
图6B为本发明所制备PEG修饰Gd-MoS2纳米花中Mo元素X射线光电子能谱分析(XPS)图谱;
图6C为本发明所制备PEG修饰Gd-MoS2纳米花中S元素X射线光电子能谱分析(XPS)图谱;
图6D为本发明所制备PEG修饰Gd-MoS2纳米花中Gd元素X射线光电子能谱分析(XPS)图谱;
图7A为本发明所制备PEG修饰Gd-MoS2纳米花的肾癌细胞生物相容性评估图;
图7B为本发明所制备PEG修饰Gd-MoS2纳米花的人正常结直肠粘膜细胞生物相容性评估图。
具体实施方式
下面结合附图对本发明作进一步说明。
实施例一:
A. 0.1g的钼酸铵与0.8g分子量为400的聚乙二醇分散于5mL的水中,搅拌均匀;
B. 随后加入2mL 2mmol硫代乙酰胺搅拌形成均一透明溶液;
C. 最后加入0.02g六水合硝酸钆搅拌均匀后转入高压反应釜中,在150度的温度下加热15小时;
D. 得到的产物离心后乙醇、水洗各三遍,产物再经过冷冻干燥得到成品即PEG功能化Gd-MoS2纳米花。
实施例二:
A. 0.1766g的钼酸铵与0.5g分子量为400的聚乙二醇分散于20mL的水中,搅拌均匀;
B. 随后加入10mL 2mmol硫代乙酰胺搅拌形成均一透明溶液;
C. 最后加入0.036g六水合硝酸钆搅拌均匀后转入高压反应釜中,在180度的温度下加热18小时;
D. 得到的产物离心后乙醇、水洗各三遍,产物再经过冷冻干燥得到成品即PEG功能化Gd-MoS2纳米花。
实施例三:
A. 0.2g的钼酸铵与0.3g分子量为400的聚乙二醇分散于40mL的水中,搅拌均匀;
B. 随后加入20mL 2mmol硫代乙酰胺搅拌形成均一透明溶液;
C. 最后加入0.04g六水合硝酸钆搅拌均匀后转入高压反应釜中,在200度的温度下加热20小时;
D. 得到的产物离心后乙醇、水洗各三遍,产物再经过冷冻干燥得到成品即PEG功能化Gd-MoS2纳米花。
如图1A、图1B、图1C、图1D、图2A、图2B所示,本发明制备的Gd-MoS2纳米花粒径在103 nm左右、大小均一、分散性好,弛豫率为37.9 mM.s-1;EDS元素分布图谱显示制备的Gd-MoS2纳米花由Mo,S,Gd,O等元素组成。
如图3所示,在相同激光强度(808nm,1W/cm2)和相同照射时间下,PEG功能化Gd-MoS2纳米花的温度升高较水有显著提高,200 mg/L PEG功能化Gd-MoS2纳米花在1W/cm2 的激光下照射5 分钟温度升高20℃,而同样条件下的水温度只升高4.6℃,说明所制备的PEG功能化Gd-MoS2纳米花具有良好的光热转化效率。
如图4所示,2916 cm-1处有C-H收缩峰;在1630 cm-1处有C=O振动峰;在1114 cm-1处有C-O-C振动峰,说明PEG功能化Gd-MoS2纳米花表面成功修饰上聚乙二醇分子。
如图5所示,PEG功能化Gd-MoS2纳米花的XRD图谱显示MoS2的(002),(100),(101),(103),(110)晶面的布雷格反射,说明MoS2晶型的存在。
如图6A所示,XPS 谱图中的284.8,395.08,532.5, 229.7,162.2,143.98eV六个峰分别归属为C1s,N1s,O1s,Mo3d,S2p 和Gd4d,说明所制备的Gd-MoS2纳米材料含有Mo,S,Gd,O,N,C元素。如图6B所示,对于Mo3d,231.8eV是Mo3d3/2,225.8eV是S2s轨道信号,228.7eV是Mo3d5/2;如图6C所示,对于S2p,161.5eV是S2p3/2,162.2eV是S2p1/2;如图6D所示,对于Gd4d,143.98eV是Gd4d。XPS图谱结果说明Gd-MoS2纳米材料的形成。
如图7A所示,将不同浓度的PEG修饰Gd-MoS2纳米花溶液与肾癌786-0细胞株共培养24小时后,与未加入纳米材料的对照组细胞相比较,发现聚乙二醇修饰的Gd-MoS2纳米花具有良好的生物相容性。
如图7B所示,将不同浓度的PEG功能化Gd-MoS2纳米花溶液与人正常结直肠粘膜细胞株FHC共培养24小时后,与未加入纳米材料的对照组细胞相比较,发现加入本发明提供的PEG修饰Gd-MoS2纳米花具有良好的生物相容性。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种磁性纳米粒子与超滤膜结合处理废弃乳化液的方法与流程
- 一种多肽修饰纳米粒子在制备治疗急性肺损伤的药物中的应用的制作方法与工艺
- 一种金纳米花修饰的离子液体功能化石墨烯纸电极、其制备方法和应用与流程
- 一种新型的透明质酸修饰的多级纳米颗粒及其制备与应用的制作方法与工艺
- 一种核壳结构的磁性纳米粒子及其制备与应用的制作方法与工艺
- 一种室温固相反应制备的纳米铁修饰的铁基氨合成催化剂及其制备方法和应用与流程
- 一种丁氧基修饰的TiO2单晶空心四方纳米锥材料、制备方法及其应用与流程
- 一种改性粒子修饰的有机无机杂化聚合物涂料的制作方法与工艺
- 一种表面修饰片状纳米铜及含有该纳米铜的复合润滑油的制备方法与流程
- 一种用于简便修饰磁性纳米粒子的手性拆分添加剂的制备和应用的制作方法与工艺