一种利西拉来的制备方法与流程
本发明涉及多肽药物合成技术领域,尤其涉及一种利西拉来的制备方法。
背景技术:
利西拉来(lixisenatide)是胰高血糖素样肽-1(glp-1)受体激动剂,是基于具降糖活性的glp-1类似物exendin-4的c末端6个赖氨酸残基的修饰而合成的新型glp-1类似物,能耐受体内二肽基肽酶ⅳ(dpp4)的降解作用。利西拉来的结构如式i所示:
其肽序为:
h-his-gly-glu-gly-thr-phe-thr-ser-asp-leu-ser-lys-gln-met-glu-glu-glu-ala-val-arg-leu-phe-ile-glu-trp-leu-lys-asn-gly-gly-pro-ser-ser-gly-ala-pro-pro-ser-lys-lys-lys-lys-lys-lys-nh2
作为glp-1类似物的一种,利西拉来适用于服用二甲双胍、磺脲类、噻唑烷二酮类、二甲双胍和磺脲类联用、二甲双胍和噻唑烷二酮类联用的ii型糖尿 病患者中,不能有效控制血糖的患者的辅助治疗,以改善对血糖的控制。
目前一种常规合成利西拉来的方法是固相逐步合成(spps)法,该方法具有操作简单、设备要求低等特点。但是因为利西拉来由44个氨基酸组成,固相逐步合成法的产品收率低,肽在合成树脂上容易发生二级结构的弯曲,导致反应位点被包裹,得到的利西拉来粗肽纯度低,杂质繁杂,给产品纯化带来困难,不易得到较高纯度的利西拉来。
对于解决偶联困难的氨基酸问题,片段合成法是固相合成方法中一种常用的手段。片段合成法是先将偶联困难的序列制备成全保护肽片段,按照氨基酸序列将其作为整体直接偶联到指定肽树脂上,从而避开偶联困难的氨基酸位点,避免逐个氨基酸偶联产生的缺损等副反应,能够获得纯度相对高的粗肽,降低纯化难度。但片段合成法采用了常规的树脂外,还需使用大量价格较昂贵的2-ctc树脂制备片段肽树脂,且2-ctc树脂酸敏感性高,偶联时肽容易从树脂上脱落,从而导致制备的片段收率不高,操作步骤相对繁琐,生产成本也大幅度提高。
技术实现要素:
有鉴于此,本发明要解决的技术问题在于提供一种利西拉来的制备方法,该方法操作简便,总收率高,所得产物纯度较高。
本发明提供了一种利西拉来的制备方法,包括:
步骤1:固相合成fmoc-lys-树脂;
步骤2:根据利西拉来的肽序在所述fmoc-lys-树脂上偶联氨基酸或二肽制得利西拉来肽树脂;所述二肽选自-gly-thr、-phe-thr、-thr-ser、-leu-ser、-ser-ser或-pro-ser;
步骤3:所述利西拉来肽树脂经裂解制得利西拉来。
本发明提供的方法将利西拉来肽序中第4~5位(-gly-thr,记为二肽a)、第6~7位(-phe-thr,记为二肽b)、第7~8位(-thr-ser,记为二肽c)、第10~11位(-leu-ser,记为二肽d)、第32~33位(-ser-ser,记为二肽e)或第31~32位、第37~37位(-pro-ser,记为二肽f)的氨基酸以二肽为原料进行偶联,选用的二肽原料为二肽a~f中任一种或多种,不采用二肽为原料的位点则采用单个氨基酸为原料进行偶联。该方法能够有效防止肽键旋转,抑 制肽链卷曲剂收缩,使活性官能团(伯胺)充分暴露,从而有利于氨基酸的偶联,减少缺损等副反应的发生。
在本发明的实施例中,
偶联-gly-thr采用fmoc-gly-thr(psime,mepro)-oh;
偶联-phe-thr采用fmoc-phe-thr(psime,mepro)-oh;
偶联-thr-ser采用fmoc-thr(tbu)-ser(psime,mepro)-oh;
偶联-leu-ser采用fmoc-leu-ser(psime,mepro)-oh;
偶联-ser-ser采用fmoc-ser(tbu)-ser(psime,mepro)-oh;
偶联-pro-ser采用fmoc-pro-ser(psime,mepro)-oh。
其中,fmoc-gly-thr(psime,mepro)-oh的结构如式ii-a;
fmoc-phe-thr(psime,mepro)-oh的结构如式ii-b;
fmoc-thr(tbu)-ser(psime,mepro)-oh的结构如式ii-c;
fmoc-leu-ser(psime,mepro)-oh的结构如式ii-d;
fmoc-ser(tbu)-ser(psime,mepro)-oh的结构如式ii-e;
fmoc-pro-ser(psime,mepro)-oh的结构如式ii-f。
在本发明中,fmoc-lys-树脂的树脂为rinkamide树脂、rinkamide-mbha树脂、rinkamide-am树脂或siber树脂。
其中,lys的保护基为boc。
作为优选,fmoc-lys(boc)-树脂的替代度为0.1mmol/g~0.6mmol/g。优选的,替代度范围为0.2mmol/g~0.4mmol/g。
在本发明的实施例中,偶联的偶联剂为hobt与dic的混合物;其中hobt与dic的摩尔比为1:1。
在本发明中,所述偶联的步骤包括:脱除fmoc保护后,以dcm和dmf的混合液为溶剂,与偶联剂混合后进行偶联反应。
作为优选,脱除保护的树脂与待偶联氨基酸的摩尔比为1:3。
重复偶联的步骤直至合成整个肽链。
在本发明中,偶联反应的条件为室温反应2h。所述室温为10℃~30℃。
作为优选,如偶联反应不完全则继续偶联反应1h。
在本发明中,偶联反应结束后以甲醇收缩,树脂真空干燥过夜。
在本发明的实施例中,裂解的裂解剂为裂解的裂解剂包括tfa与b组分;所述b组分选自phsme、phome、edt、h2o、tis或phoh。
作为优选,裂解剂中tfa、phsme、phome、edt、h2o、tis、phoh的体积比为(80~90):(0~5):(0~3):(0~5):(0~5):(0~2):(0~5)。
优选的,裂解液中tfa、phsme、edt、tis、h2o的体积比为84:5:5:5:1。
优选的,裂解剂中tfa、phsme、edt、h2o的体积比为91:3:3:3。
优选的,裂解剂中tfa、phsme、edt、phome的体积比为90:5:3:2。
优选的,裂解剂中tfa、edt、h2o的体积比为90:5:5。
优选的,裂解剂中tfa、phsme、phoh、edt、h2o的体积比为85:5:3:5:2。
在本发明中,裂解的步骤包括:将利西拉来肽树脂与裂解液混合,室温裂解2.5h~3h后,以tfa洗涤树脂、以无水乙醚沉淀,获得利西拉来线性粗肽。
作为优选,无水乙醚沉淀的温度为0~4℃。
作为优选,利西拉来肽树脂与裂解液的质量-体积比为1:8~15。
在本发明的实施例中,步骤3后还包括纯化、转盐的步骤。
具体的,纯化的色谱采用novaseprp-hplc系统,检测波长220nm,色谱柱为反相c18柱,流动相a相为体积分数为0.1%的tfa水溶液,流动相b相为乙腈。洗脱梯度为18%乙腈-48%乙腈45min,48%等度15min:纯化后经转盐色谱,转盐。
具体的转盐为转化为醋酸盐,盐酸盐,枸橼酸盐,磷酸盐,三氟乙酸盐,钠盐,钾盐或铵盐。
在一些实施例中,仅引入二肽a,二肽c、二肽d、二肽e、二肽f,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-ser(psime,mepro)-oh、fmoc-phe-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽a,二肽b、二肽d、二肽f,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、 fmoc-ser(tbu)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽a,二肽b、二肽d、二肽e,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽b、二肽d、二肽e,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、 fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽c、二肽e,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-ser(psime,mepro)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽e,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、 fmoc-thr(tbu)-oh、fmoc-phe--oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
在一些实施例中,仅引入二肽d,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe--oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh或boc-his(trt)-oh。
在一些实施例中,仅引入二肽a,二肽b,二肽d,二肽e,二肽f,制备利西拉来。
偶联具体为依次偶联:fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh和boc-his(trt)-oh。
本发明根据利西拉来肽的肽序结构,采用特定的保护的丝氨酸二肽作为 原料偶联到肽序中,由于形成了类似脯氨酸的环状结构,能有效的防止肽键旋转,抑制肽链卷曲剂收缩,使活性官能团(伯胺)充分暴露,从而有利于氨基酸的偶联,减少缺损等副反应的发生。根据实验,本发明精肽收率可高达25.8%~28.8%,优于顺序逐个偶联方法(约15.4%)。同时,本发明精肽的纯度为99.3%。在保证了纯度的同时保证了收率。
附图说明
图1示实施例1制得制得粗肽的质谱图;
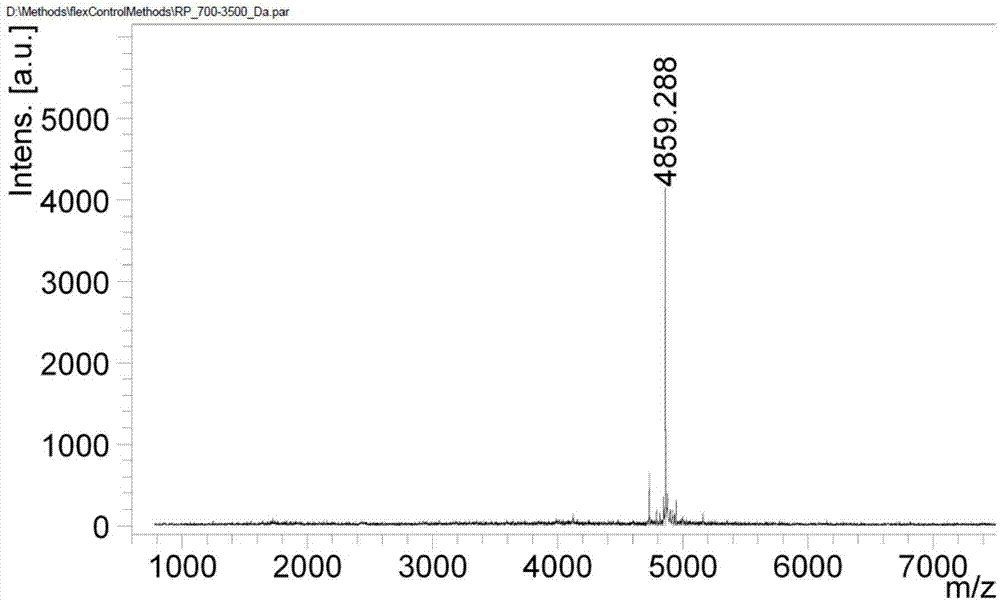
图2示对比例1制得制得粗肽的质谱图。
具体实施方式
本发明提供了一种利西拉来的制备方法,本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明采用的试剂或仪器皆为普通市售品,皆可于市场购得。
其中,各材料的名称及缩写如表1:
表1各材料的名称及缩写
下面结合实施例,进一步阐述本发明:
实施例1
本实施例仅引入二肽a,二肽c、二肽d、二肽e、二肽f,制备利西拉来。
1.1fmoc-lys(boc)-rinkamide-mbharesin的制备
称取干燥rinkamide-mbharesin380g(替代度为0.45mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将238.9gfmoc-lys(boc)-oh(510mmol)、72.4ghoat(536mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic67.5g(535mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-mbharesin421克,检测树脂替代度为0.406mmol/g。
1.2lixisenatide肽树脂的制备
取1.1方法制备的替代度为0.406mmol/g的fmoc-lys(boc)-rinkamide-mbharesin421g(230mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,。将239.1g(510mmol)fmoc-lys(boc)-oh,72.2g(536mmol)hobt,67.7g(535mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-ser(psime,mepro)-oh、fmoc-phe-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到2018克lixisenatide肽树脂。
1.3lixisenatide肽树脂的裂解和精肽制备
取1.2得到的lixisenatide肽树脂700g置于裂解反应器中,以8ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:edt:tis:h2o=84:5:5:5:1,(v/v)),室温搅拌2.5h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽341g,质谱(图1)maldi-tof:(m+h)+=4859.216。粗肽重量收率为 99.4%,hplc纯度为69.1%。
取1.3中得到的lixisenatide粗肽44g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽12.6g,hplc纯度99.3%,精肽收率28.8%。
实施例2
本实施例仅引入二肽a,二肽b、二肽d、二肽f,制备利西拉来。
2.1fmoc-lys(boc)-rinkamideresin的制备
称取干燥rinkamideresin356g(替代度为0.42mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将210.9gfmoc-lys(boc)-oh(450mmol)、63.8ghobt(473mmol)、170.6ghbtu(450mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dipea87.6g(675mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamideresin390克,检测树脂替代度为0.385mmol/g。
2.2lixisenatide肽树脂的制备
取2.1方法制备的替代度为0.385mmol/g的fmoc-lys(boc)-rinkamideresin421g(150mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,。将211.3g(450mmol)fmoc-lys(boc)-oh,64.8g(473mmol)hobt,63.9g(473mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-oh、 fmoc-pro-ser(psime,mepro)-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到1611克lixisenatide肽树脂。
2.3lixisenatide肽树脂的裂解和精肽制备
取2.2得到的lixisenatide肽树脂600g置于裂解反应器中,以10ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:edt:h2o=91:3:3:3,(v/v)),室温搅拌2.5h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽251g,质谱maldi-tof:(m+h)+=4859.017。粗肽重量收率为101.2%,hplc纯度为66.6%。
取2.3中得到的lixisenatide粗肽47g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽12.4g,hplc纯度99.1%,精肽收率26.4%。
实施例3
本实施例仅引入二肽a,二肽b、二肽d、二肽e,制备利西拉来。
3.1fmoc-lys(boc)-siberresin的制备
称取干燥siberresin155g(替代度为0.35mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将77.6gfmoc-lys(boc)-oh(165mmol)、23.5g hobt(173mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic22.1g(173mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-siberresin368克,检测树脂替代度为0.323mmol/g。
3.2lixisenatide肽树脂的制备
取3.1方法制备的替代度为0.323mmol/g的fmoc-lys(boc)-siberresin368g(54mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,。将77.9g(165mmol)fmoc-lys(boc)-oh,23.5g(173mmol)hobt,22.4g(173mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到831克lixisenatide肽树脂。
3.3lixisenatide肽树脂的裂解和精肽制备
取3.2得到的lixisenatide肽树脂800g置于裂解反应器中,以12ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:edt:phome=90:5:3:2,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无 水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽241g,质谱maldi-tof:(m+h)+=4859.512。粗肽重量收率为98.9%,hplc纯度为68.4%。
取3.3中得到的lixisenatide粗肽50g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽13.7g,hplc纯度99.2%,精肽收率27.4%。
实施例4
本实施例仅引入二肽b、二肽d、二肽e,制备利西拉来。
4.1fmoc-lys(boc)-rinkamide-mbharesin的制备
称取干燥rinkamide-mbharesin135g(替代度为0.24mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将46.8gfmoc-lys(boc)-oh(100mmol)、14.2ghobt(105mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic13.5g(105mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-siberresin143克,检测树脂替代度为0.223mmol/g。
4.2lixisenatide肽树脂的制备
取4.1方法制备的替代度为0.223mmol/g的fmoc-lys(boc)-rinkamide-mbharesin143g(32mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,将45.6g(96mmol)fmoc-lys(boc)-oh,13.8g(101mmol)hobt,12.7g(101mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、 fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到401克lixisenatide肽树脂。
4.3lixisenatide肽树脂的裂解和精肽制备
取4.2得到的lixisenatide肽树脂400g置于裂解反应器中,以15ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:edt:phoh:h2o=85:5:3:5:2,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽156g,质谱maldi-tof:(m+h)+=4859.347。粗肽重量收率为102.6%,hplc纯度为67.9%。
取4.3中得到的lixisenatide粗肽46g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽11.6g,hplc纯度99.3%,精肽收率27.1%。
实施例5
本实施例仅引入二肽c、二肽e,制备利西拉来。
5.1fmoc-lys(boc)-rinkamide-amresin的制备
称取干燥rinkamide-amresin547g(替代度为0.56mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将431.2gfmoc-lys(boc)-oh(918mmol)、130.5g hobt(964mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic121.5g(964mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-amresin621克,检测树脂替代度为0.508mmol/g。
5.2lixisenatide肽树脂的制备
取5.1方法制备的替代度为0.508mmol/g的fmoc-lys(boc)-rinkamide-amresin207g(105mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,。将147.6g(315mmol)fmoc-lys(boc)-oh,44.8g(330mmol)hobt,41.6g(330mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-thr(tbu)-ser(psime,mepro)-oh、fmoc-phe--oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到1046克lixisenatide肽树脂。
5.3lixisenatide肽树脂的裂解和精肽制备
取5.2得到的lixisenatide肽树脂1000g置于裂解反应器中,以10ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:edt:h2o=90:5:5,(v/v)), 室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽487g,质谱maldi-tof:(m+h)+=4859.109。粗肽重量收率为100.6%,hplc纯度为67.1%。
取5.3中得到的lixisenatide粗肽43g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽11.9g,hplc纯度99.3%,精肽收率28.1%。
实施例6
本实施例仅引入二肽e,制备利西拉来。
6.1fmoc-lys(boc)-rinkamide-amresin的制备
称取干燥rinkamide-amresin547g(替代度为0.56mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将431.2gfmoc-lys(boc)-oh(918mmol)、130.5ghobt(964mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic121.5g(964mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-amresin621克,检测树脂替代度为0.508mmol/g。
6.2lixisenatide肽树脂的制备
取6.1方法制备的替代度为0.508mmol/g的fmoc-lys(boc)-rinkamide-amresin137g(70mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次。将98.5g(210mmol)fmoc-lys(boc)-oh,30.6g(220mmol)hobt,27.9g(220mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe--oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到728克lixisenatide肽树脂。
6.3lixisenatide肽树脂的裂解和精肽制备
取6.2得到的lixisenatide肽树脂728g置于裂解反应器中,以10ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:edt:h2o=90:5:5,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽338.9g,质谱maldi-tof:(m+h)+=4859.205。粗肽重量收率为99.6%,hplc纯度为61.8%。
取6.3中得到的lixisenatide粗肽58g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽14.9g,hplc纯度99.2%,精肽收率25.8%。
实施例7
本实施例仅引入二肽d,制备利西拉来。
7.1fmoc-lys(boc)-rinkamide-amresin的制备
称取干燥rinkamide-amresin547g(替代度为0.56mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀 树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将431.2gfmoc-lys(boc)-oh(918mmol)、130.5ghobt(964mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic121.5g(964mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-amresin621克,检测树脂替代度为0.508mmol/g。
7.2lixisenatide肽树脂的制备
取7.1方法制备的替代度为0.508mmol/g的fmoc-lys(boc)-rinkamide-amresin137g(70mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次。将98.5g(210mmol)fmoc-lys(boc)-oh,31.6g(220mmol)hoat,27.9g(220mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe--oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到742克lixisenatide肽树脂。
7.3lixisenatide肽树脂的裂解和精肽制备
取7.2得到的lixisenatide肽树脂742g置于裂解反应器中,以10ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:phoh:edt:h2o=85:5:3:5:2,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽341.3g,质谱maldi-tof:(m+h)+=4859.318。粗肽重量收率为100.8%,hplc纯度为59.6%。
取7.3中得到的lixisenatide粗肽48g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽12.8g,hplc纯度99.1%,精肽收率26.6%。
实施例8
本实施例仅引入二肽a,二肽b,二肽d,二肽e,二肽f,制备利西拉来。
8.1fmoc-lys(boc)-rinkamide-amresin的制备
称取干燥rinkamide-amresin547g(替代度为0.56mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将431.2gfmoc-lys(boc)-oh(918mmol)、130.5ghobt(964mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic121.5g(964mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-amresin621克,检测树脂替代度为0.508mmol/g。
8.2lixisenatide肽树脂的制备
取8.1方法制备的替代度为0.508mmol/g的fmoc-lys(boc)-rinkamide-amresin136g(70mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次。将98.5g(210mmol)fmoc-lys(boc)-oh,31.6g(220mmol)hoat,109.5g (210mmol)pyaop,54.3g(420mmol)dipea溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-pro-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-ser(psime,mepro)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-ser(psime,mepro)-oh、fmoc-asp(otbu)-oh、fmoc-ser(tbu)-oh、fmoc-phe-thr(psime,mepro)-oh、fmoc-gly-thr(psime,mepro)-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到751克lixisenatide肽树脂。
8.3lixisenatide肽树脂的裂解和精肽制备
取8.2得到的lixisenatide肽树脂742g置于裂解反应器中,以10ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:phoh:edt:h2o=85:5:3:5:2,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽335.6g,质谱maldi-tof:(m+h)+=4859.478。粗肽重量收率为97.6%,hplc纯度为68.9%。
取8.3中得到的lixisenatide粗肽52g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽14.5g,hplc纯度99.2%,精肽收率27.9%。
对比例1
d1.1fmoc-lys(boc)-rinkamide-amresin的制备
称取干燥rinkamide-amresin410g(替代度为0.56mmol/g)加入到固相反应柱中,首先dmf洗涤树脂2遍,再用2~3倍树脂床层体积dmf溶胀树脂30分钟,dmf洗涤3次,dcm洗涤2次,等待投料。
在冰浴冷却的条件下,将323.5gfmoc-lys(boc)-oh(690mmol)、97.9ghobt(725mmol)溶于dmf和dcm的混合溶剂中,待氨基酸溶解后,慢慢加入dic92.4g(725mmol),活化3min后将反应液倒入反应柱中,鼓气搅拌反应;采用茚三酮检测树脂反应透明时停止反应,dmf洗涤3遍,甲醇收缩、减压干燥得fmoc-lys(boc)-rinkamide-amresin462克,检测树脂替代度为0.51mmol/g。
d1.2顺序偶联制备lixisenatide肽树脂
取d1.1方法制备的替代度为0.51mmol/g的fmoc-lys(boc)-rinkamide-amresin462g(230mmol),加入固相反应柱中,用dmf洗涤2次,用dmf溶胀树脂30分钟后,用dblk脱除fmoc保护,然后用dmf洗涤6次,。将323.6g(690mmol)fmoc-lys(boc)-oh,98.1g(725mmol)hobt,92.4g(724mmol)dic溶于体积比为1:1的dcm和dmf混合溶液,加入固相反应柱中,室温反应2h(反应终点以茚三酮法检测为准,如果树脂无色透明,则反应完全,树脂显色,表示反应不完全,需再偶联反应1h至树脂检测透明)。
重复上述脱除fmoc保护和加入相应氨基酸偶联的步骤,按照片段的顺序,采用一定的偶联方法,依次完成fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-pro-oh、fmoc-ala-oh、fmoc-gly-oh、fmoc-ser(tbu)-oh、fmoc-ser(tbu)-oh、fmoc-pro-oh、fmoc-gly-oh、fmoc-gly-oh、fmoc-asn(trt)-oh、fmoc-lys(boc)-oh、fmoc-leu-oh、fmoc-trp(boc)-oh、fmoc-glu(otbu)-oh、fmoc-ile-oh、fmoc-phe-oh、fmoc-leu-oh、fmoc-arg(pbf)-oh、fmoc-val-oh、fmoc-ala-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-glu(otbu)-oh、fmoc-met-oh、fmoc-gln(trt)-oh、fmoc-lys(boc)-oh、fmoc-ser(tbu)-oh、fmoc-leu-oh、fmoc-asp(otbu)-oh、 fmoc-ser(tbu)-oh、fmoc-thr(tbu)-oh、fmoc-phe-oh、fmoc-thr(tbu)-oh、fmoc-gly-oh、fmoc-glu(otbu)-oh、fmoc-gly-oh、boc-his(trt)-oh的偶联。反应结束后用甲醇收缩,树脂真空干燥过夜,得到2350克lixisenatide肽树脂。
d1.3lixisenatide肽树脂的裂解和精肽制备
称取d1.2得到的lixisenatide肽树脂800克置于裂解反应器中,以12ml/g(裂解液/树脂)的裂解液用量入裂解试剂(tfa:phsme:phoh:edt:h2o=85:5:3:5:2,(v/v)),室温搅拌3h。反应物用砂芯漏斗过滤,收集滤液,树脂再用少量tfa洗涤2次,合并滤液后减压浓缩。加入冰冻的无水乙醚沉淀、离心,无水乙醚洗涤粗肽滤饼3次,真空干燥得到白色粉末固体,lixisenatide粗肽370.6g,质谱(图2)maldi-tof:(m+h)+=4859.288。粗肽重量收率为96.8%,hplc纯度为44.5%。
取d1.3中得到的lixisenatide粗肽49g进行精制,溶解后采用novaseprp-hplc系统,波长220nm,色谱柱为反相c18柱,常规0.1%tfa/水、乙腈流动相体系纯化后转盐,收集目的峰馏分,旋转蒸发浓缩,冻干得到lixisenatide精肽7.5g,hplc纯度98.6%,精肽收率15.4%。
实施例9
检测实施例1~8和对比例1制得的精肽。其中,对实施例1制得粗肽的质谱图如图1,对对比例1制得粗肽的质谱图如图2。其他各实施例制得产品的质谱图与此相似。各实施例获得多肽纯度和收率如表2:
表2多肽纯度和收率
结果显示,引入二肽片段的技术方案无论从粗肽纯度、精肽纯度还是精肽收率上都高于对比例方案。
以上仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!