含氟杂环化合物及其制备方法与流程
本发明涉及含氟杂环化合物的合成,具体涉及一种利用CO2由烯丙胺类化合物制备含三氟甲基的2-噁唑啉酮类化合物的制备方法。
背景技术:
众所周知,CO2的温室效应对全球环境造成了很多不利的影响,如何将CO2进行有效利用,是一个亟待解决的问题。通过化学转化实现其高效利用是一条非常有效的途径,而且这条途径还可以为解决资源问题提供可能。在有机合成中,CO2可以作为一种廉价易得,安全无毒,并且可重复利用的C1合成子,有着广阔的应用前景。但到目前为止,可以高效利用二氧化碳的化学手段十分有限,这与其热力学稳定性和动力学惰性是分不开的。
由于CO2的热力学稳定性和动力学惰性,实现其化学转化通常采用以下4种策略:(1)使用能量较高的原料,例如环氧化合物、氢气、炔烃、烯烃和胺类等物质,(2)将CO2通过化学转化生成低能量产物,如碳酸盐、氨基甲酸盐、芳香酸和酯等物质;(3)通过移除反应中的其他产物以促使反应平衡移动,使反应向生成目标产物的方向移动;(4)提供额外的能源如电能或光能活化CO2。在CO2的各种化学转化中,催化剂的使用一般都是必不可少的,至今已经发展了多种催化体系,主要有过渡金属类催化剂、氮杂环卡宾类催化剂、胺类催化剂和“受阻的路易斯酸碱对”类催化剂等。通过不同催化剂的使用,化学工作者相应地发展了多种CO2参与合成高附加值化学品的新途径,获得许多种类的化学品。尽管在CO2化学转化方面已开展了大量研究工作,但在温和条件下实现CO2的转化利用仍存在着诸多挑战。
另一方面,由于杂环化合物的独特性质,其在各类医药、农药及特种材料等方面有着不可替代的重要作用。在各种杂环化合物中,含氟杂环化合物由于具有广泛的生理活性和独特的物理化学性质,一直都是合成方法学研究尤其是有机氟化学研究的重要方向之一。含氟杂环化合物的性质独特,一般认为是由于氟原子的独特性质引起的。
2-噁唑啉酮作为一类重要的杂环化合物,在有机合成中是一种非常有用的中间体。因具有良好的抑菌活性,其广泛存在于各种抗菌药物中。而且,通过三氟甲基的引入,可以提升其生理活性,合成一系列含氟的噁唑啉酮类杂环化合物,为药物筛选提供基础。目前,各种引入三氟甲基的方法,尤其是C(sp3)—CF3键的构建已经得以报道。在复杂分子结构中实现关于烯烃的三氟甲基化的双官能团化如碳三氟甲基化、卤素三氟甲基化、氧三氟甲基化、氮三氟甲基化已经取得显著的进展。尽管已经报道过许多合成2-噁唑啉酮的方法,但目前还没有一种由廉价易得且便于处理的原料来合成含三氟甲基的2-噁唑啉酮的方法。
技术实现要素:
为了解决上述问题,发明人在广泛研究的基础上提出了一种利用二氧化碳由烯丙胺类化合物制备含三氟甲基的2-噁唑啉酮类化合物的方法。
根据本发明方法,如方案1所示,式1所示的烯丙胺类化合物与CO2在铜催化剂、碱和三氟甲基化试剂的存在下于溶剂中发生反应,制备得到如式2所示的含三氟甲基的2-噁唑啉酮类化合物。
方案1:
其中,R1、R2、R4和R5各自独立地为H,卤素,氰基,烷基、羰基、酯基、芳基和杂芳基等,进一步地R4或R5可任选地与R1成环,所述烷基、羰基、酯基、芳基和杂芳基可任选地被卤素、烷基等取代;R3为H、卤素、烷基、芳基等。
所述铜催化剂包括有机铜催化剂,例如乙酰丙酮酸铜或四乙氰铜六氟磷酸盐;以及无机铜催化剂,例如氯化亚铜或溴化亚铜。优选地,所述铜催化剂为氯化亚铜或溴化亚铜。
所述碱包括常用的弱碱和强碱,例如氟化铯、碳酸钠、碳酸铯、叔丁醇钠或1,8-二氮杂二环十一碳-7-烯(DBU)等。优选地,所述碱为 碳酸铯、叔丁醇钠或DBU。更优选地,所述碱为DBU。
所述三氟甲基化试剂为Tognis试剂和Umemoto试剂,例如一代或二代Tognis试剂。优选地,所述三氟甲基化试剂为二代Tognis试剂。
所述溶剂为任何可以溶解反应体系中所含物质的有机溶剂,包括强极性溶剂和弱极性溶剂,例如1,2-二氯乙烷、二氯甲烷、四氢呋喃、甲醇、N,N-二甲基甲酰胺、乙腈等。优选地,所述溶剂为N,N-二甲基甲酰胺或乙腈。
底物与催化剂的投料摩尔比为20:1~5:1,优选为10:1;底物与碱的投料摩尔比为1:1~1:3,优选为1:2;底物与三氟甲基化试剂的投料摩尔比为1:1~1:2,优选为1:1.1。
本发明方法反应条件温和,对反应温度、压力没有特别地要求。优选地,本发明方法在25摄氏度下和1atm反应压力下进行。
通过本发明方法构建含三氟甲基的2-噁唑啉酮化合物时,可以在氧化还原电中性的条件下就可以实现,而且反应条件温和,可以高效地实现氧三氟甲基化,构建包含螺环化合物在内的重要化合物。另外,该方法中二氧化碳的引入使得反应的化学选择性由氮三氟甲基化转变为氧三氟甲基化,反应同时具有非常好的化学选择性,区域选择性和非对映异构体选择性;因此能够从简单的原料合成含三氟甲基的2-噁唑啉酮,避免了有毒物质如一氧化碳、光气等的使用。也就是说,本发明方法不但能够简单高效地合成含三氟甲基的2-噁唑啉酮化合物,而且能够为温室气体的合理高效利用开辟了一条重要的途径,实现节能环保的目的。
附图说明
图1为本发明制备含三氟甲基的2-噁唑啉酮化合物的反应示意图;
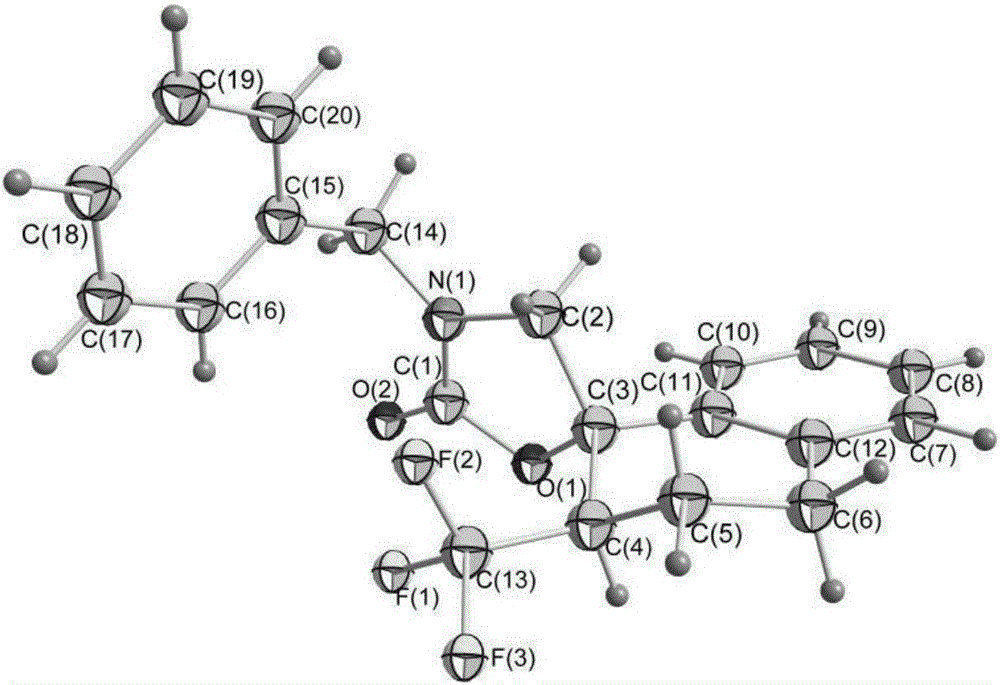
图2为化合物2ae的结构图。
具体实施方式
本发明提供一种利用二氧化碳由烯丙胺类化合物制备含三氟甲基的2-噁唑啉酮类化合物的方法。
根据本发明方法,如方案1所示,式1所示的烯丙胺类化合物与CO2在铜催化剂、碱和三氟甲基化试剂的存在下于溶剂中发生反应,制备得到如式2所示的含三氟甲基的2-噁唑啉酮类化合物。
方案1:
其中,R1、R2、R4和R5各自独立地为H,卤素,氰基,烷基、羰基、酯基、芳基和杂芳基等,进一步地R4或R5可任选地与R1成环,所述烷基、羰基、酯基、芳基和杂芳基可任选地被卤素、烷基等取代;R3为H、卤素、烷基、芳基等。
卤素包括氟、氯、溴、碘。所述烷基优选为具有1-20个碳原子的直链烷基、支链烷基、环烷基,例如甲基、乙基、异丙基、正丁基、异丁基等。所述芳基优选为具有6-20个碳原子的芳基,例如苯基、苄基、萘基等。所述杂芳基为具有6-20个碳原子的杂芳基,例如喹啉、异喹啉、吡啶、噻吩等。
所述铜催化剂包括有机铜催化剂,例如乙酰丙酮酸铜或四乙氰铜六氟磷酸盐;以及无机铜催化剂,例如氯化亚铜或溴化亚铜。优选地,所述铜催化剂为氯化亚铜或溴化亚铜。
所述碱包括常用的弱碱和强碱,例如氟化铯、碳酸钠、碳酸铯、叔丁醇钠或1,8-二氮杂二环十一碳-7-烯(DBU)等。优选地,所述碱为碳酸铯、叔丁醇钠或DBU。更优选地,所述碱为DBU。
所述三氟甲基化试剂为Togni’s试剂或Umemoto(Umemoto’s reagent)试剂,例如一代Togni’s试剂(Togni’s reagentⅠ)或二代Togni’s(Togni’s reagentⅡ)试剂。优选地,所述三氟甲基化试剂为二代Tognis试剂。
所述溶剂为任何可以溶解反应体系中所含物质的有机溶剂,包括强极性溶剂和弱极性溶剂,例如1,2-二氯乙烷、二氯甲烷、四氢呋喃、甲醇、N,N-二甲基甲酰胺、乙腈等。优选地,所述溶剂为N,N-二甲基 甲酰胺或乙腈。
底物与催化剂的投料摩尔比为20:1~5:1,优选为10:1;底物与碱的投料摩尔比为1:1~1:3,优选为1:2;底物与三氟甲基化试剂的投料摩尔比为1:1~1:2,优选为1:1.1。上述用量比是发明人在大量实验研究的基础上得到的,在保证合成产率的情况下,使物料的用量比尽可能得到优化控制。
本发明方法反应条件温和,对反应温度、压力没有特别地要求。优选地,本发明方法在25度下和1atm反应压力下进行。
在本发明方法优选的实施方案中,式1所示的化合物中R3为苄基,具体化合物可以包括以下化合物:
在底物中乙烯基芳环上存在取代基时,甲氧基或苯氧基取代的底物都是可以很好兼容的。对于萘环取代的烯丙胺衍生物,反应也可以顺利地进行,但是位阻较大的底物相对位阻小的底物,反应性能稍差一些,原料未能完全转化。另外,杂芳环的底物以较好的收率得到了目标产物,而没有监测到芳环三氟甲基化的产物,显示了反应的选择性。
对于其它取代类型的烯丙胺衍生物,例如氮的α位存在甲基的底物在最优条件下显示出很好的反应性。进一步地,环烯丙胺类衍生物也以较高收率得到了相应的螺环产物,而且经过后续的分析检测,发现产物具有非常高的非对映立体选择性。另外,丙烯酸酯类衍生物也可以高效地进行反应。
实施例
以下结合实施例对本发明作进一步的阐述。实施例仅用于说明本发明,而不能理解为对本发明的限制。
实验仪器和试剂:
核磁(1H NMR,13C NMR):Bruker Advance-400核磁共振仪 (0.5%TMS为内标)
气相-质谱联用仪(GC-MS):SHIMADZU GCMS-QP2010SE
电喷雾质谱(ESI-MS):Bruker Daltonics Micro TOF-Q
柱层析硅胶(200-300目):青岛海洋化工厂,未活化。
所用试剂和药品均为分析纯或化学纯,除特别注明外,未经进一步处理。无水试剂均来自实验室溶剂处理系统或购自百灵威、伊诺凯等试剂公司。其他原料试剂均购买自百灵威、伊诺凯、瑞欧克、科龙等试剂公司。
烯丙胺类化合物底物(以下简称底物)的合成:
1.底物1a的合成
在500mL带磁子的圆底烧瓶中依次加入18.7g N-溴代丁二酰亚胺(NBS),1.72g对甲苯磺酸,然后加入300mL THF,最后加入13mLα-甲基苯乙烯,剧烈搅拌下升温至回流状态(100℃),反应4h。TLC监控至原料基本消失后,旋干溶剂,湿法过柱(PE:EA=20:1),得15g A的粗品,黄色油状物。
取化合物A 7.5g溶于300mL乙腈中,然后搅拌条件下依次加入5.25g碳酸钾,12.4mL苄胺,加热升温至回流,反应12h。TLC监控至原料基本消失后,用乙酸乙酯萃取三次,合并有机相,加入Na2SO4干燥,过滤,旋蒸,干法上样过柱(PE:EA=1:1),分离提纯获得浅黄色油状液体7.0g。
1H NMR(400MHz,CDCl3)δ7.47–7.39(m,2H),7.37–7.19(m,8H),5.46–5.39(m,1H),5.26(d,J=1.3Hz,1H),3.80(s,2H),3.67(d,J=0.6Hz,2H).
2.底物1s的合成
在250mL带磁子的圆底烧瓶中加入21.97g甲基三苯基溴化膦和6.90g叔丁醇钾,用150mL超干THF溶解,在室温下搅拌约0.5h之后,缓慢滴加6.15g 3-甲氧基苯乙酮溶于30mL超干THF形成的溶液,室温下搅拌12h。TLC监控到原料基本消失后,加水淬灭,分液得到有机相与水相,水相再用乙酸乙酯萃取3次,合并有机相,有机相用饱和食盐水洗涤,分液,加入Na2SO4干燥,过滤,旋蒸,湿法上样过柱(PE:EA=20:1),分离提纯获得无色油状液体4.15g,收率68%。
在N2氛围下,将4.15g化合物B溶于68mL超干DCM和17mL超干THF的混合溶剂中,依次加入l26μL三甲基氯硅烷,5.99g N-溴代丁二酰亚胺和174mg三氟甲烷磺酸镱,室温下搅拌1h,整个过程在N2氛围下完成。TLC监控至原料基本消失后,旋干溶剂,干法拌样过柱(PE:EA=20:1),分离得粗品3.41g。
取化合物C 3.41g溶于60mL乙腈中,然后搅拌条件下依次加入2.07g碳酸钾,4.92mL苄胺,加热升温至回流,反应12h。TLC监控至原料基本消失后,用乙酸乙酯萃取三次,合并有机相,加入Na2SO4干燥,过滤,旋蒸,干法上样过柱(PE:EA=1:1),分离提纯获得浅黄色油状液体1.98g。
1H NMR(400MHz,CDCl3)δ7.35–7.28(m,4H),7.28–7.21(m,2H),7.05–6.97(m,2H),6.84(ddd,J=8.2,2.6,0.8Hz,1H),5.43(d,J=1.2Hz,1H),5.26(d,J=1.3Hz,1H),3.81(d,J=5.5Hz,5H),3.65(d,J=0.6Hz,2H).
3.底物1q的合成
操作步骤参考底物1z,分离纯化得产物528mg。
1H NMR(400MHz,CDCl3)δ7.43–7.38(m,2H),7.37–7.29(m,6H),7.27–7.22(m,1H),7.14–7.08(m,1H),7.05–6.94(m,4H),5.41–5.38(m,1H),5.23(d,J=1.3Hz,1H),3.81(s,2H),3.66(d,J=0.6Hz,2H).
4.底物1x的合成
操作步骤参考底物1b,分离提纯得最终产物3.4g。
5.底物1y的合成
操作步骤参考1b,分离提纯得最终产物5.4g。
1H NMR(400MHz,CDCl3)δ8.12–7.99(m,1H),7.83(dd,J=6.0,3.5Hz,1H),7.76(d,J=8.2Hz,1H),7.51–7.38(m,3H),7.36–7.15(m,6H),5.61(s,1H),5.25(s,1H),3.83(s,2H),3.65(d,J=0.4Hz,2H), 1.50(s,1H).
6.底物1z的合成
在250mL带磁子的干燥史莱克瓶依次加入10.40g 6-溴喹啉,449mg醋酸钯,1.65g 1,3-双(二苯基膦)丙烷(DPPP),然后在双排管上抽置换N2三次,接着在N2氛围下依次加入100mL DMF,17mL烯丙醇和11.12mL三乙胺,加完后封管,在125℃条件下反应30h。反应结束后,冷却至室温,点板监测反应情况,旋干拌样过柱(PE:EA=3:1),分离纯化得棕红色固体2.12g。
取2g化合物D溶于18mL超干DCM中,搅拌条件下加入1.80mL三乙胺,然后在0℃下分批加入2.47g对甲苯磺酰氯,加完后室温下搅拌2h。点板检测原料消失后,用15mL水淬灭反应,用DCM萃取三次,合并有机相,加入Na2SO4干燥,过滤,旋蒸,干法上样过柱(PE:EA=30:1),分离提纯获得浅黄色油状液体1.01g。
将1g化合物E和408mg碳酸钾加入到20mL乙腈中,搅拌下加入966μL苄胺,搅拌回流反应12h。点板检测原料消失后,用乙酸乙酯萃取三次,合并有机相,加入Na2SO4干燥,过滤,旋蒸,干法上样过柱(PE:EA=1:1),分离提纯获得产物516mg(浅黄色油状液体)。
1H NMR(400MHz,CDCl3)δ8.86(dd,J=4.2,1.7Hz,1H),8.13–7.99(m,2H),7.87–7.76(m,2H),7.38–7.28(m,5H),7.25(td,J=4.8,2.6Hz,1H),5.59(s,1H),5.40(d,J=1.0Hz,1H),3.83(s,2H),3.76(s,2H).
7.底物1aa的合成
称取3.79g化合物F溶于250mL THF中,在0℃下依次加入7.38g三苯基膦,4.14g邻苯二甲酰亚胺,5.70mL偶氮二甲酸二乙酯(DEAD),然后在室温下搅拌20h。TLC监测到原料基本消失后,旋干溶剂,加入乙醚和石油醚的1:1混合溶剂500mL使三苯基氧化膦沉淀下来,垫硅藻土抽滤,收集滤液,旋干拌样过柱(PE:EA=30:1),分离纯化得白色固体3.60g。
取3.60g化合物G溶于100mL无水乙醇中,然后向体系中滴加4.74mL水合肼(80%),滴加完后,搅拌回流反应3h。点板监测反应至原料消失后,体系中产生沉淀,垫硅藻土抽滤,滤饼用乙醚冲涤3次,收集滤液,旋干拌样过柱(PE:EA=10:1,DCM:MeOH=30:1),分离纯化得白色固体H 1.36g。
在50mL茄型瓶中加入469mg苯甲醛,用15mL乙醇溶解,然后在搅拌条件下加入500mg化合物H,升温回流反应4h。点板监测至原料基本消失后,冷却至0℃,分批加入386mg硼氢化钠,加完后室温下搅拌反应4h。点板监测反应完全后,搅拌条件下缓慢加入饱和NaHCO3溶液至体系澄清,用乙酸乙酯萃取3次,合并有机相,加入Na2SO4干燥,过滤,旋蒸,干法上样过柱(PE:EA=10:1),分离提纯获得浅黄色油状液体367mg。
1H NMR(400MHz,CDCl3)δ7.32–7.14(m,10H),5.23(dd,J=4.2,1.1Hz,2H),3.79(d,J=13.0Hz,1H),3.70–3.62(m,2H),1.15(d,J=6.6Hz,3H).
8.底物1ae的合成
操作步骤参考底物1b的合成过程,分离提纯得最终产物4.4g。
1H NMR(400MHz,CDCl3)δ7.37–7.30(m,4H),7.26(dd,J=7.4,2.3Hz,2H),7.21–7.12(m,3H),6.04(t,J=4.4Hz,1H),3.85(s,2H),3.63(s,2H),2.76(t,J=8.0Hz,2H),2.29(dd,J=12.4,8.0Hz,2H),1.63(s,1H).
9.底物1af的合成
操作步骤参考底物1f的合成过程,分离提纯得最终产物2.4g。
1H NMR(400MHz,CDCl3)δ7.33(d,J=4.5Hz,5H),6.19–6.18(m,1H),5.67(dd,J=2.9,1.5Hz,1H),3.78(s,2H),3.45(s,2H),1.76(s,1H),1.50(s,9H).
实施例1 3-苄基-5-苯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(3-benzyl-5-phenyl-5-(2,2,2-trifluoroethyl)oxazolidin-2-one)(以下称为化合物2a)的制备
表1:反应条件的优化选择
[a]:表中所列收率为用正十二烷作内标的GC收率,括号里的为分离收率;[b]:碱的用量0.6mmol;[c]:25摄氏度;[d]:使用一代Togni试剂;[e]:使用Umemoto试剂;N.D.=未检出;[f]:80摄氏度;[g]0.1atm;[h]20atm.
按照表1所示的条件以1a为底物制备化合物2a,具体操作如下:在25mL带磁子的Schlenk管中依次加入0.04mmol催化剂、0.44mmol二代Tognis试剂(139mg),以上操作在手套箱里完成,然后将反应管拿出手套箱,用CO2气体抽置换三次,接着在CO2氛围下用注射器依次加入0.40mmol烯丙胺衍生物1a、4mL溶剂、0.80mmol碱。然后,在一个大气压的CO2氛围下拧紧反应管,室温下搅拌反应16h。反应完后,旋干反应液,干法上样过柱(PE:EA 10:1~5:1),分离提纯获得目标产物。
Rf(pentane/EtOAc 5:1):0.35
1H NMR(400MHz,CDCl3)δ7.42–7.27(m,8H),7.19(dd,J=7.3,1.8Hz,2H),4.43(dd,J=47.4,14.9Hz,2H),3.68(dd,J=62.1,9.2Hz,2H),2.89–2.70(m,2H);13C NMR(101MHz,CDCl3)δ156.40,140.89, 135.06,128.93,128.91,128.67,128.17,128.08,124.46(q J=278.6Hz),124.29,78.11(q,J=2.2Hz),55.13,48.26.44.35(q,J=27.7Hz);19F NMR(376MHz,CDCl3)δ-60.54;HRMS(ESI+):calcd for C18H17F3NO2+[M+H]+336.1206,found 336.1212。
实施例2至实施例32 2-噁唑啉酮类化合物2aa、2ab、2ac、2ad、2ae、2af、2b-2z的制备
说明:2-噁唑啉酮类化合物2aa表示该化合物由底物1aa制备而得,其它2-噁唑啉酮类化合物的命名规则同此。
按照表2和表3所示的条件制备2-噁唑啉酮类化合物2aa、2ab、2ac、2ad、2ae、2af、2b-2z,具体操作如下:在25mL带磁子的Schlenk管中依次加入0.04mmol四乙氰铜六氟磷酸盐(14.9mg),0.44mmol二代Tognis试剂(139mg),0.40mmol烯丙胺衍生物(如果底物为固体的话),以上操作在手套箱里完成,然后将反应管拿出手套箱,用CO2气体抽置换三次,接着在CO2氛围下用注射器依次加入0.40mmol烯丙胺衍生物(如果底物为液体的话)、4mL无水乙腈、0.80mmol(120μL)1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)。然后,在一个大气压的CO2氛围下拧紧反应管,室温下(25℃)搅拌反应16h。反应完后,旋干反应液,干法上样过柱(PE:EA 10:1~5:1),分离提纯获得目标产物。
表2
表2中,“1a,81%”表示以底物1a,按表中反应式进行反应时,所得产物的产率为81%;表中类似标注含义同此。“1d,R=Ph,trace”表示底物的命名为1d,其R取代基为Ph,按表中反应式进行反应时,得到痕量产物。“1e,R=Ts,N.D”表示底物的命名为1e,其R取代基为Ts,按表中反应式进行反应时,未检测到产物生产;表中类似标注含义同此。
表3
[b]:反应时间30h;[c]:未检出非对映异构体;[d]:d.r.>16:1。
3-丁基-5-苯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2b)
表3中,“2i:F,79%”意为当R取代基为F时,产率为79%,
其余类似标注同此理解。
3-butyl-5-phenyl-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
98mg,产率82%,无色油状物;Rf(pentane/EtOAc 3:1):0.3;
1H NMR(400MHz,CDCl3)δ7.48–7.32(m,5H),3.85(dd,J=88.8,9.1Hz,2H),3.36–3.17(m,2H),2.86(q,J=10.2Hz, 2H),1.55–1.45(m,2H),1.35–1.21(m,2H),0.90(t,J=7.3Hz,3H);13C NMR(101MHz,CDCl3)δ156.31,141.24,128.88,128.58,124.59(q,J=278.4Hz),124.23,77.78(q,J=2.2Hz),55.74(d,J=1.4Hz),44.33(q,J=27.6Hz),43.79,29.18,19.71,13.61;19F NMR(376MHz,CDCl3)δ-60.58;HRMS(ESI+):calcd for C15H19F3NO2+[M+H]+302.1362,found 302.1371。
3-(1-苯乙基)-5-苯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2c)
5-phenyl-3-(1-phenylethyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
45mg,产率32%yield,白色固体;Rf(pentane/EtOAc 5:1):0.4;
1H NMR(400MHz,CDCl3)δ7.48–7.28(m,10H),5.23(q,J=7.1Hz,1H),3.55(dd,J=79.4,9.1Hz,2H),2.84–2.57(m,2H),1.47(d,J=7.1Hz,3H);13C NMR(101MHz,CDCl3)δ155.80,140.94,138.92,128.91,128.86,128.62,128.19,127.10,124.35(q,J=278.5Hz),124.28,78.11(q,J=2.0Hz),51.73(d,J=1.2Hz),51.64,44.20(q,J=27.7Hz),15.99;19F NMR(376MHz,CDCl3)δ-60.45;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1357。
3-(1-苯乙基)-5-苯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2c′)
5-phenyl-3-(1-phenylethyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
40mg,产率29%,白色固体;Rf(pentane/EtOAc 5:1):0.35;
1H NMR(400MHz,CDCl3)δ7.41–7.22(m,8H),7.21– 7.13(m,2H),5.25(q,J=7.1Hz,1H),3.62(dd,J=204.0,9.1Hz,2H),2.94–2.74(m,2H),1.64(d,J=7.1Hz,3H);13C NMR(101MHz,CDCl3)δ155.86,140.86,138.83,128.83,128.70,128.60,127.89,126.82,124.55(d,J=278.3Hz),124.29,78.22(q,J=2.1Hz),51.41,51.04(d,J=1.6Hz),44.33(q,J=27.7Hz),16.34;19F NMR(376MHz,CDCl3)δ-60.52;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1361。
3-苄基-5-(4-氟苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2i)
3-benzyl-5-(4-fluorophenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
112mg,产率79%,白色固体;Rf(pentane/EtOAc 3:1):0.40;
1H NMR(400MHz,CDCl3)δ7.40–7.26(m,5H),7.24–7.15(m,2H),7.11–7.01(m,2H),4.43(q,J=15.0Hz,2H),3.67(dd,J=68.6,9.2Hz,2H),2.80(q,J=10.1Hz,2H);13C NMR(101MHz,CDCl3)δ162.59(d,J=248.1Hz),156.24,136.58(d,J=3.2Hz),135.00,128.96,128.22,128.03,126.37(d,J=8.4Hz),124.41(q,J=278.4Hz),115.85(d,J=21.8Hz),77.84(q,J=2.1Hz),55.33,48.21,44.29(q,J=27.7Hz);19F NMR(376MHz,CDCl3)δ-60.48,-112.95;HRMS(ESI+):calcd for C18H16F4NO2+[M+H]+354.1112,found 354.1100。
3-苄基-5-(4-氯苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2j)
3-benzyl-5-(4-chlorophenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
125mg,产率84%,无色油状物;Rf(pentane/EtOAc 4:1):0.35;
1H NMR(400MHz,CDCl3)δ7.38–7.27(m,7H),7.22–7.15(m,2H),4.42(dd,J=34.4,15.0Hz,2H),3.65(dd,J=72.5,9.2Hz,2H),2.79(q,J=10.0Hz,2H);13C NMR(101MHz,CDCl3)δ156.14,139.27,134.93,134.67,129.09,128.98,128.26,128.04,125.91,124.35(q,J=278.4Hz),77.75(q,J=2.2Hz),55.24(d,J=1.4Hz),48.24,44.17(q,J=27.8Hz);19F NMR(376MHz,CDCl3)δ-60.41;HRMS(ESI+):calcd for C18H15ClF3NNaO2+[M+Na]+392.0636,found 392.0627。
3-苄基-5-(4-溴苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2k)
3-benzyl-5-(4-bromophenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
126mg,产率76%,黄色油状物;Rf(pentane/EtOAc 4:1):0.35;
1H NMR(400MHz,CDCl3)δ7.54–7.48(m,2H),7.35–7.27(m,3H),7.27–7.15(m,4H),4.42(q,J=36.7,14.9Hz,2H),3.65(dd,J=73.2,9.2Hz,2H),2.79(q,J=10.0Hz,2H);13C NMR(101MHz,CDCl3)δ156.13,139.80,134.90,132.06,129.00,128.28,128.06,126.20,124.33(q,J=278.4Hz),122.82,77.79(q,J=2.2Hz),55.19(d,J=1.3Hz),48.24,44.12(q,J=27.8Hz);19F NMR(376MHz,CDCl3)δ-60.39;HRMS(ESI+):calcd for C18H15BrF3NNaO2+[M+Na]+436.0130,found 436.0122。
3-苄基-5-(4-甲基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2l)
3-benzyl-5-(p-tolyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
105mg,产率75%,白色固体;Rf(pentane/EtOAc 3:1):0.44;
1H NMR(400MHz,CDCl3)δ7.34–7.26(m,3H),7.26–7.14(m,6H),4.42(dd,J=46.4,15.0Hz,2H),3.66(dd,J=61.0,9.1Hz,2H),2.77(q,J=10.4Hz,2H),2.34(s,3H);13C NMR(101MHz,CDCl3)δ156.50,138.54,137.96,135.14,129.53,128.92,128.14,128.09,124.53(q,J=278.5Hz),124.22,78.15(q,J=2.1Hz),55.19,48.25,44.33(q,J=27.5Hz),21.07;19F NMR(376MHz,CDCl3)δ-60.49;HRMS(ESI+):calcd for C19H18F3NNaO2+[M+Na]+372.1182,found 372.1172。
3-苄基-5-(4-三氟甲基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2m)
3-benzyl-5-(2,2,2-trifluoroethyl)-5-(4-(trifluoromethyl)phenyl)oxazolidin-2-one
125mg,产率77%,白色固体;Rf(pentane/EtOAc 5:1):0.25;
1H NMR(400MHz,CDCl3)δ7.65(d,J=8.3Hz,2H),7.51(d,J=8.2Hz,2H),7.36–7.25(m,3H),7.24–7.15(m,2H),4.43(dd,J=35.7,14.9Hz,2H),3.69(dd,J=84.4,9.3Hz,2H),2.85(q,J=10.0Hz,2H);13C NMR(101MHz,CDCl3)δ156.03,144.68,134.83,130.92(q,J=32.8Hz),128.98,128.29,128.03,125.93(q,J=3.7Hz),124.99,124.31(q,J=278.4Hz),123.76(q,J=272.3Hz),77.77(q,J=2.1Hz),55.30,48.23,44.03(q,J=28.0Hz);19F NMR(376MHz,CDCl3)δ-60.44,-62.76;HRMS(ESI+):calcd for C19H15F6NNaO2+[M+Na]+426.0899,found 426.0893。
3-苄基-5-(4-硝基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2n)
3-benzyl-5-(4-nitrophenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
130mg,产率85%,浅黄色固体;Rf(pentane/EtOAc 3:1):0.10;
1H NMR(400MHz,CDCl3)δ8.25(d,J=8.9Hz,2H),7.59(d,J=8.9Hz,2H),7.38–7.28(m,3H),7.24–7.16(m,2H),4.45(dd,J=40.2,14.9Hz,2H),3.71(dd,J=82.3,9.3Hz,2H),2.88(q,J=9.8Hz,2H);13C NMR(101MHz,CDCl3)δ155.75,147.92,147.40,134.66,129.06,128.41,128.09,125.79,124.16,124.15(q,J=278.5Hz),77.61(q,J=2.2Hz),55.32(d,J=0.9Hz),48.30,44.08(q,J=28.2Hz);19F NMR(376MHz,CDCl3)δ-60.31;HRMS(ESI+):calcd for C18H15F3N2NaO4+[M+Na]+403.0876,found 403.0860。
3-苄基-5-(4-苯甲酸叔丁酯基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2o)
tert-butyl-4-(3-benzyl-2-oxo-5-(2,2,2-trifluoroethyl)oxazolidin-5-yl)benzoate
122mg,产率70%,白色泡沫状固体;Rf(pentane/EtOAc 3:1):0.27;
1H NMR(400MHz,CDCl3)δ8.01(d,J=8.5Hz,2H),7.43(d,J=8.6Hz,2H),7.35–7.27(m,3H),7.24–7.11(m,2H),4.44 (dd,J=41.3,14.9Hz,2H),3.68(dd,J=73.8,9.2Hz,2H),2.83(q,J=10.0Hz,2H),1.60(s,9H);13C NMR(101MHz,CDCl3)δ164.95,156.13,144.90,134.89,132.40,130.00,128.97,128.24,128.04,124.32(q,J=278.4Hz),124.31,81.51,77.94(q,J=2.2Hz),55.27,48.27,44.16(q,J=27.9Hz),28.14;19F NMR(376MHz,CDCl3)δ-60.41;HRMS(ESI+):calcd for C23H25F3NO4+[M+H]+436.1730,found 436.1735。
3-苄基-5-(4-三氟甲氧基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2p)
3-benzyl-5-(2,2,2-trifluoroethyl)-5-(4-(trifluoromethoxy)phenyl)oxazolidin-2-one
139mg,产率83%,白色固体;Rf(pentane/EtOAc 3:1):0.3;
1H NMR(400MHz,CDCl3)δ7.41(d,J=8.8Hz,2H),7.35–7.28(m,3H),7.27–7.16(m,4H),4.44(dd,J=33.2,14.9Hz,2H),3.68(dd,J=74.9,9.2Hz,2H),2.81(q,J=10.0Hz,2H);13C NMR(101MHz,CDCl3)δ156.09,149.23(d,J=1.7Hz),139.38,134.88,128.96,128.27,128.04,126.14,120.37(q,J=257.8Hz),121.29,120.37(q,J=257.8Hz),77.71(q,J=2.1Hz),55.19(d,J=1.1Hz),48.22,44.21(q,J=27.9Hz);19F NMR(376MHz,CDCl3)δ-57.92,-60.52;HRMS(ESI+):calcd for C19H15F6NNaO3+[M+Na]+442.0848,found 442.0832。
3-苄基-5-(4-苯氧基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2q)
3-benzyl-5-(4-phenoxyphenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
134mg,产率78%,白色固体;Rf(pentane/EtOAc 3:1):0.3;
1H NMR(400MHz,CDCl3)δ7.40–7.26(m,7H),7.21(dd,J=8.7,6.8Hz,2H),7.13(t,J=7.4Hz,1H),7.07–6.92(m,4H),4.43(dd,J=35.4,14.9Hz,2H),3.67(dd,J=54.3,9.2Hz,2H),2.97–2.66(m,2H);13C NMR(101MHz,CDCl3)δ157.72,156.49,156.34,135.20,135.09,129.94,128.94,128.20,128.11,125.99,124.45(q,J=278.4Hz),123.90,119.32,118.68,77.99(q,J=2.2Hz),55.11,48.28,44.41(q,J=27.6Hz);19F NMR(376MHz,CDCl3)δ-60.48.HRMS(ESI+):calcd for C24H21F3NO2+[M+H]+428.1468,found 428.1475。
3-苄基-5-(3-甲基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2r)
3-benzyl-5-(m-tolyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
126mg,产率90%,浅黄色固体;Rf(pentane/EtOAc 3:1):0.25;
1H NMR(400MHz,CDCl3)δ7.21–7.06(m,7H),7.05–6.98(m,2H),4.30(dd,J=50.6,15.0Hz,2H),3.56(dd,J=69.3,9.2Hz,2H),2.67(q,J=10.2Hz,2H),2.22(s,3H);13C NMR(101MHz,CDCl3)δ156.53,141.03,138.75,135.15,129.37,128.93,128.81,128.16,128.11,124.87,124.61(q,J=278.8Hz),121.29,78.16(q,J=2.1Hz),55.25,48.20,44.21(q,J=27.6Hz),21.51; 19F NMR(376MHz,CDCl3)δ-60.45;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1367。
3-苄基-5-(3-甲氧基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2s)
3-benzyl-5-(3-methoxyphenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
112mg,产率77%,白色固体;Rf(pentane/EtOAc 3:1):0.28;
1H NMR(400MHz,CDCl3)δ7.26–7.14(m,4H),7.13–7.03(m,2H),6.85(t,J=2.0Hz,1H),6.77(d,J=8.5Hz,2H),4.33(dd,J=49.5,14.9Hz,2H),3.69(s,3H),3.58(dd,J=62.1,9.2Hz,2H),2.69(m,2H);13C NMR(101MHz,CDCl3)δ159.96,156.36,142.66,135.07,130.07,128.92,128.16,128.09,124.50(q,J=278.5Hz),116.35,113.93,110.23,78.00(q,J=4.2,2.0Hz),55.37,55.16,48.25,44.25(q,J=27.7Hz);19F NMR(376MHz,CDCl3)δ-60.53;HRMS(ESI+):calcd for C19H19F3NO3+[M+H]+366.1312,found 366.1309。
3-苄基-5-(3-(2,2,2-三甲基乙酰氨基)苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2t)
N-(3-(3-benzyl-2-oxo-5-(2,2,2-trifluoroethyl)oxazolidin-5-yl)phenyl)pivalamide
142mg,产率82%,白色泡沫状固体;Rf(pentane/EtOAc 3:1):0.15;
1H NMR(400MHz,CDCl3)δ7.63(t,J=1.9Hz,1H),7.53(dd,J=8.1,1.3Hz,1H),7.48(s,1H),7.38–7.27(m,4H),7.20(dd,J=7.4,1.8Hz,1H),7.10(d,J=7.9Hz,1H),4.42(dd,J=90.1,14.9Hz,2H),3.67(dd,J=56.6,9.2Hz,2H),2.77(q,J=10.0Hz,2H),1.32(s,9H);13C NMR(101MHz,CDCl3)δ177.35,156.42,141.91,139.03,134.91,129.42,128.92,124.46(q,J=278.5Hz), 128.18,128.04,120.12,119.51,115.78,78.07(q,J=2.1Hz),55.25,48.19,44.07(q,J=27.7Hz),39.71,27.49;19F NMR(376MHz,CDCl3)δ-60.52;HRMS(ESI+):calcd for C23H26F3N2O3+[M+H]+435.1890,found 435.1869。
3-苄基-5-(3-(2,2,2-三甲基乙酸)苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2u)
3-(3-benzyl-2-oxo-5-(2,2,2-trifluoroethyl)oxazolidin-5-yl)phenylpivalate
136mg,产率78%,白色固体;Rf(pentane/EtOAc 3:1):0.20;
1H NMR(400MHz,CDCl3)δ7.41(t,J=8.0Hz,1H),7.37–7.28(m,3H),7.27–7.12(m,4H),7.08(d,J=8.0Hz,1H),4.45(dd,J=75.5,14.9Hz,2H),3.69(dd,J=64.6,9.2Hz,2H),2.88–2.71(m,2H),1.37(s,9H);13C NMR(101MHz,CDCl3)δ176.87,156.17,151.49,142.68,134.94,129.96,128.96,128.21,128.09,124.39(q,J=278.5Hz),121.98,121.37,117.88,77.69(d,J=2.1Hz),55.04(d,J=0.9Hz),48.27,44.26(q,J=27.8Hz),39.11,27.11;19F NMR(376MHz,CDCl3)δ-60.52;HRMS(ESI+):calcdfor C23H25F3NO4+[M+H]+436.1730,found 436.1730。
3-苄基-5-(2-甲基苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2v)
3-benzyl-5-(o-tolyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
104mg,产率74%,白色固体;Rf(pentane/EtOAc 3:1):0.45;
1H NMR(400MHz,CDCl3)δ7.68–7.53(m,1H),7.43–7.07(m,9H),4.44(dd,J=82.2,15.0Hz,2H),3.75(dd,J=107.3,9.1Hz,2H),2.81(q,J=10.2Hz,2H),2.26(s,3H).13C NMR(101MHz,CDCl3)δ156.00,139.07,135.09,132.55,132.33,128.94,128.74,128.17,128.09,126.52,125.23,124.66(q,J=278.6Hz),78.56(q,J=2.1Hz),54.64,48.25,42.88(q,J=27.6Hz),20.79; 19F NMR(376MHz,CDCl3)δ-61.09;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1347。
3-苄基-5-(2-氯苯基)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2w)
3-benzyl-5-(2-chlorophenyl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
110mg,产率74%,白色固体;Rf(pentane/EtOAc 3:1):0.40;
1H NMR(400MHz,CDCl3)δ7.83(dd,J=7.6,1.8Hz,1H),7.41–7.27(m,6H),7.26–7.20(m,2H),4.44(dd,J=101.4,15.0Hz,2H),3.81(dd,J=88.2,9.8Hz,2H),3.14–2.87(m,2H); 13C NMR(101MHz,CDCl3)δ155.65,138.15,135.04,130.87,130.22,129.53,128.96,128.19,128.08,127.61,127.39,124.62(q,J=278.6Hz),77.71(q,J=2.1Hz),54.81(d,J=0.7Hz),48.20,41.75(q,J=27.9Hz);19F NMR(376MHz,CDCl3)δ-61.02;HRMS(ESI+):calcd for C18H15ClF3NNaO2+[M+Na]+392.0636,found 392.0619。
3-苄基-5-(2-萘)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2x)
3-benzyl-5-(naphthalen-2-yl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
116mg,产率75%,白色固体;Rf(pentane/EtOAc 4:1):0.35;
1H NMR(400MHz,CDCl3)δ7.92(d,J=1.6Hz,1H),7.87–7.78(m,3H),7.49(dd,J=6.3,3.2Hz,2H),7.34–7.16(m,6H),4.42(dd,J=55.9,15.0Hz,2H),3.74(dd,J=54.0,9.2Hz,2H),2.87(q,J=10.1Hz,2H);13C NMR(101MHz,CDCl3)δ156.50,137.98,135.07,132.99,132.90,129.11,128.96,128.41,128.20,128.10,127.71,126.95,126.95,124.57(q,J=278.6Hz),78.28(q,J=2Hz),55.19,48.29,44.17(q,J=27.7Hz);19F NMR(376MHz,CDCl3)δ-60.39;HRMS(ESI+):calcd for C22H19F3NO2+[M+H]+386.1362,found 386.1350。
3-苄基-5-(1-萘)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2y)
3-benzyl-5-(naphthalen-1-yl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
101mg,产率65%,白色固体;Rf(pentane/EtOAc 3:1):0.30;
1H NMR(400MHz,CDCl3)δ7.92(t,J=6.3Hz,2H),7.86(d,J=8.2Hz,1H),7.56–7.45(m,4H),7.36–7.20(m,5H),4.44(dd,J=144.2,15.1Hz,2H),4.02(dd,J=147.3,9.2Hz,2H),3.22–2.89(m,2H);13C NMR(101MHz,CDCl3)δ155.82,136.73,135.07,134.58,130.20,129.98,128.93,128.16,128.07,127.89,126.96,125.77,125.40,124.87(q,J=278.7Hz),123.43,122.70,78.46(d,J=1.9Hz),54.47(d,J=0.9Hz),48.29,43.59(q,J=27.6 Hz);19F NMR(376MHz,CDCl3)δ-60.87;HRMS(ESI+):calcd for C22H19F3NO2+[M+H]+386.1362,found 386.1370。
3-苄基-5-(6-喹啉)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2z)
3-benzyl-5-(quinolin-6-yl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
90mg,产率58%,浅黄色固体;Rf(pentane/EtOAc 1:3):0.4;
1H NMR(400MHz,CDCl3)δ8.98(d,J=2.9Hz,1H),8.20(d,J=8.0Hz,1H),8.15(d,J=8.9Hz,1H),7.99(d,J=1.8Hz,1H),7.54(dd,J=8.9,2.0Hz,1H),7.48(dd,J=8.3,4.2Hz,1H),7.35–7.29(m,3H),7.24–7.15(m,2H),4.47(dd,J=52.0,14.9Hz,2H),3.78(dd,J=56.5,9.2Hz,2H),2.93(q,J=10.0Hz,2H);13C NMR(101MHz,CDCl3)δ156.20,151.42,147.85,138.57,136.54,134.88,130.63,128.96,128.24,128.06,127.82,125.30,124.36(q,J=278.5Hz),123.82,122.07,77.99(q,J=2.1Hz),55.14(d,J=1.4Hz),48.32,44.17(q,J=27.9Hz);19F NMR(376MHz,CDCl3)δ-60.45;HRMS(ESI+):calcd for C21H17F3N2NaO2+[M+Na]+409.1134,found 409.1141。
3-苄基-4-甲基-5-苯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2aa)
3-benzyl-4-methyl-5-phenyl-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
110mg,产率78%,白色固体;Rf(pentane/EtOAc 3:1):0.20;
1H NMR(400MHz,CDCl3)δ7.42–7.30(m,5H),7.23–7.13(m,3H),7.03–6.93(m,2H),4.41(dd,J=287.7,15.5Hz,2H),3.63(q,J=6.6Hz,1H),2.95–2.71(m,2H),1.29(d,J=6.6Hz,3H);13C NMR(101MHz,CDCl3)δ156.37,140.29,135.29,128.74,128.74,128.45,127.85,127.54,124.92(q,J=278.5Hz),124.33,81.12(dd,J=3.9,1.8Hz),61.66,45.71,38.95(q,J=28.2Hz),13.29;19F NMR(376MHz,CDCl3)δ-59.01;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1371。
3-苄基-5-苯基-5-(1-三氟甲基乙基)-2-噁唑啉酮(2ab)
3-benzyl-5-phenyl-5-(1,1,1-trifluoropropan-2-yl)oxazolidin-2-one
99mg,产率71%yield,浅黄色固体(外消旋混合物Z:E=1.14:1);105mg,产率75%,白色固体(起始物为Z构型);
Rf(pentane/EtOAc 5:1):0.30;
1H NMR(400MHz,CDCl3)δ7.43–7.32(m,5H),7.31–7.24(m,3H),7.20–7.12(m,2H),4.41(q,J=14.9Hz,2H),3.94(d,J=9.4Hz,1H),3.58(d,J=9.3Hz,1H),2.76(qd,J=8.5,1.2Hz,1H),1.08(d,J=7.1Hz,3H);13C NMR(101MHz,CDCl3)δ156.44,141.46,135.07,128.82,128.81,128.51,128.07,126.59(q,J=281.6Hz),124.69,80.95,53.70(q,J=2.4Hz),48.24,46.63(q,J=24.9Hz),9.77(q,J=2.9Hz);19F NMR(376MHz,CDCl3)δ-65.66;HRMS(ESI+):calcd for C19H19F3NO2+[M+H]+350.1362,found 350.1368。
3-苄基-5-苯基-5-(1,1,1-三氟-2-甲基丙基)-2-噁唑啉酮(2ac)
3-benzyl-5-phenyl-5-(1,1,1-trifluoro-2-methylpropan-2-yl)oxazolidin-2-one
50mg,产率34%,白色固体;Rf(pentane/EtOAc 3:1):0.50;
1H NMR(400MHz,CDCl3)δ7.47–7.39(m,2H),7.38–7.31(m,3H),7.30–7.23(m,3H),7.14–7.06(m,2H),4.39(dd,J=55.7,15.1Hz,2H),3.84(dd,J=111.4,9.6Hz,2H),1.20(d,J=22.1Hz,6H);13C NMR(101MHz,CDCl3)δ156.36,139.67,135.09,128.83,128.59,128.03,127.84,127.83,127.81(q,J=284.5Hz),126.99,83.52,52.88(q,J=2.9Hz),48.10,47.89(q,J=22.8Hz),18.25(q,J=2.3Hz),17.99(q,J=2.3Hz);19F NMR(376MHz,CDCl3)δ-70.02;HRMS(ESI+):calcd for C20H20F3NNaO2+[M+Na]+386.1338,found 386.1324。
3-苄基-6-三氟甲基-1-氧杂-3-氮杂螺[4.5]癸-2-酮(2ad)
3-benzyl-6-(trifluoromethyl)-1-oxa-3-azaspiro[4.5]decan-2-one
70mg,产率56%,白色固体;Rf(pentane/EtOAc 5:1):0.40;
1H NMR(400MHz,CDCl3)δ7.42–7.21(m,5H),4.44(q,J=14.9Hz,2H),3.32(dd,J=187.3,9.3Hz,2H),2.54–2.38(m,1H),2.08–1.97(m,1H),1.92–1.66(m,4H),1.42–1.16(m,3H); 13C NMR(101MHz,CDCl3)δ156.62,135.40,128.83,128.15,128.03,126.33(q,J=281.6Hz),77.85(d,J=0.5Hz),49.47(d,J=1.7Hz),48.33,47.67(q,J=24.6Hz),38.36,23.10,23.07,21.94; 19F NMR(376MHz,CDCl3)δ-65.67;HRMS(ESI+):calcd for C16H18F3NNaO2+[M+Na]+336.1182,found 336.1169。
3'-苄基-2-三氟甲基-3,4-二氢-2H-螺[萘-1,5'-噁唑啉]-2'-酮(2ae)
3'-benzyl-2-(trifluoromethyl)-3,4-dihydro-2H-spiro[naphthalene-1,
5'-oxazolidin]-2'-one
113mg,产率78%,白色固体;Rf(pentane/EtOAc 3:1):0.40;
1H NMR(400MHz,CDCl3)δ7.33–7.09(m,8H),7.03–6.94(m,1H),4.40(dd,J=38.2,14.8Hz,2H),3.75(d,J=9.8Hz,1H),3.22(d,J=9.8Hz,1H),2.94–2.59(m,3H),2.26–2.02(m,1H),1.78–1.54(m,1H);13C NMR(101MHz,CDCl3)δ157.05,138.61,135.20,134.63,128.85,128.74,128.64,128.34,128.16,127.51,126.50(q,J=281.1Hz),125.27,77.73,53.40(d,J=1.9Hz),48.41,46.36(q,J=25.4Hz),27.61,20.10(d,J=2.4Hz);19F NMR(376MHz,CDCl3)δ-66.39;HRMS(ESI+):calcd for C20H19F3NO2+[M+H]+362.1362,found 362.1358。
3-苄基-5-甲酸叔丁酯基-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2af)
tert-butyl-3-benzyl-2-oxo-5-(2,2,2-trifluoroethyl)oxazolidine-5-carboxylate
99mg,产率69%,白色固体;Rf(pentane/EtOAc 3:1):0.4;
1H NMR(400MHz,CDCl3)δ7.39–7.29(m,3H),7.26(d,J=7.5Hz,2H),4.44(dd,J=82.8,15.0Hz,2H),3.53(dd,J=96.5,9.6Hz,2H),2.96–2.69(m,2H),1.45(s,9H);13C NMR(101MHz, CDCl3)δ167.38,155.82,134.97,128.96,128.24,128.00,124.33(q,J=278.0Hz),84.56,75.89(q,J=2.3Hz),51.56,48.06,39.92(q,J=29.3Hz),27.55;19F NMR(376MHz,CDCl3)δ-60.94;HRMS(ESI+):calcd for C17H20F3NNaO4+[M+Na]+382.1237,found 382.1221。
3-苄基-5-(4,4,4-三氟-1-丁烯)-5-(2,2,2-三氟乙基)-2-噁唑啉酮(2ag)
(E)-3-benzyl-5-(4,4,4-trifluorobut-1-en-1-yl)-5-(2,2,2-trifluoroethyl)oxazolidin-2-one
32mg,产率23%,浅黄色固体;Rf(pentane/EtOAc 5:1)=0.16;
1H NMR(400MHz,CDCl3)δ7.41–7.29(m,3H),7.25–7.17(m,2H),5.92(dt,J=15.4,7.0Hz,1H),5.76(d,J=15.7Hz,1H),4.43(dd,J=75.7,15.0Hz,2H),3.38(dd,J=52.2,9.3Hz,2H),2.96–2.77(m,2H),2.73–2.50(m,2H);13C NMR(101MHz,CDCl3)δ156.04,134.99,134.97,128.98,128.24,127.94,125.34(dd,J=553.5,276.7Hz),124.41(q,J=277.7Hz),120.45(q,J=3.5Hz),75.80(q,J=2.3Hz),53.47(d,J=1.7Hz),48.15,42.93(q,J=28.0Hz),36.68(q,J=30.3Hz);19F NMR(376MHz,CDCl3)δ-60.59,-66.10.HRMS(ESI+):calcd for C16H16F6NO2+[M+H]+368.1080,found 368.1091。
实施例33至实施例35化合物2a的应用
通过化合物2a可以以高产率获得化合物3、4和5。具体制备方法如下所述。
N-苄基-N-(4,4,4,-三氟-2-羟基-2-苯基丁基)-3-烯丁酰胺(化合物3)
N-benzyl-N-(4,4,4-trifluoro-2-hydroxy-2-phenylbutyl)but-3-enamide
在-78℃下向0.2mmol(67mg,1.0equiv)化合物2a的THF(1mL)溶液中滴加0.6mmol(3.0equiv)的烯丙基溴化镁。保持在上述温度下反应3小时后,加入1mL饱和氯化铵溶液,待反应体系升至室温时,用乙醚萃取3次(3×5mL),然后旋干,进行柱层析(PE:EA=5:1)分离提纯获得目标化合物3(72mg),为无色油状液体,产率96%。
Rf(pentane/EtOAc 5:1)=0.5;1H NMR(400MHz,CDCl3)δ7.57–7.44(m,2H),7.44–7.37(m,2H),7.37–7.26(m,4H),6.95(d,J=6.9Hz,2H),5.87(ddt,J=16.8,10.2,6.4Hz,1H),5.70(s,1H),5.10(dddd,J=46.1,17.2,2.8,1.4Hz,2H),4.36(dd,J=33.6,15.9Hz,2H),3.36(dd,J=154.9,15.9Hz,2H),3.14–3.00(m,2H),2.84–2.59(m,2H);13C NMR(101MHz,CDCl3)δ174.64,141.78,134.42,129.50,128.08,127.36,126.89,126.56,125.03,124.72(q,J=278.7Hz),124.40,117.44,74.63(d,J=1.9Hz),56.84(d,J=1.7Hz),52.00,42.61(q,J=26.1Hz),37.43;19F NMR(376MHz,CDCl3)δ-58.68.HRMS(ESI+):calcd for C21H22F3NNaO2+[M+Na]+400.1495,found 400.1500。
1-(甲基苄基氨基)-4,4,4-三氟-2-苯基丁-2-醇(化合物4)
1-(benzyl(methyl)amino)-4,4,4-trifluoro-2-phenylbutan-2-ol
室温下向25mL Schlenk管中依次加入1.0mmol氢化铝锂(38mg,,5.0equiv)、4mL THF、0.2mmol化合物2a(67mg,1.0equiv)的THF(4mL)溶液。然后保持回流反应1小时,接着加入2mL氢氧化钠水溶液(2M)淬灭反应。硅藻土过滤,旋干溶剂,柱层析(PE:EA=10:1)分离提纯获得目标化合物4(62mg),白色固体,产率96%。
Rf(pentane/EtOAc 5:1)=0.6;1H NMR(400MHz,CDCl3)δ7.50–7.34(m,2H),7.31–7.02(m,8H),4.66(s,1H),3.33(dd,J=31.1,13.0Hz,2H),2.97–2.77(m,2H),2.60–2.38(m,2H),1.92(s,3H);13C NMR(101MHz,CDCl3)δ144.72,138.12,129.05,128.46,128.29,127.48,127.11,125.64(q,J=278.6Hz),125.22,71.23(q,J=1.9Hz),67.12(d,J=1.1Hz),63.57,44.89(q,J=26.1Hz),43.79;19F NMR(376MHz,CDCl3)δ-59.15;HRMS(ESI+):calcd for C18H21F3NO+[M+H]+324.1570,found 324.1574。
化合物5和5’的制备
向0.4mmol化合物2a(134mg,1.0equiv)的甲醇(4mL)溶液中加入10.4mmol氢氧化钠(416mg,26.0equiv),然后在65℃条件下搅拌反应2小时,待反应体系冷却至室温后,加入1N盐酸中和,待调至中性时,用二氯甲烷萃取3次(3×10mL),无水硫酸钠干燥,旋干,柱层析(PE:EA=10:1)分离提纯获得 目标化合物5和5’,浅黄色油状无物(95.6mg,产率82%)。
其中,(Z)-N-苄基-4,4,4-三氟-2-苯基丁-2-烯-1-胺(化合物5)为57.8mg,产率50%;Rf(pentane/EtOAc 5:1)=0.6;1H NMR(400MHz,CDCl3)δ7.52–7.26(m,5H),7.25–7.05(m,5H),5.84(q,J=8.6Hz,1H),3.79(d,J=0.9Hz,2H),3.64(s,2H);13C NMR(101MHz,CDCl3)δ150.82(q,J=5.3Hz),138.66,137.50,128.21,127.79,127.33,127.14,126.05,125.79,122.23(q,J=271.3Hz),116.98(q,J=34.1Hz),52.10,46.44;19F NMR(376MHz,CDCl3)δ-55.87.HRMS(ESI+):calcd for C17H17F3N+[M+H]+292.1308,found 292.1308。
(E)-N-苄基-4,4,4-三氟-2-苯基丁-2-烯-1-胺(5’)为37.8mg,产率32%;Rf(pentane/EtOAc 5:1)=0.5;1H NMR(400MHz,CDCl3)δ7.41–7.23(m,8H),7.23–7.15(m,2H),6.00(qt,J=8.2,1.6Hz,1H),3.81(s,2H),3.56–3.47(m,2H);13C NMR(101MHz,CDCl3)δ150.82(q,J=5.3Hz),138.60,135.96,127.49,127.25,127.16,127.08,126.33(d,J=1.7Hz),126.19,122.13(d,J=270.8Hz),114.36(q,J=33.7Hz),54.51,51.83;19F NMR(376MHz,CDCl3)δ-55.90.HRMS(ESI+):calcd for C17H17F3N+[M+H]+292.1308,found 292.1309。
- 还没有人留言评论。精彩留言会获得点赞!