芘炔基有机多孔聚合物及其制备方法与流程
本申请涉及一种共价连接的芘炔基有机多孔聚合物及其制备方法。
背景技术:
共价连接的有机多孔聚合物近年来受到人们的关注。由于有机多孔聚合物的高稳定性、耐酸碱性、结构刚性与多孔性使得其在如气体吸附、物质分离等方面具有潜在应用价值。需要合成新型的有机多孔聚合物。
技术实现要素:
根据本公开的一个方面,提供了一种共价连接的芘炔基有机多孔聚合物,包含:基本上呈平面构型的芳香基团A,包含至少一个芘环;与连接基团B,包含至少两个炔基。
根据一些实施例,所述有机聚合物中的芳香基团A中包含的芘环具有如下结构:
根据一些实施例,所述有机聚合物中的R1,R2,R3,R4,R5,R6独立地为氢、甲基、乙基、氧甲基。
根据一些实施例,所述有机聚合物中的R1,R2,R3,R4,R5,R6都为氢。
根据一些实施例,所述有机聚合物中的连接基团B具有以下结构:
根据一些实施例,所述有机聚合物进一步包含连接基团C,具有以下结构:
根据本公开的另一个方面,提供了一种制备共价连接的有机聚合物的方法,包含:将一种单体A0、催化剂与溶剂混合,得到一种混合物;加热所述混合物,得到一种固体;与过滤所述固体,得到一种共价连接的有机聚合物;其中,所述单体A0具有一下结构:
其中,R1,R2,R3,R4,R5,R6独立地为氢、甲基、乙基、氧甲基。
根据一些实施例,所述方法中的催化剂包含双三苯基膦二氯化钯、氯化亚铜、溴化亚铜、碘化亚铜、氰化亚铜和氧化亚铜中的至少一种。
根据一些实施例,所述方法中的溶剂包含二甲基亚砜、二甲基甲酰胺、二甲基乙酰胺、N,N-二异丙基胺、乙腈、苯乙腈、甲苯等中的至少一种。
根据一些实施例,所述方法中的加热是在50-100度范围内进行的。
附图描述
本文所述附图仅用于例证的目的并非旨在以任何方式限制本公开内容的范围。
图1是1,3,6,8-四(三甲硅基乙炔基)芘的红外光谱图;
图2是1,3,6,8-四乙炔基芘的红外光谱图;
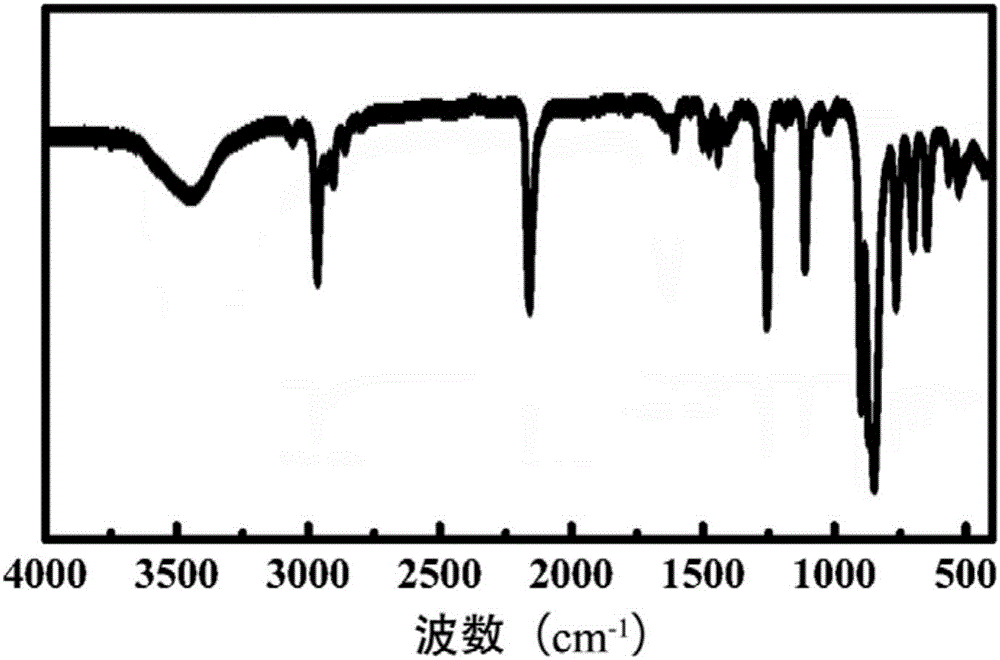
图3是共价连接的有机聚合物LKK-COF的红外光谱图;
图4是LKK-COF的13C核磁共振谱图;
图5是LKK-COF的粉末X射线衍射图;
图6A与图6B是LKK-COF的扫描电子显微图;
图7是LKK-COF的热重分析图;
图8是LKK-COF的N2吸附脱附图;
图9是LKK-COF的孔径分布图;
图10是LKK-COF在273K和298K下的CO2吸附脱附图;
图11显示的是LKK-COF的CO2吸附热;
图12是LKK-COF在273K和298K下的CH4吸附脱附图;
图13显示的是LKK-COF的CH4吸附热;
图14是LKK-COF的H2吸附图;
图15显示的是LKK-COF对CO2、CH4与N2的吸附选择性;
图16显示的是LKK-COF对CO2、CH4与N2的吸附选择性;
图17显示的是LKK-COF对CO2与CH4的吸附选择性;
图18显示的是LKK-COF对CO2与CH4的吸附选择性。
详细描述
可以理解,虽然通过举例说明本发明不同的具体实施方案,说明书和具体实施例旨在例证的目的而非打算限制本发明的范围。
如此处所用,在一个未端具有原子且另一个未端无原子的化学式中的线表示:所述式指在另一实体的无连接原子未端键合至所述实体的化学片段。有时为了强调,波浪线将与所述线相交。
【合成】
合成过程中的所有试剂,如无另外声明,都可以直接采购商业产品,不需要进一步纯化处理。在一些实施例中,可以先对溶剂、反应试剂或催化剂进行除水等纯化操作。
1,3,6,8-四溴化芘
作为有机聚合物的合成前体,1,3,6,8-四溴化芘按照如下过程合成:
往500mL三颈圆底烧瓶中加入6.0678g芘(30mmol),并加入120mL硝基苯作为溶剂,搅拌以混合均匀,得到溶液。
将6.7mL溴(130mmol)滴加至溶液中,同时进行剧烈搅拌。当滴加完成后,加热反应混合物至120℃,并维持该温度达6至24小时,然后自然冷却到室温。溶液中形成浅绿色沉淀。过滤沉淀,并用乙醇洗涤,真空下干燥,得到14.4036g产品(92%)。该产品经核磁和红外等表征为1,3,6,8-四溴化芘,不溶于常见有机溶剂。
在一些实施例中,可以通过含有芳香基团A的化合物通过溴化反应,制备类似的溴化物。
芳香基团A的结构为:
其中,R1至R6各自独立地为取代基,选自氢、甲基、乙基、氧甲基。
生成的溴化物为:
1,3,6,8-四(三甲硅基乙炔基)芘
往250mL三颈圆底烧瓶中加入5.17g的1,3,6,8-四溴化芘(12.0mmol),并加入35mL无水甲苯作为溶剂,通入N2气氛保护。向体系中加入0.4211g双三苯基磷二氯化钯(0.6mmol)、0.1143g碘化亚铜(0.6mmol)、0.3148g三苯基膦(1.2mmol)、90mL三乙胺与10mL三甲硅基乙炔(72mmol),搅拌以混合均匀。维持反应混合物80℃达12至48小时。冷却反应混合物,将其转移至300mL二氯甲烷中,用水洗涤数次。分离有机相,利用无水硫酸镁干燥。过滤,将滤液减压蒸馏,得到一种粗产品。通过硅胶色谱柱纯化粗产品,流动相为二氯甲烷:石油醚(体积比为1:1),得到4.35g橙红色固体(7.4mmol,产率约61.8%)。核磁(CDCl3):δ=8.59(s,4H),8.28(s,2H),0.39(s,36H)ppm。
在一些实施例中,可以通过含有芳香基团A的四溴化物通过与三甲硅基乙炔反应,制备类似的化合物。
芳香基团A的结构为:
其中,R1至R6各自独立地为取代基,选自氢、甲基、乙基、氧甲基。
制备的化合物结构为:
1,3,6,8-四乙炔基芘
往500mL圆底烧瓶中加入2.1425g的1,3,6,8-四(三甲硅基乙炔基)芘(3.6mmol),并加入200mL甲醇,搅拌使固体悬浮,加入4.1157g碳酸钾。加热反应混合物至30℃,放置4至24小时。减压使低沸点成分挥发,加入水,洗涤混合物直至洗出液呈近中性(pH值为6-8)。真空下100℃干燥6至12小时,得到0.8423g浅黄色固体产物(2.8mmol)。核磁(CDCl3):δ=8.68(s,4H),8.34(s,2H),4.28(s,4H)ppm。
反应过程中,K2CO3主要起到碱的作用,帮助三甲硅基乙炔基上的三甲硅基以硅醇离去。类似K2CO3的碱可以包括,Na2CO3、Cs2CO3与LiOH等。
在一些实施例中,可以通过含有芳香基团A的四溴化物通过醇解反应,制备类似的端炔A0,作为缩聚反应的单体。
芳香基团A的结构为:
其中,R1至R6各自独立地为取代基,选自氢、甲基、乙基、氧甲基。
制备的化合物结构为:
制备的端炔A0结构为:
LKK-COF
在N2气氛下,将1.617g的1,3,6,8-四乙炔基芘(5.43mmol)、0.284g三苯基膦(1.08mmol)、0.245g双三苯基磷二氯化钯(0.35mmol)与0.067g碘化亚铜(0.35mmol)加入到500mL三颈圆底烧瓶中。加入100mL的DMF与200mL的N,N-二异丙基胺,搅拌以混合均匀。加热反应混合物至70℃达12至48小时。冷却至室温后,将产物过滤,置于索氏提取器中用三氯甲烷、四氢呋喃与甲醇的混合溶液洗涤12至48小时。在60℃真空干燥6至18小时得到0.566g紫黑色固体LKK-COF(产率35%)
制备聚合物的过程如下式:
在一些实施例中,可以通过含有芳香基团A的端炔A0通过缩聚反应,制备类似的有机聚合物。
芳香基团A的结构为:
其中,R1至R6各自独立地为取代基,选自氢、甲基、乙基、氧甲基。制备的有机聚合物为:
由于缩聚反应的方向可能是随机的,因此结构中的R1至R6取代基的位置可能是随机的。R是R1至R6中的任意一个。
缩聚反应中,两个端炔基生成了连接基团B,具有以下结构:
在缩聚反应中,CuI和PdCl2(PPh3)2起到催化剂的作用。催化活性位点为Cu(I)原子和Pd(II)原子。在一些实施例中,可以只用Cu(I)化合物或者Pd(II)化合物。在一些实施例中,可以用至少一种Cu(I)化合物和至少一种Pd(II)化合物的混合物。Cu(I)化合物包括但不限于,CuCl、CuBr、CuI、CuCN、Cu2O、CuOAc(乙酸亚铜)等。Pd(II)化合物包括但不限于,PdCl2、PdBr2、PdI2等。
反应体系中的DMF和N,N-二异丙基胺起到混合溶剂的作用。在一些实施例中,可以选择单一溶剂,如DMF或N,N-二异丙基胺。在一些实施例中,可以选择二甲基亚砜、二甲基甲酰胺、二甲基乙酰胺、N,N-二异丙基胺、乙腈、苯乙腈、甲苯中的至少一种作为溶剂。
聚合反应可以在加热条件下进行。在一些实施例中,加热可以在50-100℃范围内。加热温度的选择,可以根据溶剂的沸点、催化剂的组分或反应单体的组分而确定。
【表征】
在Bruker公司的Advance 400MHz核磁仪上,采用氘代氯仿作溶剂对1,3,6,8-四乙炔基芘进行核磁谱图表征。固态交叉极化魔角旋转(CP/MAS)核磁谱图在Bruker Advance II WB 400MHz核磁仪上利用4mm DVT CP/MAS探针在10kHzMAS速率下对LKK-COF进行测量。
红外谱图在Shimadzu 8400傅立叶变换红外光谱仪(FTIR)上,使用溴化钾片对LKK-COF进行傅立叶变换红外光谱表征。
LKK-COF的粉末X射线衍射在Bruker D8Advance X射线衍射仪上用Cu-Kα射线(波长0.154nm)进行测量。
LKK-COF的热重分析在TGA/SDT-Q600热重分析仪上空气气氛下测量,升温速率10度/分钟,从20度至800度。
LKK-COF的扫描电子显微(SEM)在Hitachi S-4800扫描电子显微镜下测量。LKK-COF的气体吸附-脱附等温线在ASAP 2020HD88分析仪上测量。测量前对样品在423K下做12小时脱气处理。比表面积利用Brunauer-Emmett-Teller(BET)方法计算。孔径分布利用非局域密度泛函理论方法计算。
图1中,2958cm-1附近存在较强的甲基C-H伸缩振动峰。在图2中,这一吸收峰不再存在,证明分子中已不存在甲基,三甲基硅基已被脱去。图3中,在3280cm-1附近,LKK-COF几乎已不存在尖锐的伸缩振动吸收峰,说明在单体中的端炔基C-H键(–C≡C–H)已经基本不存在。单体通过缩合连接在一起。
连接基团B(–C≡C–C≡C–)的存在由图4中大约82.1ppm处的sp杂化碳原子吸收峰所证实。与芳基相连的炔基碳原子(–Car–C≡C–)的存在由图4中大约94.5ppm处的sp杂化碳原子吸收峰所证实。C≡C键的吸收峰由2011cm-1变为2169cm-1,说明几乎所有C≡C键都已发生了二聚。图4中,sp2杂化的碳原子的特征峰分布在约117.5至128.3ppm范围内,说明芘环上具有很大的无序结构。这可能与聚合反应本身的随机性有关。
此外,图4中,大约25ppm处的宽吸收峰指示存在sp2杂化的碳原子(非芳香环上的碳原子),由于聚合产品中不存在sp2杂化的碳原子上的C-H键,因此可以推断存在如下结构C:
这一结构可能是由于如下反应生成:
另外,如图5所示,LKK-COF的粉末X射线衍射呈现出范围较宽的信号分布,但不存在明显的衍射峰,可以说明LKK-COF是非晶型结构。这与LKK-COF的13CCP-NMR谱图上表现出的无序性符合得很好。
如图6A和6B所示,SEM图表明LKK-COF呈絮状形态,这可能与LKK-COF的相互穿插结构有关。如图7所示,LKK-COF的热重分析显示LKK-COF能够在氮气氛围下直到800℃仍保持稳定,不发生明显的分解。LKK-COF的热稳定性可能与其较强的共价键及内部穿插结构有关。
【多孔性】
在77.3K与1个大气压条件下,对LKK-COF的多孔性进行了N2吸附测量,如图8所示。在N2吸附测量前,新鲜制备的LKK-COF样品在150℃下脱气12小时。如图8所示,LKK-COF的N2吸附等温线呈国际纯粹与应用化学联盟(IUPAC)所定义的I型曲线。LKK-COF的N2吸附过程是几乎完全可逆的。在相对较低的压力(小于0.05大气压)下,随着压力增大,N2吸附量有较陡的升高,这表明LKK-COF可能存在永久的微孔结构。
通过将非局域密度泛函理论应用于拟合N2吸附量,可以得到图9所示的LKK-COF的孔径分布。LKK-COF的孔径约为0.59nm,这也证实了其微孔特征。与一些其他的聚合物网络结构类似,LKK-COF的N2吸附曲线表现出迟滞现象。迟滞现象可能说明LKK-COF骨架在吸附液氮过程中会发生胀缩。将N2吸附等温线用Brunauer-Emmett-Teller(BET)公式拟合,估算得到其比表面积约为467m2g-1,总体积为0.371cm3g-1,t-图微孔体积为0.185m3g-1。
【气体吸附】
在273K和298K下,测量了LKK-COF的CO2吸附等温线,如图10所示。这两个温度下的CO2等温线在脱附时同样表现出轻微的迟滞现象。在273K与1个大气压压力下,LKK-COF的CO2吸附量可达9.78wt%(重量分数)。在298K与1个大气压压力下,LKK-COF的CO2吸附量可达6.08wt%。在273K下,LKK-COF的这一指标比此前报道过的一些多孔材料,例如ACMP-C(6.88wt%,比表面积629m2g-1,Chem.Commun.,2013,49,3321)、MOP-3(8.0%,比表面积509m2g-1,Chem.Commun.,2014,50,13910)、PIN-1(7.92wt%,比表面积458m2g-1,J.Mater.Chem.A.,2015,3,18492)、COF-102(8.6wt%,比表面积3620m2g-1,J.Am.Chem.Soc.,2009,131,8875)与ILCOF-1(6.0wt%,比表面积2723m2g-1,Chem.Eur.J.,2013,19,3324)都要高。尽管LKK-COF的比表面积并不高,但其CO2吸附量却高于其他多孔聚合物。这一现象可能是由于LKK-COF的孔大小接近CO2的动力学半径,LKK-COF内部存在对CO2产生分子筛效应的结构。这一结构可以增大CO2与孔的作用,因而提高吸附量。
通过273K和298K下的CO2吸附等温线,可以根据克劳修斯-克拉贝龙公式计算得到LKK-COF对CO2的吸附焓。根据图11所示,低覆盖度时LKK-COF对CO2的吸附焓为35.0kJ/mol,这种吸附焓属于较强的物理吸附(通常小于40kJ/mol)。另外,这一数值比其他多孔材料的吸附焓数值稍高。
此外,也研究了LKK-COF在一个大气压、273K和298K两个温度下对甲烷的吸附。如图12所示,LKK-COF在273K下可以吸附1.14wt%的甲烷。而在298K下,吸附量为0.57wt%。如图13所示,在全负载范围内,LKK-COF对甲烷的吸附焓经计算为22至27kJ/mol。
除了CO2和甲烷,LKK-COF对氢气的吸附也进行了测量。如图14所示,当氢气分压增大时,LKK-COF的氢气吸附量也随之增大。在77K和1个大气压条件下,LKK-COF能吸附0.85wt%的氢气。
【选择性吸附】
如图15所示,在298K下,LKK-COF对CO2的吸附量明显高于CH4或N2。即便在压力较低的情况下,图16表明,LKK-COF对这三种气体的吸附几乎和压力成正比,满足亨利定律。在298K下,LKK-COF对CO2/N2的选择性达到约82.9。为了对LKK-COF分离纯化天然气的应用前景进行评估,测定了LKK-COF对CO2/CH4体系的吸附性能。吸附选择性实验表明,LKK-COF表现出高的CO2选择系数。图17是298K下,LKK-COF在0-1大气压范围内对两种气体的吸附曲线。图18是298K下,LKK-COF在低压范围内对两种气体的吸附曲线。如图18所示,在273K下,LKK-COF对低压的CO2和CH4的选择系数(吸附的CO2体积与吸附的CH4体积之比)约为20.7。在298K下,选择系数约为18.9。
以上描述仅仅是示例性的,因此那些不偏离本公开内容精神的变化确定为在发明范围内。这样的变化不被视为偏离本公开的精神和范围。
- 还没有人留言评论。精彩留言会获得点赞!