同时提取循环肿瘤细胞DNA和肿瘤游离DNA的试剂盒的制作方法
本发明涉及肿瘤基因突变检测技术领域,特别涉及从人类外周血中富集提取循环肿瘤细胞DNA和肿瘤游离DNA为模板进行qPCR肿瘤相关基因突变检测方法,具体为一种同时提取循环肿瘤细胞DNA和肿瘤游离DNA的试剂盒。
背景技术:
随着分子生物学的迅速发展,人们对肿瘤的认识达到了分子水平。许多肿瘤相关基因已被发现,肿瘤药物的靶向治疗也取得了很好的疗效。根据不同药物的疗效与肿瘤基因类型有相关性的特点,检测肿瘤基因类型能帮助临床医生采取精准的治疗方案。美国食品药品监督管理局于2003年5月批准了美国阿斯利康(Aotrazeneca)公司生产的小分子基因靶点药物吉非替尼(Gefitinib,也称为易瑞沙/Iressa)用于治疗晚期非小细胞肺癌(NSCLC)。吉非替尼是一种口服的小分子EGFR酪氨酸激酶抑制剂(EGFR-TKI),它对EGFR突变的肺癌患者有很好的治疗敏感性,通过抑制该酶的活性可以抑制肿瘤的增长、增殖,却无明显的化疗副作用。卫生部2010年11月首次发布了《结直肠癌诊疗规范》,明确规定:确诊为复发或转移性结直肠癌时,应进行相关基因状态检测,制定个体化治疗方案,患者确定为复发或转移性结直肠癌接受爱必妥、帕尼单抗(抗EGFR单抗)时,必须检测肿瘤组织的KRAS基因状态,通过检测KRAS基因有否突变,医生就可以有针对性地区别给药。
目前,针对肿瘤基因突变的检测方法主要有直接测序法、荧光定量PCR法和高分辨率熔解曲线法,这些方法所需要的DNA样本都来自石蜡包埋的肿瘤组织,然而石蜡样本在那些临床上不允许进行手术的肿瘤患者中无法获得,阻碍了肿瘤的精准治疗和患者治疗进展的时实监控。因此现在需要一个新的方法来解决这个问题。
近年的研究发现,在肿瘤患者的外周血游离DNA(cfDNA)中,存在全身各处原发灶的多种异常基因。采用荧光定量PCR的ARMS方法检测外周血中游离DNA的突变情况是一种无创性肿瘤诊断的新方法,也为肿瘤早期诊断提供了新的希望。但由于游离DNA中循环肿瘤DNA含量很小,只有转移性肿瘤患者血液中游离DNA含量会维持较高水平,所以仅仅提取游离DNA在现有的检测技术上实施突变基因检测,只能局限于中晚期患者才具有较高的检出率。
随着肿瘤分子诊断广泛应用的发展,使得无创伤性的外周血检验肿瘤突变基因成为了趋势,但是当前现有的方法仅仅只是简单粗略的将之前的石蜡提取DNA样本换成的血浆提取DNA样本,由于血浆提取的游离DNA相对石蜡样本提取的DNA含量稳定性差,波动范围发严重影响了血检的有效性。
技术实现要素:
为了克服现有检测方法的局限,本发明将肿瘤组织细胞脱落进入人体外周血中的肿瘤细胞,即循环肿瘤细胞(Circulating Tumor Cells,CTCs),同游离DNA一同从外周血中富集出,将这两种来源的DNA一同提取出来,互为补充,从而获得更多的肿瘤DNA用来检测相关基因突变类型,提高突变基因的检出率。具体来说:游离DNA单独检测为阳性结果的样本,在CTC单独提取DNA检测的结果不一定为阳性,反过来也是如此,由此将二者的结果综合起来,两种样本只要有一个为阳性就可判定患者为阳性结果,这就相当于将CTC的DNA和游离DNA混合一起用于进行突变基因的检测。本方法会提高以外周血为样本的肿瘤基因突变的检出率,而且检测成本能有效控制,操作简单快捷。因此本方法有利于临床的肿瘤突变基因外周血检测的推广。
本发明提供的一种同时提取循环肿瘤细胞DNA和肿瘤游离DNA的试剂盒,包括:
细胞密度梯度分离液;
多孔隔膜分离管;
5mL容积的离心管;
血液游离DNA提取试剂盒。
优选地,所述细胞密度梯度分离液为德国Geriner公司的产品Oncoquick肿瘤细胞密度梯度分离液。这种密度梯度分离液是专门为分离循环肿瘤细胞优化了配方,可以高效快速地对循环肿瘤细胞进行特异性的分离,同时可以有效去除血液中的红细胞和白细胞。
优选地,所述多孔隔膜分离管为武汉海吉力生物科技有限公司的产品:多孔隔膜分离管,容积为15ml。本离心管避免了加样时样本和离心介质的预混合,降低了由于离心机不稳定造成的污染,消除了取样时人为扰动造成试验结果干扰,提高了试验成功率和细胞回收率。
优选地,所述血液游离DNA提取试剂盒为武汉海吉力生物科技有限公司的产品:核酸提取试剂(ZD-E型),产品号HGN-tq1150。该试剂盒的优势在于:在产品缓冲液体系的作用下,DNA从血液样本中快速释放,吸附于高性能的固相基质,洗脱后即可获得高纯度DNA。
本发明还提供了以上任一所述的同时提取循环肿瘤细胞DNA和肿瘤游离DNA的试剂盒的使用方法,其包括以下步骤:
(1)将细胞密度梯度分离液加入多孔隔膜分离管中快速离心沉底;
(2)取肿瘤患者外周血加入步骤(1)的分离管中,在1200g重力加速度上离心25分钟;离心后外周血分为血浆层和红细胞层,血浆层在分离液上面,红细胞层在分离液下面,肿瘤细胞处于血浆与分离液层界面上,吸取出75%~85%体积血浆单独保存,注意不要吸到CTC细胞层,以免造成细胞的丢失;
(3)取出分离管多孔隔膜上目的细胞层以及分离液,加入到5ml离心管中与PBS缓冲液混匀,200g重力加速度离心,去上清,将细胞沉淀用单独保存的血浆重悬;
(4)重悬后的细胞采用血液游离DNA提取试剂盒从CTC细胞和血浆混合物中提取DNA。
与现有技术相比,本发明具有以下有益效果:
外周血中游离DNA(cfDNA)含量稀少,而且肿瘤循环DNA(ctDNA)量仅占外周血总游离DNA量中小于1%。另外CTC的含量也非常稀少,所以这给肿瘤突变基因的有效检测造成障碍。现有检测方法都是单独将肿瘤患者游离DNA从外周血中提取出做相关qPCR检测,这样的方法具有很大的局限性,突变基因检出率非常低。而本发明的方法根据游离DNA和循环肿瘤细胞DNA的突变基因检出率和发生无相关性的特点,利用二者检测结果的互补性,创意性的将游离DNA和循环肿瘤细胞DNA两种来源叠加提高样本量,这样能有效的提高患者肿瘤突变基因的检出率,达到临床的检测要求,从而使无创液态活检得以更好更广的运用,使更多的不同条件类型的肿瘤患者能从肿瘤分子诊断中获益。而且操作过程也方便简单,检测成本远低于单细胞检测技术,医生容易掌握,适合临床应用推广。
附图说明
图1是外周血加入到Oncoquick分离液上表面上的示意图;
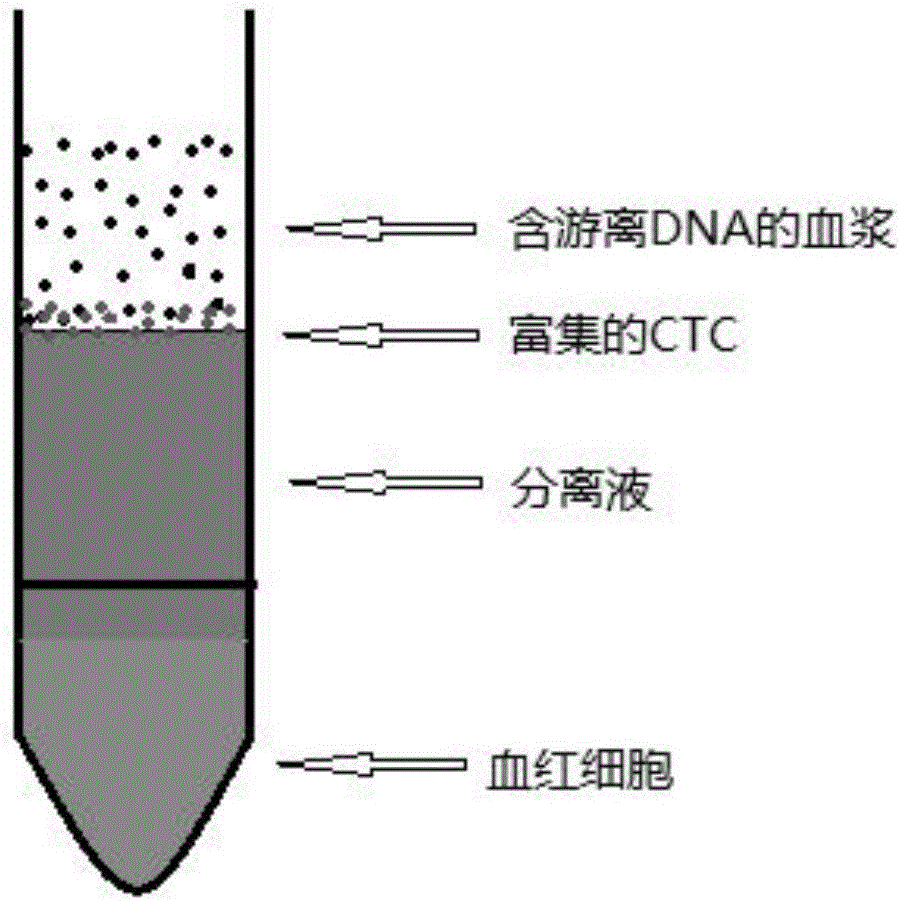
图2是经过梯度密度离心后血液发生了分层的示意图;
图3是游离DNA和循环肿瘤细胞DNA混合样本的qPCR检测结果;
图4是循环肿瘤细胞DNA单独样本的qPCR检测结果;
图5是游离DNA单独样本的qPCR检测结果。
具体实施方式
以人类EGFR基因突变检测试剂盒(荧光PCR法)(武汉海吉力生物科技有限公司)作为下游检测试剂盒为例。选取20位肺癌肿瘤患者提供的外周血作为实验对象,结合附图对本发明作进一步说明,但所举实施例不作为对本发明的限定。
实施例1:外周血中游离DNA和循环肿瘤细胞DNA混合样本提取分析
本实施例是从非小细胞肺癌患者外周血中提取肿瘤游离DNA和循环肿瘤细胞DNA,具体详述如下。
1、样本处理
(1)选取20位肺癌肿瘤患者作为实验对象,采用EDTA抗凝管抽取这20位患者的静脉血5ml。他们的FFPE组织EGFR基因的测序结果中(金标准)有15个EGFR阳性患者和5个EGFR阴性患者作为样本供者,总阳性率为75%。做好标记4℃保存。需要在3小时内将外周血进行密度梯度离心分离。
(2)向15ml分离管中分装3ml的Oncoquick分离液(分装20管),然后将20个患者的抗凝新鲜外周血分别轻轻加入各分离管分离液上层,避免外周血与分离液发生混合现象,见附图1。
(3)加好抗凝新鲜外周血后进行密度梯度离心,在1600g离心力下离心30分钟,离心温度保持在4℃。离心好后,能看到明显的血液分层,最上一层是血浆层,它与Oncoquick分离液层之间夹着目的细胞层,这一层富集有较多的CTCs。见附图2。
(4)用移液器分别将最上层的血浆层取到新的2ml EP管中,20份血浆做好标记放入4℃保存。
(5)用移液器分别将20个分离管的粒细胞层和Oncoquick分离液层取到新的离心管中,向里加入2ml的PBS缓冲液,混匀,再进行300g离心力,4℃离心10分钟,去除上清,留下细胞沉淀,CTCs就在沉淀中,然后200μl的PBS重悬。做好标记放4℃保存。
(6)分别将20个患者的细胞重悬液与上述血浆混合,提取DNA(按照核酸提取试剂(ZD-E型),操作说明进行)。
2、使用人类EGFR基因突变检测试剂盒(荧光PCR法)(武汉海吉力生物科技有限公司)对提取的DNA进行qPCR扩增,检测肿瘤基因突变类型,具体检测方法如下:
a.在试剂准备间取一支超纯水用于作为试剂盒的阴性对照。
b.在样本制备间取出阳性对照,先解冻再混匀。然后将8联PCR反应条、热启动Taq DNA聚合酶和阳性对照快速离心。
c.在样本制备间分别取20份样本的游离DNA和20份循环肿瘤DNA各40μl与4μl的热启动Taq DNA聚合酶在涡旋器上混匀。取超纯水和阳性对照各40μl,分别加入4μl热启动Taq DNA聚合酶在涡旋器上混匀。
d.轻轻揭开8联PCR反应条盖,将混好DNA聚合酶的样品加入到8联PCR条中,一个8联PCR条检测一个DNA样品,共40份样品。每个PCR反应孔加5μl样品。
e.盖上8联PCR反应条盖,简单离心。
f.将8联管放入实时定量PCR仪中。
g.设置PCR程序:
第一阶段:94℃5min;
第二阶段:94℃20s,62℃20s,15个循环;
第三阶段:94℃20s,60℃40s,31个循环;
信号收集:第三阶段60℃时收集FAM和JOE信号。
经过80分钟后,得到荧光定量PCR的结果,结果以图的形式表现,数据以表的形式表现,参见表1-2和图3。
实施例2:循环肿瘤细胞DNA单独样本提取分析
实验过程如实施例1,其中被提取的样本改为仅为分离出来的CTC细胞。本实施例证明了该试剂盒CTC细胞的富集能力以及CTC细胞DNA的单独提取能力。检测结果参见表1-2和图4。
实施例3:外周血游离DNA单独样本提取分析
实验过程如实施例1,其中被提取的样本改为实施例1中分离出来的血浆。本实施例证明了该试剂盒血浆游离DNA的单独提取能力。检测结果参见表1-2和图5。
统计结果分析:
对游离DNA和循环肿瘤细胞DNA混合样本、循环肿瘤细胞DNA单独样本、游离DNA单独样本,三类样本的检测结果进行统计分析,结果如下:
表1结果数据统计
表2.表1结果数据分析
根据上述结果可以看出,本试剂盒可以有效的分离并提取出CTC的DNA以及游离DNA,并能够使用提取出来的DNA进行相关的下游检测。混合样本的阳性结果覆盖了任意单一样本的阳性结果,其阳性符合率明显高于任意一种样本的单独检测结果。
以上所述实施例仅是为充分说明本发明而所举的较佳的实施例,本发明的保护范围不限于此。本技术领域的技术人员在本发明基础上所作的等同替代或变换,均在本发明的保护范围之内。本发明的保护范围以权利要求书为准。
- 还没有人留言评论。精彩留言会获得点赞!