杂交瘤细胞株及基于杂交瘤细胞株的抗CRH抗体C‑D17及其检测方面的应用的制作方法
本发明属于生物工程
技术领域:
,尤其涉及一种杂交瘤细胞株,以及一种抗肾上腺皮质激素释放激素(crh)的单克隆抗体,及其试剂盒。
背景技术:
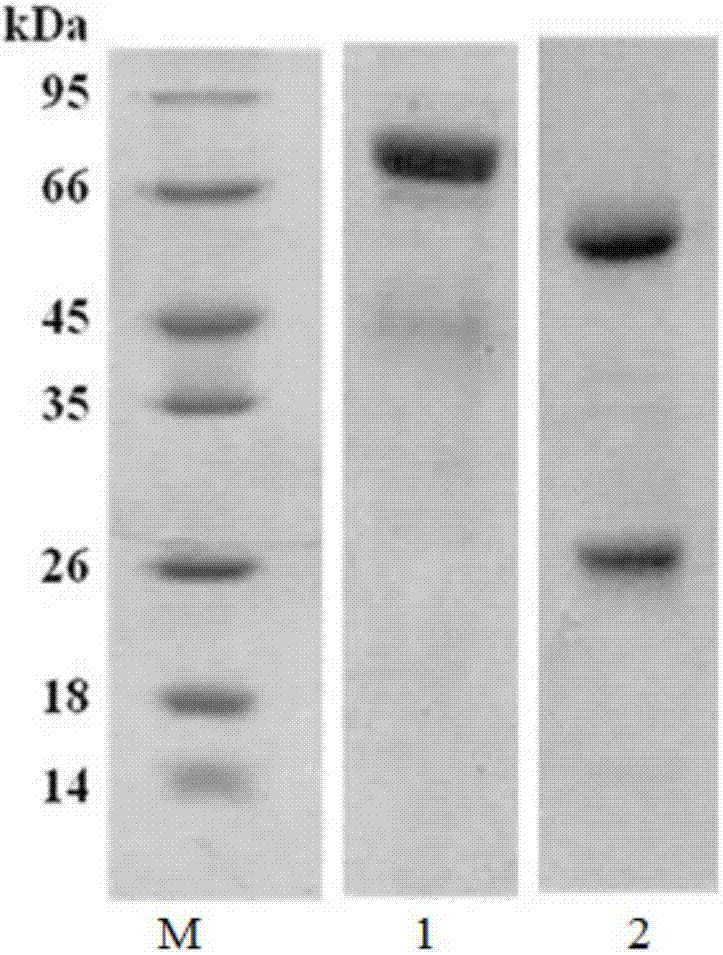
:据世界卫生组织1996年报告,全世界居住在海拔2500m以上人口总数为1.4亿,而且每年约有4000万人来到高山和高原地区,急性高原病是进入高山、高原地区的一大类常见病和多发病,人体急进暴露于低氧环境后产生的各种病理性反应。如果预防或治疗不当,急性高原病还会进一步发展为高原脑水肿、肺水肿,对高原工作、旅游及救援人员的健康带来很大的威胁。因此,如何实现进驻高原人群的预防性诊断,及早诊断出易患病人群,对高原病的防治具有重要意义。大脑是高原缺氧应激最敏感器官,在低氧环境下,为保证大脑氧供给,下丘脑-垂体-肾上腺轴(hpaaxis)发挥了关键调节作用,其中,肾上腺皮质激素释放激素(crh)触发了hpa轴的开启。crh是由41个氨基酸组成的多肽,在哺乳动物脑组织内主要由下丘脑室旁核小细胞部的神经元合成并分泌。通过正中隆起,crh被分泌到垂体,刺激垂体分泌促肾上腺皮质激素(acth),进而促进身上腺皮质激素的分泌。crh在应激条件反应中起重要调节作用。现有研究表明,基础血浆crh>50pg/ml或者唾液crh>21pg/ml的人群中,到达高原后,超过80%个体发生ams,高水平的crh和急性高原病(acutemountainsickness,ams)的发生具有直接关联。基础crh水平检测在预测急性高原病的发生中具有重要意义,通过预测,可以指导ams易患病人群提前做好必要的防治措施,从而将ams的危害降至最低。技术实现要素:本发明要解决的问题是针对crh抗体及相关技术的不足,提供一种杂交瘤细胞株。为解决上述技术问题,本发明采用的技术方案是:一种杂交瘤细胞株,于2016年5月31日保藏于中国典型培养物保藏中心,地址为中国武汉武汉大学,分类命名为杂交瘤细胞,保藏编号为cctccno.c2015215。本发明同时提供一种抗肾上腺皮质激素释放激素(crh)的单克隆抗体c-d17,其特征在于:由权利要求1所述杂交瘤细胞株产生。所述单克隆抗体c-d17能识别crh的n端表位,crh的c端表位序列为seqidno:1中所示序列。所述单克隆抗体c-d17为igg1型,轻链为κ型;本发明所述单克隆抗体c-d17的制备方法,其特征在于,包括以下步骤:s01:将crhc与klh偶联,形成klh-crhc偶联肽,作为免疫原;s02:以klh-crhc偶联肽与免疫佐剂混合,免疫balb/c小鼠后,取小鼠脾细胞;s03:将小鼠脾细胞与sp2/0小鼠骨髓瘤细胞融合,获得所述杂交瘤细胞,体内诱生或体外培养,经纯化,即得。本发明还提供所述的抗crh的单克隆抗体c-d17的应用,其特征在于:应用于制备检测crh方面的检测工具或在制备检测与crh有关疾病的试剂方面的应用。进一步,所述与人crh有关疾病为急性高原病。本发明的另一目的在于提供一种检测crh的双抗体夹心elisa试剂盒,包括所述的单克隆抗体c-d17;还包括单克隆抗体n-d19;所述单克隆抗体n-d19是保藏编号为cctccno.c2015215的杂交瘤细胞株产生,能识别crh的n端表位,crh的n端表位序列为seqidno:2中所示序列。进一步,所述试剂盒包括预包被单克隆抗体n-d19的酶标板和hrp标记的单克隆抗体c-d17;或预包被单克隆抗体c-d17的酶标板和hrp标记的单克隆抗体n-d19。优选的,所述试剂盒包括预包被单克隆抗体c-d17的酶标板和hrp标记的单克隆抗体n-d19。进一步,所述预包被单克隆抗体c-d17或n-d19的包被方法为:将单克隆抗体c-d17或n-d19用包被液稀释至10ug/ml,按100ul/孔加入到酶标板中,4℃包被过夜,洗涤液洗涤,再加入封闭液,封闭2h,洗涤液洗涤。优选的,所述包被液为0.05mmol/l的碳酸盐缓冲液(ph9.6);所述封闭液为pbs和质量分数为1%的bsa。进一步,所述hrp标记单克隆抗体c-d17或n-d19的方法为:首先称取10mghrp干粉,于5ml双蒸水中充分溶解,加入新鲜配制的0.2mol/lnaio4溶液0.5ml,避光于4℃水平摇床上轻轻摇动30min,加入已经透析至碳酸盐缓冲液的单克隆抗体c-d17或n-d19抗体10mg,混匀后,将溶液装入截留分子量为50kda的已预先处理好的透析袋中,将其对0.05mol/l的ph9.6的碳酸盐缓冲液4℃透析,每6h更换一次透析液,透析四次;透析结束后,取出透析袋中液体,向其中加入浓度为5mg/ml的nabh4100μl,4℃静置4h;加入等体积的饱和硫酸铵溶液,4℃放置过夜;5000rpm离心10min,用1ml0.05mmol/l的pbs(ph7.4)重悬后,对0.05mmol/l的pbs(ph7.4)缓冲液4℃透析,每6h更换一次透析液,透析四次;取出透析后的溶液,向其中加入标记液中加入等体积的甘油,即得纯化好的hrp标记得单克隆抗体c-d17或n-d19。进一步,所述试剂盒还包括crh标准品;标准品或样品稀释液:ph为7.4的pbs缓冲液;酶标抗体稀释液:pbs和质量分数为1%bsa;洗涤液:0.02mol/lpbs和质量分数为0.05%吐温20;显色液:tmb显色液;终止液:2mol/lh2so4。本发明所述试剂盒的使用方法,包括如下步骤:向预包被的酶标板中加入待测样品、hrp标记的单克隆抗体c-d17或n-d19,显色液显色,终止液终止,检测od450。优选的,所述hrp标记的单克隆抗体c-d17或n-d19的保存的浓度为1mg/ml,工作时稀释体积倍数为1:10000。本发明具有的优点和积极效果是:本发明提供了一种杂交瘤细胞株,于2016年5月31日保藏于中国典型培养物保藏中心,分类命名为杂交瘤细胞,保藏编号为cctccno.c2015215。基于所属杂交瘤细胞可产生具有优异特异性的抗crh单克隆抗体c-d17。本发明提供的抗crh单克隆抗体c-d17,可以识别crh的c端表位;具有良好的特异性与较高的效价,其效价可达1:4×106。本发明的检测crh的双抗体夹心elisa试剂盒,具有很好的特异性及较高的灵敏度:通过双抗夹心elisa对crh抗原检测,检测限可以达到15.6pg/ml,与现有技术产品比较,灵敏度有明显提高。另外,本试剂盒稳定性很好,在4℃条件下可以保存两年。同时,本检测试剂盒所用材料耗费少,检测样本的用量在微升水平,检测成本较低,适用于易感人群的普筛,适合大规模推广。经验证,采用本发明提供的试剂盒对10例急性高原病患者血清样本进行鉴定,其检测结果与预期完全一致,准确性可达100%。附图说明图1为c-d17经proteing亲和纯化后电泳图(m:marker;1:还原电泳;2:非还原电泳)图2为klh-crhc偶联肽免疫小鼠血清效价检测(m:marker;1:还原电泳;2:非还原电泳)图3为c-d17特异性检测图4为n-d19经proteing亲和纯化电泳图图5为klh-crhn偶联肽免疫小鼠血清效价图图6为n-d19特异性检测图7为crh检测标准曲线具体实施方式除非另外说明,本文中所用的术语均具有本领域技术人员常规理解的含义,本发明采用的仪器皆为常规市售品,皆可于市场购得。为了便于理解本发明,将本文中使用的一些术语进行了下述定义。在说明书和权利要求书中使用的,单数型“一个”和“这个”包括复数参考,除非上下文另有清楚的表述。例如,术语“(一个)细胞”包括复数的细胞,包括其混合物。所有的数字标识,例如ph、温度、时间、浓度,包括范围,都是近似值。要了解,虽然不总是明确的叙述所有的数字标识之前都加上术语“约”。同时也要了解,虽然不总是明确的叙述,本文中描述的试剂仅仅是示例,其等价物是本领域已知的。实施例1本发明所述单克隆抗体c-d17的制备与纯化。1、制备免疫原1.1制备crhc合成肽:合成crh的c端表位,序列为seqidno:2中所示序列,纯度大于99%。1.2klh-crhc偶联肽的获得:称取3mg间-马来酰亚胺苯甲酸-n-羟基琥珀酰亚胺酯(mbs)溶解在200μl二甲基甲酰胺(dmf),取1.5mgklh溶解在0.5ml0.05mol/l的磷酸盐缓冲液(ph7.0),向其中添加配置好的mbs溶液70μl,室温搅拌30min;klh/mbs混合溶液过pd-10脱盐柱,0.05mol/l磷酸盐缓冲液(ph6.0)洗脱,收集得到3.5ml纯化的klh/mbs;添加0.5ml去离子水、5mgcrhc合成肽溶于100μldmf,迅速加入1ml纯化的klh/mbs,快速震荡并立即用2nnaoh调节ph至7.0-7.2,将该混合溶液4℃放置过夜;最后添加3ml0.1mol/lnh4hco3,冷冻干燥得到klh-crhc偶联肽,即为用于制备抗体的免疫原。2、动物免疫及抗血清效价监测实验动物:6周龄雌性balb/c小鼠购自北京维通利华实验动物公司,免疫佐剂quickantibody购自北京康碧泉生物技术有限公司,小鼠骨髓瘤细胞sp2/0由本单位保存。2.1小鼠免疫:取50μgklh-crhc偶联肽(in250μlpbs),与等体积的免疫佐剂吹打混匀后,100μl每只小鼠,腿部肌肉多点注射;每隔10天免疫一次。2.2效价检测:分别在免疫前、每次免疫后第7天取血,监测抗血清效价。步骤包括:(1)包被:用0.05mol/l碳酸盐缓冲液(ph9.0)将klh-crhc偶联肽(或klh)稀释至10μg/ml,加入到聚苯乙烯微96孔板中,每孔100μl,4℃包被过夜,弃去孔内液体,用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(2)封闭:每孔加入300μlbsa封闭液,37℃封闭2h,弃去液体,并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(3)将待测效价的血清样本用bsa封闭液倍比稀释后,以100μl每孔加入到上述酶标板中,每个稀释倍数做三个复孔,37℃孵育1h,弃去液体并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(4)用酶标抗体稀释液(pbs+1%bsa)将羊抗鼠igg/hrp5000倍稀释后,以100μl每孔加入到上述酶标板中,37℃孵育0.5h,弃去液体并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(5)每孔加入100μltmb底物显色液,室温避光显色10min后,每孔加入50μl终止液(2mol/lh2so4)终止反应,测450nm吸收值,以免疫前小鼠血清作为阴性对照,以测定值/对照值≥2.1为阳性来判断免疫血清效价;每个采血时间点,各组小鼠均进行内眼眶采血,通过上述elisa实验检测小鼠血清效价,四次免疫后,将效价最高,且效价>105免疫小鼠安排细胞融合实验。3、细胞融合、细胞株建株及抗体制备3.1实验准备:融合前一天,处死正常小鼠一只,去小鼠腹腔液体制备小鼠饲养细胞;融合当天,取效价达到(或超过)105的小鼠,处死后,无菌条件下取出小鼠脾脏,碾碎并经无菌200目筛网过滤,置于无菌生理盐水中吹打洗涤后进行细胞计数;骨髓瘤细胞sp2/0细胞用rpmi-1640培养基培养,同脾细胞步骤洗涤并计数;3.2细胞融合:将准备好的sp2/0与脾细胞按1:10比例充分混合,1min内加入预先放置在37℃水浴保温的融合剂(无菌peg-4000,50%)1ml,37℃静置1min后,于2min内沿管壁缓慢加入5mlrpmi-1640不完全培养液(37℃预温),同时轻轻转动离心管;然后加入预热的rpmi-1640液至20ml终止融合,800rpm离心10min,用hat培养液重悬沉淀细胞并将细胞分种于96孔细胞培养板培养,每天观察并记录细胞生长状态。融合后第3天用hat培养液半量换液,第7天、第10天用ht培养液半量换液,之后改用完全培养液(rpmi-1640内含15%胎牛血清)换液培养。3.3阳性杂交瘤细胞株建株:参照《体外培养的原理与技术》,融合后第10-14天选择培养板中有细胞团的培养上清进行elisa检测,同时包被klh作为阴性对照。取阳性的细胞孔内的细胞,扩大培养至48孔后,再次检测效价,选择继续为阳性的细胞用有限稀释亚克隆法进行培养,选择四次亚克隆后仍为阳性的细胞,将该细胞株保存至中国普通微生物菌种保藏管理中心,保藏编号为cctccno.c2015215;并用其扩大培养后冻存细胞并制备腹水。3.4制备腹水:取8周龄的雌性balb/c小鼠,腹腔注射0.5ml液体石蜡,一周后,收集扩大培养的杂交瘤细胞,每只小鼠注射2×105个细胞,第6天起小鼠陆续开始产生腹水,收集小鼠腹水10,000rpm离心15min,腹水用等体积磷酸盐缓冲液(ph7.4)稀释并经0.45μm微孔滤膜过滤,于4℃备用或者-20℃保存。3.5单克隆抗体的纯化:proteing亲和填料购自美国法玛西亚公司,用2ml填料纯化10ml上述保存的腹水,洗脱的抗体经sephadexg-25脱盐处理后,以sds-page测定单克隆抗体的纯度,c-d17抗体纯度均达到90%以上。c-d17经proteing亲和纯化后电泳图见图1。4、单克隆抗体c-d17的特性鉴定4.1浓度测定:采用pierce公司bsa蛋白定量试剂盒测定纯化得到的抗体浓度,c-d17为1.72mg/ml。4.2亚类鉴定:采用北京五康新兴科技有限公司的抗体亚类快速鉴定试纸鉴定从腹水纯化的c-d17单克隆抗体,c-d17抗体为igg1型,轻链为κ型。4.3效价评估:采用elisa方法测:单克隆抗体的效价。首先分别用包被缓冲液将klh-crhc偶联肽与klh稀释至10μg/ml,以100μl/孔包被酶标板,37℃包被2h后,用bsa封闭液封闭后,向各孔加入倍比稀释的n-d19抗体,37℃孵育1h,洗板,加入1:5000稀释的羊抗鼠igg/hrp,继续孵育30min,充分洗板,加入tmb显色试剂避光显色10min,用2mol/lh2so4终止显色反应,读取450nm的吸光值。结果见图2。图2结果表明,c-d179抗体的效价可达到1:4×106。4.4特异性及交叉反应性鉴定:采用间接elisa方法检测c-d17抗体的特异性及与klh、klh偶联肽、crh、促黄体生成素(lh)等的交叉反应性,未免疫小鼠血清纯化的抗体作为对照(con),elisa结果见图3。结果表明,c-d17对除klh-crhc与crh外的其他蛋白均没有结合,而且c-d17对klh-crhc的结合能力与对crh的结合能力没有明显差异。实施例2本发明所述单克隆抗体n-d19的制备与纯化。1、制备免疫原1.1制备crhn合成肽:合成crh的n端表位,序列为seqidno:1中所示序列,纯度大于99%。1.2klh-crhn偶联肽的获得:称取3mg间-马来酰亚胺苯甲酸-n-羟基琥珀酰亚胺酯(mbs)溶解在200μl二甲基甲酰胺(dmf),取1.5mgklh溶解在0.5ml0.05mol/l的磷酸盐缓冲液(ph7.0),向其中添加配置好的mbs溶液70μl,室温搅拌30min;klh/mbs混合溶液过pd-10脱盐柱,0.05mol/l磷酸盐缓冲液(ph6.0)洗脱,收集得到3.5ml纯化的klh/mbs;添加0.5ml去离子水、5mgcrhn合成肽溶于100μldmf,迅速加入1ml纯化的klh/mbs,快速震荡并立即用2nnaoh调节ph至7.0-7.2,将该混合溶液4℃放置过夜;最后添加3ml0.1mol/lnh4hco3,冷冻干燥得到klh-crhn偶联肽,即为用于制备抗体的免疫原。2、动物免疫及抗血清效价监测实验动物:6周龄雌性balb/c小鼠购自北京维通利华实验动物公司,免疫佐剂quickantibody购自北京康碧泉生物技术有限公司,小鼠骨髓瘤细胞sp2/0由本单位保存。2.1小鼠免疫:取50μgklh-crhn偶联肽(in250μlpbs),与等体积的免疫佐剂吹打混匀后,100μl每只小鼠,腿部肌肉多点注射;每隔10天免疫一次。2.2效价检测:分别在免疫前、每次免疫后第7天取血,监测抗血清效价。步骤包括:(1)包被:用0.05mol/l碳酸盐缓冲液(ph9.0)将klh-crhn偶联肽(或klh)稀释至10μg/ml,加入到聚苯乙烯微96孔板中,每孔100μl,4℃包被过夜,弃去孔内液体,用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(2)封闭:每孔加入300μlbsa封闭液,37℃封闭2h,弃去液体,并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(3)将待测效价的血清样本用bsa封闭液倍比稀释后,以100μl每孔加入到上述酶标板中,每个稀释倍数做三个复孔,37℃孵育1h,弃去液体并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(4)用酶标抗体稀释液(pbs+1%bsa)将羊抗鼠igg/hrp5000倍稀释后,以100μl每孔加入到上述酶标板中,37℃孵育0.5h,弃去液体并用洗涤缓冲液pbst(0.02mol/lpbs内含0.05%tween-20)洗3次,每次3分钟;(5)每孔加入100μltmb底物显色液,室温避光显色10min后,每孔加入50μl终止液(2mol/lh2so4)终止反应,测450nm吸收值,以免疫前小鼠血清作为阴性对照,以测定值/对照值≥2.1为阳性来判断免疫血清效价;每个采血时间点,各组小鼠均进行内眼眶采血,通过上述elisa实验检测小鼠血清效价,四次免疫后,将效价最高,且效价>105免疫小鼠安排细胞融合实验。3、细胞融合、细胞株建株及抗体制备3.1实验准备:融合前一天,处死正常小鼠一只,去小鼠腹腔液体制备小鼠饲养细胞;融合当天,取效价达到(或超过)105的小鼠,处死后,无菌条件下取出小鼠脾脏,碾碎并经无菌200目筛网过滤,置于无菌生理盐水中吹打洗涤后进行细胞计数;骨髓瘤细胞sp2/0细胞用rpmi-1640培养基培养,同脾细胞步骤洗涤并计数;3.2细胞融合:将准备好的sp2/0与脾细胞按1:10比例充分混合,1min内加入预先放置在37℃水浴保温的融合剂(无菌peg-4000,50%)1ml,37℃静置1min后,于2min内沿管壁缓慢加入5mlrpmi-1640不完全培养液(37℃预温),同时轻轻转动离心管;然后加入预热的rpmi-1640液至20ml终止融合,800rpm离心10min,用hat培养液重悬沉淀细胞并将细胞分种于96孔细胞培养板培养,每天观察并记录细胞生长状态。融合后第3天用hat培养液半量换液,第7天、第10天用ht培养液半量换液,之后改用完全培养液(rpmi-1640内含15%胎牛血清)换液培养。3.3阳性杂交瘤细胞株建株:参照《体外培养的原理与技术》,融合后第10-14天选择培养板中有细胞团的培养上清进行elisa检测,同时包被klh作为阴性对照。取阳性的细胞孔内的细胞,扩大培养至48孔后,再次检测效价,选择继续为阳性的细胞用有限稀释亚克隆法进行培养,选择四次亚克隆后仍为阳性的细胞,将该细胞株保存至中国普通微生物菌种保藏管理中心,保藏编号为cctccno.c2015216;并用其扩大培养后冻存细胞并制备腹水。3.4制备腹水:取8周龄的雌性balb/c小鼠,腹腔注射0.5ml液体石蜡,一周后,收集扩大培养的杂交瘤细胞,每只小鼠注射2×105个细胞,第6天起小鼠陆续开始产生腹水,收集小鼠腹水10,000rpm离心15min,腹水用等体积磷酸盐缓冲液(ph7.4)稀释并经0.45μm微孔滤膜过滤,于4℃备用或者-20℃保存。3.5单克隆抗体的纯化:proteing亲和填料购自美国法玛西亚公司,用2ml填料纯化10ml上述保存的腹水,洗脱的抗体经sephadexg-25脱盐处理后,以sds-page测定单克隆抗体的纯度,n-d19抗体纯度均达到90%以上。n-d19经proteing亲和纯化电泳图见图4。4、单克隆抗体n-d19的特性鉴定4.1浓度测定:采用pierce公司bsa蛋白定量试剂盒测定纯化得到的抗体浓度,n-d19为2.33mg/ml。4.2亚类鉴定:采用北京五康新兴科技有限公司的抗体亚类快速鉴定试纸鉴定从腹水纯化的n-d19单克隆抗体,n-d19抗体为igg2a型,轻链为κ型。4.3效价评估:采用elisa方法测:单克隆抗体的效价。首先分别用包被缓冲液将klh-crhn偶联肽与klh稀释至10μg/ml,以100μl/孔包被酶标板,37℃包被2h后,用bsa封闭液封闭后,向各孔加入倍比稀释的n-d19抗体,37℃孵育1h,洗板,加入1:5000稀释的羊抗鼠igg/hrp,继续孵育30min,充分洗板,加入tmb显色试剂避光显色10min,用2mol/lh2so4终止显色反应,读取450nm的吸光值。结果见图5。图5结果表明,n-d19抗体的效价可达到1:4×106。4.4特异性及交叉反应性鉴定:采用间接elisa方法检测n-d19抗体的特异性及与klh、klh偶联肽、crh、促黄体生成素(lh)等的交叉反应性,elisa结果见图6。结果表明,n-d19对除klh-crhn与crh外的其他蛋白均没有结合,而且n-d19对klh-crhn的结合能力与对crh的结合能力没有明显差异。实施例3本发明检测crh的双抗体夹心elisa试剂盒的组成和最佳工作浓度检测1、制备hrp标记的抗人crh单克隆抗体c-d17或n-d19hrp标记单克隆抗体c-d17或n-d19的方法为:首先称取10mghrp干粉,于5ml双蒸水中充分溶解,加入新鲜配制的0.2mol/lnaio4溶液0.5ml,避光于4℃水平摇床上轻轻摇动30min,加入已经透析至碳酸盐缓冲液的单克隆抗体c-d17或n-d19抗体10mg,混匀后,将溶液装入截留分子量为50kda的已预先处理好的透析袋中,将其对0.05mol/l的ph9.6的碳酸盐缓冲液4℃透析,每6h更换一次透析液,透析四次;透析结束后,取出透析袋中液体,向其中加入浓度为5mg/ml的nabh4100μl,4℃静置4h;加入等体积的饱和硫酸铵溶液,4℃放置过夜;5000rpm离心10min,用1ml0.05mmol/l的pbs(ph7.4)重悬后,对0.05mmol/l的pbs(ph7.4)缓冲液4℃透析,每6h更换一次透析液,透析四次;取出透析后的溶液,向其中加入标记液中加入等体积的甘油,即得纯化好的hrp标记得单克隆抗体c-d17或n-d19。2、酶标抗体的标记验证采用elisa方法检测n-d19/hrp和c-d17/hrp的标记效果。将稀释后的c-d17(或n-d19)(1μg/ml)包被在酶标板上(4℃过夜),用封闭液37℃封闭2h,依次加入倍比稀释的crh抗原、n-d19/hrp(c-d17/hrp),继续孵育1h,充分洗板后,经tmb显色并终止液终止显色反应后,读取od450(见表1)。c-d17抗体包被,n-d19作为检测抗体为最佳组合,为减少本底的影响,检测抗体浓度为:1:10000。表1crh双抗夹心elisa检测(od450)3、试剂盒检测限及检测范围检测灵敏度15.6pg/ml,最佳检测范围15.6~1000pg/ml。4、试剂盒组成及检测方法试剂盒主要包括:c-d19预包被的酶标板、pbst洗涤缓冲液、n-d19/hrp检测抗体、酶标抗体稀释液、tmb显色液、终止液。本发明所述试剂盒的使用方法,包括如下步骤:(1)两倍稀释离心收集的血清,加入预包被的酶标板,37℃放置2h;(2)pbst洗涤3次;(3)用酶标抗体稀释液(pbs+1%bsa)将hrp标记抗体n-d1910000倍稀释后,以100μl每孔加入到上述酶标板中,37℃孵育1h,弃去液体并用洗涤缓冲液pbst洗3次,每次3分钟;(4)每孔加入100μltmb底物显色液,室温避光显色10min后,每孔加入50μl终止液(2mol/lh2so4)终止反应,测450nm吸收值。实施例4本发明检测crh的双抗体夹心elisa试剂盒的检测人血清样品1、血清样品收集收集10例急性高原病患者血清样本,另外收集10例正常。2、绘制标准曲线以od450为纵坐标,以倍比稀释的crh浓度(pg/ml)为横坐标,绘制标准曲线,并建立回归方程。绘得标准曲线如图7所示,其回归方程为:y=0.001x+0.427,其中r2=0.993符合线性关系的判断标准。3、依照实施例3的检测方法对血清样品进行检测根据标准曲线,读取各血清样品中crh含量,结果如表2所示:高原病人crh含量(pg/ml)健康人crh含量(pg/ml)187.2155.9291.5256.3399.4347.8481.8453.5580.7555.5696.9661.3792.6749.8884.7854.3982.3963.41078.71052.7平均值87.58平均值55.05标准差7.17标准差4.72结果表明:健康人血清中crh含量平均含量为55.05pg/ml,高原病人清中crh含量平均含量为87.58pg/ml,患者血清中crh含量高于健康人血清中crh含量。采用spss13.0软件分析,差异具有统计学意义(p<0.01)。可见:采用本发明提供的试剂盒,根据测得的crh在血清中含量可以准确的判定患者是否有高原病。而本实施例作为典型举例的10例高原病患者的血清中crh蛋白的含量皆高于10个健康人的血清中crh含量。表明本发明提供的方法具有良好的准确性,能够与预期结果完全一致,准确率可达100%。以上对本发明的实施例进行了详细说明,但所述内容仅为本发明的较佳实施例,不能被认为用于限定本发明的实施范围。凡依本发明范围所作的均等变化与改进等,均应仍归属于本专利涵盖范围之内。当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1
- 杂交瘤细胞系(My‑C‑cC0C2‑235‑3H8)及其生产抗人心脏肌球蛋白结合蛋白C(C蛋白、MYBPC3、cMyBP‑C或者My‑C)单克隆抗体的应用的制作方法与工艺
- 一种杂交瘤细胞株、其分泌的单克隆抗体及应用的制作方法与工艺
- 杂交瘤细胞株QW8#及其产生的抗Ⅰ型拟除虫菊酯通用单克隆抗体的制作方法与工艺
- 杂交瘤细胞株7G11及其抗体的制作方法与工艺
- 一种杂交瘤细胞株及其产生的狂犬病毒磷蛋白单克隆抗体的制作方法与工艺
- 一种杂交瘤细胞株1A5、分泌的抗舒巴坦单克隆抗体及应用的制作方法与工艺
- 杂交瘤细胞无血清培养液的制作方法与工艺
- 一株降钙素原单克隆抗体杂交瘤细胞株CS12‑1及其应用的制作方法与工艺
- 一株抗甲基汞单克隆抗体杂交瘤细胞株GZ02及其应用的制作方法与工艺
- 一株多效唑单克隆抗体杂交瘤细胞株CS12‑1及其应用的制作方法与工艺
- 杂交瘤细胞系(My‑C‑cC0C2‑259‑1A4)及其生产抗人心脏肌球蛋白结合蛋白C(C蛋白、MYBPC3、cMyBP‑C或者My‑C)单克隆抗体的应用的制作方法与工艺
- 杂交瘤细胞系(My‑C‑cC0C2‑235‑3H8)及其生产抗人心脏肌球蛋白结合蛋白C(C蛋白、MYBPC3、cMyBP‑C或者My‑C)单克隆抗体的应用的制作方法与工艺
- 一种杂交瘤细胞株、其分泌的单克隆抗体及应用的制作方法与工艺
- 杂交瘤细胞株QW8#及其产生的抗Ⅰ型拟除虫菊酯通用单克隆抗体的制作方法与工艺
- 杂交瘤细胞株7G11及其抗体的制作方法与工艺
- 一种杂交瘤细胞株及其产生的狂犬病毒磷蛋白单克隆抗体的制作方法与工艺
- 一种杂交瘤细胞株1A5、分泌的抗舒巴坦单克隆抗体及应用的制作方法与工艺
- 杂交瘤细胞无血清培养液的制作方法与工艺
- 筛选抗微生物剂的方法与流程
- 一株抗甲基汞单克隆抗体杂交瘤细胞株GZ02及其应用的制作方法与工艺