一种替诺福韦艾拉酚胺的制备方法与流程
本发明涉及药物合成技术领域,具体是一种替诺福韦艾拉酚胺的制备方法。
背景技术:
富马酸替诺福韦酯(TDF){9-R-[(2-膦酰甲氧基)丙基]腺嘌呤}是人类免疫缺陷病毒1型(HIV-1)复制的强力体外体内抑制剂,一种核苷酸类抗病毒药。它不仅能抑制病毒复制所需要酶的合成,而且能作为底物类似物参与竞争,掺入病毒复制的DNA中,阻断DNA链的延长,从而抑制病毒复制,是近年来发展较快的一类抗病毒药,已成为全球医药市场范围内令人瞩目的药物之一。
富马酸替诺福韦艾拉酚胺(TAF)是比富马酸替诺福韦酯(TDF)更新一代的替诺福韦(TFV)前药。临床数据显示:TAF比TDF剂量小10倍而清除病毒的能力相当,且有更高的安全性与耐受性。目前,含有TAF的四种治疗艾滋病的复方药物已经先后获得美国FDA的批准上市;另外,单方以TAF为活性成分的乙肝(HBV)治疗药物也在2016年11月获得美国FDA的批准上市,被认为是迄今为止最好的治疗乙肝(HBV)的药物。
替诺福韦艾拉酚胺是富马酸替诺福韦艾拉酚胺(TAF)的游离碱形式,目前文献报道过的合成路线主要有三条。
合成路线1(参见CN103732594,CN100402539,US7390791B):
;
合成路线2(参见WO2012053917(US20130316970)):
;
合成路线3(参见CN201510206002):
,
;
路线1以亚磷酸二乙酯为原料,经与多聚甲醛缩合、酯化制得中间体(C),在烷氧基镁催化下与(R)-9-(2-羟丙基)腺嘌呤缩合得中间体(F),经水解得中间体(G)(替诺福韦),再经酯化得半富马酸替诺福韦艾拉酚胺关键中间体(3),再经氯化、缩合、结晶制得替诺福韦艾拉酚胺。操作步骤较为繁琐,收率也不高。
路线2提及以亚磷酸二苯酯为原料,经与氯甲基苄醚缩合,再经水解、氯化、缩合、拆分、脱保护、酯化,制得酰氧基甲基膦酸酯,在碱性条件下与(R)-9-(2-羟丙基)腺嘌呤缩合得到替诺福韦艾拉酚胺,但无具体的说明实例。
路线2中所用到脱保护条件需要使用贵金属催化氢化,对设备要求较高。
路线3中主要对替诺福韦艾拉酚胺的关键中间体的合成方法进行了改进,将得到的磷酸二苯酯水解一个苯酯得到关键中间体。该方法有一定的借鉴意义,但是起始物料(1)并没有规模化的供应,需要通过两步反应合成。
研究开发新的、更适合产业化、低碳环保的制备替诺福韦艾拉酚胺的方法十分必要。
技术实现要素:
本发明的目的在于提供一种原料易得、成本较低的替诺福韦艾拉酚胺的制备方法,以解决上述背景技术中提出的问题。
为实现上述目的,本发明提供如下技术方案:
一种替诺福韦艾拉酚胺的制备方法,具体步骤如下:
(1)PMPA经过与氯化试剂加热反应得到PMPA-2Cl;化学反应式如下:
(1);
(2)PMPA-2Cl通过一锅法先后与苯酚和L-丙氨酸异丙酯反应得到TAF-RS;化学反应式如下:
(2);
(3)TAF-RS经过纯化得到替诺福韦艾拉酚胺;化学反应式如下:
(3)。
作为本发明进一步的方案:所述步骤(1)在有机溶剂或无溶剂的体系中反应。
作为本发明进一步的方案:所述有机溶剂为乙腈、甲苯或苯。
作为本发明进一步的方案:所述步骤(1)中的氯化试剂为氯化亚砜、三氯化磷、五氯化磷、草酰氯中的一种。
作为本发明进一步的方案:所述步骤(2)中一锅法是在-40~-10℃温度条件下,在有机溶剂中将PMPA-2Cl在有机碱存在下先与苯酚反应后,再加入L-丙氨酸异丙酯反应。
作为本发明进一步的方案:所述有机溶剂为二氯甲烷、甲苯、1,2-二氯乙烷或乙腈。
作为本发明再进一步的方案:所述一锅法的温度为-30~-20℃。
与现有技术相比,本发明的有益效果是:
本发明的合成工艺,避免繁琐的操作流程,简化了反应步骤,且原料易得,反应温和,成本较低,适合工业化生产。
附图说明
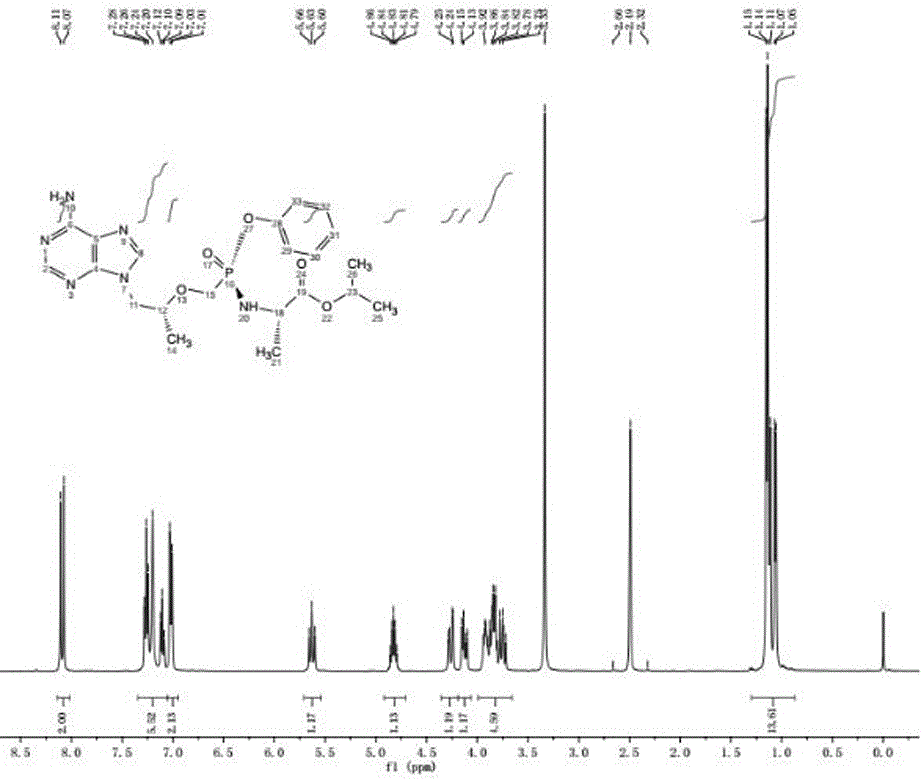
图1为本发明得到产物替诺福韦艾拉酚胺的H-NMR谱图。
图2为本发明得到产物替诺福韦艾拉酚胺的HPLC图谱。
图3为本发明得到产物替诺福韦艾拉酚胺的MS谱图。
具体实施方式
下面结合具体实施方式对本专利的技术方案作进一步详细地说明。
请参阅图1,一种替诺福韦艾拉酚胺的制备方法,具体步骤如下:
(1)PMPA经过与氯化试剂加热反应得到PMPA-2Cl;化学反应式如下:
(1);
(2)PMPA-2Cl通过一锅法先后与苯酚和L-丙氨酸异丙酯反应得到TAF-RS;化学反应式如下:
(2);
(3)TAF-RS经过纯化得到替诺福韦艾拉酚胺;化学反应式如下:
(3)。
所述步骤(1)在有机溶剂或无溶剂的体系中反应;所述有机溶剂为乙腈、甲苯或苯。
所述氯化试剂可以选用氯化亚砜、三氯化磷、无氯化磷、草酰氯中的一种;进一步的,优选氯化亚砜;
所述步骤(2)中一锅法是在-40~-10℃温度条件下,在有机溶剂中将PMPA-2Cl在有机碱存在下先与苯酚反应后,再加入L-丙氨酸异丙酯反应。
所述步骤(2)中由PMPA-2Cl合成TAF-RS的工艺中,有机溶剂选用二氯甲烷、甲苯、1,2-二氯乙烷、乙腈等溶剂;进一步的,有机溶剂优选二氯甲烷。
所述步骤(2)中由PMPA-2Cl合成TAF-RS的工艺中,反应温度控制在-40~-10℃;进一步的,优选反应温度-30~-20℃。
下面结合实施例,进一步说明本发明的技术方案。
实施例1
一种替诺福韦艾拉酚胺的制备方法,具体步骤如下:
(1)PMPA经过与氯化试剂加热反应得到PMPA-2Cl;化学反应式如下:
(1);
将PMPA(5g,17.8mmol)加入至25ml乙腈中,在室温下加入氯化亚砜10ml,搅拌并升温至回流反应2小时后,体系中固体溶解,取样加入至无水甲醇中监控原料转化完全;将反应液减压浓缩,除去溶剂得到泡沫状固体PMPA-2Cl重为6.5g;
(2)PMPA-2Cl通过一锅法先后与苯酚和L-丙氨酸异丙酯反应得到TAF-RS;化学反应式如下:
(2);
在干净的250ml三口瓶中加入二氯甲烷60ml,加入5g的PMPA-2Cl以及三乙胺5.6g(55.2mmol),加完后在氮气氛围下搅拌降温至-30℃。控温在-30~-20℃下滴加苯酚1.3g(13.8mmol)与40ml二氯甲烷形成的混合溶液,加完后搅拌反应1h。继续控温在-30~-20℃下滴加2.6g的L-丙氨酸异丙酯与20ml二氯甲烷形成的混合溶液。加完后缓慢升温至10~15℃搅拌反应2h,向反应液中加入10%氯化铵水溶液100ml,搅拌后分液。下层有机相用10%磷酸二氢钠水溶液100ml洗涤三次后,收集有机相用无水硫酸镁干燥5h,滤去干燥剂,滤液浓缩至干,得到TAF-RS为4.2g粘稠泡沫状固体;
(3)TAF-RS经过纯化得到替诺福韦艾拉酚胺;化学反应式如下:
(3);
在100ml三口瓶中加入4.0g的TAF-RS,加入乙腈10ml升温至40℃搅拌溶解后,缓慢降温至10~15℃搅拌5h逐渐析出固体后过滤,得到固体经45℃真空干燥10h,得到白色固体TAF为2.0g。LCMS:M+1显示477.5,HNMR(D6-DMSO)1HNMR(400MHz,D2O):δ1.05~1.15(m,12H),3.75~3.86(m,4H),4.13(dd,1H),4.24(dd,1H),4.79~4.86(m,1H),5.60~5.66(t,1H),7.01~7.28(m,7H),8.07(dd,2H)。见附图1。
实施例2
一种替诺福韦艾拉酚胺的制备方法,具体步骤如下:
(1)PMPA经过与氯化试剂加热反应得到PMPA-2Cl;化学反应式如下:
(1);
将PMPA(5g,17.8mmol)加入至20ml氯化亚砜中,搅拌并升温至回流反应1.5小时后,体系中固体溶解,取样加入至无水甲醇中监控原料转化完全。将反应液减压浓缩至干,得到泡沫状固体PMPA-2Cl,重为6.7g;
(2)PMPA-2Cl通过一锅法先后与苯酚和L-丙氨酸异丙酯反应得到TAF-RS;化学反应式如下:
(2);
在干净的250ml三口瓶中加入二氯甲烷60ml,加入5g的PMPA-2Cl以及三乙胺5.6g(55.2mmol),加完后在氮气氛围下搅拌降温至-30℃。控温在-30~-20℃下滴加苯酚1.3g(13.8mmol)与40ml二氯甲烷形成的混合溶液,加完后搅拌反应1h。继续控温在-30~-20℃下滴加2.6g的L-丙氨酸异丙酯与20ml二氯甲烷形成的混合溶液。加完后缓慢升温至10~15℃搅拌反应2h,向反应液中加入10%氯化铵水溶液100ml,搅拌后分液。下层有机相用10%磷酸二氢钠水溶液100ml洗涤三次后,收集有机相用无水硫酸镁干燥5h,滤去干燥剂,滤液浓缩至干,得到TAF-RS为4.2g粘稠泡沫状固体;
(3)TAF-RS经过纯化得到替诺福韦艾拉酚胺;化学反应式如下:
(3);
在100ml三口瓶中加入4.0g的TAF-RS,加入乙腈10ml升温至40℃搅拌溶解后,缓慢降温至10~15℃搅拌5h逐渐析出固体后过滤,得到固体经45℃真空干燥10h,得到白色固体TAF为2.0g。LCMS: M+1显示477.5,HNMR(D6-DMSO)1HNMR(400MHz,D2O):δ1.05~1.15(m,12H),3.75~3.86(m,4H),4.13(dd,1H),4.24(dd,1H),4.79~4.86(m,1H),5.60~5.66(t,1H),7.01~7.28(m,7H),8.07(dd,2H)。见附图1。
本发明的合成工艺,避免繁琐的操作流程,简化了反应步骤,且原料易得,反应温和,成本较低,适合工业化生产。
上面对本专利的较佳实施方式作了详细说明,但是本专利并不限于上述实施方式,在本领域的普通技术人员所具备的知识范围内,还可以在不脱离本专利宗旨的前提下作出各种变化。
- 还没有人留言评论。精彩留言会获得点赞!