有机多孔聚合物及其制备方法和应用与流程
本发明主要涉及多孔材料的技术领域,具体是有机多孔聚合物及其制备方法和应用。
背景技术:
有机多孔聚合物具有骨架密度低、比表面积高、孔径可控、良好的化学物理性以及制备多样性等特点,通常采用多步f-c反应和由金属铂催化的buchwald-hartwing、sonogashira-hagihara交联反应进行制备,多步f-c反应制备单体合成比较繁琐、合成步骤多、交联反应需要昂贵的催化剂等增加了聚合物制备成本,不适合工业推广应用,随这环保意识的提高,对这类多孔材料的研究,寻找简单安全的合成途径,使其在有效降低合成成本的同时合成具有较高的比表面积和丰富微孔结构的聚合物,拓展有机多孔聚合物在重金属吸附方面的应用,将成为将后的研究方向。
技术实现要素:
为解决现有技术中的不足,本发明提供一种有机多孔聚合物及其制备方法和应用,制备的聚合物具有较高的比表面积和丰富的孔结构,易与重金属离子配位,在重金属吸附尤其是对铅离子、铜离子具有较好的吸附。
本发明为实现上述目的,通过以下技术方案实现:
有机多孔聚合物,其结构式是:
其中n=2~500。
有机多孔聚合物的制备方法,
步骤1:将三聚氰胺、间苯二甲醛溶于二甲亚砜中,搅拌至固体完全溶解,三聚氰胺和间苯二甲醛按照摩尔比为2∶1.5~2∶4,三聚氰胺与二甲亚砜的用量比为2摩尔∶7~12升;
步骤2:加热并不断搅拌,加热至50℃时通入n2,并持续一段时间排除体系内的原有气体;
步骤3:氮气保护、搅拌条件下在130~180℃下两种单体进行缩聚反应,加热回流,反应48~80h,冷却至室温;
步骤4:将反应后的进行抽滤,抽滤所得固体经机溶剂进行洗涤、干燥后得有机多孔聚合物。
所述有机溶剂是丙酮、四氢呋喃、二氯甲烷。
将抽滤所得固体依次用10~30ml的丙酮、四氢呋喃、二氯甲烷分别洗涤2~3次。
有机多孔聚合物在重金属吸附方面的应用,将待吸附溶液ph调至4~8,温度30~80℃,吸附时间2~4h。
对比与现有技术,本发明有益效果在于:
1、本发明制备得到的聚合物具有较高的比表面积和丰富的孔结构,富含氮元素含氮量为40%,n原子上含孤对电子,是一个良好的配体,易与重金属离子配位。
2、本发明以三聚氰胺和间苯二甲醛为反应原料,二甲基亚砜为溶剂反应制得有机多孔聚合物,反应简单易操作,三聚氰胺与间苯二甲醛通过缩聚反应连接起来,逐渐形成分子链,分子链之间通过链端的官能团缩聚组成更大的分子链,最终聚合物形成三维网络状结构。
3、本发明在吸附金属离子时,将带吸附溶液的ph调节至接近中性,胺基、亚胺基渐渐非质子化,故而能充分与铅离子结合,金属离子浓度越来越少,吸附剂表面的有效吸附点位也越来越少,金属离子需要长程扩散,经过吸附剂表面的孔进入到其内部与有效吸附点位结合,因此过程耗时长,吸附速率会变低,因此吸附时长要控制在2~4h。
附图说明
附图1是实施例1的红外光谱图;
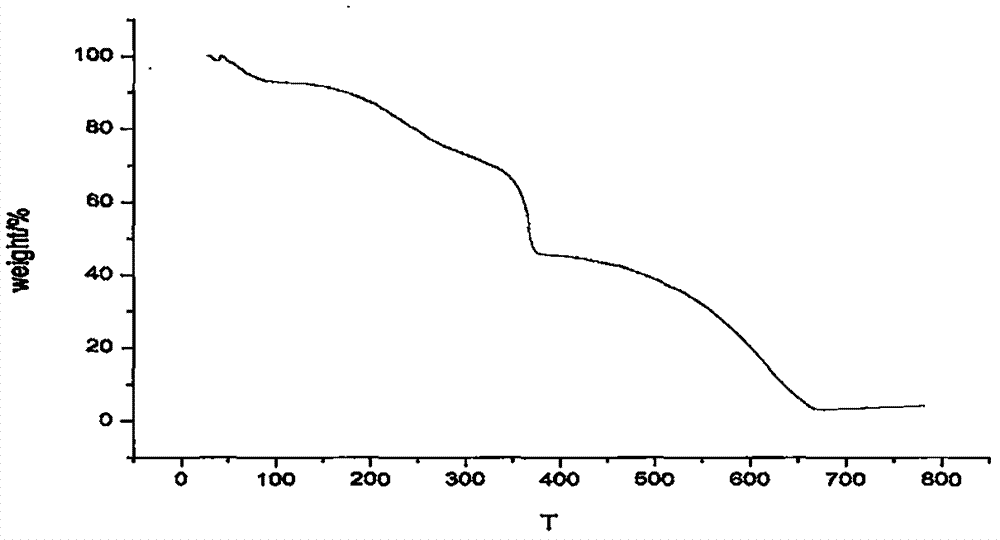
附图2是实施例1的热重图谱;
附图3是实施例1的氮气吸脱附等温线;
附图4是实施例1有机多孔聚合物的孔径分布曲线;
附图5是吸附时间和金属离子平衡吸附量的关系示意图;
附图6是ph对吸附性能的影响示意图;
附图7是温度对吸附性能的影响示意图。
具体实施方式
结合附图和具体实施例,对本发明作进一步说明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。此外应理解,在阅读了本发明讲授的内容之后,本领域技术人员可以对本发明作各种改动或修改,这些等价形式同样落于本申请所附权利要求书所限定的范围。
实施例1:
制备方法如下:
步骤1:称取2.5g三聚氰胺和4.0g间苯二甲醛溶于130的二甲亚砜中,搅拌至固体完全溶解;
步骤2:加热并不断搅拌,加热至50℃时通入n2,并持续一段时间排除体系内的原有气体;
步骤3:氮气保护、搅拌条件下在160℃下两种单体进行缩聚反应,加热回流,反应60h,冷却至室温,在反应过程中要不断的搅拌,并保持通冷凝水,以使挥发的dmso回流。
步骤4:将反应后的进行抽滤,抽滤所得固体用30ml的四氢呋喃进行洗涤3次、洗涤后的产物放入40℃烘箱中干燥12h,最终得有机多孔聚合物。
反应原理:
以三聚氰胺和间苯二甲醛为原料在dmso溶剂中发生schiff碱式反应,属于缩聚反应。该反应涉及到胺基和醛基的亲核加成、重排和消除等过程,生成亚胺(>c=n-)结构,dmso溶剂反应条件下,伯胺与亚胺的反应活性较其与醛的反应活性大,形成的亚胺双键继续被伯胺进攻,生成缩醛胺结构。在反应过程中,由于亲核加成反应为控速步骤,在亲核加成反应中,醛基上的c原子由sp2杂化变为sp3杂化,键角由120°变为109.5°,醛基上的c原子连接的基团为h原子和芳基,h原子较小的空间位阻和芳基的吸电子作用将使反应形成的过渡态更加稳定,利于反应的进行,三聚氰胺的结构使其伯胺-nh2基团上的n原子的负电荷较为集中,增强了三聚氰胺亲核反应的活性,有利于反应的进行。
由于间苯二甲醛在参与反应时,空间位阻更大,反应相对难以进行,而且反应是在热力学控制下,在反应初期,体系有利于形成更多的低聚物,随后以相对缓慢的速率链接形成微孔网状结构,更有利于微孔的形成与保持,以至于有更高的比表面积。
1、利用傅里叶红外光谱(ftir)对三聚氰胺和间苯二甲醛的产物有机多孔聚合物进行表征分析,如图1所示,3470cm-1处的峰是伯胺-nh2基团的伸缩振动峰及1650cm-1处的峰是伯胺-nh2基团的变形振动峰。红外光谱中发现2870cm-1(c-h伸缩振动峰)与1690cm-1(c=o伸缩振动峰)大幅消减,因此表面醛基和胺基之间发生了脱水缩合反应。另外图中1547cm-1与1476cm-1的吸收峰对应三聚氰胺中三嗪的c=n伸缩振动峰。综上所推断出该多孔材料中具有苯环与三嗪的结构,并且官能团醛基已经参与了反应,说明二者已经成功连接成一体。
2、热重分析,图2给出有机多孔聚合物的热重分析曲线,从图中可看出该材料的热失重可分为三个阶段:
在温度逐渐升至300℃过程中,此区域有明显的下降,主要是产品中的结合水与游离水的脱除,还可能是未洗涤干净的挥发性溶剂;
第二个阶段是300-400℃,此阶段失重最快,多孔材料在这个温度内失去大部分,多孔材料结构遭到破坏,尤其在360℃这个点快速下降,官能团快速分解,不断有小分子溢出;
第三阶段失重相对缓慢,产品逐渐碳化;
综上所述,由三聚氰胺与间苯二甲醛合成出的有机多孔聚合物具有较高的热稳定性,可应用于广泛的领域。
3、氮气的吸脱附表征:吸附过程一般包括微孔填充、单层-多层吸附和毛细管凝聚现象。
在相对压力p/po<0.1时微孔为主要吸附作用;在相对压力p/po>0.1时,吸附主要在介孔和大孔内发生。
从图3中我们可以看出该多孔材料在
p/po<0.1与p/po>0.1阶段都具有吸附量,这就说明合成出的多孔材料又具有微孔,又具有介孔和大孔。
在p/po<0.1时,氮气吸附量占总吸附量的25%左右,这就说明了有机多孔聚合物中具有不少的微孔。在0.6-0.9阶段存在毛细凝聚段,具有iv类等温线特征,说明材料中具有大量的介孔结构。
从图4中我们又可以分析出,有机多孔聚合物的孔径范围在1-77nm,孔径范围较宽,具有大量的微孔、介孔和大孔。
通过傅里叶红外光谱进行分析可知,有机多孔聚合物中具有苯环和三嗪的结构,并且官能团已经参与了反应,这说明二者已经成功连接成一体。从热重的图谱中可知合成出的有机多孔聚合物具有较高的热稳定性,这可广泛的应用于许多条件严格的领域。从氮气吸脱附等温线和孔径分布曲线可知,多孔材料具有丰富的微孔结构,且也具有一定量的介孔、大孔,bet比表面积为290.0565m2/g。因此,这种合成方法简单,原料廉价易得,对环境无害,且合成出的有机多孔聚合物对重金属离子具有很好的吸附效果,具有良好的应用前景。
实施例2:
有机多孔聚合物的制备方法,
步骤1:将2.6三聚氰胺和2.1g间苯二甲醛溶于130ml的二甲亚砜中,搅拌至固体完全溶解;
步骤2:加热并不断搅拌,加热至50℃时通入n2,并持续一段时间排除体系内的原有气体;
步骤3:氮气保护、搅拌条件下在180℃下两种单体进行缩聚反应,加热回流,反应48h,冷却至室温;
步骤4:将反应后的进行抽滤,抽滤所得固体依次使用20ml的四氢呋喃、二氯甲烷洗涤2次,干燥后得有机多孔聚合物,其性能表征结果在允许误差范围内与实施例1相同。
实施例3:
有机多孔聚合物的制备方法,
称取2.6g三聚氰胺和5.4g间苯二甲醛加入250ml的三口瓶中,加入180ml的二甲基亚砜,安装回流冷凝装置,室温下持续通n2,保持三口瓶内为n2氛围,在集热式磁力搅拌器中加热并不断搅拌,在130℃下反应80h,在反应过程中要不断的搅拌,并保持通冷凝水,以使挥发的dmso回流。待反应结束,将混合物冷至室温后抽滤,所得沉淀依次用25ml的丙酮、四氢呋喃、二氯甲烷洗涤2次,洗涤后的产物放入40℃烘箱中干燥,最终得白色粉末即为有机多孔聚合物,其性能表征结果在允许误差范围内与实施例1相同。
实施例4:
有机多孔聚合物在重金属吸附方面的应用,以pb2+为例:将待吸附溶液ph调至7,温度80℃,吸附时间2h。
1、探究吸附时间对吸附性能的影响,采用控制变量法,吸附剂0.1025g、pb2+初始浓度0.0100mol/l、体系ph为7、pb2+与缓冲溶液的总体积50ml,
由图5可知,有机多孔聚合物对水溶液中pb2+的吸附量随的增加而增大,当进行到2个小时,吸附已基本达到平衡,继续增加,吸附量增长的并不明显。在前1个小时内增长的很快,分析原因主要是因为在反应初始阶段,溶液中pb2+浓度很大,吸附剂表面有许多的有效吸附点位。而在反应后阶段,pb2+浓度越来越少,吸附剂表面的有效吸附点位也越来越少,pb2+需要长程扩散,经过吸附剂表面的孔进入到其内部与有效吸附点位结合,因此过程耗时长,吸附速率低。
2、探究ph值对吸附性能的影响,采用控制变量法,吸附剂0.1025g、pb2+初始浓度0.0100mol/l、吸附时间2h、pb2+与缓冲溶液的总体积50ml。
由图6可知,在吸附pb2+过程中,溶液的酸碱度起着非常重要的作用。本实验是在ph为4-8之间进行的,在ph为4-5之间平衡吸附量增加的特别快,在ph为5-7之间增加的较为快,ph为7-8之间基本不怎么增加了。在较低的ph环境下,溶液中含有大量h+,而h+与pb2+互相竞争与有机多孔聚合物表面的胺基、亚胺基结合,从而导致胺基、亚胺基质子化,无法与pb2+结合,所以吸附量比较低;但随着ph值得增大,胺基、亚胺基渐渐非质子化,故而能充分与pb2+结合,因此ph值为7时,吸附量最大,吸附性能最好。
3、温度对金属离子吸附的影响
探究温度对吸附性能的影响,采用控制变量法,吸附剂0.1025g、pb2+初始浓度0.0300mol/l、吸附时间2h、pb2+与缓冲溶液的总体积50ml。
由图7可知,在20℃的条件下,吸附2h的吸附实验中,吸光度已经有所下降,说明有机多孔聚合物的吸附反应正在进行,且有显著效果,在图中可以看出在该温度范围内吸附作用为下降的状态,且吸附作用明显,30℃以后吸附溶液吸光度下降速度增加,说明30℃以后有机多孔聚合物吸附效果比较好,随着温度的升高,有利于吸附反应的进行,随着待吸附溶液温度的升高,有利于吸附反应的进行,但由于考虑到溶液加热耗费能量较大,增加吸附成本,故将吸附温度控制在80℃。
实施例5:
有机多孔聚合物在重金属吸附方面的应用,以cu2+为例:将待吸附溶液ph调至5,温度70℃,吸附时间3h。
探究方法与实施例4相同,分析得到最佳吸附条件:吸附时间为3h,ph为5,随着带吸附溶液温度的升高,有利于吸附反应的进行,但由于考虑到溶液加热耗费能量较大,增加吸附成本,故将吸附温度控制在70℃。
- 还没有人留言评论。精彩留言会获得点赞!