一种HER2基因表达检测试剂盒及其检测方法与流程
本发明涉及基因检测领域,具体涉及到一种her2基因表达检测试剂盒及其检测方法。
背景技术:
研究发现her受体能够与其对应的配体、her家族其他受体或自身形成同源-异源二聚体而激活受体酪氨酸激酶的活性,从而激活并调控体内的多条信号转导通路,最终导致肿瘤的发生发展。her家族包含4个成员:her-1、her2、her-3和her-4。her2是一种原癌基因,可通过下游信号的转导参与肿瘤细胞增殖、凋亡、浸润及转移等的调控,与多种肿瘤的发生、发展及预后密切相关,成为肿瘤靶向治疗药物选择的一个重要靶点。her2是乳腺癌明确的预后指标和药物治疗效果的预测指标。24%~30%的原发性浸润性乳腺癌患者可以发现her2的基因扩增或her2蛋白的过度表达。her2阳性乳腺癌的侵袭性强,恶性程度高,her2阳性的乳腺癌的复发转移风险至少为中危或高危。在胃癌患者中有10-20%存在her2过表达现象,胃食管结合部腺癌中her2的阳性率相对更高。研究表明,her2的过表达与胃癌的分化程度、淋巴结转移及组织分型密切相关。膀胱癌组织中her2阳性表达率(72.60%)显著高于正常膀胱组织(7.69%)。
目前,已上市的以her2为靶点的分子靶向药物,主要包括抗her2单克隆抗体(曲妥珠单抗和帕妥珠单抗等)、小分子酪氨酸激酶抑制剂(拉帕替尼)以及药物耦联抗her2单克隆抗体(曲妥珠单抗-ematansine,trastuzumabemtansine,t-dm1)。目前her2阳性乳腺癌的标准治疗是以曲妥珠单抗为基础的治疗。全球有超过3000个患者参与的hera、bcirg006、ncctgn9831、nsabpmb-31四个大型前瞻性临床试验的长期随访结果均证实了曲妥珠单抗的使用能显著降低her2阳性乳腺癌患者的复发风险和死亡风险。美国综合癌症网(nccn)和中国cnccn乳腺癌临床实践指南都将曲妥珠单抗辅助治疗作为her2阳性乳腺癌术后标准治疗。fda也已批准了t-dm1作为her2阳性晚期乳腺癌患者二线治疗选择之一。
her2阳性状态是抗her2治疗的绝对必要条件,因此正确评价her2状态至关重要。目前国内外相关指南推荐her2检测的主要方法包括免疫组织化学法(ihc)和荧光原位杂交法(fish),推荐的主要流程为:一般可先经ihc检测;ihc3+为her2阳性,ihc0和1+为her2阴性;ihc2+为her2不确定病例,需进一步行her2基因扩增的fish检测。asco和cap已提出完善的her2检测指南,推荐对于新确诊的浸润性乳腺癌进行her2检测,但该指南同时也承认,在解释ihc和fish的her2检测结果时,偶尔也会出现一些模棱两可的类型,这说明her2的实际结果是连续的,而应不是ihc表现出的分类结果。临床试验中也发现,有的患者虽经ihc检测判断为her2阳性,但对曲妥珠单抗治疗并不敏感。这说明利用ihc方法通过检测her2表达来建议临床用药具有局限性。
技术实现要素:
本发明提供了检测her2基因表达的引物、探针。该引物、探针能够检测her2基因表达水平,灵敏度高,特异性强。
本发明还提供了一种her2基因表达检测试剂盒,该试剂盒能够快速、高效、准确检测her2基因表达水平。
本发明还提供了使用上述试剂盒检测her2基因表达的检测方法,该方法检测方法操作简便,灵敏度高,特异性高,检测结果真实可靠且易于推广等优点。
本发明包括如下内容:
所述的检测试剂盒包括针对her2基因mrna的引物及其相对应的探针,所述的引物如下:
her2-fo:tacctgcccaccaatgcc
her2-re:tcacttggttgtgagcgatga
所述的检测探针如下:
her2-pr:fam-ctgcaggatatccaggagg-mgb
优选地,所述的检测试剂盒包括针对her2基因mrna和内参calm2基因和b2m基因mrna检测的引物以及探针,所述的检测引物如下:
her2-fo:tacctgcccaccaatgcc
her2-re:tcacttggttgtgagcgatga
calm2-fo:ataaggatggcaatggctatattagt
calm2-re:ttccctgatcatttcatcaacttc
b2m-fo:acagcccaagatagttaagtggg
b2m-re:aagcagaatttggaattcatcca
所述的检测探针如下:
her2-pr:fam-ctgcaggatatccaggagg-mgb
calm2-pr:hex-cttcgccatgtgatgaca-mgb
b2m-pr:cy5-atgtaagcagcatcatgga-mgb。
优选地,所述的her2基因表达检测试剂盒包括her2基因探针引物混合液、酶混合液、阴性对照品、阳性对照品;
所述的her2引物探针混合液中0.2-1um引物、0.2-1um探针;
所述的酶混合液包括逆转录酶、dna聚合酶、0.25mmdntp、3mmmgcl2、pcrbuffer;
所述的阴性对照品为灭菌超纯水;
所述的阳性对照品为体外转录的her2基因、calm2基因和b2m基因片段rna混合液。
一种检测her2基因表达的方法,所述的检测方法包括使用her2基因表达的引物、探针或检测her2基因表达的试剂盒检测her2基因表达的步骤;
所述检测方法采用多重荧光定量pcr技术进行her2基因表达的检测,具体步骤如下:
步骤一、提取待检的肿瘤样本rna,作为检测模板;
步骤二、体系配制
根据待检测样本数(含1个阳性对照和1个阴性对照),计算并配制反应混合液,将配制好的检测反应液分别分装到八联pcr反应管;
步骤三、分别将待检样本、阳性对照品、阴性对照品加入到对应pcr反应管中;
步骤四、进行多重荧光定量pcr检测,多重pcr扩增程序为:50℃10分钟;94℃10分钟;94℃30秒,60℃30秒收集荧光信号,40个循环;
步骤五、检测数据分析
her2基因定量结果以40-δδcq公式进行处理,获得代表每个患者样本her2基因表达水平的分值。
本发明的具体组分见下表:
与现有技术相比,本发明有以下优点:
1、所需样本量少,使用多重荧光pcr技术进行检测,含有内控系统,能更加准确、稳定地对样本进行检测,确保结果真实可信;
2、较ihc更加敏感可靠,可以连续定量检测rna,实现自动化、人为误差较小,且操作简便、经济省时、可批量操作,结果判读简单客观,便于分析,比ihc方法更具优越性。
附图说明
为了更清楚地说明本发明实施例或现有技术中的技术方案,下面将对实施例或现有技术描述中所需要使用的附图作简单地介绍,显而易见地,下面描述中的附图仅仅是本发明的一些实施例,对于本领域普通技术人员来讲,在不付出创造性劳动性的前提下,还可以根据这些附图获得其他的附图。
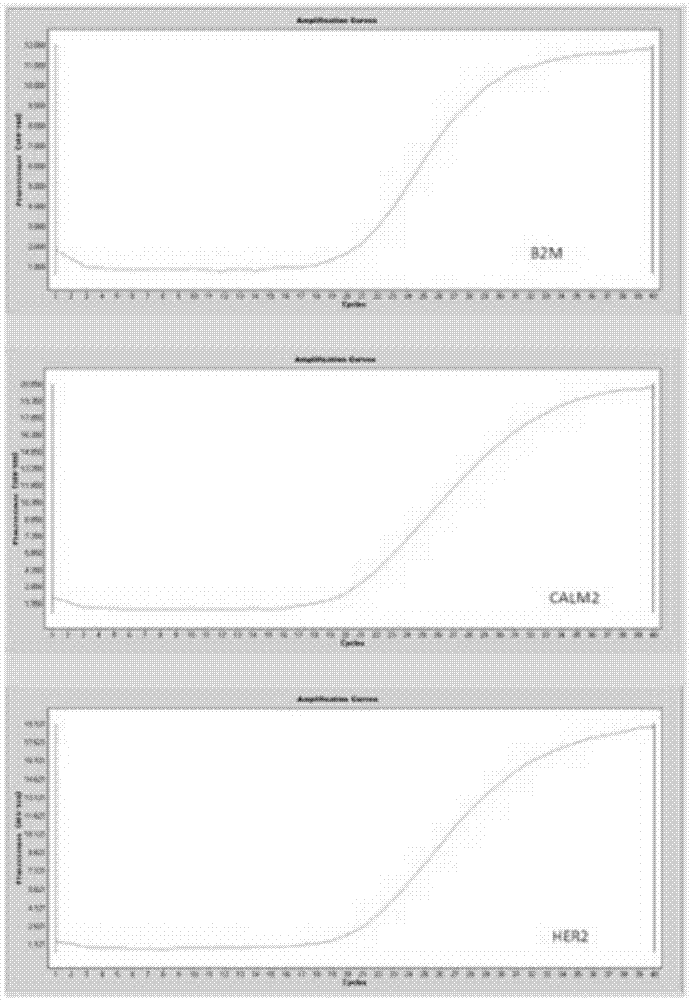
图1为本发明实施例3中阳性对照品检测图。
图2为本发明实施例3中肿瘤ffpe组织rna样本her2基因表达水平检测图;
图3为本发明实施例3中肿瘤ffpe组织免疫组化图。
具体实施方式
以下结合附图和具体实施例来详细说明本发明,以下实施例中如无特殊说明,所使用原料来源于市售,所采用方法均为本领域技术人员公知的常规操作方法。
实施例1一种检测her2基因表达的试剂盒
根据目标基因序列设计特异性引物,设计的引物和探针可以按照现有方法进行人工合成。具体引物如下所示:
her2-fo:tacctgcccaccaatgcc
her2-re:tcacttggttgtgagcgatga
calm2-fo:ataaggatggcaatggctatattagt
calm2-re:ttccctgatcatttcatcaacttc
b2m-fo:acagcccaagatagttaagtggg
b2m-re:aagcagaatttggaattcatcca
her2-pr:fam-ctgcaggatatccaggagg-mgb
calm2-pr:hex-cttcgccatgtgatgaca-mgb
b2m-pr:cy5-atgtaagcagcatcatgga-mgb
本发明提供的一种her2基因表达检测试剂盒包含以下四组分,分别为:
her2引物混合液:包含用于检测her2、calm2和b2m基因表达的特异性引物和探针。引物和探针为如上所述序列。
酶混合液包括逆转录酶、dna聚合酶、pcrbuffer、mgcl2和dntps。
阳性对照品为体外转录的her2基因、calm2基因和b2m基因片段rna混合液;阴性对照品为灭菌超纯水。
实施例2her2基因表达检测方法
采用本发明实施例1的试剂盒检测her2基因表达,包括以下步骤:
(1)待测样本处理和模板提取;
取石蜡包埋肿瘤组织按照提取试剂盒说明书提取rna。提取的rna稀释到20ng/μl后作为pcr扩增模板。
(2)体系配制
将试剂盒中所有组分冰上融化,根据待检测样本数,计算并配制pcr反应混合液(见表2)。
表2pcr反应液配制公式
将pcr反应工作液按20μl/孔加入到pcr反应管,将待检样本rna、阳性对照品和阴性对照品分别以5μl/孔加入到对应pcr反应管中,进行pcr扩增。
(3)pcr扩增
pcr扩增程序见表3
表3pcr扩增程序
(4)结果判定
阈值设定:根据不同机型设定阈值。ct值确定:选择阳性对照品反应管,阴性对照品和样品反应管一并划定阈值,得到her2和内参cq值。
.阴性无模板空白对照(ntc)应无扩增曲线升起;
her2基因定量结果以40-δδcq公式进行处理,获得代表每个患者样本her2基因表达水平的分值
δδcq=δcq样本-δcq阳性对照品
δcq样本=cq样本her2-cq样本calm2+b2m平均值
δcq阳性对照=cq阳性对照her2-cq阳性对照calm2+b2m平均值
40-δδcq≥40阳性,her2基因表达阳性
40-δδcq<40阴性,her2基因表达阴性
实施例3检测方法的实际应用
采用本发明试剂盒和检测方法检测肿瘤患者her2基因表达,方法如下:
(1)待检样本的处理
一例肿瘤ffpe组织采用
(2)体系配制
将试剂盒中所有组分冰上融化,根据待检测样本数,计算并配制pcr反应混合液(见表4)。
表4pcr反应液配制表
将pcr反应工作液按20μl/孔加入到pcr反应管,将待检的肿瘤ffpe组织rna、阳性对照品和阴性对照品分别以5μl/孔加入到对应pcr反应管中,进行pcr扩增。
(3)pcr扩增
pcr扩增程序见表5
表5pcr扩增程序
(4)结果分析
阳性对照品及肿瘤ffpe组织样本检测结果见图1-2,具体检测cq见表6。根据公式计算40-δδcq=40-(δcq样本-δcq阳性对照品)=40-(-3.66)=43.66>40
根据40-δδcq值判定该样本为her2阳性,结果与免疫组化结果符合。
表6检测cq值
此外,需要说明的是,本说明书中所描述的具体实施例,其原料试剂名称等可以不同。凡依本发明专利构思所述的原理所做的等效或简单变化,均包括于本发明专利的保护范围内。本发明所属技术领域的技术人员可以对所描述的具体实施例做各种各样的修改或补充或采用类似的方式替代,只要不偏离本发明的结构或者超越本权利要求书所定义的范围,均应属于本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 大豆低温诱导人工合成启动子SP5及应用的制造方法与工艺
- 一种棒状杆菌组成型表达载体启动子、含有该启动子及gnd基因的表达载体的制造方法与工艺
- 一种棒状杆菌组成型表达载体启动子、含有该启动子及lrp基因的表达载体的制造方法与工艺
- 一种二值卷积神经网络处理器及其使用方法与流程
- 检测NUP214‑ABL1基因相对表达量的试剂盒和方法与流程
- 环介导的级联放大策略用于高灵敏检测DNA甲基转移酶活性的制造方法与工艺
- 一种基于高压静电场来促进作物优质高效安全生产的嫁接方法与流程
- 一种酶性DNA机器用于miRNA检测的方法与流程
- 转基因玉米MON87403品系特异性实时荧光PCR检测引物、探针、方法和试剂盒与流程
- 葡萄早熟基因VvWRKY13在调控植物中乙烯生物合成中的应用的制造方法与工艺