叔胺类阳离子脂质衍生物及其在RNA药物递送系统的应用的制作方法
本发明涉及化学与制剂领域,具体涉及叔胺类阳离子脂质衍生物及其在rna药物递送系统的应用。
背景技术:
rna药物是在蛋白水平上游的rna水平调控生物通路从而发挥治疗作用的一类药物,已经成为继化学药物、生物蛋白药物之后的第三大新型药物。基于rna干扰技术的sirna药物是目前rna药物在临床上最主流的类型。通过小干扰rna(smallinterferingrna,sirna)特异性地作用于靶细胞内的同源mrna序列,促使其降解,从而阻断相关基因的表达,具有选择性强,毒性低等优点。这种选择性基因沉默具有治疗各种疾病的潜力,如病毒感染,癌症和自身免疫性疾病等。但是,sirna在生理环境下不稳定,在血液循环中易被血浆中的核酸酶降解,易被肾小球过滤而排出体外,易被网状内皮系统(res)清除。另外,sirna是亲水的负电性双链rna,难以跨过细胞膜到达胞质发挥作用。因此,rna干扰疗法的主要挑战是构建满足治疗需求的sirna递送载体。
与病毒载体相比,非病毒载体具有无免疫原性,不限制载体容量,化学结构可控,以及可大量制备等优点,因此受到越来越多的关注。其中,阳离子脂质体是一种类似于生物膜的具有双分子层结构的封闭囊泡,由阳离子脂质分子和辅助脂质(如磷脂,胆固醇等)制备而成,可利用其正电性与负电性的rna药物形成稳定复合物用于rna药物的递送,是rna治疗领域应用最广泛的一种非病毒载体。由alnylampharmaceuticals公司研发的rna干扰新药patisiran(aln-ttr02)就是以阳离子脂质体为递送载体,用于治疗转甲状腺素相关淀粉样变性。这是首个顺利完成三期临床试验的rna干扰药物,已于2018年8月11日获得fda批准上市。
尽管已经报道大量阳离子脂质体用于细胞水平和动物水平的rna药物递送研究,但是在实际应用中仍然存在着一系列科学问题,其中阳离子脂质体的安全性和低转染效率是限制阳离子脂质体在临床上广泛应用的关键问题,这些问题都与阳离子脂质分子的化学结构密切相关。因此,本发明通过设计新型的阳离子脂质解决上述问题。
针对阳离子脂质体的安全性问题,本发明选择叔胺片段作为阳离子脂质分子的亲水部分,与伯胺结构相比,虽然叔胺结构同样具有正电性,但在正常生理条件下其正电性弱于伯胺,可以减少正电性相关的体内毒性;并选择氨基酸作为阳离子脂质分子的骨架,在一定程度上提高其生物相容性;同时选择生物可降解的酯键为阳离子脂质分子的连接键,以提高其生物可降解性。通过三种不同片段分子的选择,最终提高了阳离子脂质及其相应脂质体的体内安全性,有利于临床上进一步推广应用。而针对目前阳离子脂质体转染效率低的问题,本发明同样利用叔胺片段细胞溶酶体弱酸性环境中的质子海绵作用,促进rna药物脂质体从溶酶体逃逸进入细胞质,从而提高阳离子脂质体的转染效率;并选择与细胞膜具有高亲和力的烷烃结构作为阳离子脂质分子的疏水部分,进一步提高阳离子脂质体跨过细胞膜的能力,最终提高阳离子脂质体的转染效率。
本发明的阳离子脂质分子及其所制备的阳离子脂质体具有高转染效率和低细胞毒性的特点,在一定程度上解决了目前临床上应用的阳离子脂质体存在的转染效率低和安全性隐患,这对于开发具有我国自主知识产权的生物功能载体材料具有重要意义。
技术实现要素:
本发明公开一种叔胺类阳离子脂质衍生物,具有通式(i)或(ii)的结构。
其中,
n=1或2;
m代表1-4的整数;
r1=
p代表2-4的整数,q代表1-3的整数,r代表1-2的整数,s代表0-3的整数,r5代表甲基、羟甲基、乙基、羟乙基、正丙基、异丙基、正丁基、异丁基或叔丁基,r6代表甲基、乙基或苄基,r7代表吡啶基、吡嗪基、嘧啶基、哒嗪基、吡咯基、吡唑基或咪唑基;
其中,叔胺片段作为阳离子脂质分子的亲水部分,一方面为所制备的脂质体提供正电荷,与负电性rna药物通过静电相互作用,自组装形成稳定的阳离子脂质体/rna二元复合物,保护荷载的rna药物不被核酸酶降解,提高rna药物在血液循环中的稳定性,同时二元复合物的纳米级粒径和表面多余的正电荷有利于提高细胞摄取;另一方面在溶酶体偏酸性的环境,叔胺片段质子化从而发挥质子海绵作用帮助sirna药物脂质体实现溶酶体逃逸,克服胞内屏障将所载sirna递送到胞质,从而提高阳离子脂质体的转染效率。此外,叔胺片段作为阳离子脂质分子的亲水部分而非伯胺结构,可以使所制备的阳离子脂质体稳定包载sirna的同时表现出较低的表面电位,从而降低阳离子脂质体的细胞毒性。
氨基酸作为阳离子脂质分子的骨架,可增强阳离子脂质体的生物相容性。通式(i)的骨架是谷氨酸(或天冬氨酸),可连接两条疏水链,通式(ii)的骨架是甘氨酸(或苯丙氨酸,丙氨酸,缬氨酸,亮氨酸,异亮氨酸,色氨酸,蛋氨酸,脯氨酸,丝氨酸,丝氨酸,天冬酰胺,谷氨酰胺,酪氨酸),可连接一条疏水链。并且通过一段疏水性短链(丙二酸-葵二酸)连接亲水部分和骨架部分。
阳离子脂质分子的连接键为生物可降解的酯键,体内可被酯酶水解,从而赋予阳离子脂质生物可降解性。
以烷烃结构(正辛醇-正二十醇或胆固醇)作为阳离子脂质分子的疏水部分,利用其与细胞膜的高度亲和力,有利于促进阳离子脂质体跨过细胞膜。
本发明提供一种上述叔胺类阳离子脂质衍生物的合成方法。该合成方法不涉及保护脱保护步骤,高效快捷,通用性好,收率高,合成成本低,合成过程环境友好,适宜工业化放大生产。
1)通式i所示阳离子脂质衍生物的合成方法,其合成步骤如下:
a.将二元羧基氨基酸(i-1)溶解于无水甲苯(或苯,或环己烷),搅拌下加入对甲基苯磺酸,升温至110~150℃,回流反应1~3h。冷却至室温,加入脂肪醇,升温至100~150℃,回流反应6~20h。反应结束后,旋蒸除去甲苯(或苯,或环己烷),浓缩后溶解于氯仿(或二氯甲烷,或乙酸乙酯),用饱和碳酸氢钠(或碳酸钠,或碳酸钾)水溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,抽滤后浓缩,用甲醇(或乙醇,或丙酮)重结晶,得到脂肪醇-二元羧基氨基酸(i-2)。
脂肪醇-二元羧基氨基酸(i-2)合成反应式:
b.将二元酸溶解于二氯甲烷(或四氢呋喃,或氯仿),放置于0℃,搅拌下依次加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc.hcl),4-二甲氨基吡啶(dmap)和脂肪醇-二元羧基氨基酸(i-2),转移至室温,搅拌下反应6~20h。反应结束后,依次用水,10%柠檬酸水溶液和饱和食盐水洗涤反应液,无水硫酸钠干燥,抽滤后浓缩,用甲醇(或乙醇,或丙酮)重结晶,得到羧基化-脂肪醇-二元羧基氨基酸(i-3)。
羧基化-脂肪醇-二元羧基氨基酸(i-3)合成反应式:
c.将羧基化-脂肪醇-二元羧基氨基酸(i-3)溶解于氯仿(或四氢呋喃,或二氯甲烷),放置于0℃,搅拌下依次加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc.hcl)和1-羟基苯并三唑(hobt),转移至室温,搅拌下反应1~3h。将r1h和三乙胺溶解于氯仿(或四氢呋喃,或二氯甲烷),搅拌下室温反应1~3h。再将两个反应体系混合,搅拌下室温反应6~20h。反应结束后,依次用水,10%柠檬酸水溶液和饱和食盐水洗涤反应液,无水硫酸钠干燥,抽滤后浓缩,经过二氯甲烷/甲醇柱层析,得到叔胺-羧基化-脂肪醇-二元羧基氨基酸(i)。
叔胺-羧基化-脂肪醇-二元羧基氨基酸(i)合成反应式:
2)通式ii所示阳离子脂质衍生物的合成方法,其合成步骤如下:
a.将单羧基氨基酸(ii-1)溶解于无水甲苯(或苯,或环己烷),搅拌下加入对甲基苯磺酸,升温至110~150℃,回流反应1~3h。冷却至室温,加入脂肪醇,升温至100~150℃,回流反应6~20h。反应结束后,旋蒸除去甲苯(或苯,或环己烷),浓缩后溶解于氯仿(或二氯甲烷,或乙酸乙酯),用饱和碳酸氢钠(或碳酸钠,或碳酸钾)水溶液洗涤,饱和食盐水洗涤,无水硫酸钠干燥,抽滤后浓缩,用甲醇(或乙醇,或丙酮)重结晶,得到脂肪醇-单羧基氨基酸(ii-2)。
脂肪醇-单羧基氨基酸(ii-2)合成反应式:
b.将二元酸溶解于二氯甲烷(或四氢呋喃,或氯仿),放置于0℃,搅拌下依次加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc.hcl),4-二甲氨基吡啶(dmap)和脂肪醇-单羧基氨基酸(ii-2),转移至室温,搅拌下反应6~20h。反应结束后,依次用水,10%柠檬酸水溶液和饱和食盐水洗涤反应液,无水硫酸钠干燥,抽滤后浓缩,用甲醇(或乙醇,或丙酮)重结晶,得到羧基化-脂肪醇-单羧基氨基酸(ii-3)。
羧基化-脂肪醇-单羧基氨基酸(ii-3)合成反应式:
c.将羧基化-脂肪醇-单羧基氨基酸(ii-3)溶解于氯仿(或四氢呋喃,或二氯甲烷),放置于0℃,搅拌下依次加入1-乙基-(3-二甲基氨基丙基)碳酰二亚胺盐酸盐(edc.hcl)和1-羟基苯并三唑(hobt),转移至室温,搅拌下反应1~3h。将r1h和三乙胺溶解于氯仿(或四氢呋喃,或二氯甲烷),搅拌下室温反应1~3h。再将两个反应体系混合,搅拌下室温反应6~20h。反应结束后,依次用水,10%柠檬酸水溶液和饱和食盐水洗涤反应液,无水硫酸钠干燥,抽滤后浓缩,经过二氯甲烷/甲醇柱层析,得到叔胺-羧基化-脂肪醇-单羧基氨基酸(ii)。
叔胺-羧基化-脂肪醇-单羧基氨基酸(ii)合成反应式:
本发明公开的空白阳离子脂质体含有权利要求1的阳离子脂质衍生物和常用脂质,其特征是具有20~300nm的平均粒径,+10~+50mv的表面电位。其中常用脂质为二油酰基磷脂酰乙醇胺(dope),二硬脂酰基磷脂酰乙醇胺(dspe),二硬脂酰基磷脂酰胆碱(dspc),1-棕榈酰基-2-油酰基卵磷脂(popc),二油酰基卵磷脂(dopc),二芥酰基卵磷脂(depc),二棕榈酰基卵磷脂(dppc)和胆固醇等,优选dope和胆固醇。其中阳离子脂质衍生物和常用脂质的摩尔比为5:1~1:5,优选2:1~1:2。
本发明公开的空白阳离子脂质体制备方法包括:薄膜分散法,过膜挤压发,french挤压法,逆向蒸发法和化学梯度法。空白阳离子脂质体制备方法优选薄膜分散法。
采用薄膜分散法制备空白阳离子脂质体的过程如下:称取适量磷脂,胆固醇和阳离子脂质的一种或多种,溶于氯仿/甲醇混合溶剂,减压蒸发成膜,真空干燥过夜除去残留的有机溶剂。室温下水化脂膜,将得到的脂质体混悬液采用超声波细胞粉碎机分散,并且依次通过0.8μm,0.45μm,0.22μm微孔滤膜,即得到空白阳离子脂质体溶液。
本发明公开的rna药物脂质体,含有rna药物和权利要求4的空白阳离子脂质体,其特征是具有50~600nm的平均粒径,+5~+40mv的表面电位。其中rna药物为寡核苷酸、sirna、shrna、microrna和mrna等,优选sirna。其中阳离子脂质衍生物和rna药物的氮磷比为1:1~10:1,优选3:1~7:1。
本发明公开的rna药物脂质体的制备过程如下:将上述制备得到的空白阳离子脂质体和rna药物按一定氮磷比(1:1~10:1)混合,室温静置15~120min,即得到rna药物脂质体。
本发明公开的rna药物脂质体能稳定荷载sirna(见实施例25)。本发明的阳离子脂质体/egfp-sirna二元复合物能高效转染hela-egfp细胞而产生显著的基因沉默效果(见实施例27),基因沉默效果优于阳性对照lipofectamine2000,同时基因沉默效果不受血清的影响(见实施例28),并且对hela细胞不产生明显毒性(见实施例26),通过初筛实验筛选出转染效率高和细胞毒性低的阳离子脂质体a13。进一步通过体外westernblot和q-pcr测试,本发明的阳离子脂质体a13/apob-sirna二元复合物能显著降低hepg2细胞中apob-mrna的含量和apob蛋白的表达量,效果与阳性对照lipofectamine2000相当(见实施例30),并且对hepg2细胞不产生明显毒性(见实施例29)。本发明的阳离子脂质体a13/survivin-sirna二元复合物能显著降低mcf-7细胞中survivin-mrna的含量和survivin蛋白的表达量,效果与阳性对照lipofectamine2000相当(见实施例32),并且对mcf-7细胞不产生明显毒性(见实施例31)。
本发明的创新之处是针对阳离子脂质体转染效率低和细胞毒性大的问题对阳离子脂质分子进行化学结构设计,筛选出高转染效率和低细胞毒性的阳离子脂质体。本发明可为临床提供转染效率高,细胞毒性小的rna药物递送载体。
附图说明
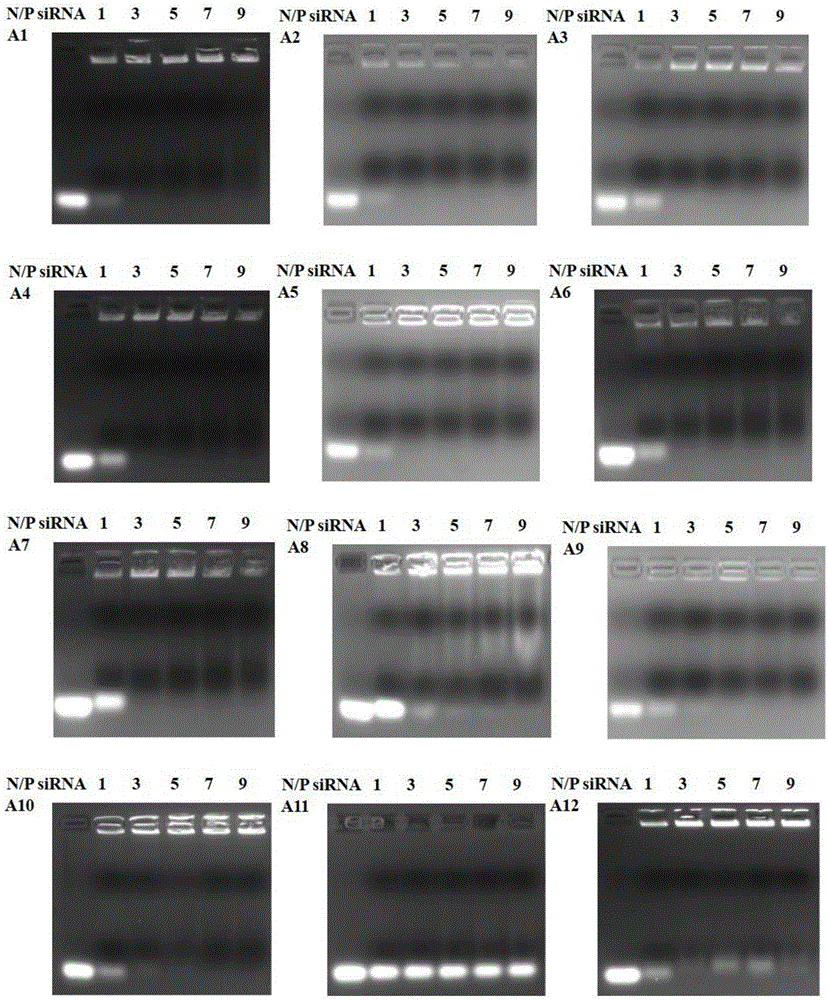
图1是本发明的阳离子脂质体/乱序sirna二元复合物的琼脂糖凝胶电泳图;
图2是本发明的阳离子脂质体/乱序sirna二元复合物在不同氮磷比下的粒径和电位;
图3是本发明的阳离子脂质体/egfp-sirna二元复合物对hela-egfp细胞存活率的影响;
图4是本发明的阳离子脂质体/egfp-sirna二元复合物转染hela-egfp细胞的基因沉默效果(比例尺:100μm);
图5是倒置荧光显微镜观察本发明的阳离子脂质体egfp-sirna二元复合物转染hela-egfp细胞后绿色荧光蛋白的表达情况;
图6是本发明的阳离子脂质体/egfp-sirna二元复合物在血清存在下转染hela-egfp细胞的基因沉默效果(比例尺:100μm);
图7是倒置荧光显微镜观察本发明的阳离子脂质体/egfp-sirna二元复合物在血清存在下转染hela-egfp细胞后绿色荧光蛋白的表达情况;
图8是本发明的阳离子脂质体a13/apob-sirna二元复合物对hepg2细胞存活率的影响;
图9是本发明的阳离子脂质体a13/apob-sirna二元复合物转染hepg2细胞后细胞中apob-mrna的表达水平;
图10是本发明的阳离子脂质体a13/apob-sirna二元复合物转染hepg2细胞后细胞表达apob蛋白的情况。
图11是本发明的阳离子脂质体a13/乱序sirna二元复合物对mcf-7细胞存活率的影响;
图12是本发明的阳离子脂质体a13/survivin-sirna二元复合物转染mcf-7细胞后细胞中survivin-mrna的表达水平;
图13是本发明的阳离子脂质体a13/survivin-sirna二元复合物转染mcf-7细胞后细胞表达survivin蛋白的情况。
具体实施方式
通过以下实施例对本发明进一步解释,但这些实施例不对本发明构成任何限制。
实施例1
制备谷氨酸双十四醇酯(ta2-glu),化学结构式如下:
将l-谷氨酸(20.00g,135.9mmol)溶解于500ml无水甲苯,搅拌下加入对甲基苯磺酸(28.45g,149.6mmol),升温至140℃,回流反应2h。冷却至室温,加入十四醇(61.2g,285.5mmol),升温至150℃,回流反应过夜。反应结束后,旋蒸除去甲苯,得到黄色油状物。溶解于400ml氯仿,用饱和碳酸氢钠水溶液洗涤(400ml×2),饱和食盐水洗涤(400ml×1),无水硫酸钠干燥,抽滤后浓缩得到黄色油状物,用甲醇重结晶两次(200ml×2),得到白色固体40.77g,收率:56%。
1hnmr(300mhz,cdcl3):δ(ppm)4.11(t,j=6.8hz,2h,cooch2),4.07(t,j=6.8hz,2h,cooch2),3.52–3.43(m,1h,nh2ch),2.46(t,j=7.6hz,2h,ch2co),2.15–2.01(m,1h,nh2chch2),1.92–1.80(m,1h,nh2chch2),1.68–1.58(m,4h,cooch2ch2),1.33–1.23(m,44h,ch2(myristoyl)),0.88(t,j=6.9hz,6h,ch2ch3).hrms,esi+,m/z:calcdforc33h66no4[m+h]+,540.4914;found,540.5006.
实施例2
制备羧基化谷氨酸双十四醇酯(ta2-glu-cooh),化学结构式如下:
将谷氨酸双十四醇酯(40.77g,75.6mmol)溶解于四氢呋喃/二氯甲烷(150ml:150ml)混合溶剂,搅拌下加入丁二酸酐(11.34g,113.3mmol),室温反应过夜。反应结束后,旋蒸除去溶剂,得到白色固体。用甲醇重结晶两次(150ml×2),得到白色固体40.23g,收率:83%。1hnmr(300mhz,cdcl3):δ(ppm)6.62(d,j=7.8hz,1h,nh),4.66–4.56(m,1h,nhch),4.13(t,j=6.8hz,2h,cooch2),4.06(t,j=6.8hz,2h,cooch2),2.75–2.65(m,2h,coohch2),2.56(t,j=6.5hz,2h,ch2coo),2.46–2.33(m,2h,ch2conh),2.25–2.13(m,1h,nhchch2),2.07–1.93(m,1h,nhchch2),1.68–1.56(m,4h,cooch2ch2),1.33–1.23(m,44h,ch2(myristoyl)),0.88(t,j=6.7hz,6h,ch2ch3).13cnmr(75mhz,cdcl3):δ(ppm)176.27(1c,cooh),173.08(1c,conhch),171.92(1c,ch2cooch2),171.79(1c,nhchco),65.94(1c,cooch2),65.07(1c,cooch2),51.91(1c,nhch),31.90(2c,ch2ch2ch3),30.56(1c,ch2cooch2),30.28(1c,coohch2),29.63(8c,ch2(myristoyl)),29.57(2c,ch2(myristoyl)),29.51(1c,ch2(myristoyl)),29.48(1c,ch2(myristoyl)),29.33(2c,ch2(myristoyl),1c,nhchch2),29.25(1c,ch2(myristoyl)),29.19(1c,ch2(myristoyl)),28.56(1c,och2ch2),28.47(1c,och2ch2),27.37(1c,coohch2ch2),25.87(1c,och2ch2ch2),25.79(1c,och2ch2ch2),22.65(2c,ch2ch3),14.06(2c,ch2ch3).hrms,esi+,m/z:calcdforc37h70no7[m+h]+,640.5074;found,640.5127.
实施例3
制备化合物a1,化学结构式如下:
将羧基化谷氨酸双十四醇酯(484mg,0.757mmol)溶解于25ml氯仿并放置于0℃,搅拌下依次加入edci(232mg,1.211mmol)和hobt(164mg,1.211mmol)。加料完毕后转移至室温搅拌3h,得反应液a;将n,n-二甲基乙二胺(83μl,0.757mmol)溶解于10ml氯仿,搅拌下加入三乙胺(316μl,2.270mmol),室温搅拌1h,得反应液b。将反应液b缓慢滴入反应液a,室温搅拌过夜。反应结束后,用适量水洗涤两次,适量10%柠檬酸水溶液洗涤两次,适量饱和食盐水洗涤一次,无水硫酸钠干燥,抽滤浓缩后得到黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=20︰1)得到黄色颗粒状固体210mg,收率:39%。1hnmr(300mhz,cdcl3):δ(ppm)7.99(brs,1h,nhcoch2),7.38(d,j=7.5hz,1h,conhch),4.59–4.47(m,1h,nhch),4.10(t,j=6.6hz,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.68(brs,2h,ch2ch2nh),3.31(brs,2h,ch2ch2nh),2.92(s,6h,(ch3)2n),2.80–2.66(m,2h,nhcoch2),2.65–2.57(m,2h,ch2coo),2.48–2.38(m,2h,ch2conh),2.22–2.11(m,1h,nhchch2),2.08–1.97(m,1h,nhchch2),1.67–1.57(m,4h,cooch2ch2),1.33–1.24(m,44h,ch2(myristoyl)),0.88(t,j=6.8hz,6h,ch2ch3).13cnmr(75mhz,cdcl3):δ(ppm)174.13(1c,nhcoch2),173.17(1c,conhch),172.96(1c,ch2cooch2),172.28(1c,nhchco),65.79(1c,cooch2),64.97(1c,cooch2),57.35(1c,(ch3)2nch2),51.95(1c,nhch),43.65(2c,(ch3)2n),31.92(2c,ch2ch2ch3),31.35(1c,(ch3)2nch2ch2),31.00(1c,ch2cooch2),30.38(1c,nhcoch2ch2),29.71(8c,ch2(myristoyl)),29.66(2c,ch2(myristoyl)),29.58(2c,ch2(myristoyl)),29.36(4c,ch2(myristoyl),1c,nhchch2),28.58(1c,och2ch2),28.49(1c,och2ch2),27.00(1c,coch2ch2co),25.91(1c,och2ch2ch2),25.88(1c,och2ch2ch2),22.68(2c,ch2ch3),14.10(2c,ch2ch3).hrms,esi+,m/z:calcdforc41h80n3o6[m+h]+,710.5969;found,710.5986.
实施例4
制备化合物a2,化学结构式如下:
标题化合物a2以羧基化谷氨酸双十四醇酯(540mg,0.844mmol)和3-二甲胺基丙胺(107μl,0.844mmol)为原料,按照制备a1的方法,得到粗产物粉红色固体,经柱层析纯化(二氯甲烷︰甲醇=30︰1)得到黄白色颗粒状固体313mg,收率:51%。1hnmr(300mhz,cdcl3):δ(ppm)7.41(brs,1h,nhcoch2),6.96(d,j=7.2hz,1h,conhch),4.55–4.51(m,1h,nhch),4.11(t,j=6.7hz,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.41–3.32(m,2h,(ch3)2nch2ch2ch2),2.88(t,j=6.7hz,2h,nhcoch2),2.62(s,6h,(ch3)2n),2.59–2.49(m,2h,ch2coo,2h,(ch3)2nch2),2.44–2.33(m,2h,ch2conh),2.24–2.11(m,1h,nhchch2),2.07–1.96(m,1h,nhchch2),1.96–1.89(m,2h,(ch3)2nch2ch2),1.67–1.56(m,4h,cooch2ch2),1.34–1.22(m,44h,ch2(myristoyl)),0.88(t,j=6.8hz,6h,ch2ch3).13cnmr(75mhz,cdcl3):δ(ppm)172.82(1c,nhcoch2),172.58(1c,conhch),172.24(1c,ch2cooch2),171.93(1c,nhchco),65.69(1c,cooch2),64.89(1c,cooch2),56.43(1c,(ch3)2nch2ch2ch2),51.85(1c,nhch),43.78(2c,(ch3)2n),37.08(1c,(ch3)2nch2ch2ch2),31.86(2c,ch2ch2ch3),31.37(1c,ch2cooch2),30.31(1c,nhcoch2ch2),29.60(8c,ch2(myristoyl)),29.55(2c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.46(1c,ch2(myristoyl)),29.29(2c,ch2(myristoyl),1c,nhchch2),29.23(1c,ch2(myristoyl)),29.18(1c,ch2(myristoyl)),28.56(1c,och2ch2),28.47(1c,och2ch2),27.26(1c,coch2ch2co),25.86(1c,och2ch2ch2),25.78(1c,och2ch2ch2),25.03(1c,(ch3)2nch2ch2),22.62(2c,ch2ch3),14.04(2c,ch2ch3).hrms,esi+,m/z:calcdforc42h82n3o6[m+h]+,724.6125;found,724.6164.
实施例5
制备化合物a3,化学结构式如下:
标题化合物a3以羧基化谷氨酸双十四醇酯(544mg,0.851mmol)和n,n-二乙基乙二胺(120μl,0.851mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=30︰1)得到黄白色固体254mg,收率:41%。1hnmr(300mhz,cdcl3):δ(ppm)6.79(d,j=7.2hz,1h,conhch),6.52(brs,1h,nhcoch2),4.63–4.53(m,1h,nhch),4.12(t,j=6.8hz,2h,cooch2),4.05(t,j=6.8hz,2h,cooch2),3.38–3.28(m,2h,(ch3ch2)2nch2ch2),2.63–2.54(m,6h,(ch3ch2)2nch2,2h,nhcoch2ch2),2.49–2.30(m,2h,ch2conh,2h,ch2coo),2.26–2.12(m,1h,nhchch2),2.05–1.91(m,1h,nhchch2),1.70–1.55(m,4h,cooch2ch2),1.40–1.20(m,44h,ch2(myristoyl)),1.04(t,j=7.2hz,6h,ch2ch3),0.88(t,j=6.8hz,6h,ch2ch3(myristoyl)).13cnmr(75mhz,cdcl3):δ(ppm)172.83(1c,nhcoch2),172.11(1c,conhch),171.89(1c,ch2cooch2,1c,nhchco),65.72(1c,cooch2),64.91(1c,cooch2),51.77(1c,nhch),51.47(1c,(ch3ch2)2nch2),46.70(1c,(ch3ch2)2nch2ch2),36.78(2c,ch2ch3),31.91(2c,ch2ch2ch3),31.52(1c,ch2cooch2),30.30(1c,coch2ch2co),29.64(8c,ch2(myristoyl)),29.58(2c,ch2(myristoyl)),29.52(1c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.34(2c,ch2(myristoyl),1c,nhchch2),29.27(1c,ch2(myristoyl)),29.21(1c,ch2(myristoyl)),28.59(1c,och2ch2),28.49(1c,och2ch2),27.44(1c,coch2ch2co),25.89(1c,och2ch2ch2),25.80(1c,och2ch2ch2),22.67(2c,ch2(myristoyl)ch3),14.09(2c,ch2ch3(myristoyl)),11.33(2c,ch2ch3).hrms,esi+,m/z:calcdforc43h83n3o6na[m+na]+,760.6180;found,760.6196.
实施例6
制备化合物a4,化学结构式如下:
标题化合物a4以羧基化谷氨酸双十四醇酯(546mg,0.854mmol)和3-二乙胺基丙胺(136μl,0.854mmol)为原料,按照制备a1的方法,得到粗产物黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=40︰1)得到白色固体310mg,收率:48%。1hnmr(300mhz,cdcl3):δ(ppm)7.58(t,j=5.8hz,1h,nhcoch2),7.03(d,j=7.5hz,1h,conhch),4.58–4.47(m,1h,nhch),4.11(t,j=6.8hz,2h,cooch2),4.05(t,j=6.8hz,2h,cooch2),3.46–3.33(m,2h,(ch3ch2)2nch2ch2ch2),3.20–3.03(m,4h,(ch3ch2)2nch2,2h,(ch3ch2)2nch2),2.69–2.48(m,2h,ch2coo,2h,nhcoch2ch2),2.47–2.32(m,2h,ch2conh),2.24–2.12(m,1h,nhchch2),2.12–1.92(m,1h,nhchch2,2h,(ch3ch2)2nch2ch2),1.70–1.54(m,4h,cooch2ch2),1.37(t,j=7.2hz,6h,ch2ch3),1.33–1.23(m,44h,ch2(myristoyl)),0.88(t,j=6.9hz,6h,ch2ch3(myristoyl)).13cnmr(75mhz,cdcl3):δ(ppm)173.03(1c,nhcoch2),172.83(1c,conhch),172.23(1c,ch2cooch2),172.01(1c,nhchco),65.68(1c,cooch2),64.88(1c,cooch2),51.89(1c,nhch),49.50(1c,(ch3ch2)2nch2),46.70(1c,(ch3ch2)2nch2ch2ch2),36.29(2c,ch2ch3),31.87(2c,ch2ch2ch3),31.34(1c,ch2cooch2),30.35(1c,coch2ch2),29.61(8c,ch2(myristoyl)),29.56(2c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.48(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.24(1c,ch2(myristoyl)),29.19(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.48(1c,och2ch2),27.22(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.79(1c,och2ch2ch2),23.97(1c,(ch3ch2)2nch2ch2),22.63(2c,ch2(myristoyl)ch3),14.05(2c,ch2ch3(myristoyl)),8.41(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h86n3o6[m+h]+,752.6517;found,752.6537.
实施例7
制备化合物a5,化学结构式如下:
标题化合物a5以羧基化谷氨酸双十四醇酯(570mg,0.891mmol)和1-(2-氨乙基)吡咯烷(113μl,0.891mmol)为原料,按照制备a1的方法,得到粗产物黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=35︰1)得到白色固体299mg,收率:46%。1hnmr(500mhz,cdcl3):δ(ppm)7.75(brs,1h,nhcoch2),7.18(d,j=7.6hz,1h,conhch),4.57–4.51(m,1h,nhch),4.10(t,j=6.8hz,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.68–3.56(m,2h,(ch2ch2)2nch2ch2),3.24(brs,4h,(ch2ch2)2n),3.20–3.13(m,2h,(ch2ch2)2nch2),2.73–2.62(m,2h,nhcoch2),2.62–2.54(m,2h,ch2coo),2.48–2.34(m,2h,ch2conh),2.22–2.14(m,1h,nhchch2),2.11–2.05(m,4h,ch2ch2nch2ch2),2.05–1.96(m,1h,nhchch2),1.67–1.57(m,4h,cooch2ch2),1.32–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.1hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.86(1c,nhcoch2),172.78(1c,conhch),172.27(1c,ch2cooch2),172.16(1c,nhchco),65.65(1c,cooch2),64.85(1c,cooch2),55.20(1c,(ch2ch2)2nch2),54.28(2c,ch2ch2nch2ch2),51.87(1c,nhch),36.13(1c,(ch2ch2)2nch2ch2),31.86(2c,ch2ch2ch3),31.24(1c,ch2cooch2),30.39(1c,coch2ch2co),29.64,29.62,29.60(8c,ch2(myristoyl)),29.55(2c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.46(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.24(1c,ch2(myristoyl)),29.19(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.48(1c,och2ch2),27.23(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.80(1c,och2ch2ch2),23.27(2c,(ch2ch2)2n),22.62(2c,ch2ch3),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc43h82n3o6[m+h]+,736.6204;found,736.6209.
实施例8
制备化合物a6,化学结构式如下:
标题化合物a6以羧基化谷氨酸双十四醇酯(552mg,0.863mmol)和1-(3-氨基丙基)吡咯烷(109μl,0.863mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=20︰1)得到黄白色固体223mg,收率:35%。1hnmr(500mhz,cdcl3):δ(ppm)7.61(brs,1h,nhcoch2),7.16(d,j=7.3hz,1h,conhch),4.55–4.48(m,1h,nhch),4.15–4.07(m,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.76(brs,2h,(ch2ch2)2nch2ch2ch2),3.38(d,j=4.9hz,2h,ch2ch2nch2ch2),3.20(d,j=5.6hz,2h,ch2ch2nch2ch2),2.96–2.86(m,2h,(ch2ch2)2nch2),2.64–2.54(m,2h,nhcoch2,2h,ch2coo),2.47–2.30(m,2h,ch2conh),2.23–2.12(m,1h,nhchch2,2h,(ch2ch2)2nch2ch2),2.12–1.96(m,1h,nhchch2,4h,ch2ch2nch2ch2),1.67–1.57(m,4h,cooch2ch2),1.32–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)173.30(1c,nhcoch2),172.85(1c,conhch),172.64(1c,ch2cooch2),171.95(1c,nhchco),65.73(1c,cooch2),64.92(1c,cooch2),53.77(2c,(ch2ch2)2n),52.88(1c,(ch2ch2)2nch2),51.94(1c,nhch),36.26(1c,(ch2ch2)2nch2ch2ch2),31.87(2c,ch2ch2ch3),31.33(1c,ch2cooch2),30.34(1c,coch2ch2co),29.63,29.61(8c,ch2(myristoyl)),29.56(2c,ch2(myristoyl)),29.50(1c,ch2(myristoyl)),29.48(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.25(1c,ch2(myristoyl)),29.20(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.48(1c,och2ch2),27.18(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.80(1c,och2ch2ch2),25.65(1c,(ch2ch2)2nch2ch2),23.25(2c,(ch2ch2)2n),22.62(2c,ch2ch3),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h84n3o6[m+h]+,750.6360;found,750.6360.
实施例9
制备化合物a7,化学结构式如下:
标题化合物a7以羧基化谷氨酸双十四醇酯(519mg,0.812mmol)和n-甲基-2-(2-氨乙基)-吡咯烷(105μl,0.812mmol)为原料,按照制备a1的方法,得到淡黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=25︰1)得到乳白色固体227mg,收率:37%。1hnmr(300mhz,cdcl3):δ(ppm)7.62(brs,1h,nhcoch2),7.35(t,j=8.7hz,1h,conhch),5.46(brs,6h,ch2n(ch3)ch),4.54–4.47(m,1h,nhch),4.17–3.97(m,4h,cooch2),3.42–3.26(m,2h,n(ch3)chch2ch2nh),3.08–2.92(m,2h,n(ch3)chch2ch2nh),2.91–2.85(m,2h,nhcoch2),2.64–2.52(m,2h,ch2coo,1h,n(ch3)chch2ch2),2.47–2.29(m,2h,ch2conh,1h,n(ch3)chch2),2.17–1.97(m,2h,nhchch2,1h,n(ch3)chch2,1h,n(ch3)chch2ch2),1.69–1.53(m,4h,cooch2ch2),1.37–1.19(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(75mhz,cdcl3):δ(ppm)173.54(1c,nhcoch2),173.00(1c,conhch),172.42(1c,ch2cooch2),172.07(1c,nhchco),71.26(1c,n(ch3)ch),67.42(1c,n(ch3)ch2),65.84(1c,cooch2),65.04(1c,cooch2),56.16(1c,n(ch3)),51.96(1c,nhch),39.74(1c,n(ch3)chch2ch2nh),36.43(1c,n(ch3)chch2ch2nh),31.92(2c,ch2ch2ch3),31.28(1c,ch2cooch2),31.25(1c,n(ch3)chch2ch2ch2),30.34(1c,coch2ch2),29.69(8c,ch2(myristoyl)),29.66(2c,ch2(myristoyl)),29.57(1c,ch2(myristoyl)),29.55(1c,ch2(myristoyl)),29.36(2c,ch2(myristoyl),1c,nhchch2),29.32(1c,ch2(myristoyl)),29.29(1c,ch2(myristoyl)),28.58(1c,och2ch2),28.49(1c,och2ch2),27.09(1c,coch2ch2co),25.91(1c,och2ch2ch2),25.86(1c,och2ch2ch2),22.68(2c,ch2ch3),21.60(1c,n(ch3)chch2ch2),14.10(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h84n3o6[m+h]+,750.6360;found,750.6367.
实施例10
制备化合物a8,化学结构式如下:
标题化合物a8以羧基化谷氨酸双十四醇酯(527mg,0.824mmol)和4-甲基-1-哌嗪乙胺(124μl,0.824mmol)为原料,按照制备a1的方法,得到粗产物淡黄色固体,经柱层析纯化(二氯甲烷︰甲醇=15︰1)得到白色颗粒状固体478mg,收率:76%。1hnmr(500mhz,cdcl3):δ(ppm)7.70(brs,1h,nhcoch2),7.43(brs,1h,conhch),4.53–4.46(m,1h,nhch),4.15–4.06(m,2h,cooch2),4.04(t,j=6.8hz,2h,cooch2),3.53(m,8h,n(ch2ch2)2nch3,2h,nch2ch2nh),3.22(brs,2h,nch2ch2nh),2.90(brs,3h,nch3),2.71–2.50(m,2h,ch2coo,2h,coch2ch2co),2.48–2.34(m,2h,ch2conh),2.19–2.09(m,1h,nhchch2),2.06–1.96(m,1h,nhchch2),1.67–1.57(m,4h,cooch2ch2),1.31–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.1hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)173.51(1c,nhcoch2),172.82(1c,conhch),172.78(1c,ch2cooch2),172.07(1c,nhchco),65.71(1c,cooch2),64.91(1c,cooch2),56.27(1c,nch2ch2nh),51.96(1c,nhch),51.28(2c,n(ch2ch2)2nch3),49.56(2c,n(ch2ch2)2nch3),43.45(1c,nch3),34.73(1c,nch2ch2nh),31.87(2c,ch2ch2ch3),31.13(1c,ch2cooch2),30.35(1c,coch2ch2co),29.67(2c,ch2(myristoyl)),29.65(8c,ch2(myristoyl)),29.61(2c,ch2(myristoyl)),29.54(2c,ch2(myristoyl),1c,nhchch2),29.30(1c,ch2(myristoyl)),29.28(1c,ch2(myristoyl)),28.58(1c,och2ch2),28.50(1c,och2ch2),27.06(1c,coch2ch2co),25.89(1c,och2ch2ch2),25.86(1c,och2ch2ch2),22.62(2c,ch2ch3),14.02(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h85n4o6[m+h]+,765.6469;found,765.6464.
实施例11
制备化合物a9,化学结构式如下:
标题化合物a9以羧基化谷氨酸双十四醇酯(531mg,0.830mmol)和1-(3-氨丙基)-4-甲基哌嗪(141μl,0.830mmol)为原料,按照制备a1的方法,得到粗产物淡黄色固体,经柱层析纯化(二氯甲烷︰甲醇=10︰1)得到乳白色凝胶状固体344mg,收率:53%。1hnmr(500mhz,cdcl3):δ(ppm)7.63(brs,1h,nhcoch2),7.39(brs,1h,conhch),4.51–4.45(m,1h,nhch),4.15–4.06(m,2h,cooch2),4.04(t,j=7.0hz,2h,cooch2),3.55(brs,8h,n(ch2ch2)2nch3),3.33(brs,2h,nch2ch2ch2nh),3.18(brs,2h,nch2ch2ch2nh),2.89(s,3h,nch3),2.66–2.49(m,2h,ch2coo,2h,coch2ch2co),2.47–2.34(m,2h,ch2conh),2.19–2.09(m,1h,nhchch2),2.06–1.95(m,1h,nhchch2,2h,nch2ch2ch2nh),1.65–1.57(m,4h,cooch2ch2),1.30–1.25(m,44h,ch2(myristoyl)),0.88(t,j=6.7hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)173.29(1c,nhcoch2),172.83(1c,conhch),172.71(1c,ch2cooch2),172.08(1c,nhchco),65.72(1c,cooch2),64.93(1c,cooch2),54.66(1c,nch2ch2ch2nh),51.95(1c,nhch),50.94(2c,n(ch2ch2)2nch3),49.38(2c,n(ch2ch2)2nch3),43.52(1c,nch3),36.66(1c,nch2ch2ch2nh),31.88(2c,ch2ch2ch3),31.22(1c,ch2cooch2),30.38(1c,coch2ch2co),29.68(2c,ch2(myristoyl)),29.67(8c,ch2(myristoyl)),29.30(2c,ch2(myristoyl)),29.25(2c,ch2(myristoyl),1c,nhchch2),29.21(2c,ch2(myristoyl)),28.58(1c,och2ch2),28.48(1c,och2ch2),27.25(1c,coch2ch2co),25.91(1c,och2ch2ch2),25.87(1c,och2ch2ch2),24.20(1c,nch2ch2ch2nh),22.63(2c,ch2ch3),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc45h87n4o6[m+h]+,779.6626;found,779.6631.
实施例12
制备化合物a10,化学结构式如下:
标题化合物a10以羧基化谷氨酸双十四醇酯(518mg,0.810mmol)和n-(3-氨基丙基)二乙醇胺(123μl,0.810mmol)为原料,按照制备a1的方法,得到粗产物黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=10︰1)得到白色颗粒状固体322mg,收率:51%。1hnmr(300mhz,cdcl3):δ(ppm)7.85(brs,1h,nhcoch2),7.60(d,j=7.1hz,1h,conhch),4.78(brs,6h,(hoch2ch2)2nch2ch2ch2),4.51–4.44(m,1h,nhch),4.09–3.97(m,4h,cooch2,2h,(hoch2ch2)2n),3.52–3.35(m,6h,(hoch2ch2)2nch2ch2ch2),2.68–2.50(m,2h,nhcoch2,2h,ch2coo),2.46–2.35(m,2h,ch2conh),2.19–1.95(m,2h,nhchch2,2h,(hoch2ch2)2nch2ch2ch2),1.67–1.56(m,4h,cooch2ch2),1.34–1.22(m,44h,ch2(myristoyl)),0.88(t,j=6.9hz,6h,ch2ch3).13cnmr(75mhz,cdcl3):δ(ppm)173.87(1c,nhcoch2),173.05(1c,conhch),172.90(1c,ch2cooch2),172.14(1c,nhchco),65.73(1c,cooch2),64.95(1c,cooch2),55.91(2c,(hoch2ch2)2n),55.65(2c,(hoch2ch2)2n),52.14(1c,(hoch2ch2)2nch2),51.96(1c,nhch),36.33(1c,(hoch2ch2)2nch2ch2ch2),31.89(2c,ch2ch2ch3),31.20(1c,ch2cooch2),30.39(1c,coch2ch2co),29.68(8c,ch2(myristoyl)),29.64(2c,ch2(myristoyl)),29.57(2c,ch2(myristoyl)),29.33(4c,ch2(myristoyl),1c,nhchch2),28.59(1c,och2ch2),28.51(1c,och2ch2),27.00(1c,coch2ch2co),25.90(1c,och2ch2ch2),25.89(1c,och2ch2ch2),23.87(1c,(hoch2ch2)2nch2ch2),22.64(2c,ch2ch3),14.04(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h86n3o8[m+h]+,784.6415;found,784.6407.
实施例13
制备化合物a11,化学结构式如下:
标题化合物a11以羧基化谷氨酸双十四醇酯(519mg,0.812mmol)和1-(3-氨基丙基)咪唑(97μl,0.812mmol)为原料,按照制备a1的方法,得到粗产物黄色凝胶状固体,经柱层析纯化(二氯甲烷︰甲醇=10︰1)得到白色凝胶状固体356mg,收率:59%。1hnmr(300mhz,cdcl3):δ(ppm)8.02(brs,1h,imidazole),7.27(brs,2h,imidazole),4.66–4.47(m,1h,nhch),4.32–3.94(m,4h,cooch2,2h,nch2),3.23(brs,2h,nch2ch2ch2),2.64(brs,2h,nch2ch2,2h,coch2ch2co),2.44(brs,1h,nhchch2,2h,ch2coo),2.17–1.98(m,1h,nhchch2,2h,ch2conh),1.65–1.55(m,4h,cooch2ch2),1.32–1.24(m,44h,ch2(myristoyl)),0.88(t,j=6.9hz,6h,ch2ch3).hrms,esi+,m/z:calcdforc43h79n4o6[m+h]+,747.6000;found,747.6002.
实施例14
制备化合物a12,化学结构式如下:
标题化合物a12以羧基化谷氨酸双十四醇酯(511mg,0.799mmol)和4-氨基-1-甲基哌啶(101μl,0.799mmol)为原料,按照制备a1的方法,得到粗产物淡黄色固体,经柱层析纯化(二氯甲烷︰甲醇=20︰1)得到白色凝胶状固体221mg,收率:38%。1hnmr(500mhz,cdcl3):δ(ppm)7.01(brs,1h,conhch),4.57–4.51(m,1h,nhch),4.15–4.08(m,2h,cooch2),4.05(t,j=6.8hz,2h,cooch2),3.93(brs,1h,ch3n(ch2ch2)2ch)),3.28–3.19(m,2h,ch3n(ch2ch2)2ch),2.73–2.64(m,2h,ch3n(ch2ch2)2ch),2.61(s,3h,nch3),2.59–2.52(m,2h,coch2ch2co,2h,ch2coo),2.45–2.32(m,2h,ch2conh),2.21–2.12(m,1h,nhchch2),2.11–2.04(m,2h,ch3n(ch2ch2)2ch),2.03–1.95(m,1h,nhchch2),1.94–1.85(m,2h,ch3n(ch2ch2)2ch),1.67–1.57(m,4h,cooch2ch2),1.32–1.25(m,44h,ch2(myristoyl)),0.88(t,j=6.8hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.81(1c,nhcoch2),172.28(1c,conhch),171.91(1c,nhchco,1c,ch2cooch2),65.74(1c,cooch2),64.92(1c,cooch2),53.60(2c,ch3n(ch2ch2)2ch),51.84(1c,nhch),44.43(1c,nch3,1c,ch3n(ch2ch2)2ch),31.87(2c,ch2ch2ch3),31.50(1c,ch2cooch2),30.34(1c,coch2ch2co),29.81(2c,ch3n(ch2ch2)2ch),29.64,29.62(8c,ch2(myristoyl)),29.57(2c,ch2(myristoyl)),29.51(1c,ch2(myristoyl)),29.48(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.25(1c,ch2(myristoyl)),29.21(1c,ch2(myristoyl)),28.56(1c,och2ch2),28.47(1c,och2ch2),27.37(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.80(1c,och2ch2ch2),22.62(2c,ch2ch3),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc43h82n3o6[m+h]+,736.6204;found,736.6199.
实施例15
制备化合物a13,化学结构式如下:
标题化合物a13以羧基化谷氨酸双十四醇酯(369mg,0.578mmol)和1-甲基-3-氨基吡咯烷盐酸盐(100mg,0.578mmol)为原料,按照制备a1的方法,得到粗产物黄色固体,经柱层析纯化(二氯甲烷︰甲醇=25︰1)得到白色凝胶状固体142mg,收率:34%。1hnmr(300mhz,cdcl3):δ(ppm)8.08(t,j=7.3hz,1h,nhcoch2),7.35(d,j=8.3hz,1h,conhch),4.82(brs,1h,ch3n(ch2ch2)(ch2)ch),4.59–4.50(m,1h,nhch),4.11–4.02(m,4h,cooch2),3.89–3.61(m,2h,ch3n(ch2ch2)(ch2)ch),3.30–3.04(m,2h,ch3n(ch2ch2)(ch2)ch),2.94(s,3h,nch3),2.66–2.53(m,2h,coch2ch2co,2h,ch2coo),2.47–2.36(m,2h,ch2conh),2.36–2.09(m,1h,nhchch2,2h,ch3n(ch2ch2)(ch2)ch),2.07–1.95(m,1h,nhchch2),1.66–1.57(m,4h,cooch2ch2),1.33–1.24(m,44h,ch2(myristoyl)),0.88(t,j=6.9hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.80(1c,nhcoch2),172.75(1c,conhch),172.27(1c,ch2cooch2),172.17(1c,nhchco),65.95(1c,ch3n(ch2ch2)(ch2)ch),65.86(1c,cooch2),64.99(1c,ch3n(ch2ch2)(ch2)ch),64.97(1c,cooch2),56.32(1c,ch3n),51.94(1c,ch3n(ch2ch2)(ch2)ch),51.80(1c,nhch),48.89(1c,ch3n(ch2ch2)(ch2)ch),31.88(2c,ch2ch2ch3),31.38(1c,ch2cooch2),30.62(1c,coch2ch2co),29.65(8c,ch2(myristoyl)),29.61(2c,ch2(myristoyl)),29.58(1c,ch2(myristoyl)),29.52(1c,ch2(myristoyl)),29.31(2c,ch2(myristoyl),1c,nhchch2),29.28(1c,ch2(myristoyl)),29.26(1c,ch2(myristoyl)),28.63(1c,och2ch2),28.56(1c,och2ch2),27.50(1c,coch2ch2co),25.91(1c,och2ch2ch2),25.87(1c,och2ch2ch2),22.64(2c,ch2ch3),14.05(2c,ch2ch3).hrms,esi+,m/z:calcdforc42h80n3o6[m+h]+,722.6047;found,722.6062.
实施例16
制备化合物a14,化学结构式如下:
标题化合物a14以羧基化谷氨酸双十四醇酯(531mg,0.830mmol)和n-(2-氨基乙基)吗啉(109μl,0.830mmol)为原料,按照制备a1的方法,得到粗产物淡黄色固体,经柱层析纯化(二氯甲烷︰甲醇=25︰1)得到白色凝胶状固体280mg,收率:51%。1hnmr(500mhz,cdcl3):δ(ppm)8.12(brs,1h,nhcoch2),7.32(d,j=3.7hz,1h,conhch),4.54–4.47(m,1h,nhch),4.17–3.97(m,4h,cooch2,4h,o(ch2ch2)2n),3.70(brs,4h,o(ch2ch2)2n),3.34(brs,2h,nch2ch2nh),3.04(brs,2h,nch2ch2nh),2.72–2.56(m,2h,coch2ch2co,2h,ch2coo),2.48–2.35(m,2h,ch2conh),2.19–2.11(m,1h,nhchch2),2.06–1.96(m,1h,nhchch2),1.66–1.59(m,4h,cooch2ch2),1.31–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)176.27(1c,nhcoch2),173.08(1c,conhch),171.92(1c,ch2cooch2),172.09(1c,nhchco),65.80(1c,cooch2),64.98(1c,cooch2),63.69(2c,o(ch2ch2)2n),57.49(1c,nch2ch2nh),52.67(1c,o(ch2ch2)2n),52.59(1c,o(ch2ch2)2n),52.01(1c,nhch),33.73(1c,nch2ch2nh),31.88(2c,ch2ch2ch3),31.10(1c,ch2cooch2),30.34(1c,coch2ch2co),29.65,29.64,29.62(8c,ch2(myristoyl)),29.59(2c,ch2(myristoyl)),29.52(1c,ch2(myristoyl)),29.50(1c,ch2(myristoyl)),29.31(2c,ch2(myristoyl),1c,nhchch2),29.27(1c,ch2(myristoyl)),29.24(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.48(1c,och2ch2),27.07(1c,coch2ch2co),25.88(1c,och2ch2ch2),25.82(1c,och2ch2ch2),22.63(2c,ch2ch3),14.04(2c,ch2ch3).hrms,esi+,m/z:calcdforc43h82n3o7[m+h]+,752.6153;found,752.6149.
实施例17
制备化合物a15,化学结构式如下:
标题化合物a15以羧基化谷氨酸双十四醇酯(525mg,0.821mmol)和n-(3-氨丙基)吗啉(120μl,0.821mmol)为原料,按照制备a1的方法,得到粗产物黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=25︰1)得到白色凝胶状固体286mg,收率:46%。1hnmr(500mhz,cdcl3):δ(ppm)7.70(brs,1h,nhcoch2),7.19(brs,1h,conhch),4.52–4.47(m,1h,nhch),4.20–3.98(m,4h,cooch2,4h,o(ch2ch2)2n),3.53(brs,2h,o(ch2ch2)2n),3.37(brs,2h,nch2ch2ch2nh),3.18(brs,2h,nch2ch2ch2nh),2.96(brs,2h,o(ch2ch2)2n),2.63–2.58(m,2h,coch2ch2co),2.57(brs,2h,ch2coo),2.47–2.33(m,2h,ch2conh),2.19–2.12(m,1h,nhchch2),2.09(brs,2h,nch2ch2ch2nh),2.04–1.96(m,1h,nhchch2),1.66–1.59(m,4h,cooch2ch2),1.31–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)173.41(1c,nhcoch2),172.85(1c,conhch),172.63(1c,ch2cooch2),172.01(1c,nhchco),65.74(1c,cooch2),64.94(1c,cooch2),63.74(2c,o(ch2ch2)2n),55.17(1c,nch2ch2ch2nh),52.03(2c,o(ch2ch2)2n),51.94(1c,nhch),36.24(1c,nch2ch2ch2nh),31.87(2c,ch2ch2ch3),31.16(1c,ch2cooch2),30.33(1c,coch2ch2co),29.64,29.62,29.60(8c,ch2(myristoyl)),29.57(2c,ch2(myristoyl)),29.51(1c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.26(1c,ch2(myristoyl)),29.22(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.48(1c,och2ch2),27.14(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.81(1c,och2ch2ch2),23.46(1c,nch2ch2ch2nh),22.62(2c,ch2ch3),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h84n3o7[m+h]+,766.6309;found,766.6308.
实施例18
制备化合物a16,化学结构式如下:
标题化合物a16以羧基化谷氨酸双十四醇酯(536mg,0.838mmol)和1-(2-氨乙基)哌啶(115μl,0.838mmol)为原料,按照制备a1的方法,得到粗产物黄白色固体,经柱层析纯化(二氯甲烷︰甲醇=10︰1)得到白色凝胶状固体326mg,收率:52%。1hnmr(500mhz,cdcl3):δ(ppm)6.78(d,j=7.7hz,1h,conhch),6.59(brs,1h,nhcoch2),4.60–4.54(m,1h,nhch),4.11(t,j=6.7hz,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.42–3.33(m,2h,nch2ch2nh),2.64–2.45(m,2h,coch2ch2co,2h,ch2coo,6h,ch2(ch2ch2)2nch2),2.43–2.32(m,2h,ch2conh),2.23–2.15(m,1h,nhchch2),2.03–1.94(m,1h,nhchch2),1.66–1.57(m,4h,cooch2ch2,4h,ch2(ch2ch2)2n),1.50–1.43(m,2h,ch2(ch2ch2)2n),1.31–1.24(m,44h,ch2(myristoyl)),0.88(t,j=7.1hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.78(1c,nhcoch2),172.11(1c,conhch),171.91(1c,ch2cooch2),171.86(1c,nhchco),65.68(1c,cooch2),64.87(1c,cooch2),57.19(1c,nch2ch2nh),54.25(2c,ch2(ch2ch2)2n),51.78(1c,nhch),35.86(1c,nch2ch2nh),31.88(2c,ch2ch2ch3),31.52(1c,ch2cooch2),30.30(1c,coch2ch2co),29.65,29.63,29.61(8c,ch2(myristoyl)),29.56(2c,ch2(myristoyl)),29.50(1c,ch2(myristoyl)),29.46(1c,ch2(myristoyl)),29.31(2c,ch2(myristoyl),1c,nhchch2),29.24(1c,ch2(myristoyl)),29.18(1c,ch2(myristoyl)),28.58(1c,och2ch2),28.49(1c,och2ch2),27.43(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.78(1c,och2ch2ch2),25.41(2c,ch2(ch2ch2)2n),24.01(1c,ch2(ch2ch2)2n),22.64(2c,ch2ch3),14.04(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h84n3o6[m+h]+,750.6360;found,750.6367.
实施例19
制备化合物a17,化学结构式如下:
标题化合物a17以羧基化谷氨酸双十四醇酯(511mg,0.799mmol)和4-(2-氨乙基)吡啶(95μl,0.799mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=40︰1)得到白色凝胶状固体165mg,收率:28%。1hnmr(500mhz,cdcl3):δ(ppm)8.55(brs,2h,n(chch)2c),7.34(brs,2h,n(chch)2c),6.83(brs,1h,nhcoch2),6.64(brs,1h,conhch),4.58–4.52(m,1h,nhch),4.12(t,j=6.3hz,2h,cooch2),4.05(t,j=6.8hz,2h,cooch2),3.54(brs,2h,cch2ch2nh),2.91(brs,2h,cch2ch2nh),2.55(brs,2h,ch2coo),2.48(brs,2h,ch2conh),2.44–2.32(m,2h,ch2conh),2.23–2.14(m,1h,nhchch2),2.04–1.95(m,1h,nhchch2),1.66–1.58(m,4h,cooch2ch2),1.31–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.83(1c,nhcoch2),172.31(1c,conhch),172.21(1c,ch2cooch2),171.81(1c,nhchco),151.64(2c,n(chch)2c),147.23(1c,n(chch)2c),125.23(2c,n(chch)2c),65.80(1c,cooch2),64.98(1c,cooch2),51.94(1c,nhch),39.53(1c,cch2ch2nh),35.30(1c,cch2ch2nh),31.87(2c,ch2ch2ch3),31.39(1c,ch2cooch2),30.32(1c,coch2ch2co),29.65,29.63,29.61(8c,ch2(myristoyl)),29.55(2c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.47(1c,ch2(myristoyl)),29.30(2c,ch2(myristoyl),1c,nhchch2),29.24(1c,ch2(myristoyl)),29.18(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.49(1c,och2ch2),27.24(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.79(1c,och2ch2ch2),22.63(2c,ch2ch3),14.04(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h78n3o6[m+h]+,744.5891;found,744.5899.
实施例20
制备化合物a18,化学结构式如下:
标题化合物a18以羧基化谷氨酸双十四醇酯(450mg,0.703mmol)和1-(3-氨基丙基)哌啶(100mg,0.703mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=30︰1)得到白色凝胶状固体173mg,收率:32%。1hnmr(500mhz,cdcl3):δ(ppm)7.81(brs,1h,nhcoch2),7.22(brs,1h,conhch),4.55–4.48(m,1h,nhch),4.10(t,j=6.7hz,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.58(brs,2h,nch2ch2ch2nh),3.38(brs,2h,ch2(ch2ch2)2n),3.10(brs,2h,ch2(ch2ch2)2n),2.75–2.65(m,2h,nch2ch2ch2nh),2.61(brs,2h,coch2ch2co,2h,ch2coo),2.48–2.34(m,2h,ch2conh),2.26–2.15(m,1h,nhchch2,2h,ch2(ch2ch2)2n),2.15–2.07(m,2h,ch2(ch2ch2)2n),2.06–1.97(m,1h,nhchch2),1.93–1.83(m,1h,ch2(ch2ch2)2n,2h,nch2ch2ch2nh),1.67–1.58(m,4h,cooch2ch2),1.49–1.38(m,1h,ch2(ch2ch2)2n),1.32–1.25(m,44h,ch2(myristoyl)),0.88(t,j=6.8hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)173.24(1c,nhcoch2),172.79(1c,conhch),172.41(1c,ch2cooch2),171.98(1c,nhchco),65.67(1c,cooch2),64.86(1c,cooch2),54.55(2c,ch2(ch2ch2)2n),53.37(1c,nch2ch2ch2nh),53.28(1c,nch2ch2ch2nh),51.95(1c,nhch),36.20(1c,nch2ch2ch2nh),31.86(2c,ch2ch2ch3),31.32(1c,ch2cooch2),30.39(1c,coch2ch2co),29.62,29.60(8c,ch2(myristoyl)),29.55(2c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.47(1c,ch2(myristoyl)),29.29(2c,ch2(myristoyl),1c,nhchch2),29.24(1c,ch2(myristoyl)),29.20(1c,ch2(myristoyl)),28.57(1c,och2ch2),28.49(1c,och2ch2),27.16(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.80(1c,och2ch2ch2),23.77(2c,ch2(ch2ch2)2n),22.62(2c,ch2ch3),22.11(1c,ch2(ch2ch2)2n),14.03(2c,ch2ch3).hrms,esi+,m/z:calcdforc45h86n3o6[m+h]+,764.6517;found,764.6527.
实施例21
制备化合物a19,化学结构式如下:
标题化合物a19以羧基化谷氨酸双十四醇酯(550mg,0.860mmol)和(1-甲基-4-哌啶)甲胺(122μl,0.860mmol)为原料,按照制备a1的方法,得到粗产物黄色凝胶状固体,经柱层析纯化(二氯甲烷︰甲醇=25︰1)得到白色凝胶状固体283mg,收率:44%。1hnmr(500mhz,cdcl3):δ(ppm)7.36(brs,1h,nhcoch2),7.30(brs,1h,conhch),4.53–4.47(m,1h,nhch),4.15–4.07(m,2h,cooch2),4.04(t,j=7.1hz,2h,cooch2),3.43(d,j=11.4hz,2h,ch3n(ch2ch2)2chch2),3.24–3.15(m,2h,ch3n(ch2ch2)2ch),2.82–2.75(m,2h,ch3n(ch2ch2)2ch),2.74(s,3h,nch3),2.64–2.59(m,2h,coch2ch2co),2.59–2.55(m,2h,ch2coo),2.47–2.35(m,2h,ch2conh),2.20–2.11(m,1h,nhchch2),2.05–1.98(m,1h,nhchch2),1.96–1.90(m,2h,ch3n(ch2ch2)2ch),1.87–1.75(m,1h,ch3n(ch2ch2)2ch,2h,ch3n(ch2ch2)2ch),1.67–1.57(m,4h,cooch2ch2),1.32–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.0hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.85(1c,nhcoch2),172.80(1c,conhch),172.47(1c,ch2cooch2),171.94(1c,nhchco),65.63(1c,cooch2),64.87(1c,cooch2),54.31(2c,ch3n(ch2ch2)2ch),51.93(1c,nhch),43.69(1c,ch3n),43.56(1c,ch3n(ch2ch2)2chch2),33.37(1c,ch3n(ch2ch2)2ch),31.85(2c,ch2ch2ch3),31.57(1c,ch2cooch2),30.39(1c,coch2ch2co),29.62,29.59(8c,ch2(myristoyl)),29.55(2c,ch2(myristoyl)),29.48(1c,ch2(myristoyl)),29.46(1c,ch2(myristoyl)),29.28(2c,ch2(myristoyl),1c,nhchch2),29.23(1c,ch2(myristoyl)),29.19(1c,ch2(myristoyl)),28.56(1c,och2ch2),28.47(1c,och2ch2),27.11(1c,coch2ch2co),26.99(2c,ch3n(ch2ch2)2ch),25.86(1c,och2ch2ch2),25.80(1c,och2ch2ch2),22.60(2c,ch2ch3),14.02(2c,ch2ch3).hrms,esi+,m/z:calcdforc44h84n3o6[m+h]+,750.6360;found,750.6379.
实施例22
制备化合物a20,化学结构式如下:
标题化合物a20以羧基化谷氨酸双十四醇酯(515mg,0.805mmol)和1-苄基-3-氨基吡咯烷(139μl,0.805mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=40︰1)得到白色固体254mg,收率:40%。1hnmr(500mhz,cdcl3):δ(ppm)7.32(s,2h,c6h5ch2),7.31(s,2h,c6h5ch2),7.26(s,1h,c6h5ch2),6.64(t,j=8.2hz,1h,nhcoch2),6.27(brs,1h,conhch),4.59–4.54(m,1h,nhch),4.48–4.40(m,1h,n(ch2ch2)(ch2)ch),4.13–4.08(m,2h,cooch2),4.05(t,j=6.7hz,2h,cooch2),3.68–3.62(m,2h,c6h5ch2),2.93–2.85(m,1h,n(ch2ch2)(ch2)ch),2.64–2.59(m,2h,n(ch2ch2)(ch2)ch),2.57–2.52(m,2h,coch2ch2co),2.49–2.45(m,2h,ch2coo),2.41–2.30(m,2h,ch2conh,1h,n(ch2ch2)(ch2)ch),2.29–2.22(m,1h,n(ch2ch2)(ch2)ch),2.21–2.13(m,1h,nhchch2),2.01–1.93(m,1h,nhchch2),1.65–1.58(m,4h,cooch2ch2,1h,n(ch2ch2)(ch2)ch),1.29–1.25(m,44h,ch2(myristoyl)),0.88(t,j=7.1hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.80(1c,nhcoch2),172.00(1c,conhch),171.82(1c,ch2cooch2),171.17(1c,nhchco),128.91(1c,c6h5ch2),128.37(4c,c6h5ch2),127.30(1c,c6h5ch2),65.74(1c,cooch2),64.91(1c,cooch2),60.46(1c,n(ch2ch2)(ch2)ch),59.91(1c,c6h5ch2),52.49(1c,n(ch2ch2)(ch2)ch),51.82(1c,nhch),48.69(1c,n(ch2ch2)(ch2)ch),32.36(1c,n(ch2ch2)(ch2)ch),31.91(2c,ch2ch2ch3),31.51(1c,ch2cooch2),30.30(1c,coch2ch2co),29.68,29.64(8c,ch2(myristoyl)),29.59(2c,ch2(myristoyl)),29.52(1c,ch2(myristoyl)),29.49(1c,ch2(myristoyl)),29.34(2c,ch2(myristoyl),1c,nhchch2),29.27(1c,ch2(myristoyl)),29.20(1c,ch2(myristoyl)),28.61(1c,och2ch2),28.51(1c,och2ch2),27.45(1c,coch2ch2co),25.90(1c,och2ch2ch2),25.81(1c,och2ch2ch2),22.66(2c,ch2ch3),14.07(2c,ch2ch3).hrms,esi+,m/z:calcdforc48h84n3o6[m+h]+,798.6360;found,798.6368.
实施例23
制备化合物a21,化学结构式如下:
标题化合物a21以羧基化谷氨酸双十四醇酯(516mg,0.807mmol)和4-氨基-1-苄基哌啶(165μl,0.807mmol)为原料,按照制备a1的方法,得到粗产物黄色油状物,经柱层析纯化(二氯甲烷︰甲醇=35︰1)得到黄白色固体192mg,收率:29%。1hnmr(500mhz,cdcl3):δ(ppm)7.30(s,2h,c6h5ch2),7.29(s,2h,c6h5ch2),7.26–7.22(m,1h,c6h5ch2),6.66(t,j=7.0hz,1h,nhcoch2),5.89(brs,1h,conhch),4.59–4.54(m,1h,nhch),4.11(t,j=6.7hz,2h,cooch2),4.04(t,j=6.9hz,2h,cooch2),3.82–3.73(m,1h,ch3n(ch2ch2)2ch),3.49(s,2h,c6h5ch2),2.83–2.75(m,2h,n(ch2ch2)2ch),2.58–2.53(m,2h,coch2ch2co),2.53–2.44(m,2h,ch2coo),2.43–2.29(m,2h,ch2conh),2.22–2.16(m,1h,nhchch2),2.16–2.09(m,2h,n(ch2ch2)2ch),2.02–1.93(m,1h,nhchch2),1.91–1.84(m,2h,n(ch2ch2)2ch),1.67–1.56(m,4h,cooch2ch2),1.51–1.42(m,2h,n(ch2ch2)2ch),1.31–1.23(m,44h,ch2(myristoyl)),0.88(t,j=6.7hz,6h,ch2ch3).13cnmr(125mhz,cdcl3):δ(ppm)172.79(1c,nhcoch2),172.10(1c,conhch),171.77(1c,ch2cooch2),171.18(1c,nhchco),129.06(1c,c6h5ch2),128.19(4c,c6h5ch2),127.04(1c,c6h5ch2),65.74(1c,cooch2),64.91(1c,cooch2),62.98(1c,c6h5ch2),52.14(2c,n(ch2ch2)2ch),51.82(1c,nhch),46.56(1c,n(ch2ch2)2ch),32.02(2c,n(ch2ch2)2ch),31.89(2c,ch2ch2ch3),31.62(1c,ch2cooch2),30.29(1c,coch2ch2co),29.66,29.64,29.62(8c,ch2(myristoyl)),29.57,29.56(2c,ch2(myristoyl)),29.51(1c,ch2(myristoyl)),29.47(1c,ch2(myristoyl)),29.31(2c,ch2(myristoyl),1c,nhchch2),29.25(1c,ch2(myristoyl)),29.18(1c,ch2(myristoyl)),28.58(1c,och2ch2),28.49(1c,och2ch2),27.39(1c,coch2ch2co),25.87(1c,och2ch2ch2),25.78(1c,och2ch2ch2),22.64(2c,ch2ch3),14.05(2c,ch2ch3).hrms,esi+,m/z:calcdforc49h86n3o6[m+h]+,812.6517;found,812.6504.
实施例24
空白阳离子脂质体的制备与表征
制备方法:按照2:1摩尔比称取适量实施例1的阳离子脂质分子和辅助脂质dope,用4ml氯仿和1ml甲醇溶解,旋蒸除去溶剂,在瓶壁形成一层薄膜,真空干燥过夜。加入适量去离子水,37℃水合30分钟,探头超声15分钟,再依次过0.8μm,0.45μm,0.22μm微孔滤膜,即得到空白阳离子脂质体溶液,置于4℃保存备用。空白阳离子脂质体的粒径,电位和多分散系数(pdi)如表1所示。
表1本发明的空白阳离子脂质体的性质(n=3)
上述数据表明,本发明的空白阳离子脂质体的粒径在50~200nm之间,符合作为基因载体粒径大小的要求;多分散系数pdi均小于0.3,表明通过薄膜分散法所制备的阳离子脂质体的粒径均一规整;zeta电位在+10~+40mv之间,表明所制备的空白阳离子脂质体具有与负电性核酸通过静电相互作用发生结合并有效压缩核酸的能力。
实施例25
阳离子脂质体/乱序sirna二元复合物的制备与表征
按照不同的氮磷比(n/p=1,3,5,7,9)将质量一定乱序sirna(如2μg)(正义链:5’-uucuccgaacgugucacgudtdt-3’,反义链:5’-tdtdaagaggcuugcacagugca-3’)和上述空白阳离子脂质体溶液混合,用水稀释至总体积200μl,涡旋10s,室温孵育30分钟,即得到阳离子脂质体/乱序sirna二元复合物。通过琼脂糖凝胶电泳实验考察阳离子脂质体对乱序sirna的荷载能力(如图1所示),并测定二元复合物的粒径和电位(如图2所示)。
上述实验表明,除阳离子脂质a11,a12,a14和a15所制备的脂质体例外,本发明的阳离子脂质体在n/p为5时均能荷载sirna不发生泄漏,且二元复合物的粒径在100~300nm之间,zeta电位在+10~+40mv之间,可进一步用于细胞转染实验。
实施例26
阳离子脂质体/egfp-sirna二元复合物对hela-egfp细胞的毒性考察
实验方法:按上述方法制备阳离子脂质体/egfp-sirna(gzru-sip05815122144)二元复合物(n/p=5)。取对数生长期的hela-egfp细胞,调整细胞密度为1×105个/ml的细胞悬液,接种于96孔细胞板中,每孔接种细胞悬液200μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入50μl阳离子脂质体egfp-sirna二元复合物和75μl1640培养液,使egfp-sirna终浓度为200nm(n=3),继续培养6h。弃去1640培养液,用pbs洗涤三次,加入125μl含10%胎牛血清的1640培养液,继续培养。72h后每孔加入20μl的mtt工作液继续培养4h。弃去上清,每孔加入150μldmso,用酶标仪测定波长570nm处的吸光值,重复测定三次。用excel软件计算阳离子脂质体/egfp-sirna二元复合物存在下的细胞存活率。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体对hela细胞的毒性。实验结果如表2和图3所示。(细胞存活率=(制剂组细胞吸光值/空白组细胞吸光值)*100%)
表2本发明的阳离子脂质体/egfp-sirna二元复合物对hela-egfp细胞的毒性(n=3)
上述实验结果表明,本发明的阳离子脂质体/egfp-sirna二元复合物hela-egfp对细胞不产生明显毒性,细胞存活率均大于80%(脂质a19所制备的脂质体例外),其中阳离子脂质a7,a8,a9,a10,a13所制备的脂质体与egfp-sirna的二元复合物对hela-egfp细胞基本没有毒性作用,细胞存活率均大于90%,与阳性对照lipofectamine2000的细胞存活率相当。
实施例27
阳离子脂质体/egfp-sirna二元复合物转染hela-egfp细胞
实验方法:按上述方法制备阳离子脂质体/egfp-sirna二元复合物(n/p=5)。取对数生长期的hela-egfp细胞,调整细胞密度为4×105个/ml的细胞悬液,接种于24孔细胞板,每孔接种细胞悬液500μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入200μl阳离子脂质体/egfp-sirna二元复合物和300μl1640培养液,使egfp-sirna终浓度为200nm(n=3),继续培养6h。弃去1640培养液,用pbs洗涤三次,加入500μl含10%胎牛血清的1640培养液,继续培养。72h后采用倒置荧光显微镜定性观察hela-egfp细胞中绿色荧光蛋白的表达情况,并用流式细胞仪定量考察hela-egfp细胞中的绿色荧光强度。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体的基因沉默效率。实验结果如表3,图4和图5所示。(平均荧光强度降低百分比=(空白组细胞平均荧光强度-制剂组细胞平均荧光强度)/空白组细胞平均荧光强度*100%)
表3本发明的阳离子脂质体/egfp-sirna二元复合物转染hela-egfp细胞的基因沉默效率(n=3)
上述实验结果表明,本发明的阳离子脂质体/egfp-sirna二元复合物能高效转染hela-egfp细胞而产生显著的基因沉默效果。其中,阳离子脂质a6,a7,a8,a9,a10,a13,a18,a19所制备的脂质体与egfp-sirna的二元复合物的基因沉默效果优于阳性对照lipofectamine2000。
实施例28
阳离子脂质体/sirna二元复合物在血清存在下转染hela-egfp细胞
实验方法:按上述方法制备阳离子脂质体/egfp-sirna二元复合物(n/p=5)。取对数生长期的hela-egfp细胞,调整细胞密度为4×105个/ml的细胞悬液,接种于24孔细胞板,每孔接种细胞悬液500μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入200μl阳离子脂质体/egfp-sirna二元复合物和300μl含胎牛血清的1640培养液,使sirna终浓度为200nm,血清含量为10%(n=3),继续培养6h。弃去含胎牛血清的1640培养液,用pbs洗涤三次,加入500μl含10%胎牛血清的1640培养液,继续培养。72h后用倒置荧光显微镜定性观察hela-egfp细胞中绿色荧光蛋白的表达情况,用流式细胞仪定量考察hela-egfp细胞中的绿色荧光强度。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体在血清存在下的基因沉默效率。实验结果如表4,图6和图7所示。(平均荧光强度降低百分比=(空白组细胞平均荧光强度-制剂组细胞平均荧光强度)/空白组细胞平均荧光强度*100%)
表4本发明阳离子脂质体/egfp-sirna二元复合物在血清存在下转染hela-egfp细胞的基因沉默效率(n=3)
上述实验结果表明,本发明的阳离子脂质体/egfp-sirna二元复合物在血清存在下能保持高效转染hela-egfp细胞的能力而产生显著的基因沉默效果。其中,阳离子脂质a7,a9,a10,a13所制备的脂质体与egfp-sirna的二元复合物在血清存在下的基因沉默效果优于阳性对照lipofectamine2000。
实施例29
阳离子脂质体a13/apob-sirna二元复合物对hepg2细胞的毒性考察
实验方法:按上述方法制备阳离子脂质体a13/apob-sirna(正义链:5’-gucaucacacugaauaccaau-3’,反义链:5’-auugguauucagugugaugacacdtdt-3’)二元复合物(n/p=5),取对数生长期的hepg2细胞,调整细胞密度为1×105个/ml的细胞悬液,接种于96孔细胞板中,每孔接种细胞悬液200μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入50μl阳离子脂质体/apob-sirna二元复合物和75μl1640培养液,使apob-sirna终浓度为200nm(n=3),继续培养6h。弃去1640培养液,用pbs洗涤三次,加入125μl含10%胎牛血清的1640培养液,继续培养。72h后每孔加入20μl的mtt工作液继续培养4h。弃去上清,每孔加入150μldmso,用酶标仪测定波长570nm处的吸光值,重复测定三次。用excel软件计算阳离子脂质体a13/apob-sirna二元复合物存在下的细胞存活率。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体a13对hepg2细胞的毒性。实验结果如图8所示。(细胞存活率=(制剂组细胞吸光值/空白组细胞吸光值)*100%)
上述实验结果表明,本发明的阳离子脂质体a13/apob-sirna二元复合物对hepg2细胞不产生明显毒性,细胞存活率大于85%,与阳性对照lipofectamine2000的细胞存活率相当。
实施例30
阳离子脂质体a13/apob-sirna二元复合物转染hepg2细胞
实验方法:按上述方法制备阳离子脂质体a13/apob-sirna二元复合物(n/p=5),并转染hepg2细胞。通过westernblot和q-pcr实验考察hepg2细胞中apobmrna和对应蛋白表达量。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体a13的基因沉默效率。实验结果如图9和图10所示。(平均apob-mrna含量降低百分比=(空白组细胞平均apob-mrna含量-制剂组细胞平均apob-mrna含量)/空白组细胞平均apob-mrna含量*100%)
上述实验结果表明,本发明的阳离子脂质体a13/apob-sirna二元复合物能显著降低hepg2细胞中apob-mrna的含量和apob蛋白的表达量,基因沉默效果与阳性对照lipofectamine2000相当。
实施例31
阳离子脂质体a13/乱序sirna二元复合物对mcf-7细胞的毒性考察
实验方法:按上述方法制备阳离子脂质体a13/乱序sirna二元复合物(n/p=5),取对数生长期的mcf-7细胞,调整细胞密度为1×105个/ml的细胞悬液,接种于96孔细胞板中,每孔接种细胞悬液200μl,置于37℃,5%co2恒温培养箱内继续培养到细胞密度达80%左右。弃去培养液,用磷酸缓冲盐溶液(pbs)洗涤两次,各孔依次加入50μl阳离子脂质体/乱序sirna二元复合物和75μl1640培养液,使乱序sirna终浓度为200nm(n=3),继续培养6h。弃去1640培养液,用pbs洗涤三次,加入125μl含10%胎牛血清的1640培养液,继续培养。72h后每孔加入20μl的mtt工作液继续培养4h。弃去上清,每孔加入150μldmso,用酶标仪测定波长570nm处的吸光值,重复测定三次。用excel软件计算阳离子脂质体a13/乱序sirna二元复合物存在下的细胞存活率。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体a13对mcf-7细胞的毒性。实验结果如图11所示。(细胞存活率=(制剂组细胞吸光值/空白组细胞吸光值)*100%)
上述实验结果表明,本发明的阳离子脂质体a13/乱序sirna二元复合物对mcf-7细胞不产生明显毒性,细胞存活率大于85%,与阳性对照lipofectamine2000的细胞存活率相当。
实施例32
阳离子脂质体a13/survivin-sirna二元复合物转染mcf-7细胞
实验方法:按上述方法制备阳离子脂质体a13/survivin-sirna(正义链:5’-gaauuugaggaaacugcgatt-3’,反义链:5’-ucgcaguuuccucaaauuctt-3’)二元复合物(n/p=5),并转染mcf-7细胞。通过westernblot和q-pcr实验考察mcf-7细胞中survivinmrna和对应蛋白表达量。本实验以商业化转染试剂lipofectamine2000为阳性对照,比较评价本发明所提供的阳离子脂质体a13的基因沉默效率。实验结果如图12和图13所示。(平均survivin-mrna含量降低百分比=(空白组细胞平均survivin-mrna含量-制剂组细胞平均survivin-mrna含量)/空白组细胞平均survivin-mrna含量*100%)
上述实验结果表明,本发明的阳离子脂质体a13/survivin-sirna二元复合物能显著降低mcf-7细胞中survivin-mrna的含量和survivin蛋白的表达量,基因沉默效果与阳性对照lipofectamine2000相当。
需要指出的是,上述实施例仅为说明本发明的技术构思及特点,其目的在于让熟悉此项技术的人士能够了解本发明的内容并据以实施,并不能以此限制本发明的保护范围。凡根据本发明精神实质所作的等效变化或修饰,都应涵盖在本发明的保护范围之内。
- 还没有人留言评论。精彩留言会获得点赞!