一种用于检测犬呼吸多重病原体的核酸组合物及其试剂盒和方法与流程
本发明涉及分子生物技术体外诊断领域,具体而言,涉及一种用于检测犬呼吸多重病原体的核酸组合物及其试剂盒和方法。
背景技术:
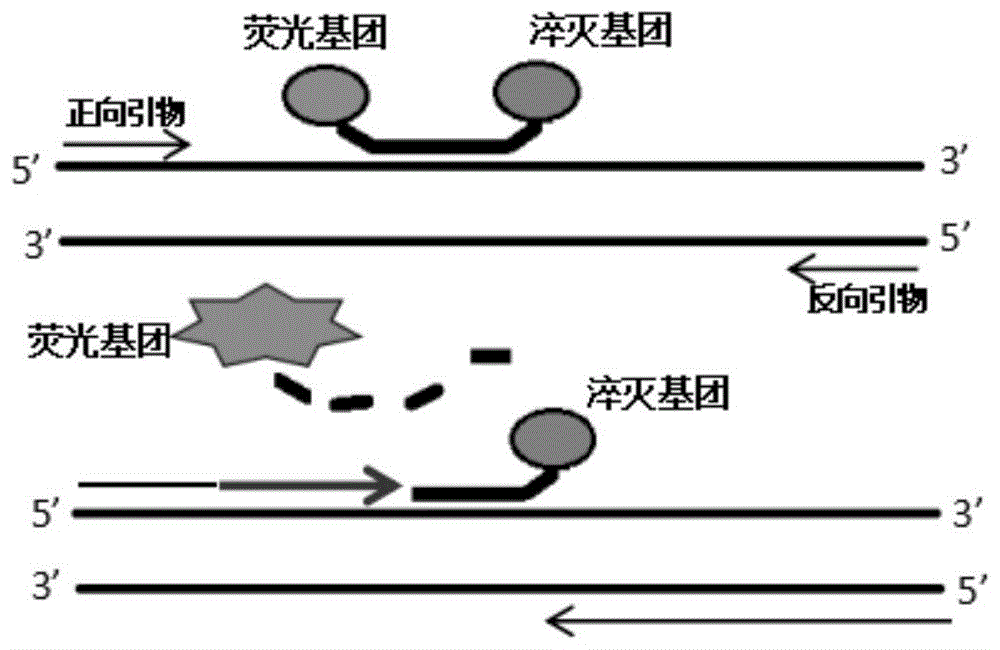
:犬传染性呼吸道疾病(canineinfectiousrespiratorydisease,cird)是指一种由多种病原体引起的犬急性传染性呼吸系统疾病综合征,临床上以频繁咳嗽和流涕为主要特征,初生幼犬更易受到侵害,故而又俗称“犬窝咳”。引起cird病原种类较多,且常发生多重病原体共同感染的情况,常见的病原有犬瘟热病毒、犬副流感病毒、犬腺病毒2型和支气管败血波氏杆菌。犬副流感病毒(canineparainfluenzavirus,cpiv)作为引起cird的主要病原之一,其传染性强,会引起犬的剧烈咳嗽、咽炎、鼻涕等,在犬舍中容易传播。犬腺病毒2型(canineadenovirustype2,cav-2)单独感染后临床症状轻微,常见干咳、食欲不振,发热等,但与其它病原混合感染时临床表现严重。犬瘟热病毒(caninedistempervirus,cdv)感染引起的犬瘟热是一种高度接触性传染病,发病率80%-100%。患犬在早期表现出急性鼻卡他,眼结膜炎,病毒血症等临床症状。支气管败血波氏杆菌(bordetellabronchiseptica,bb)是在crid发病犬中发现的主要病原体之一,临床表现与年龄呈明显的相关性,4-12周龄的幼犬表现较严重的临床症状,如水样分泌物转变为脓性鼻分泌物,剧烈干咳,干呕,时有少量痰液,bb在cird的发病机制中起到关键作用。引发犬传染性呼吸道疾病的多种病原体的临床症状类似,且常常协同感染,导致严重的呼吸系统疾病和死亡。这使得临床诊断与治疗更加重要。目前市面上没有同时检测犬呼吸道多重病原体的实时荧光定量pcr试剂盒。鉴于此,特提出本发明。技术实现要素:本发明的目的在于提供一种用于检测犬呼吸多重病原体的核酸组合物及其试剂盒和方法。本发明是这样实现的:第一方面,本发明实施例提供了一种用于检测犬呼吸多重病原体的核酸组合物,其包括:用于检测犬副流感病毒的第一试剂,用于检测犬瘟热病毒的第二试剂、用于检测犬腺病毒2型的第三试剂中的任意1种或几种的组合;所述第一试剂包括序列如seqidno.1~2所示的引物对1和/或序列如seqidno.3所示的探针1;所述第二试剂包括序列如seqidno.4~5所示的引物对2和/或序列如seqidno.6所示的探针2;所述第三试剂包括序列如seqidno.7~8所示的引物对3和/或序列如seqidno.9所示的探针3。第二方面,本发明实施例提供了一种用于检测犬呼吸多重病原体的试剂盒,其包括如前述实施例所述的核酸组合物。第三方面,本发明实施例提供了一种用于检测检测犬呼吸多重病原体的方法,其包括采用如前述实施例所述的用于检测犬呼吸多重病原体的核酸组合物、或如前述实施例所述的用于检测犬呼吸多重病原体的试剂盒对待测样品进行检测;所述方法不以疾病的诊断或治疗为直接目的。本发明具有以下有益效果:本发明提供了一种用于检测犬呼吸多重病原体的核酸组合物,其包括:用于检测犬副流感病毒的第一试剂,用于检测犬瘟热病毒的第二试剂、用于检测犬腺病毒2型的第三试剂中的任意1种或几种的组合;所述第一试剂包括序列如seqidno.1~2所示的引物对1和/或序列如seqidno.3所示的探针1;所述第二试剂包括序列如seqidno.4~5所示的引物对2和/或序列如seqidno.6所示的探针2;所述第三试剂包括序列如seqidno.7~8所示的引物对3和/或序列如seqidno.9所示的探针3。上述试剂可以进行随机组合,组合后的引物探针可以进行多重pcr检测,检测的灵敏度高,特异性好,为犬呼吸道疾病的临床诊断提供快速准确的检测方法。附图说明为了更清楚地说明本发明实施例的技术方案,下面将对实施例中所需要使用的附图作简单地介绍,应当理解,以下附图仅示出了本发明的某些实施例,因此不应被看作是对范围的限定,对于本领域普通技术人员来讲,在不付出创造性劳动的前提下,还可以根据这些附图获得其他相关的附图。图1为实时荧光定量pcr的原理图;图2为验证例1中第一试剂的扩增对比结果图;图3为验证例1中第二试剂的扩增对比结果图;图4为验证例1中第三试剂的扩增对比结果图;图5为验证例1中第四试剂的扩增对比结果图;图6为验证例2特异性测试中cpiv检测通道的结果;图7为验证例2特异性测试中cdv检测通道的结果;图8为验证例2特异性测试中cav-2检测通道的结果;图9为验证例2特异性测试中bb检测通道的结果;图10为验证例3中cpiv的线性测试的检测结果;图11为验证例3中cdv的线性测试的检测结果;图12为验证例3中cav-2的线性测试的检测结果;图13为验证例3中bb的线性测试的检测结果;图14为验证例4中cpiv在最低检测限时的扩增图;图15为验证例4中cdv在最低检测限时的扩增图;图16为验证例4中cav-2在最低检测限时的扩增图;图17为验证例4中bb在最低检测限时的扩增图;图18为验证例5中相同浓度的cpiv核酸在单重与多重pcr体系的扩增结果;图19为验证例5中相同浓度的cdv核酸在单重与多重pcr体系的扩增结果;图20为验证例5中相同浓度的cav-2核酸在单重与多重pcr体系的扩增结果;图21为验证例5中相同浓度的bb核酸在单重与多重pcr体系的扩增结果;图22为实施例4中的反应条件下的扩增图;图23为实施例5中的反应条件下的扩增图。具体实施方式为使本发明实施例的目的、技术方案和优点更加清楚,下面将对本发明实施例中的技术方案进行清楚、完整地描述。实施例中未注明具体条件者,按照常规条件或制造商建议的条件进行。所用试剂或仪器未注明生产厂商者,均为可以通过市售购买获得的常规产品。本发明中使用的多重实时荧光,可实现快速准确地同时检测引起犬呼吸道疾病的多重病原体,对犬呼吸道疾病的临床诊断及治疗有着重要的意义。首先,本发明实施例提供了一种用于检测犬呼吸多重病原体的核酸组合物,其包括:用于检测犬副流感病毒的第一试剂,用于检测犬瘟热病毒的第二试剂、用于检测犬腺病毒2型的第三试剂中的任意1种或几种的组合;所述第一试剂包括序列如seqidno.1~2所示的引物对1和/或序列如seqidno.3所示的探针1;所述第二试剂包括序列如seqidno.4~5所示的引物对2和/或序列如seqidno.6所示的探针2;所述第三试剂包括序列如seqidno.7~8所示的引物对3和/或序列如seqidno.9所示的探针3。需要说明的是,引物组合的方式可以是多种,例如,可以选择引物对1、引物对2和引物对3中的任意2种或3种,亦或是引物对1~3中的任意一对与后续引物对4的组合,还可以是引物对1~3中任意2对与引物对4的组合。若核酸组合物中的引物对数量少,则成本低,检测精准,若核酸组合物中的引物对数量多,可以检出的病原体则多,且可以同时进行,在准确检测目的病原体的同时,节省检测时间。只要是根据上述引物对1、引物对2、引物对3和引物对4进行组合所得到的核酸组合物均属于本发明的保护范围内。上述核酸组合物可以进行进行二重pcr、三重pcr或四重pcr反应,为犬副流感病毒、犬瘟热病毒、犬腺病毒2型以及支气管败血波氏杆菌的有效检测提供了途径。上述引物对1~4中均包括一上游引物和一下游引物,例如在引物对1中,序列如seqidno.1所示的序列为引物对1的上游引物,序列如seqidno.2所示的序列为引物对1的下游引物,引物对2~4以此类推。优选地,所述核酸组合物还包括:用于检测支气管败血波氏杆菌的第四试剂;所述第四试剂包括序列如seqidno.10~11所示的引物对4和/或序列如seqidno.12所示的探针4。优选地,所述探针1~4序列的5’端均标记有荧光报告基团,3’端均标记有荧光淬灭基团。优选地,所述荧光报告基团选自fam、vic、hex、cy3、ned、txr、rox、cy5中的任意一种,荧光淬灭基团选自tamra、bhq1、bhq2、bhq3、qsy中的任意一种。本发明实施例还提供了一种用于检测犬呼吸多重病原体的试剂盒,其包括如前述实施例所述的核酸组合物。优选地,所述试剂盒还包括pcr检测试剂。优选地,所述pcr检测试剂选自逆转录酶、taqdna聚合酶、dntp和mgcl2中的至少一种或多种的组合。可选地,所述试剂盒还可以包括用于检测内参基因的引物对。此外,本发明实施例还提供了一种用于检测检测犬呼吸多重病原体的方法,其包括采用如前述任一实施例所述的用于检测犬呼吸多重病原体的核酸组合物、或如前述任一实施例所述的用于检测犬呼吸多重病原体的试剂盒对待测样品进行检测;所述方法不以疾病的诊断或治疗为直接目的。待测样本可以为生物样品或非生物样品,生物样品包括血液样品或组织样品,非生物样品可以为采集的来自环境中的、非生物样品。优选地,所述检测为pcr检测,原理见附图1,当包括引物对1~引物对4时,所述引物对1~引物对4的工作浓度均为0.2~0.4μm;当包括探针1~探针4时,所述探针1~探针4的工作浓度均为0.4~0.6μm。在一些实施方式中,引物对1~4的工作浓度均为0.2~0.4μm是指,引物对1~4的上游引物和下游引物的工作浓度均可以选自0.2μm、0.3μm和0.4μm中的任意浓度,优选地,引物对1的上下游引物的工作浓度均为0.3μm,探针1的工作浓度为0.5μm;引物对2的上下游引物的工作浓度均为0.4μm,探针2的工作浓度为0.5μm;引物对2的上下游引物的工作浓度均为0.3μm,探针3的工作浓度为0.5μm,引物对4的上下游引物的工作浓度均为0.4μm,探针4的工作浓度为0.5μm。优选地,所述pcr检测的反应条件为:48~52℃10~20min;93~97℃2~3min;93~97℃5~10s;58~62℃20~30s;循环次数为38~42。在该反应条件下,多重pcr引物对在一个体系内能够同时对多种病原体进行检测,且检测的特异性更好。以下结合实施例对本发明的特征和性能作进一步的详细描述。实施例1本实施例提供了一种用于检测犬呼吸多重病原体的试剂盒,其包括第一试剂、第二试剂、第三试剂以及第四试剂,其中包括的引物的退火温度为60℃左右,序列信息参照表1。表1序列信息备注:f为上游引物的缩写,r为下游引物的缩写,p为探针的缩写。实施例2一种用于检测犬呼吸多重病原体的方法,其包括采用实施例1的试剂盒进行pcr反应,采用25μl反应体系,包括18.5μlpcr反应液(具体包括逆转录酶、taqdna聚合酶、dntp、mgcl等)和各病原体的引物探针组,各引物探针组的反应浓度(同工作浓度)如表2所示,pcr反应液购自常规商业厂家。表2反应浓度pcr反应条件为:50℃10min,95℃3min,95℃5s,60℃20s,共40个循环,其中60℃设置采集荧光信号。实施例3一种用于检测犬呼吸多重病原体的试剂盒,大致和实施例1相同,包括第一试剂、第二试剂、第三试剂以及第四试剂,区别在于引物探针的序列有差异,序列信息参照表2。表2序列信息实施例4一种用于检测犬呼吸多重病原体的方法,大致与实施例2相同,区别在于pcr反应条件的不同,反应条件为:50℃15min,95℃3min,95℃10s,60℃30s,共40个循环,其中60℃设置采集荧光信号。实施例5一种用于检测犬呼吸多重病原体的方法,大致与实施例2相同,区别在于pcr反应条件的不同,反应条件为:50℃10min,95℃3min,95℃5s,60℃20s,共40个循环,其中60℃设置采集荧光信号。验证例1验证本发明提供的引物对的特异性。将上述实施例1、实施例3提供的引物探针组委托赛默飞世尔科技公司进行合成,并按照说明书进行稀释。分别对犬副流感病毒、犬瘟热病毒、犬腺病毒2型和支气管败血波氏杆菌临床样本进行核酸提取,提取后的病原体核酸先使用市售y厂家的pcr单项检测试剂进行验证,以确认各病原体为阳性。分别使用不同引物组合配制pcr试剂,并加入对应的阳性病原体核酸,进行扩增,第一试剂~第四试剂的扩增对比结果分别如图2~5所示。由结果可知,实施例1提供的第一试剂~第四试剂ct值更小,且荧光值更高。验证例2验证本发明提供的引物探针组的特异性。按照上述pcr试剂盒的组分配制,分别加入检测目标病原体和其它干扰病原体进行测试,包括犬副流感病毒、犬瘟热病毒、犬腺病毒2型、支气管败血波氏杆菌、犬冠状病毒、犬细小病毒。然后按照实施例2提供的反应条件进行扩增,图6~9为测试结果。结果显示,各病原体的引物探针只扩增该种病原体,对其余病原体均无交叉扩增。将各组引物的扩增产物进行测序,测序委托西安擎科生物科技有限公司进行。将测序结果在ncbi中进行blast序列对比,对比结果显示扩增产物确实为各病原体中的片段,符合预期。验证例3验证本发明提供的引物探针组的重复性。采用实施例1提供的试剂盒对不同病原体的样本分别进行扩增,每种样本重复扩增10次,得出表3的数据。表3重复性测试数据cpivcdvcav-2bb平均ct值32.9631.3925.633.91cv,%1.461.040.21.42由结果可知,变异系数(cv,%)均小于2%。验证例4本发明实施例1提供的引物探针组的扩增线性测试。根据各病原体的目的基因,委托西安擎科生物科技有限公司分别合成相关质粒。将cpiv的2×107copies/ml的质粒、cdv的2×107copies/ml的质粒、cav-2的2×106copies/ml的质粒、bb的3×107copies/ml的质粒按照10倍梯度稀释后,采用实施例1的引物进行扩增,测试其扩增效率,图10-13为测试结果。结果显示质粒的各个浓度与ct值间呈线性关系,质粒浓度相差10倍,ct值相差约3.3,与理论值相符。验证例5本发明实施例1提供的引物探针组的灵敏度。将各病原体质粒分别稀释至5×102copies/ml、2×102copies/ml的浓度后,分别采用实施例1提供的第一试剂~第四试剂进行pcr扩增,检出率在95%以上的最低样本浓度即为检测限浓度。第一试剂~第四试剂的结果分别如图14~17所示。由结果可知,cpiv、cdv、cav-2、bb的检测下限均为5×102copies/ml。验证例6干扰测试。采用实施例1提供的试剂盒,对cpiv、cdv、cav-2、bb分别进行单重扩增及多重扩增,如:设置实验组1与对照组1,实验组1的pcr反应体系中仅含有一种病原体的引物探针,对照组1中pcr反应体系含有cpiv、cdv、cav-2、bb共4种引物探针。分别加入相同浓度的对应病原核酸进行扩增,结果如图18~图21所示。由以上结果可知,多重体系并未对pcr的扩增产生影响。验证例7采用实施例4和5提供的方法对含多重病原体的样品进行多重pcr检测。实施例4的pcr反应条件为:50℃15min,95℃3min,95℃10s,60℃30s,共40个循环,其中60℃设置采集荧光信号,扩增结果如图22。实施例5的pcr反应条件为:50℃10min,95℃3min,95℃5s,60℃20s,共40个循环,其中60℃设置采集荧光信号,扩增结果如图23。由结果可知,本发明优化的pcr反应条件后对同一浓度的病原体样本扩增无影响。以上所述仅为本发明的优选实施例而已,并不用于限制本发明,对于本领域的技术人员来说,本发明可以有各种更改和变化。凡在本发明的精神和原则之内,所作的任何修改、等同替换、改进等,均应包含在本发明的保护范围之内。序列表<110>上海基灵生物科技有限公司<120>一种用于检测犬呼吸多重病原体的核酸组合物及其试剂盒和方法<160>22<170>siposequencelisting1.0<210>1<211>21<212>dna<213>人工序列<400>1aacgcaccgagatggcaaaat21<210>2<211>21<212>dna<213>人工序列<400>2gcacctgagttgtcccagtct21<210>4<211>22<212>dna<213>人工序列<400>4tcctcccctggtgtctgcccga22<210>4<211>19<212>dna<213>人工序列<400>4atttggatcctgctcgcat19<210>5<211>23<212>dna<213>人工序列<400>5tcattctaaattccccgaccagt23<210>6<211>21<212>dna<213>人工序列<400>6ctcctgatactgcagccgaga21<210>7<211>20<212>dna<213>人工序列<400>7aggcttcagggacaacttgt20<210>8<211>19<212>dna<213>人工序列<400>8ccacggcattgagctgact19<210>9<211>21<212>dna<213>人工序列<400>9actgacccgccagcaccccat21<210>10<211>21<212>dna<213>人工序列<400>10gcagtccttgagcgtgatctc21<210>11<211>21<212>dna<213>人工序列<400>11gtggtgcaattgcccaagaat21<210>12<211>22<212>dna<213>人工序列<400>12cggccagcttcgtctccatcga22<210>13<211>21<212>dna<213>人工序列<400>13acacttgccaaattgaccaca21<210>14<211>21<212>dna<213>人工序列<400>14gctgccatgtaactctcgaat21<210>15<211>23<212>dna<213>人工序列<400>15cagcgggcacctgagttgtccca23<210>16<211>18<212>dna<213>人工序列<400>16gttggtgttgaacttgaa18<210>17<211>19<212>dna<213>人工序列<400>17cttggatgctatttctgac19<210>18<211>19<212>dna<213>人工序列<400>18ggcttcagggacaacttca19<210>19<211>18<212>dna<213>人工序列<400>19caagtccaccacggcatt18<210>20<211>23<212>dna<213>人工序列<400>20gatcgaatacgcctttaggtccg23<210>21<211>19<212>dna<213>人工序列<400>21cgctcaaggactgccccag19<210>22<211>21<212>dna<213>人工序列<400>22cggcccaggctcgaagtaccg21当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1