Myoferlin及其特异性抗体在制备检测鼻咽癌试剂盒中的应用的制作方法
本发明涉及诊断标志物,具体地说,涉及Myoferlin在检测鼻咽癌中的应用。
背景技术:
鼻咽癌是我国南方地区最常见的恶性肿瘤之一,其发生率和死亡率均居世界首位,严重影响国人生命健康安全。鼻咽癌几乎均为低分化鳞癌和未分化癌,恶性程度高,易早期发生颈部淋巴结和远处转移。早期转移是鼻咽癌最重要的特征之一,鼻咽癌远处转移已成为制约其疗效和预后的瓶颈,也是导致鼻咽癌患者死亡的主要原因。在鼻咽癌复杂的转移过程中,细胞表面蛋白参与其中并发挥极其关键调控作用。因此从细胞表面蛋白入手寻找鼻咽癌转移相关蛋白,筛选鼻咽癌早期诊断标志物对于提高疗效、改善预后具有重要意义。
鼻咽癌起病部位隐匿,早期症状不明显,绝大多数患者首次就诊时已发生转移。放疗是目前治疗鼻咽癌的主要手段。早期鼻咽癌放疗后5年生存率可达80%,而由于放疗抵抗和远处转移,鼻咽癌常规放疗后5年生存率仍然徘徊在40%-50%。长期以来,国内外针对提高鼻咽癌疗效进行了多方努力,但总的效果仍不够理想。因此,鼻咽癌早期诊断、转移预测对于鼻咽癌防治具有重要作用。
人Myoferlin基因(Gene ID:26509)位于染色体10q23.33区域,全长176076bp,包含59个外显子。人Myoferlin蛋白(UniProt ID:Q9NZM1)由2061个氨基酸组成,分子量234709Da。Myoferlin是一种钙/磷脂结合蛋白质,属于ferlin膜蛋白家族成员在细胞膜融合、损伤后修复、内吞及酪氨酸激酶受体活性等生物过程中发挥重要作用。Myoferlin蛋白高表达于成肌细胞和内皮细胞,参与骨骼肌发育、修复以及内皮细胞的增殖、迁移等功能,但其在鼻咽癌中的表达和功能未有报道。
技术实现要素:
为了解决现有技术中存在的问题,本发明的目的是提供一种鼻咽癌相关标志物,并提供了该标志物及其特异性抗体在制备检测鼻咽癌试剂盒中的应用。
为了实现本发明目的,本发明的技术方案如下:
第一方面,本发明提供了一种鼻咽癌相关标志物Myoferlin,基因名为人Myoferlin基因(Gene ID:26509)位于染色体10q23.33区域,全长176076bp,包含59个外显子。人Myoferlin蛋白(UniProt ID:Q9NZM1)由2061个氨基酸组成,分子量234709Da。
进一步地,本发明提供了Myoferlin或其特异性抗体在制备检测鼻咽癌的试剂或试剂盒中的应用。
所述试剂盒可为免疫组化试剂盒或酶联免疫检测试剂盒。
进一步地,本发明发现了Myoferlin蛋白在鼻咽癌组织中的表达与淋巴结转移和临床分期有关,因此,所述试剂盒可实现对具有鼻咽癌转移潜能的鼻咽癌的检测。
第二方面,本发明提供了检测Myoferlin的试剂或试剂盒在制备检测鼻咽癌的试剂或试剂盒中的应用。
进一步地,所述检测Myoferlin的试剂或试剂盒优选为可定量检测Myoferlin蛋白的试剂或试剂盒,或优选为检测Myoferlin蛋白表达水平或表达量的试剂或试剂盒。通过分析Myoferlin蛋白的表达量判断样本是否患有鼻咽癌,并进一步判断是否发生淋巴结转移。
本发明的有益效果在于:
本发明提供了鼻咽癌诊断与预后的生物标志物Myoferlin,根据Myoferlin的表达水平判断待测样本是否患有鼻咽癌,并进一步判断是否发生淋巴结转移,有利于鼻咽癌的早发现和早治疗。
本发明为有效判断人鼻咽疾病进程提供了新的科学依据。
附图说明
图1为定量蛋白质组学方法筛选鼻咽癌转移相关细胞表面蛋白实验过程。
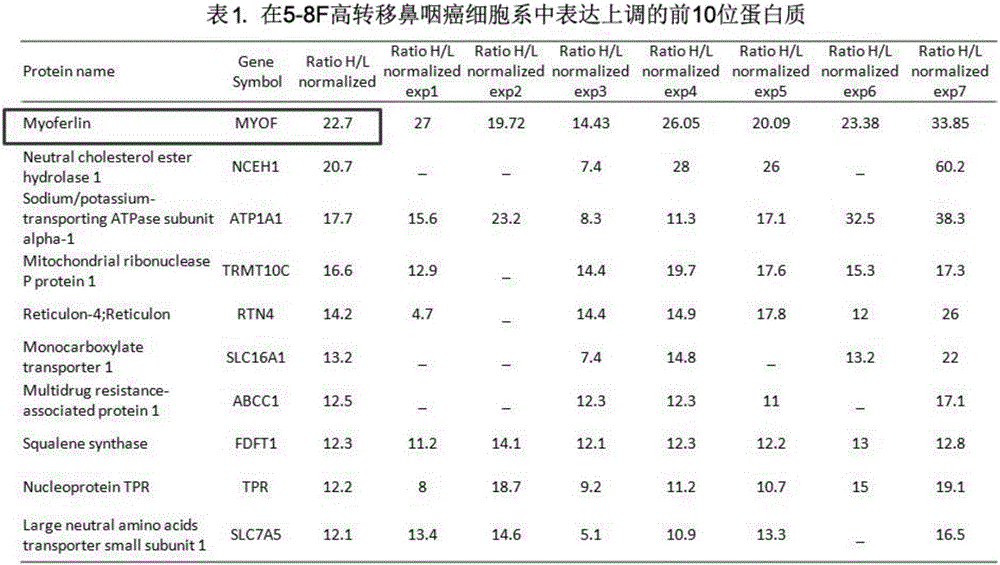
图2为经7次质谱数据分析,在5-8F高转移鼻咽癌细胞系中表达上调倍率最大的前10个蛋白质。
图3为Western blot检测Myoferlin在鼻咽癌细胞中的表达。
图4为免疫组化检测Myoferlin在正常鼻咽粘膜和鼻咽癌组织中的表达。
具体实施方式
下面将结合实施例对本发明的优选实施方式进行详细说明。需要理解的是以下实施例的给出仅是为了起到说明的目的,并不是用于对本发明的范围进行限制。本领域的技术人员在不背离本发明的宗旨和精神的情况下,可以对本发明进行各种修改和替换。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
实施例1
1、为筛选鼻咽癌转移相关细胞表面蛋白质,申请人以高转移鼻咽癌细胞系5-8F与无转移潜能鼻咽癌细胞系6-10B为研究对象,采用体内稳定同位素联合生物素标记的定量蛋白质组学方法,筛选发现Myoferlin蛋白在高转移鼻咽癌细胞系5-8F中的表达显著上调,提示Myoferlin表达上调可能与鼻咽癌的转移潜能有关。具体实验方案如下:
1)体内稳定同位素标记不同转移潜能的鼻咽癌细胞系:将稳定同位素重链(K8R10-‘heavy’),即L-lysine-(13C615N2)(K8)(Thermo公司,88209)和L-arginine-(13C615N4)(R10)(Thermo公司,89990)以及稳定同位素轻链(K0R0-‘light’),即L-lysine-(12C614N2)(K0)(Thermo公司,89987)和L-arginine(12C614N4)(R0)(Thermo公司,89989),分别加入高转移鼻咽癌细胞系5-8F与无转移潜能鼻咽癌细胞系6-10B的含10%透析型血清(Thermo公司,89986)的条件培养基中(Thermo公司,89984)进行体内标记,细胞经过6-8次传代培养后可标记完全。
2)生物素-亲和素系统(Thermo公司,89881)富集细胞表面蛋白质:稳定同位素标记好的鼻咽癌细胞培养瓶中加入生物素分子标记细胞表面蛋白质,接下来利用生物素与亲和素的特异性结合作用,将鼻咽癌细胞表面蛋白质纯化富集起来。
3)液相色谱分离结合质谱分析鉴定蛋白质:富集的蛋白样品经2D Quant Kit蛋白定量试剂盒(GE Healthcare公司,80-6483-56)精确定量后进行等量混合,接下来进行SDS-PAGE胶分离及胰酶酶解,得到的肽段首先经第一维强阳离子交换液相色谱分离,然后再经第二维反相液质联用进行质谱分析,软件采集各组分质谱数据后进行数据库查询以鉴定蛋白质。
4)生物信息学分析:采用生物信息学软件首先对质谱数据结果进行实验相关性和实验变异度分析以确定差异蛋白的筛选倍数,接下来对筛选得到的鼻咽癌转移相关细胞表面蛋白质进行系统的GO富集度分析、信号通路分析以及聚类分析,初步探明这些细胞表面差异蛋白在鼻咽癌侵袭转移过程中的整体变化规律和作用。
由图1所示,A为蛋白质组学方法筛选鼻咽癌转移相关细胞表面蛋白实验流程图。B为质谱鉴定结果的实验相关性分析,7次质谱实验(包括3次生物学重复,2-3实验重复/每次生物学重复)相关性比率R2:0.915-0.968,提示实验重复性好。C为通过生物信息学分析、筛选得到387个差异表达蛋白质。
经7次质谱数据分析,在5-8F高转移鼻咽癌细胞系中表达上调倍率最大的前10个蛋白质(如图2所示)。
2、经过定量蛋白质组学方法筛选,共得到387个差异表达蛋白质,其中Myoferlin是变化倍率最大的蛋白(在高转移5-8F鼻咽癌细胞系中上调22.7倍)。
3、对鼻咽癌转移相关细胞表面蛋白Myoferlin进行蛋白质印迹和免疫组织化学验证。
1)蛋白质印迹验证:采用Western blot进一步验证鼻咽癌转移相关蛋白质Myoferlin分别在鼻咽癌细胞总蛋白及细胞表面蛋白的差异。
操作流程如下:
a,蛋白质抽提:收集培养好的鼻咽癌细胞(5-8F、6-10B)分别分成两份,一份加入RIPA裂解液(碧云天)冰上裂解1小时,间或超声,12000rpm离心30分钟后取上清即为鼻咽癌细胞总蛋白;另一份采用方案2中生物素-亲和素方法富集鼻咽癌细胞表面蛋白质。2D Quant Kit蛋白定量试剂盒进行蛋白质定量。
b,SDS-PAGE胶电泳:取20μg蛋白样品与上样缓冲液充分混匀,95℃煮沸5分钟后迅速置于冰上冷却10分钟,1000g短暂离心后上样于8%的SDS-PAGE胶上,60V电泳30分钟,待蛋白从积层胶跑入分离胶后,将电压设置为100V进行电泳分离,待溴酚蓝指示带跑到距离分离胶底部1厘米左右时停止电泳。
c,转膜:用于转印的PVDF膜先用无水甲醇浸泡10分钟,再转移到纯水中浸泡5分钟,然后与滤纸、凝胶一起置于预冷的转膜缓冲液平衡10分钟后制成三明治。设定100V恒压转膜2小时,使蛋白从凝胶转印至PVDF膜上。
d,抗体孵育:PVDF膜用5%脱脂奶粉于室温下封闭1小时后根据蛋白分子量剪开,分别与Myoferlin特异性抗体(abcam公司,ab76746)和β-actin内参抗体(sigma,A5441)置于4℃冰箱孵育过夜,次日再分别与HRP标记的羊抗鼠二抗(KPL,04-18-06)室温下孵育1小时。
e,采用ECL化学发光,凝胶成像仪采集图像。
图3显示Western blot检测Myoferlin在鼻咽癌细胞中的表达。结果显示Myoferlin在5-8F细胞总蛋白和细胞表面蛋白中表达均高于鼻咽癌细胞系6-10B。
2)免疫组织化学分析Myoferlin在鼻咽癌组织中表达的临床意义:以Myoferlin特异性抗体(abcam公司,ab76746)联合迈新S-P免疫组织化学试剂盒(福建迈新公司)组成诊断试剂盒。
简要操作步骤如下:
a,烤片:石蜡组织切片放置于切片架上,60℃烤箱进行1小时烤片。
b,脱蜡:烤过的切片依次放入100%二甲苯(I,II)中脱蜡2次,每次20分钟。
c,水化:脱蜡后的切片依次用梯度酒精(100%、95%、75%、50%)水化5分钟,然后PBS液水洗3次,每次5分钟。
d,抗原修复:专用切片盒中加入适量枸橼酸盐缓冲液加热至沸腾后,将切片置于切片架上放入切片盒中,95℃煮沸维持15分钟,待其自然冷却至室温后(约1小时),PBS液水洗3次,每次5分钟。
e,用滤纸轻轻将组织周边的液体吸干,每片组织上加过氧化物酶阻断剂(试剂A)一滴,室温孵育10分钟。然后PBS液冲洗3次,每次5分钟。
f,封闭:用滤纸吸去PBS液,每片组织上加正常动物血清(试剂B)一滴,室温孵育10分钟。
g,轻轻除去血清,每片组织上分别加入预冷的PBS液稀释好的一抗Myoferlin(1:200,abcam公司,ab76746)置入湿盒,4℃冰箱孵育过夜。
h,第二天将湿盒从冰箱取出放置常温下,继续孵育30分钟,然后PBS液冲洗3次,每次5分钟。
i,用滤纸吸去PBS液,每片组织上加生物素标记的二抗(试剂C)一滴,室温孵育10分钟。PBS液冲洗3次,每次5分钟。
j,用滤纸吸去PBS液,,每片组织上加链霉素抗生物素-过氧化物酶溶液(试剂D)一滴,室温孵育10分钟。PBS冲洗3次,每次5分钟。
k,用滤纸吸去PBS液,根据每片组织片大小加适量新鲜配置好的DAB溶液,用显微镜仔细观察3-10分钟,掌握好适宜的染色程度。
l,用双蒸水冲洗3次,每次1分钟,每片组织上加一滴成熟苏木素复染10分钟,1%盐酸酒精分色3秒,流水返蓝15分钟。
m,梯度酒精(50%、75%、95%、100%)依次脱水,二甲苯透明5分钟,通风柜内风干30分钟,60℃烤片10分钟,中性树胶封片保存。
n,免疫组织化学染色采用双盲法,以染色强度和阳性细胞数比例综合计分,即积分法计算结果。每张切片随机选取某类细胞至少10个视野(×200),至少1000个细胞进行评分。染色强度根据染色深浅与背景着色对比,以多数细胞呈现的染色特性计分:无着色计为0分,淡黄色计为1分,棕黄色为计2分,棕褐色计为3分。阳性细胞比例:无着色为0分;<30%计为1分;30%-60%计为2分;≥60%计为3分。染色强度和阳性细胞比例两者相加计量:0-2分计为弱阳性(+);3-4分计为阳性(++);5-6分计为强阳性(+++)。染色结果用SPSS软件进行统计学分析,统计学方法为非参数检验,P<0.05被认为有统计学意义。
Myoferlin蛋白在正常鼻咽粘膜组织和鼻咽癌组织中的表达如表1所示:
表1.Myoferlin蛋白在正常鼻咽粘膜组织和鼻咽癌组织中的表达
Myoferlin蛋白在鼻咽癌组织中的表达与鼻咽癌临床病理特征的关系如表2所示:
表2.Myoferlin蛋白在鼻咽癌组织中的表达与鼻咽癌临床病理特征的关系
图4显示,Myoferlin在有转移鼻咽癌组织中的表达较无转移鼻咽癌组织高,且两者均明显高于正常鼻咽粘膜组织。A,正常鼻咽粘膜组织,B,无转移的鼻咽癌组织,C,有转移的鼻咽癌组织。
虽然,上文中已经用一般性说明及具体实施方案对本发明作了详尽的描述,但在本发明基础上,可以对之作一些修改或改进,这对本领域技术人员而言是显而易见的。因此,在不偏离本发明精神的基础上所做的这些修改或改进,均属于本发明要求保护的范围。
- 还没有人留言评论。精彩留言会获得点赞!
- 用于治疗HBV感染和相关病症的三特异性结合分子的制造方法与工艺
- 对磺胺类药物具有特异性的固相微萃取纤维的制备方法与流程
- 一种检测猪初乳中抗PEDV特异性IgA抗体的夹心ELISA试剂盒的制造方法与工艺
- 用于施用CD19xCD3双特异性抗体的给药方案的制造方法与工艺
- 双特异性抗‑VEGF/抗‑ANG‑2抗体及其在治疗眼血管疾病中的应用的制造方法与工艺
- 特异性人EWS‑FLI1融合蛋白抗体的制备方法及在制备尤文肉瘤诊断抗体试剂的应用与制造工艺
- 双特异性四价抗体及其制造和使用方法与制造工艺
- 利用特异性挥发物筛选昆虫相关嗅觉蛋白的方法与制造工艺
- 使用与表面偶联的单特异性四聚抗体复合物组合物从样品中分离出靶实体的方法与制造工艺
- 抗-WT1/HLA双特异性抗体的制造方法与工艺
- 与CD56分子特异性结合的多肽及其应用的制造方法与工艺
- 用于治疗HBV感染和相关病症的三特异性结合分子的制造方法与工艺
- 对磺胺类药物具有特异性的固相微萃取纤维的制备方法与流程
- 避免信号干扰的肌原纤维蛋白丝氨酸磷酸化水平的测定方法与流程
- 一种检测猪初乳中抗PEDV特异性IgA抗体的夹心ELISA试剂盒的制造方法与工艺
- 用于施用CD19xCD3双特异性抗体的给药方案的制造方法与工艺
- 双特异性抗‑VEGF/抗‑ANG‑2抗体及其在治疗眼血管疾病中的应用的制造方法与工艺
- 特异性人EWS‑FLI1融合蛋白抗体的制备方法及在制备尤文肉瘤诊断抗体试剂的应用与制造工艺
- 活化人CD40的抗体和针对人PD‑L1的抗体的组合疗法的制造方法与工艺
- 双特异性四价抗体及其制造和使用方法与制造工艺