以丙酰胺类化合物为活性成分的药物组合物和其在制药中的应用的制作方法
本发明涉及医药技术领域,具体涉及通式(Ⅰ)所示的吡咯烷酮类化合物,及其在抑制TNKS靶标过度表达的癌症中的应用。
背景技术:
Wnt信号通路属于一条在进化上十分保守的信号通路,在胚胎发育和中枢神经系统形成过程中起关键作用,它调控着细胞的生长、迁移和分化。由于它在人类众多肿瘤的发生发展中广泛活化,与肿瘤的关系异常密切,因此Wnt信号通路与肿瘤关系成为近年肿瘤研究的热点。Tankyrases(TNKS)是Wnt信号通道上关键的传递分子,它通过降低轴蛋白Axin的表达水平来使β-catenin增多,从而使Wnt信号上调,其在多数肿瘤中过表达。同时,TNKS也属于二磷酸腺苷核糖多聚合酶(PARP)家族中的一员,对端粒长度有重要的影响。端粒酶和其他6种端粒蛋白组成的端粒蛋白复合物(shelterin)影响端粒的长度,当TNKS过度表达时,它通过核糖基化端粒蛋白TRF1而使端粒长度增加,从而使细胞过度分裂而癌变。因此抑制TNKS的表达对于控制肿瘤的发生具有重要意义。
尽管TNKS已经被证实是多种肿瘤的重要把标,但是到目前为止一些很有希望的TNK S小分子抑制剂还处于理论研究阶段,并且都局限于体外活性测试,比如一些有代表性具有结构多样性的TNKS有抑制剂:Jo Waaler报道的JW551,Howard Bregman报道的49,还有IWR13,IWR2,XAV939,G007-LK4,JW74,WIKI45,Olaparib6,LDW6437以及黄酮类8抑制剂等。但是目前已经发现的TNKS抑制剂的生物活性、透过血脑屏障的能力、成药性等方面的性质都有待提高。
近年来国内、外开展了拮抗端粒酶活性以抑制肿瘤细胞增殖、促进凋亡的多项研究,发现仅仅阻滞其活性并不能达到抗肿瘤的理想效果。因此在成功治愈肿瘤的方法性研究中,定向于端粒长度的维持机制日益受到研究人员的重视。TNKS抑制剂通过稳定轴蛋白(Axin)和促进β连环蛋白(β-catenin)的降解来对抗Wnt信号转导途径,从而抑制肿瘤的生长。因此,抑制TNKS的活性在肿瘤治疗的方法学研究中较有前景。TNKS的发现初步阐明了其在恶性肿瘤细胞中的调节机制,为控制端粒酶作用于端粒提供了新机遇,已代替端粒酶成为癌症治疗靶标研究的新热点。端粒酶阳性的肿瘤细胞核内TNKS过表达可拮抗端粒酶抑制剂MST-312诱导端粒缩短,TNKS的这种作用可被几种已知的PARP抑制剂逆转,如3AB、PJ-34、ABT-888及XAV939等。由此可见,TNKS抑制剂的研究在肿瘤临床治疗中尤为重要。
现有技术中,未见丙酰胺类化合物及其活性的相关报道。
技术实现要素:
本发明的目的是提供式(Ⅰ)中丙酰胺类化合物,以其为活性成分的药物组合物,它们在制备端粒聚合酶(Tankyrases)抑制剂中的应用,以及它们在制备治疗肿瘤的药物中的应用。
为了实现本发明的上述目的,本发明提供了如下的技术方案:
药物组合物,含有通式(Ⅰ)所示的丙酰胺类化合物或其药用盐,以及药学上可以接受的载体,
式(Ⅰ)中,R1为:
R2为:
R3为甲基;
以及,所述的丙酰胺类化合物为如下结构式所示的丙酰胺类化合物1-3,
如所述的药物组合物中的丙酰胺类化合物或其药用盐,其中所述的药用盐是指与有机酸或无机酸形成的药学上可接受的盐,所述的有机酸为酒石酸、柠檬酸、甲酸、乙酸、乙二酸、丙酸、丁酸、草酸、马来酸、己二酸、藻酸、柠檬酸、天冬氨酸、苯磺酸、樟脑酸、樟脑磺酸、二葡糖酸、环戊烷丙酸、十二烷基硫酸、乙磺酸、葡庚糖酸、甘油磷酸、半硫酸、庚酸、己酸、延胡索酸、2-羟基乙磺酸、乳酸、甲磺酸、烟酸、2-萘磺酸、扑酸,果胶酯酸、3-苯基丙酸、苦味酸、新戊酸、琥珀酸,所述的无机酸为盐酸、氢溴酸、氢碘酸、硫酸或磷酸。
TNKS抑制剂,由丙酰胺类化合物和药用常规辅剂组成。
所述的丙酰胺类化合物在制备端粒聚合酶抑制剂中的应用。
所述的丙酰胺类化合物在制备治疗癌症的药物中的应用。
所述的药物组合物在制备端粒聚合酶抑制剂中的应用。
所述的药物组合物在制备治疗癌症的药物中的应用。
本发明丙酰胺类化合物经荧光素酶报告基因测定的wnt信号转导抑制活性筛选,并测得相应半数有效抑制浓度(IC50)。丙酰胺类化合物用作为端粒聚合酶(Tankyrases)抑制剂的新用途。
本发明丙酰胺类化合物可以以组合物的形式通过口服、鼻吸入、直肠或肠胃外给药的方式施用于需要这种治疗的患者。用于口服时,可将其制成常规的固体制剂如片剂、粉剂、粒剂、胶囊等,制成液体制剂如水或油悬浮剂或其他液体制剂如糖浆、酏剂等;用于肠胃外给药时,可将其制成注射用的溶液、水或油性悬浮剂等。本发明药物组合物的各种剂型可以按照药学领域的常规生产方法制备。例如使活性成分与一种或多种载体混合,然后将其制成所需的剂型。
本发明的药物组合物优选含有重量比为0.1%~99.5%的活性成分,最优选含有重量比为0.5%~95%的活性成分。
本发明化合物的施用量可根据用药途径、患者的年龄、体重、所治疗的疾病的类型和严重程度等变化,其日剂量可以是0.01~10mg/kg体重,优选0.1~5mg/kg体重。可以一次或多次施用。
附图说明
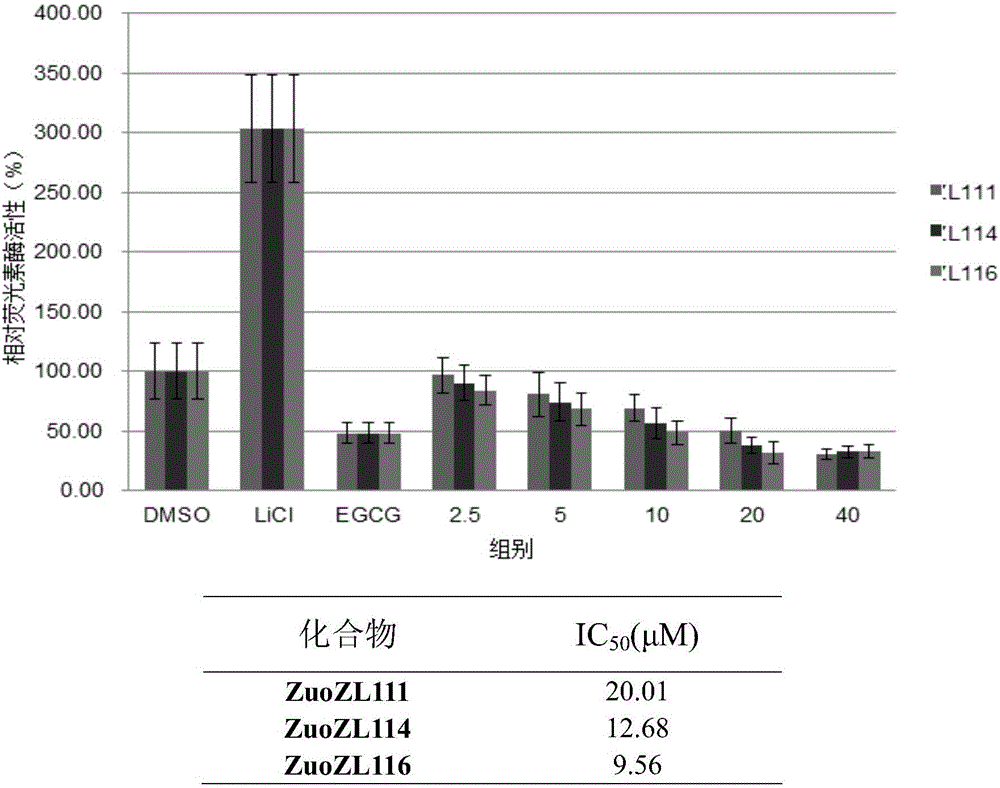
图1为本发明丙酰胺类化合物1-3对端粒聚合酶(Tankyrases)的抑制图。
具体实施方式:
下面结合附图,用本发明的实施例来进一步说明本发明的实质性内容,但并不以此来限定本发明。
实施例1:
本发明丙酰胺类化合物对端粒聚合酶(Tankyrases)的抑制作用:
1、实验原理及步骤
HEK293T细胞接种于96孔板中,培养过夜,共转染80ng SuperTopflash,8ng Renilla和64ng Wnt1质粒,3小时后,加药处理。药物处理24小时,裂解细胞,参照Dual-Luciferase Reporter Assay试剂盒操作说明检测荧光素酶活性,结果用Topflash与Renilla的比值(RLA,相对荧光素酶活性)表示。
2、试剂仪器
试剂:DMEM(HyClone),胎牛血清(HyClone),DualReporter Assay System(Promega)。
仪器:CO2培养箱(Thermo),超净工作台(Thermo),化学发光酶标仪(Thermo)。
3、实验结果
1)抑制率:抑制率=(NC-化合物吸光值平均值)/NC*100%
2)Tankyrases IC50结果:
选自式(Ⅰ)的3个丙酰胺类化合物的化学结构式及相应活性如下所示,其中百分数表示化合物反应终浓度为50μM时对Tankyrase的抑制率。
实施例2:
本发明化合物对端粒聚合酶(Tankyrases)抑制活性IC50的测定:
通过实施例1,筛选出对Tankyrases抑制活性大于或等于60%的化合物,进一步测定其抑制活性IC50值。
1、实验原理(同实施例1)。
2、试剂仪器(同实施例1)。
3、实验结果:
1)抑制率:抑制率=(NC-化合物吸光值平均值)/NC*100%
2)Tankyrases IC50结果见实施例1。
实施例3:
化合物1-3,加入4%的硫酸乙醇溶液,pH=4,过滤,干燥,制成硫酸盐化合物1-3。
实施例4:
化合物1-3,加入4%的盐酸溶液,pH=4,过滤,干燥,制成盐酸盐化合物1-4。
实施例5:
化合物1-3,加入4%的酒石酸溶液,pH=4,过滤,干燥,制成酒石酸盐化合物1-4。
实施例6:
化合物1-3,加入4%的柠檬酸溶液,pH=4,过滤,干燥,制成柠檬酸盐化合物1-4。
实施例7:
片剂:化合物1-3或实施例4-6所得的盐10mg,乳糖180mg,淀粉55mg,硬脂酸镁5mg。
制备方法:将化合物或其盐、乳糖和淀粉混和,用水均匀湿润、把湿润后的混合物过筛并干燥,再过筛,加入硬脂酸镁,然后将混合物压片,每片重250mg,化合物含量为10mg。
实施例8:
安瓿剂:化合物1-3或实施例4-6所得的盐2mg,氯化钠10mg。
制备方法:将化合物或其盐和氯化钠溶解于适量的注射用水中,过滤所得溶液,在无菌条件下装入安瓿瓶中。
实施例9:
注射用冻干剂:化合物1-3或实施例4-6所得的盐10mg,碳酸氢钠2mg,甘露醇252mg。
制备方法:将碳酸氢钠、甘露醇,加注射用水溶解,加活性碳吸附30min除热原,过滤除去活性碳,在滤液中加入化合物或其盐,超声处理使溶解,用1N盐酸调节pH为5.0-7.0,微孔滤膜滤过,加注射用水,分装,冷冻干燥,上塞,轧盖,即得。
实施例10:
胶囊剂:化合物1-3或实施例4-6所得的盐10mg,乳糖187mg,硬脂酸镁3mg。
制备方法:将化合物或其盐与助溶剂混和,过筛,均匀混合,把得到的混合物装入硬明胶胶囊,每个胶囊重200mg,活性成分含量为10mg。
- 还没有人留言评论。精彩留言会获得点赞!