人ASPP2重组腺病毒制备及其抗肿瘤应用的制作方法
本发明属于医药领域,涉及一种重组腺病毒,具体涉及重组腺病毒在抗肿瘤方面的应用。
背景技术:
ASPP2(apoptosis stimulating protein of p53 2),又被称为53BP2L,是p53结合蛋白家族的一个促凋亡成员。ASPP2蛋白全长含有1128个氨基酸,包含了多个结构和功能区:N端具有β-Grasp泛素样折叠和α螺旋结构域,中间部分是脯氨酸富含区,C末端部分是Ank-SH3结构域,包含4个Ankyrin重复序列和1个SH3结构域(Src同源3结构域)。ASPP2的不同结构域都有相互作用蛋白,其中C末端介导了P53、Bcl-2等大部分的蛋白间相互作用。ASPP2最被熟知的功能即调节p53及其家族成员(p63和p73)的促凋亡能力。ASPP2增强p53家族成员的活力并特异性促进促凋亡靶基因而不是细胞周期抑制基因的表达。体外研究证实ASPP2通过p53或非P53介导通路抑制细胞生长,促进细胞凋亡,ASPP2能够以p53依赖和非依赖途径,增强药物促凋亡和治疗的敏感性,说明ASPP2可以通过促进药物诱导的凋亡作用来抑制肿瘤。动物实验发现ASPP2等位基因敲除小鼠模型易于造成自发肿瘤和γ射线诱导肿瘤的形成,ASPP2限制癌基因Ras的入侵前特性并抑制体内肿瘤转移。临床研究显示ASPP2在人类癌症组织中常常表达下调,这种表达受抑与肿瘤的发生进展以及不良预后密切相关。提示ASPP2是一个肿瘤抑制基因,在肿瘤的发生中起重要作用,可能是肿瘤治疗的重要靶点,也可能是基因治疗的重要切入点。
技术实现要素:
本发明提供一种ASPP2重组腺病毒,所述重组腺病毒包含ASPP2全长基因序列。本发明所述的重组腺病毒,其制备方法如下:
步骤1、将ASPP2基因与穿梭质粒(pAdTrack-CMV)相连接,构建重组穿梭质粒pAdTrack-CMV-ASPP2;
步骤2、再将重组穿梭质粒线性化后与骨架质粒pAdEasy-1在大肠杆菌BJ5183中同源重组,构建重组腺病毒载体Ad-ASPP2;
步骤3、将重组腺病毒载体Ad-ASPP2在293T细胞中扩增,经过提取分离纯化得到。
以下具体说明本发明腺病毒的制备方法:
材料来源
Pcr3.1-ASPP2质粒由北京市肝病研究所构建;大肠杆菌BJ5183、穿梭质粒pAdTrack-CMV和腺病毒骨架质粒pAdEasy-1购自Strategene公司。293细胞购构自ATCC。
制备方法及结果
1 构建重组重组穿梭质粒pAdTrack-CMV-ASPP2
Pcr3.1-ASPP2质粒经KpnI和XbaI双酶切出Kb的目的基因,琼脂糖凝胶电泳,glassmilk法凝胶回收目的片段,亚克隆至经同样酶切的腺病毒穿梭质粒pAdTrack-CMV,形成pAdTrack-CMV-ASPP2。
2 细菌内同源重组构建重组腺病毒载体Ad-ASPP2
pAdTrack-CMV-ASPP2用PmeI线性化后,琼脂糖凝胶电泳,凝胶回收目的片段,用牛小肠碱性酶去磷酸化,乙醇沉淀备用。制备BJ5183点穿孔菌,pAdTrack-CMV-ASPP2和pAdEasy-1质粒电穿孔(电穿孔条件:2500V,280Ω,200μF)法共转染,电穿孔后取适量的细胞在50mg/L卡那霉素的培养板中,在37℃培养16-20h,挑取克隆,抽提的质粒即为重组病毒质粒Ad-ASPP2。
3 Ad-ASPP2扩增、纯化
用重组腺病毒Ad-ASPP2感染293细胞,在48-72h左右出现CPE效应后收集细胞。细胞反复冻融裂解细胞,12000rpm离心,小心取上清,装入超速离心管,取1.25g/mlCsCl溶液,缓慢注入超速离心管底,65000rpm离心3h。在病毒带处收集液体,将液体加入超速浓缩离心管中,并加入等体积的2×病毒缓冲液(10mM Tris-HCl pH8.0,100mM NaCl),5000rpm离心2次,收集病毒。
4 Ad-ASPP2鉴定
提取病毒基因组DNA,对重组腺病毒载体结构基因E2B和目的基因ASPP2进行PCR扩增。PCR产物经1%琼脂糖凝胶电泳分子量鉴定。E2B区引物序列为:上游引物5’-TCGTTTCTCAGCAGCTGTTG-3’,下游引物5’-CATCTGAACTCAAAGCGTGG-3’;扩增片段大小为880bp;扩增条件为:94℃变性5min;94℃变性20s,55℃复性30s,72℃延伸1min,共40个循环;72℃延伸5min。ASPP2的引物序列为:上游引物
5’-AGCTGCCATGGAGACCATCT-3’,下游引物5’-ACTGTTCTCCGTACTGGCAC-3’;扩增片段大小为220bp;扩增条件为:95℃变性3min;94℃变性1min,55℃复性1min,72℃延伸1min,共3个循环;94℃变性30s,55℃复性45s,72℃延伸45s,共27个循环;72℃延伸5min。
本发明还包括含有本发明所述的重组腺病毒的药物制剂。所述的药物制剂,其中还含有药学上可接受的载体,所述制剂优选为注射剂。
本发明还包括,本发明的重组腺病毒在制备抗肿瘤的基因药物中的应用。
本发明所述肿瘤包括:肝癌、结肠癌、乳腺癌、胰腺癌、皮肤癌、宫颈癌、胃癌、结肠癌、白血病、淋巴癌、鼻咽癌等。特别是,本发明的ASPP2重组腺病毒在治疗肝癌方面具有非常好的效果,尤其对P53突变和P53野生肝癌效果好。
本发明所述腺病毒可以高效感染肝癌细胞,体外抑制肝癌细胞增殖,体内瘤体内直接注射抑制肝癌组织生长并具有协同P53、奥沙利铂和索拉菲尼的作用。
本发明所述的重组腺病毒的抗肿瘤活性,所采用的肿瘤细胞为人肝癌hepG2,Huh7,Hep3B细胞株。
以下通过实验数据进一步说明本发明腺病毒的抗肿瘤活性:
一、Ad-ASPP2体外对肝癌细胞的抑制作用
1 Ad-ASPP2体外对肝癌细胞的抑制作用
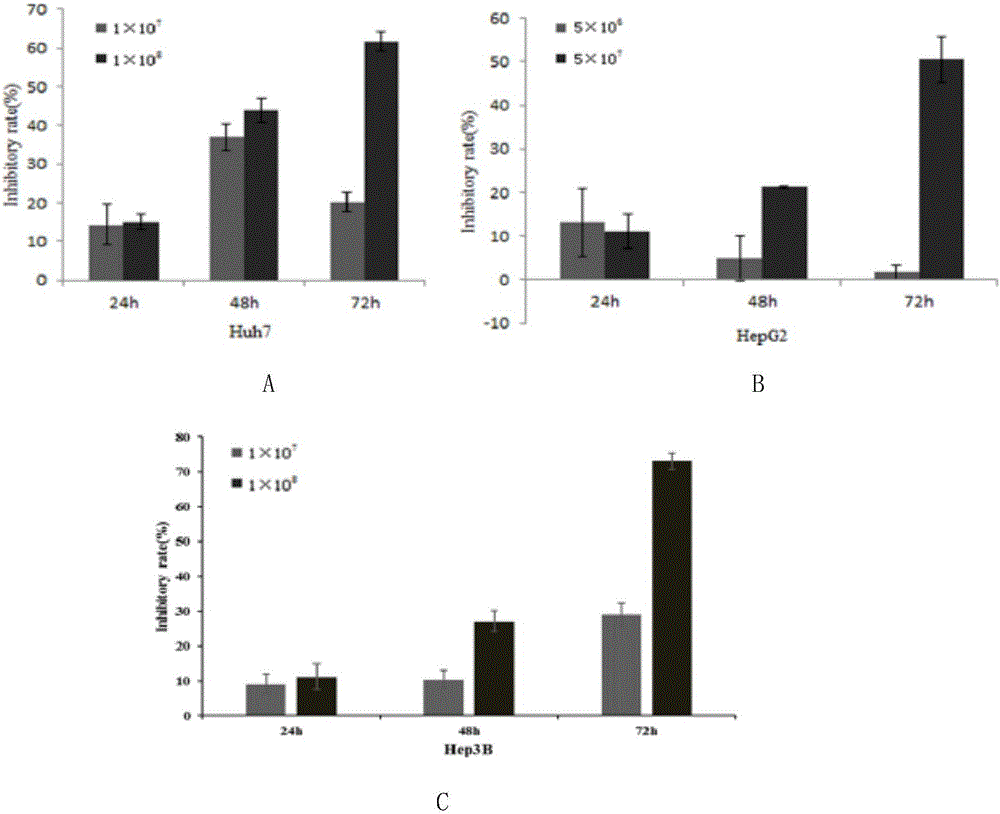
MTT法结果显示:与阴性对照相比,Ad-ASPP2在不同时间段(24-72h)都存在不同程度的生长抑制作用。当Ad-ASPP2在1×108pfu/mL滴度下作用Huh7细胞72h时的生长抑制率为61.69%;当Ad-ASPP2在5×107pfu/mL滴度下作用HepG2细胞72h时的生长抑制率为50.5%;当Ad-ASPP2在1×108pfu/mL滴度下作用Hep3B细胞72h时的生长抑制率为73.06%,说明Ad-ASPP2对肝癌HepG2、Huh7和Hep3B细胞都具有明显的生长抑制作用。
平板克隆形成能力方面:与阴性对照相比180.33±30.00,Ad-ASPP2可以明显抑制HepG2细胞形成的细胞克隆数95.66±11.59。
2 Ad-ASPP2体外联合Ad-p53对肝癌细胞的抑制作用
Ad-ASPP2联合Ad-p53作用时,三种细胞表现出不同的反应。
HepG2和Huh7细胞:在作用48-72h,Ad-ASPP2对细胞抑制作用大于Ad-p53,二者具有协同抑制细胞生长的作用。说明Ad-ASPP2对于P53野生和突变的细胞作用大于Ad-p53。
Hep3B细胞:Ad-ASPP2对细胞抑制作用小于Ad-p53,二者协同抑制细胞生长的作用不显著。说明Ad-ASPP2对于P53缺失的细胞作用不明显。
3 Ad-ASPP2体外联合索拉菲尼对肝癌细胞的抑制作用
HepG2和Hep3B细胞:索拉菲尼能够以剂量依赖性方式抑制HepG2和Hep3B细胞的增殖。我们在不同浓度梯的索拉菲尼作用下时给予滴为1×107pfu/mL的ASPP-rAd干预,MTT实验结果显示,ASPP2-rAd可以促进索拉菲尼在1.56μM、3.12μM和6.25μM三个浓度下对HepG2细胞的增殖抑制作用。
3 Ad-ASPP2体外联合奥沙利铂对肝癌细胞的抑制作用
HepG2和Hep3B细胞:Ad-ASPP2(1.25×108,6.125×107pfu/mL)可以增强奥沙利铂(10,20μg/ml)的对肝癌细胞的抑制作用oxa1:20μg/ml;oxa2:10μg/ml;ASPP2-1:1.25×108pfu/ml Ad-ASPP2;ASPP2-2:6.125×107pfu/ml Ad-ASPP2.
二、Ad-ASPP2体内对肝癌移植瘤的抑制作用
1 单纯Ad-ASPP2肝癌移植瘤的抑制作用
Ad-ASPP2(1×108pfu/次)可以明显抑制HepG2(p53野生型)移植瘤和Huh7(p53突变型)移植瘤的生长,相对肿瘤增殖率(T/C%)分别为37.27%和53.77%(评判标准T/C<60%),说明对具有明显的体内抑制肝癌移植瘤的作用。HepG2p53-/-和Hep3B(p53缺失型)的移植瘤具有一定的移植趋势。
2 Ad-ASPP2联合Ad-P53对肝癌移植瘤的抑制作用
对于HepG2和Huh7肝癌移植瘤,Ad-ASPP2的抑制作用大于Ad-P53;但Ad-ASPP2和Ad-P53协同作用不显著。
3 Ad-ASPP2联合索拉菲尼对肝癌移植瘤的抑制作用
Ad-ASPP2和索拉菲尼单独对hepG2p53-/-移植瘤抑制作用不显著,但二者联合对hepG2p53-/-移植瘤的抑制作用显著。
4 Ad-ASPP2联合奥沙利铂对肝癌移植瘤的抑制作用
Ad-ASPP2和奥沙利铂单独对hep3B移植瘤抑制作用不显著,但二者联合对hep3B移植瘤的抑制作用显著。
本发明和现有同类重组腺病毒相比,具有以下优越性:
制备方法采用Pcr3.1-ASPP2质粒,表达率高于现有技术15%。
具有优良的抗肝癌的作用。
具有优良的抗肝癌转移癌的作用。
对其他肿瘤的作用均逊于上述本发明实验的瘤株。如对肺癌效果不佳,对胃癌效果不佳,对乳腺癌效果不佳。
【附图说明】
图1,ASPP2和E2B基因的PCR产物图:其中,1-3为ASPP2的基因扩增产物,1:阴性对照;2:293T细胞;3:纯化后的Ad-ASPP2,4-6为E2B的基因扩增产物,4:293T细胞;5:纯化后的Ad-ASPP2;6:阴性对照;M:DNA marker 2000。
图2A,Ad-ASPP2体外对肝癌细胞Huh7的抑制作用,
图2B,Ad-ASPP2体外对肝癌细胞hepG2的抑制作用,
图2C,Ad-ASPP2体外对肝癌细胞Hep3B的抑制作用,
与阴性对照相比180.33±30.00,Ad-ASPP2可以明显抑制HepG2细胞形成的细胞克隆数95.66±11.59。
图3A,Ad-ASPP2体外联合Ad-p53对HepG2细胞相对生存率影响
图3B,Ad-ASPP2体外联合Ad-p53对HepG2细胞生长状态影响(白光,40倍)图3C,Ad-ASPP2体外联合Ad-p53对Huh7细胞相对生存率影响
图3D,Ad-ASPP2体外联合Ad-p53对Huh7细胞生长状态影响(白光,40倍)
图3E,Ad-ASPP2体外联合Ad-p53对Hep3B细胞相对生存率影响
图3F,Ad-ASPP2体外联合Ad-p53对Hep3B细胞生长状态影响(白光,40倍)活细胞百分率(Cell survival rate,%)=处理组OD值/对照组OD值×100%。
图4A,Ad-ASPP2体外联合索拉菲尼对肝癌细胞hepG2的抑制作用
图4B,Ad-ASPP2体外联合索拉菲尼对肝癌细胞Hep3B的抑制作用
图5A,Ad-ASPP2体外联合奥沙利铂对肝癌细胞hepG2的抑制作用(24H)
图5B,Ad-ASPP2体外联合奥沙利铂对肝癌细胞hepG2的抑制作用(48H)
图5C,Ad-ASPP2体外联合奥沙利铂对肝癌细胞Hep3B的抑制作用(24H)
图5D,Ad-ASPP2体外联合奥沙利铂对肝癌细胞Hep3B的抑制作用(48H)
其中,oxa1:20μg/ml;oxa2:10μg/ml;ASPP2-1:1.25×108pfu/ml Ad-ASPP2;ASPP2-2:6.125×107pfu/ml Ad-ASPP2.
图6A,Ad-ASPP2对HepG2皮下移植瘤的抑制作用
图6B,Ad-ASPP2对Huh7皮下移植瘤的抑制作用
图6C,Ad-ASPP2对HepG2p53-/-皮下移植瘤的抑制作用
图6D,Ad-ASPP2对Hep3B皮下移植瘤的抑制作用
图7A,Ad-ASPP2联合Ad-P53对HepG2皮下移植瘤相对肿瘤体积的影响
图7B,Ad-ASPP2联合Ad-P53对HepG2皮下移植瘤裸鼠体重的影响
图7C活体成像法观测Ad-ASPP2联合Ad-P53对HepG2皮下移植瘤的影响
图7D,Ad-ASPP2联合Ad-P53对HepG2移植瘤的相对肿瘤增殖率的影响
图8A,Ad-ASPP2联合Ad-P53对Huh7皮下移植瘤相对肿瘤体积的影响
图8B,Ad-ASPP2联合Ad-P53对Huh7皮下移植瘤裸鼠体重的影响
图8C,活体成像法观测Ad-ASPP2联合Ad-P53对Huh7皮下移植瘤的影响
图8D,Ad-ASPP2联合Ad-P53对Huh7移植瘤的相对肿瘤增殖率的影响
图9A,Ad-ASPP2联合索拉菲尼对HepG2p53-/-皮下移植瘤相对肿瘤体积的影响
图9B,Ad-ASPP2联合索拉菲尼对HepG2p53-/-皮下移植瘤裸鼠体重的影响
图9C,活体成像法观测Ad-ASPP2联合索拉菲尼对HepG2p53-/-皮下移植瘤的影响
图9D,Ad-ASPP2联合索拉菲尼对HepG2p53-/-皮下移植瘤总光密度的影响
图10A,大体观测Ad-ASPP2联合奥沙利铂对Hep3B皮下移植瘤的影响
图10B,小动物B超观测Ad-ASPP2联合奥沙利铂对Hep3B皮下移植瘤内部血供的影响
图10C,Ad-ASPP2联合奥沙利铂对Hep3B皮下移植瘤裸鼠体重的影响
图10D,Ad-ASPP2联合奥沙利铂对Hep3B皮下移植瘤相对肿瘤体积的影响
【具体实施方式】
以下通过具体实施例进一步说明本发明
实施例1
制备方法详述
本发明腺病毒的制备方法,原材料来源,产物的鉴定等内容:
材料来源
Pcr3.1-ASPP2质粒由北京市肝病研究所构建;大肠杆菌BJ5183、穿梭质粒pAdTrack-CMV和腺病毒骨架质粒pAdEasy-1购自Strategene公司。293细胞购构自ATCC。
制备方法及结果
1 构建重组重组穿梭质粒pAdTrack-CMV-ASPP2
Pcr3.1-ASPP2质粒经KpnI和XbaI双酶切出Kb的目的基因,琼脂糖凝胶电泳,glassmilk法凝胶回收目的片段,亚克隆至经同样酶切的腺病毒穿梭质粒pAdTrack-CMV,形成pAdTrack-CMV-ASPP2。
2 细菌内同源重组构建重组腺病毒载体Ad-ASPP2
pAdTrack-CMV-ASPP2用PmeI线性化后,琼脂糖凝胶电泳,凝胶回收目的片段,用牛小肠碱性酶去磷酸化,乙醇沉淀备用。制备BJ5183点穿孔菌,pAdTrack-CMV-ASPP2和pAdEasy-1质粒电穿孔(电穿孔条件:2500V,280Ω,200μF)法共转染,电穿孔后取适量的细胞在50mg/L卡那霉素的培养板中,在37℃培养16-20h,挑取克隆,抽提的质粒即为重组病毒质粒Ad-ASPP2。
3 Ad-ASPP2扩增、纯化
用重组腺病毒Ad-ASPP2感染293细胞,在48-72h左右出现CPE效应后收集细胞。细胞反复冻融裂解细胞,12000rpm离心,小心取上清,装入超速离心管,取1.25g/mlCsCl溶液,缓慢注入超速离心管底,65000rpm离心3h。在病毒带处收集液体,将液体加入超速浓缩离心管中,并加入等体积的2×病毒缓冲液(10mM Tris-HCl pH8.0,100mM NaCl),5000rpm离心2次,收集病毒。
4 Ad-ASPP2鉴定
提取病毒基因组DNA,对重组腺病毒载体结构基因E2B和目的基因ASPP2进行PCR扩增。PCR产物经1%琼脂糖凝胶电泳分子量鉴定。E2B区引物序列为:上游引物5’-TCGTTTCTCAGCAGCTGTTG-3’,下游引物5’-CATCTGAACTCAAAGCGTGG-3’;扩增片段大小为880bp;扩增条件为:94℃变性5min;94℃变性20s,55℃复性30s,72℃延伸1min,共40个循环;72℃延伸5min。ASPP2的引物序列为:上游引物
5’-AGCTGCCATGGAGACCATCT-3’,下游引物5’-ACTGTTCTCCGTACTGGCAC-3’;扩增片段大小为220bp;扩增条件为:95℃变性3min;94℃变性1min,55℃复性1min,72℃延伸1min,共3个循环;94℃变性30s,55℃复性45s,72℃延伸45s,共27个循环;72℃延伸5min。
本发明所述ASPP2是已知产物,其蛋白序列如下:
MMPMFLTVYLSNNEQHFTEVPVTPETICRDVVDLCKEPGESDCH
LAEVWCGSERPVADNERMFDVLQRFGSQRNEVRFFLRHERPPGRDIVSGPRSQDPSLKRNGVKVPGEYRRKENGVNSPRMDLTLAELQEMASRQQQQIEAQQQLLATKEQRLKFLKQQDQRQQQQVAEQEKLKRLKEIAENQEAKLKKVRALKGHVEQKRLSNGKLVEEIEQMNNLFQQKQRELVLAVSKVEELTRQLEMLKNGRIDSHHDNQSAVAELDRLYKELQLRNKLNQEQNAKLQQQRECLNKRNSEVAVMDKRVNELRDRLWKKKAALQQKENLPVSSDGNLPQQAASAPSRVAAVGPYIQSSTMPRMPSRPELLVKPALPDGSLVIQASEGPMKIQTLPNMRSGAASQTKGSKIHPVGPDWSPSNADLFPSQGSASVPQSTGNALDQVDDGEVPLREKEKKVRPFSMFDAVDQSNAPPSFGTLRKNQSSEDILRDAQVANKNVAKVPPPVPTKPKQINLPYFGQTNQPPSDIKPDGSSQQLSTVVPSMGTKPKPAGQQPRVLLSPSIPSVGQDQTLSPGSKQESPPAAAVRPFTPQPSKDTLLPPFRKPQTVAASSIYSMYTQQQAPGKNFQQAVQSALTKTHTRGPHFSSVYGKPVIAAAQNQQQHPENIYSNSQGKPGSPEPETEPVSSVQENHENERIPRPLSPTKLLPFLSNPYRNQSDADLEALRKKLSNAPRPLKKRSSITEPEGPNGPNIQKLLYQRTTIAAMETISVPSYPSKSASVTASSESPVEIQNPYLHVEPEKEVVSLVPESLSPEDVGNASTENSDMPAPSPGLDYEPEGVPDNSPNLQNNPEEPNPEAPHVLDVYLEEYPPYPPPPYPSGEPEGPGEDSVSMRPPEITGQVSLPPGKRTNLRKTGSERIAHGMRVKFNPLALLLDSSLEGEFDLVQRIIYEVDDPSLPNDEGITALHNAVCAGHTEIVKFLVQFGVNVNAADSDGWTPLHCAASCNNVQVCKFLVESGAAVFAMTYSDMQTAADKCEEMEEGYTQCSQFLYGVQEKMGIMNKGVIYALWDYEPQNDDELPMKEGDCMTIIHREDEDEIEWWWARLNDKEGYVPRNLLGLYPRIKPRQRSLA"
编码ASPP2蛋白的基因也是已知序列,序列如下:
- 还没有人留言评论。精彩留言会获得点赞!