基于层层点击键合自组装的聚乳酸材料及其制备方法与流程
本发明属于生物医用材料、高分子化学和生物大分子自组装技术领域,具体涉及一种基于层层点击键合自组装的表面血液相容性提高的聚乳酸材料及其制备方法。
背景技术:
聚乳酸是一种具有良好生物相容性、生物安全性和可降解性的生物材料,已被广泛应用于骨固定修复材料、组装工程支架材料、药物控制释放载体等生物医用材料领域。然而,聚乳酸材料疏水性强,在与血液直接接触时,容易引起血浆中一系列非特异性的蛋白质吸附,血小板粘附,最终导致凝血,从而形成血栓不良反应,因此,提高聚乳酸材料的血液相容性迫在眉睫。
采用层层自组装的方法,将生物多糖固定到聚乳酸材料表面是提高其血液相容性的一种有效途径。中国专利cn102675674a公开了一种溶菌酶和香菇多糖硫酸酯自组装修饰的聚乳酸材料及其制备方法,该申请采用静电层层自组装法将溶菌酶和香菇多糖硫酸酯交替沉积到表面氨基化的聚乳酸材料上,制备的聚乳酸材料表面血液相容性得到了改善。该申请使用静电层层自组装技术,层与层之间仅依靠弱的静电相互作用力结合,制备的溶菌酶/香菇多糖硫酸酯多层膜稳定性较差,易从聚乳酸材料基底上脱落,限制了其在实际中的应用。
点击化学是由诺贝尔化学奖获得者sharpless教授于2001年首次提出,其中最主要的一类点击化学反应是由cu(i)化合物催化叠氮化合物与含炔基化合物反应生成1,2,3-三唑五元环化合物。点击化学能将两种不同物质通过五元环共价结合起来,具备产量高、效率高、副反应少、反应条件温和等优点,因而得到了广泛应用。目前,还未见与本申请相关的报道。
技术实现要素:
本发明针对现有技术的不足,提供一种基于层层点击键合自组装的聚乳酸材料,本发明聚乳酸材料由基材和修饰层组成,基材由表面叠氮化的聚乳酸材料构成,修饰层是在所述基材的表面利用层层点击键合自组装进行表面修饰而得到;其中,修饰层中含有在所述基材表面层层点击键合自组装的含炔基纤维素硫酸酯和叠氮壳聚糖。
本发明另一目的是提供上述基于层层点击键合自组装的聚乳酸材料的制备方法,该方法通过点击反应将含叠氮基的壳聚糖与含炔基的纤维素硫酸酯交替共价固定在聚乳酸材料表面,通过组装层数的控制使得聚乳酸材料表面亲水性显著提高,从而提高材料的血液相容性。
本发明方法通过点击反应在层与层之间形成共价连接,从而进一步提高多层膜的稳定性,提高其实际应用价值。本申请中使用的壳聚糖是甲壳素脱乙酰化后的一种天然阳离子多糖,具有安全无毒、良好生物相容性和生物可降解性、以及广谱抗菌等优点,已被广泛应用于人造皮肤、人造血管、可吸收手术缝合线等生物材料领域;纤维素是自然界中存在最为广泛的一种多糖,具有来源广泛、生物相容性、可生物降解等优点,通过硫酸化改性后的纤维素已被证明具有显著的抗凝血活性。
本发明基于层层点击键合自组装的聚乳酸材料的制备方法,包括以下步骤:
(1)聚乳酸材料表面的叠氮化处理:
聚乳酸膜片的制备:按聚乳酸:二氯甲烷=(5~10)g:(50~100)ml的比例,混合搅拌均匀,待聚乳酸完全溶解后将溶液倒入平底玻璃比色皿内,在室温下干燥24~48h后,得到聚乳酸薄膜。随后用质量百分比50%的乙醇水溶液中对薄膜进行搅拌清洗2~3h,以去除表面粘附的油脂和其它杂质,然后用蒸馏水冲洗,在40~50℃下真空干燥24~36h,得到聚乳酸膜片;
聚乳酸膜片表面的胺解:将5~10g聚乳酸膜片浸泡在浓度0.05~0.09g/ml50~100ml的含1,6-己二胺的异丙醇溶液中,在37~60℃下搅拌反应2~5min,得到表面带有氨基的聚乳酸膜片,再用大量蒸馏水冲洗聚乳酸膜片,去除未反应的1,6-己二胺;
胺解聚乳酸膜片表面的叠氮化:将5~10g胺解聚乳酸膜片、0.2~0.4g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc·hcl)、0.1~0.2g对叠氮苯甲酸倒入80~100ml甲醇中搅拌,然后再向其中缓慢滴入0.5~0.8ml的n,n,n’,n’-四甲基乙二胺(temed),在室温下搅拌48~72h后,将膜片取出用甲醇反复清洗多次,然后在室温条件下避光真空干燥,得到表面含叠氮基的聚乳酸膜片,将其裁剪成2×2cm的尺寸备用;
(2)叠氮壳聚糖和含炔基纤维素硫酸酯的制备
叠氮壳聚糖的制备:将1~2g壳聚糖,0.2~0.4gedc·hcl,0.2~0.3g对叠氮苯甲酸倒入80~100ml甲醇中搅拌,然后再向混合液中缓慢滴入0.4~0.8ml的temed,在室温下搅拌48~72h,反应结束后过滤,得到叠氮壳聚糖,将得到的叠氮壳聚糖用甲醇反复清洗多次,然后在室温条件下避光真空干燥;
含炔基纤维素的制备:首先将2~6g纤维素置于50~100ml甲苯/n,n-二甲基乙酰胺(体积比2:1)混合液中,随后向混合液中添加900~1000mg对甲苯磺酰氯、400~500μl吡啶和900~1000mg5-己炔酸,70~80℃条件下搅拌反应36~48h;冷却到室温后,过滤得到含炔基纤维素;随后用大量去离子水和乙醇对含炔基纤维素进行反复冲洗,48~50℃条件下干燥48~72h;
含炔基纤维素硫酸酯的制备:取二甲基亚砜10~20ml中加入0.5~1g无水licl,待licl溶解后,加入0.5~1g含炔基纤维素,93~94℃充分溶解,冷却后,加入3~4g三氧化硫-吡啶复合物,66~70℃反应5~6h,取下烧瓶置于冰水浴中,用20mol/lnaoh溶液调节ph值至中性,以无水乙醇沉淀,离心取沉淀,并用无水乙醇洗涤3~5次;将沉淀溶于去离子水中,在常温下置于透析袋中去离子水透析72h,然后将透析液于50℃下减压蒸发浓缩,冷冻干燥,即得到含炔基纤维素硫酸酯。
(3)叠氮壳聚糖溶液、含炔基纤维素硫酸酯溶液的制备
叠氮壳聚糖溶液的制备:按叠氮壳聚糖:乙酸:硫酸铜:抗坏血酸:去离子水=(100.0~180.0)mg:3ml:(200~240)mg:(500~600)mg:147ml的比例,将上述物质混匀得到叠氮壳聚糖溶液;
含炔基纤维素硫酸酯溶液的制备:按含炔基纤维素硫酸酯:硫酸铜:抗坏血酸:去离子水=(100.0~200.0)mg:(200~240)mg:(500~600)mg:150ml的比例,将上述物质混匀得到含炔基纤维素硫酸酯溶液;
(4)叠氮壳聚糖和含炔基纤维素硫酸酯在聚乳酸材料表面的层层点击键合自组装
取上述步骤(1)制备的2×2cm尺寸的叠氮化聚乳酸膜片在室温条件下浸泡于10ml含炔基纤维素硫酸酯溶液中1~2h进行点击反应,然后取出膜片用去离子水洗涤3~5次,得到表面具有一层含炔基纤维素硫酸酯的改性膜片;利用第一层反应结合在聚乳酸膜片上的含炔基纤维素硫酸酯中没有反应的炔基与具有叠氮基的壳聚糖进行点击反应,随后将上述膜片室温条件下浸泡于10ml叠氮壳聚糖溶液中1~2h进行点击反应,取出膜片用去离子水洗涤3~5次,完成基材表面第一个双分子层自组装;反复进行上述过程,直至制得所需层数的聚乳酸材料即可结束反应;最后将膜片在35~45℃条件下真空干燥24~48h,得到纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸材料,要求纤维素硫酸酯处于材料最外层。
本发明的有益效果是:
首先,本发明采用基于点击反应的层层自组装表面修饰方法,具有操作简单易控、反应条件温和等优点,能够在室温水溶液条件下进行操作,非常有利于保持生物多糖的天然构象和生物活性,并且该方法制备的自组装多层膜层与层之间依靠强的共价键结合,具有稳定性强、不易从基底材料上脱落的优点,更利于实际应用。
其次,本发明所采用的聚乳酸材料表面修饰物质均为具有生物活性的生物多糖(壳聚糖和纤维素硫酸酯),它们来源于动植物,具有良好的亲水性和生物相容性,同时纤维素硫酸酯是一种带有硫酸基的类肝素物质,这些硫酸基在生理环境中显示出较强的负电荷,有利于排斥血浆蛋白的非特异吸附,因此,利用纤维素硫酸酯/壳聚糖多层膜进行聚乳酸材料表面修饰可有效提高其血液相容性和生物相容性。
附图说明
图1为本发明聚乳酸材料表面叠氮化处理反应示意图;
图2为本发明叠氮壳聚糖的制备反应示意图;
图3为本发明炔基纤维素硫酸酯的制备反应示意图;
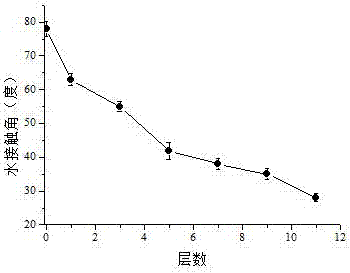
图4本发明实施例1层层点击键合自组装修饰过程中聚乳酸材料表面的静态水接触角变化情况;
图5本发明实施例1被修饰聚乳酸材料表面aptt变化图;其中ppp代表贫血小板血浆,m-0代表未被修饰聚乳酸膜片,m-2.5代表表面修饰了2.5个双分子层纤维素硫酸酯/壳聚糖多层膜的聚乳酸膜片,m-5.5表面修饰了5.5个双分子层纤维素硫酸酯/壳聚糖多层膜的聚乳酸膜片。
具体实施方式
下面结合附图和实施例对本发明作进一步详细说明,但本发明的保护范围并不限于所述内容。
实施例1:本基于层层点击键合自组装的聚乳酸材料由基材和修饰层组成,基材为表面叠氮化的聚乳酸材料,修饰层是在所述基材的表面利用层层点击键合自组装进行表面修饰而得到;其中,修饰层中含有在所述基材表面层层点击键合自组装的含炔基纤维素硫酸酯和叠氮壳聚糖。
如图1、2、3所示,上述材料的制备方法如下:
(1)聚乳酸材料表面的叠氮化处理
聚乳酸膜片的制备:按照聚乳酸:二氯甲烷=5g:50ml的比例搅拌混合2个原料,待聚乳酸完全溶解后将溶液倒入平底玻璃比色皿内,在室温下干燥24h后,得到聚乳酸薄膜。随后用质量百分比50%的乙醇水溶液中对薄膜进行搅拌清洗2h,以去除表面粘附的油脂和其它杂质,然后用蒸馏水冲洗,在40℃真空干燥24h,得到聚乳酸膜片;
聚乳酸膜片表面的胺解:将5g聚乳酸膜片浸泡在0.05g/ml50ml含1,6-己二胺的异丙醇溶液中,在37℃下搅拌反应2min,得到表面带有氨基的聚乳酸膜片,再用大量蒸馏水冲洗聚乳酸膜片,以去除未反应的1,6-己二胺;
胺解聚乳酸膜片表面的重氮化:将5g胺解聚乳酸膜片、0.2g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc·hcl)、0.1g对叠氮苯甲酸倒入80ml甲醇中搅拌,然后再向其中缓慢滴入0.5ml的n,n,n’,n’-四甲基乙二胺(temed),在室温下搅拌48h后,将膜片取出用甲醇反复清洗多次,然后在室温条件下避光真空干燥,得到表面含叠氮基的聚乳酸膜片,将其裁剪成2×2cm的尺寸备用。
(2)叠氮壳聚糖和含炔基纤维素硫酸酯的制备
叠氮壳聚糖的制备:将1g壳聚糖、0.2gedc·hcl、0.2g对叠氮苯甲酸倒入80ml甲醇中搅拌,然后再向混合液中缓慢滴入0.4ml的temed,在室温下搅拌48h,反应结束后过滤,得到叠氮壳聚糖,将得到的叠氮壳聚糖用甲醇反复清洗多次,然后在室温条件下避光真空干燥;
含炔基纤维素的制备:首先将2g纤维素置于50ml甲苯/n,n-二甲基乙酰胺(体积比2:1)混合液中,随后向混合液中添加900mg对甲苯磺酰氯、400μl吡啶和900mg5-己炔酸,70℃条件下搅拌反应36h;冷却到室温后,过滤得到含炔基纤维素,随后依次用大量去离子水和乙醇对含炔基纤维素进行反复冲洗,48℃条件下干燥48h;
含炔基纤维素硫酸酯的制备:取二甲基亚砜10ml,加入三口烧瓶中,然后加入0.5g无水licl,待licl溶解后,加入0.5g含炔基纤维素,93℃充分溶解,冷却后,加入3g三氧化硫-吡啶复合物,66℃反应5h,取下烧瓶置于冰水浴中,用20mol/lnaoh溶液调节ph值至中性,以无水乙醇沉淀,离心取沉淀,并用无水乙醇洗涤3次;将沉淀溶于400ml去离子水中,在常温条件下置于透析袋中去离子水透析72h,然后将透析液于50℃下减压蒸发浓缩,冷冻干燥,即得到含炔基纤维素硫酸酯。
(3)叠氮壳聚糖溶液、含炔基纤维素硫酸酯溶液的制备
叠氮壳聚糖溶液的制备:按叠氮壳聚糖:乙酸:硫酸铜:抗坏血酸:去离子水=100mg:3ml:200mg:500mg:147ml的比例,将上述物质混匀得到叠氮壳聚糖溶液;
含炔基纤维素硫酸酯溶液的制备:按含炔基纤维素硫酸酯:硫酸铜:抗坏血酸:去离子水=100mg:200mg:500mg:150ml的比例,将上述物质混匀得到含炔基纤维素硫酸酯溶液。
(4)叠氮壳聚糖和含炔基纤维素硫酸酯在聚乳酸材料表面的层层点击键合自组装
取上述步骤(1)制备的2×2cm尺寸的叠氮化聚乳酸膜片在室温条件下浸泡于10ml含炔基纤维素硫酸酯溶液中1h进行点击反应,然后取出膜片用去离子水洗涤3次,得到表面具有一层含炔基纤维素硫酸酯的改性膜片;利用第一层反应结合在聚乳酸膜片上的含炔基纤维素硫酸酯中没有反应的炔基与具有叠氮基的壳聚糖进行点击反应,随后将上述膜片室温条件下浸泡于10ml叠氮壳聚糖溶液中1h进行点击反应,取出膜片用去离子水洗涤3次,完成基材表面第一个双分子层自组装;反复进行上述过程,直至制得所需层数的聚乳酸材料即可结束反应;最后将膜片在35℃条件下真空干燥24h,得到纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸材料,纤维素硫酸酯处于最外层。
如图4所示,较未经修饰的聚乳酸膜片相比,本实施例经纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸膜片表面的水接触角随着组装层数的增大而降低,这是因为亲水性好的纤维素硫酸酯和壳聚糖通过点击反应固定在聚乳酸膜片表面,使得其亲水性显著提高,水接触角明显降低。
如图5所示,较未经修饰的聚乳酸膜片相比,本实施例经纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸膜的aptt随着组装层数的增大而延长,这是因为具有抗凝血活性的纤维素硫酸酯通过层层点击键合自组装固定在聚乳酸膜片表面,且组装层数越大,被固定在膜片表面的纤维素硫酸酯含量越高,使得聚乳酸膜片表面抗凝血活性增强,aptt延长。
实施例2:本基于层层点击键合自组装的聚乳酸材料由基材和修饰层组成,基材为表面叠氮化的聚乳酸材料,修饰层是在所述基材的表面利用层层点击键合自组装进行表面修饰而得到;其中,修饰层中含有在所述基材表面层层点击键合自组装的含炔基纤维素硫酸酯和叠氮壳聚糖。
上述材料的制备方法如下:
(1)聚乳酸材料表面的叠氮化处理:
聚乳酸膜片的制备:按照聚乳酸:二氯甲烷=7.5g:75ml的比例搅拌混合2个原料,待聚乳酸完全溶解后将溶液倒入平底玻璃比色皿内,在室温下干燥36h后,得到聚乳酸薄膜;随后用质量百分比50%的乙醇水溶液中对薄膜进行搅拌清洗2.5h,以去除表面粘附的油脂和其它杂质,然后用蒸馏水冲洗,在45℃真空干燥30h,得到聚乳酸膜片;
聚乳酸膜片表面的胺解:将7.5g聚乳酸膜片浸泡在0.07g/ml75ml含1,6-己二胺的异丙醇溶液中,在48℃下搅拌反应3.5min,得到表面带有氨基的聚乳酸膜片,再用大量蒸馏水冲洗聚乳酸膜片,以去除未反应的1,6-己二胺;
胺解聚乳酸膜片表面的叠氮化:将7.5g胺解聚乳酸膜片、0.3g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc·hcl)、0.15g对叠氮苯甲酸倒入90ml甲醇中搅拌,然后再向其中缓慢滴入0.65ml的n,n,n’,n’-四甲基乙二胺(temed),在室温下搅拌60h后,将膜片取出用甲醇反复清洗多次,然后在室温条件下避光真空干燥,得到表面含叠氮基的聚乳酸膜片,将其裁剪成2×2cm的尺寸备用。
(2)叠氮壳聚糖和含炔基纤维素硫酸酯的制备:
叠氮壳聚糖的制备:将1.5g壳聚糖、0.3gedc·hcl、0.25g对叠氮苯甲酸倒入90ml甲醇中搅拌,然后再向混合液中缓慢滴入0.6ml的temed,在室温下搅拌60h,反应结束后过滤,得到叠氮壳聚糖,将得到的叠氮壳聚糖用甲醇反复清洗多次,然后在室温条件下避光真空干燥;
含炔基纤维素的制备:首先将4g纤维素置于75ml甲苯/n,n-二甲基乙酰胺(体积比2:1)混合液中,随后向混合液中添加950mg对甲苯磺酰氯、450μl吡啶和950mg5-己炔酸,75℃条件下搅拌反应42h,冷却到室温后,过滤得到含炔基纤维素;随后依次用大量去离子水和乙醇对含炔基纤维素进行反复冲洗,49℃条件下干燥60h;
含炔基纤维素硫酸酯的制备:取二甲基亚砜15ml,加入三口烧瓶中,然后加入0.75g无水licl,待licl溶解后,加入0.75g含炔基纤维素,93.5℃充分溶解,冷却后,加入3.5g三氧化硫-吡啶复合物,68℃反应5.5h,取下烧瓶置于冰水浴中,用20mol/lnaoh溶液调节ph值至中性,以无水乙醇沉淀,离心取沉淀,并用无水乙醇洗涤4次;将沉淀溶于400ml去离子水中,在常温条件下置于透析袋中去离子水透析72h,然后将透析液于50℃下减压蒸发浓缩,冷冻干燥,即得到含炔基纤维素硫酸酯。
(3)叠氮壳聚糖溶液、含炔基纤维素硫酸酯溶液的制备
叠氮壳聚糖溶液的制备:按叠氮壳聚糖:乙酸:硫酸铜:抗坏血酸:去离子水=140.0mg:3ml:220mg:550mg:147ml的比例,将上述物质混匀得到叠氮壳聚糖溶液;
含炔基纤维素硫酸酯溶液的制备:按含炔基纤维素硫酸酯:硫酸铜:抗坏血酸:去离子水=150mg:220mg:550mg:150ml的比例,将上述物质混匀得到含炔基纤维素硫酸酯溶液。
(4)叠氮壳聚糖和含炔基纤维素硫酸酯在聚乳酸材料表面的层层点击键合自组装
取上述步骤(1)制备的2×2cm尺寸的叠氮化聚乳酸膜片在室温条件下浸泡于10ml含炔基纤维素硫酸酯溶液中1.5h进行点击反应,然后取出膜片用去离子水洗涤4次,得到表面具有一层含炔基纤维素硫酸酯的改性膜片;利用第一层反应结合在聚乳酸膜片上的含炔基纤维素硫酸酯中没有反应的炔基与具有叠氮基的壳聚糖进行点击反应,随后将上述膜片室温条件下浸泡于10ml叠氮壳聚糖溶液中1.5h进行点击反应,取出膜片用去离子水洗涤4次;完成基材表面第一个双分子层自组装;反复进行上述过程,直至制得所需层数的聚乳酸材料即可结束反应;最后将膜片在40℃条件下真空干燥36h,得到纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸材料,纤维素硫酸酯处于最外层。
实施例3:本基于层层点击键合自组装的聚乳酸材料由基材和修饰层组成,基材为表面叠氮化的聚乳酸材料,修饰层是在所述基材的表面利用层层点击键合自组装进行表面修饰而得到;其中,修饰层中含有在所述基材表面层层点击键合自组装的含炔基纤维素硫酸酯和叠氮壳聚糖。
上述材料的制备方法如下:
(1)聚乳酸材料表面的叠氮化处理:
聚乳酸膜片的制备:按照聚乳酸:二氯甲烷=10g:100ml的比例搅拌混合2个原料,待聚乳酸完全溶解后将溶液倒入平底玻璃比色皿内,在室温下干燥48h后,得到聚乳酸薄膜。随后用50%乙醇水溶液中对薄膜进行搅拌清洗3h,以去除表面粘附的油脂和其它杂质,然后用蒸馏水冲洗,在50℃真空干燥36h,得到聚乳酸膜片;
聚乳酸膜片表面的胺解:将10g聚乳酸膜片浸泡在0.09g/ml100ml含1,6己二胺的异丙醇溶液中,在60℃下搅拌反应5min,得到表面带有氨基的聚乳酸膜片,再用大量蒸馏水冲洗聚乳酸膜片,以去除未反应的己二胺;
胺解聚乳酸膜片表面的叠氮化:将10g胺解聚乳酸膜片、0.4g1-(3-二甲氨基丙基)-3-乙基碳二亚胺盐酸盐(edc·hcl)、0.2g对叠氮苯甲酸倒入100ml甲醇中搅拌,然后再向其中缓慢滴入0.8ml的n,n,n’,n’-四甲基乙二胺(temed),在室温下搅拌72h后,将膜片取出用甲醇反复清洗多次,然后在室温条件下避光真空干燥,得到表面含叠氮基的聚乳酸膜片,将其裁剪成2×2cm的尺寸备用。
(2)叠氮壳聚糖和含炔基纤维素硫酸酯的制备:
叠氮壳聚糖的制备:将2g壳聚糖、0.4gedc·hcl、0.3g对叠氮苯甲酸倒入100ml甲醇中搅拌,然后再向混合液中缓慢滴入0.8ml的temed,在室温下搅拌72h,反应结束后过滤,得到叠氮壳聚糖,将得到的叠氮壳聚糖用甲醇反复清洗多次,然后在室温条件下避光真空干燥、
含炔基纤维素的制备:首先将6g纤维素置于100ml甲苯/n,n-二甲基乙酰胺(体积比2:1)混合液中,随后向混合液中添加1000mg对甲苯磺酰氯、500μl吡啶和1000mg5-己炔酸,80℃条件下搅拌反应48h,冷却到室温后,过滤得到含炔基纤维素;随后依次用大量去离子水和乙醇对含炔基纤维素进行反复冲洗,50℃条件下干燥72h;
含炔基纤维素硫酸酯的制备:取二甲基亚砜20ml,加入三口烧瓶中,然后加入1g无水licl,待licl溶解后,加入1g含炔基纤维素,94℃充分溶解,冷却后,加入4g三氧化硫-吡啶复合物,70℃反应6h,取下烧瓶置于冰水浴中,用20mol/lnaoh溶液调节ph值至中性,以无水乙醇沉淀,离心取沉淀,并用无水乙醇洗涤5次;将沉淀溶于400ml去离子水中,在常温条件下置于透析袋中去离子水透析72h,然后将透析液于50℃下减压蒸发浓缩,冷冻干燥,即得到含炔基纤维素硫酸酯。
(3)叠氮壳聚糖溶液、含炔基纤维素硫酸酯溶液的制备
叠氮壳聚糖溶液的制备:按叠氮壳聚糖:乙酸:硫酸铜:抗坏血酸:去离子水=180.0mg:3ml:240mg:600mg:147ml的比例,将上述物质混匀得到叠氮壳聚糖溶液;
含炔基纤维素硫酸酯溶液的制备:按含炔基纤维素硫酸酯:硫酸铜:抗坏血酸:去离子水=200.0mg:240mg:600mg:150ml的比例,将上述物质混匀得到含炔基纤维素硫酸酯溶液。
(4)叠氮壳聚糖和含炔基纤维素硫酸酯在聚乳酸材料表面的层层点击键合自组装
取上述步骤(1)制备的2×2cm尺寸的叠氮化聚乳酸膜片在室温条件下浸泡于10ml含炔基纤维素硫酸酯溶液中2h进行点击反应,然后取出膜片用去离子水洗涤5次,得到表面具有一层含炔基纤维素硫酸酯的改性膜片;利用第一层反应结合在聚乳酸膜片上的含炔基纤维素硫酸酯中没有反应的炔基与具有叠氮基的壳聚糖进行点击反应,随后将上述膜片室温条件下浸泡于10ml叠氮壳聚糖溶液中2h进行点击反应,取出膜片用去离子水洗涤5次;完成基材表面第一个双分子层自组装;反复进行上述过程,直至制得所需层数的聚乳酸材料即可结束反应;最后将膜片在45℃条件下真空干燥48h,得到纤维素硫酸酯/壳聚糖多层膜修饰的聚乳酸材料,纤维素硫酸酯处于最外层。
- 还没有人留言评论。精彩留言会获得点赞!