水稻花药特异性表达的启动子POsFT1及其应用的制作方法
本发明涉及植物分子生物学领域,具体涉及水稻花药特异性表达的启动子posft1及其应用。
背景技术:
高等植物的生长发育是不同基因在不同时空有序表达和协同作用的结果。启动子是重要的顺式作用元件,通过与转录因子的结合进而决定了基因的表达模式与表达强度。根据启动子的转录模式不同将其分为组成型、诱导型和组织特异性启动子三类。
组织特异性启动子指器官特异性启动子,在这类启动子的驱动下,基因的表达往往只限定某些特定的器官和组织部位,并表现发育调节等特性。组织特异性启动子不仅能使目的基因的表达产物在一定器官或组织部位积累,增加区域表达量,用组织特异表达启动子来驱动目的基因表达可有效的避免用组成型表达启动子所带来的一些诸如代谢负担之类的负面效应。但是目前调控机理清楚且可用于作物遗传改良的组织特异表达启动子仍然较少。
技术实现要素:
本发明的一个目的是提供一种具有启动子功能的dna分子。
本发明所提供的具有启动子功能的dna分子,命名为posft1启动子,来源于水稻(oryzasativa),是下述a)-c)中任一的dna片段:
a)seqidno.1所示dna片段;
b)与a)限定的核苷酸序列具有90%以上同源性,且具有启动子功能的dna片段;
c)在严格条件下与a)或b)限定的核苷酸序列杂交,且具有启动子功能的dna片段。
上述严格条件可为在6×ssc,0.5%sds的溶液中,在65℃下杂交,然后用2×ssc,0.1%sds和1×ssc,0.1%sds各洗膜一次。
其中,seqidno.1共由1493个核苷酸组成。
含有所述dna分子(启动子)的重组载体、表达盒、转基因细胞系或重组菌也属于本发明的保护范围。
其中,所述重组载体可为重组表达载体,也可为重组克隆载体。
在本发明的一个实施例中,所述重组载体具体为将seqidno.1所示的dna分子插入pcambia1391z载体的psti和ecori酶切位点间,且保持pcambia1391z载体的其他序列不变得到的载体。
所述表达盒由具有启动子功能的所述dna分子,由所述dna分子启动表达的目的基因,以及转录终止序列组成;所述dna分子以功能性方式与所述目的基因连接,且所述目的基因与所述转录终止序列连接。
在本发明的一个实施例中,所述目的基因具体为gus基因(来源于所述pcambia1391z载体);所述转录终止序列具体为nos转录终止子(来源于所述pcambia1391z载体)。
本发明的另一个目的是提供posft1启动子或上述重组载体、表达盒、转基因细胞系或重组菌的新用途。
本发明提供了posft1启动子或上述重组载体、表达盒、转基因细胞系或重组菌在启动目的基因表达中的应用。
在所述应用中,所述启动目的基因表达为在植物中启动目的基因表达。
进一步地,所述表达为花药特异性表达。
进一步地,所述植物可为单子叶植物或双子叶植物。
更进一步地,所述单子叶植物可为禾本科植物。
更加具体地,所述禾本科植物可为水稻,如水稻品种日本晴。
上述posft1启动子或上述重组载体、表达盒、转基因细胞系或重组菌在植物遗传改良中的应用也属于本发明的保护范围。
本发明与现有技术相比,具有如下优点:
(1)本发明的水稻花药特异性表达启动子为posft1,其来源于水稻粳稻品种日本晴,该启动子片段大小为1493bp,所述posft1启动子具有以下特点:a)位于osft1基因的5’端及其上游;b)碱基长度为1493bp;c)具有引发转录的必要位点及转录起始点;d)在水稻花药中特异性表达。本发明提供启动子能够有效控制目的基因特异表达于花药,在其他器官组织中不表达,可避免外源基因在植物其他组织中持续表达所带来的不利影响,如:转基因漂移和花粉逃逸所带来的生物安全问题。
(2)本发明的含有花药特异表达启动子posft1的重组表达载体,转入了花药特异性表达的启动子,在重组表达载体的花药特异表达启动子posft1调控下使下游基因定位于花药表达,为植物基因工程领域研究基因在花药特异表达提供了工具,具有广泛的应用前景。
通过实验证明:本发明提供启动子posft1可有效启动目的基因在水稻花药中的特异性表达,在其他器官组织中不表达,可避免目的基因在植物其他组织中持续表达所带来的不利影响,还可以用于植物花药生长发育相关基因的功能分析和鉴定。不仅为转基因水稻育种服务,也为长远的启动子改造和设计储备资源。
附图说明
图1为posft1启动子分子检测结果图。a为pcr结果;b为双酶切结果。m1和m2:dl-5000,1:条带大小为1493bp;2:psti和ecori双酶切条带。
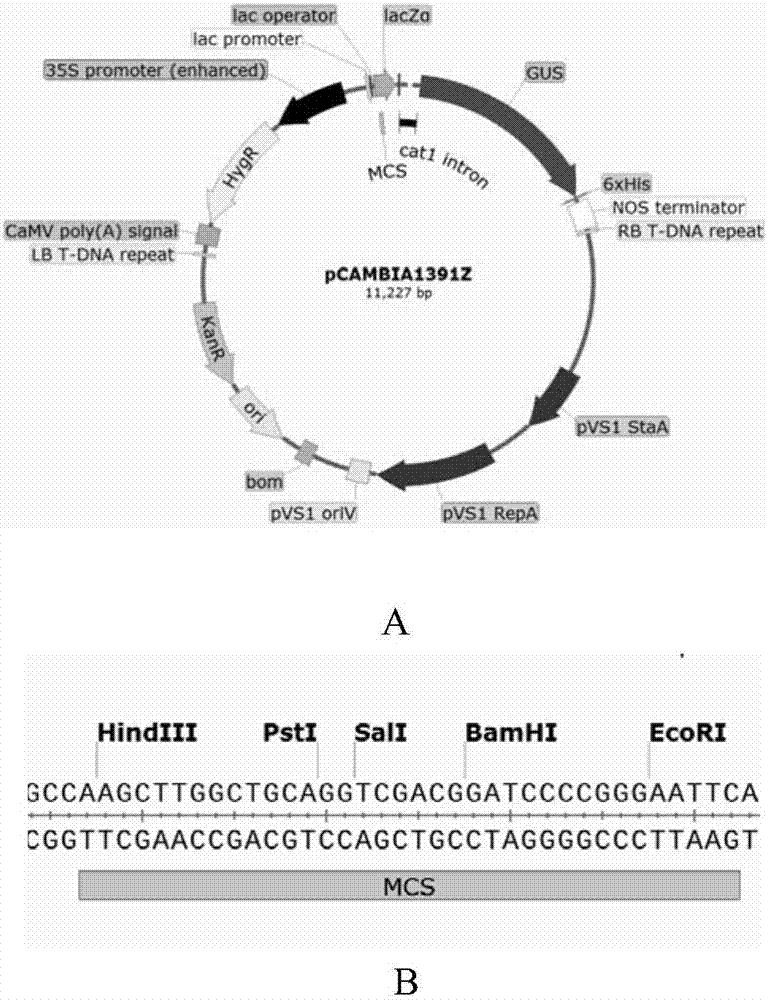
图2为表达载体pcambia1391z-posft1的t-dna区图谱。其中,a为pcambia1391z载体,lb和rb分别表示为t-dna的左边界和右边界;hyg表示潮霉素抗性基因;mcs表示多克隆位点;nos表示基因的终止子;b为多克隆位点图(mcs)。
图3为gus基因的组织化学染色结果图。其中:a代表幼根;b代表茎;c代表幼叶;d代表颖壳;e代表花药。
具体实施方式
本发明结合附图和具体实施例作进一步说明。应该理解,这些实施例仅用于说明目的,而不用于限制本发明范围。
下述实施例中所使用的实验方法如无特殊说明,均为常规方法。
下述实施例中所用的材料、试剂等,如无特殊说明,均可从商业途径得到。
下述实施例中的定量试验,均设置三次重复实验,结果取平均值。
下述实施例中的gus染色液(ph7.0):溶剂为200mmpbs缓冲液,溶质及其在染色液中的浓度分别为:100mm亚铁氰化钾、100mm铁氰化钾、0.5mmedta(ph8.0)、10mg/mlx-gluc、0.1%(体积比)吐温20。
下述实施例中所用引物均由深圳华大生物工程有限公司合成,上海生工公司测序;pteay-t1、taq酶、trans5α感受态及相关的试剂盒均购置北京全式金公司;限制性内切酶psti和ecori、t4连接酶均购自takara公司;抗生素购自上海生工和sigma公司;pcambia1391z载体和农杆菌agl1均购自北京博艾永华生物科技有限公司;其余试剂均为国产分析纯。
实施例1、水稻花药特异性启动子posft1的克隆
1、引物的设计
根据ncbi网站上公布的posft1启动子全长序列,设计pcr扩增该片段的引物,上游引物加psti的ctgcag酶切位点,下游引物加ecori的gaattc酶切位点。
引物序列如下:
引物1(上游引物):5’-ctgcagccttcgtttaccaatc-3’;
引物2(下游引物):5’-gaattcccggctgccggccgac-3’。
2、pcr扩增
以全式金公司植物基因组试剂盒提取的水稻日本晴基因组dna为模板,用步骤1中设计的上游引物和下游引物进行pcr扩增,得到pcr产物。
pcr反应条件如下:预变性:98℃10min;变性:98℃10s;退火:62℃5s;延伸:72℃2min30s,36个循环;总延伸:72℃10min。
3、pcr产物检测
pcr反应结束后,用2%琼脂糖凝胶电泳检测pcr产物;然后回收并纯化目的片段,再将回收片段与peasyt1cloningvector连接,得到重组载体peasyt1cloningvector-posft1,最后将重组载体peasyt1cloningvector-posft1转化到大肠杆菌感受态trans5α细胞中;经pcr和酶切检测筛选阳性克隆并进行测序验证(图1)。
结果表明:pcr扩增得到大小为1493bp的dna片段,其核苷酸序列如序列表中序列1所示,将序列1所示的核苷酸序列命名为posft1,其由1493个碱基组成。
实施例2、posft1启动子的功能验证
一、转基因株系的获得
1、表达载体的构建
用限制性内切酶psti和ecori双酶切实施例1步骤3中的重组载体peasyt1cloningvector-posft1,得到posft1片段;用限制性内切酶psti和ecori双酶切pcambia1391z载体(图2),得到pcambia1391z载体骨架片段;将posft1片段与pcambia1391z载体骨架片段进行连接,获得重组质粒posft1-pcambia1391z。
重组质粒posft1-pcambia1391z为将seqidno.1所示的posft1启动子插入pcambia1391z载体的psti和ecori酶切位点间,且保持pcambia1391z载体的其他序列不变得到的载体。posft1启动子用于启动pcambia1391z载体中gus基因。
2、将重组质粒posft1-pcambia1391z导入农杆菌agl1,得到重组农杆菌。
3、取步骤2制备的重组农杆菌重悬于液体共培养培养基(yep液体培养基+100mg/l乙酰丁香酮,ph5.2)中培养,得到od600nm=1.0的菌液。
4、取水稻材料日本晴(水稻材料日本晴购自中国农业科学院生物技术研究所)的胚性愈伤组织,用步骤3得到的菌液浸泡30min,然后经共培养、筛选、生根、壮苗,得到t0代转基因植株。
5.提取t0代转基因植株的dna,利用实施例1中的引物1和引物2进行pcr扩增,pcr程序同上。pcr扩增得到大小为1493bp的dna片段即为阳性转posft1启动子植株。最终经pcr检测获得的11株t0代转基因植株中共有10株阳性转posft1启动子植株。
二、转posft1启动子植株的染色
分别对阳性转posft1启动子植株不同部位进行gus组织化学染色。具体操作步骤如下:取阳性转posft1启动子植株的如下不同组织:幼根、茎、幼叶、颖壳和花药,并将各部位移入试管中;然后加入适量的gus缓冲液浸没组织块,再加入gus染色液,混匀后37℃下保存4-12h;染色结束后,将染色组织先置于75%乙醇漂洗脱色,再用50%和20%乙醇各浸泡20min以上,直到材料呈白色;最后在显微镜下观察,组织上有蓝色小点即为gus表达部位。
染色结果如图3所示。其中,a代表幼根;b代表茎;c代表幼叶;d代表颖壳;e代表花药。从图中可以看出:gus基因只在转posft1启动子植株的花药中特异性表达,而在根、茎和叶中均不表达。说明本发明的启动子posft1仅在水稻花药中特异性表达,可用于启动目的基因在花药中特异性表达。
序列表
<110>中国农业科学院生物技术研究所
<120>水稻花药特异性表达的启动子posft1及其应用
<160>1
<170>patentinversion3.5
<210>1
<211>1493
<212>dna
<213>人工序列(artificialsequence)
<400>1
ccttcgtttaccaatcacccgtcttgtctcgggtcacccataattccagatcctaatacc60
catatcaaagggctgctccctccgtttaaaaaaaattcaaaacaaaacaaagacaaactt120
attactagagatgatatattctaatacaattaatctgaacaaagtctattcagatttatt180
ttactataataaatcacatccaatcctaggattatattttgtggaacggatggaatagta240
atccttactacttccgtctcaaaatataatacgtttaagcttgaatacgatacaaataga300
gtaggtaaaatcaaatgagaaaatattatatatgattagttgagaaaagaatgtaagttg360
agttcattttgttgtgtctactattccaaagtaagtttgcttctagcgcaagtatcatca420
atttgtaaatcgttaagttttactccctcctttctaatataggtgcaacctaatatagat480
gtgacatatctaatttttttttcacgaacgcgtataagaattgcacgttaatataatata540
ttagatatatccaatgttacatttatatttttttaaccagatgttacatttatatttata600
ttgagacagatgagtattcatttagtcctcttatcgacctaccatcaatgctattttctt660
attaatgatgggcactttgatattttcttctttcacgaacacataggactaaaaagtagg720
agcaagttattttgtaatgaagggatctaaaacatacctaaggcgtgagtatatcaataa780
ctataaattcagcactgaattgcaagttttctgtttaccctgcttcttattattttttct840
gaattgatctaattatggcataagtgcgagttattgggattgacttagtaataaaaagta900
attgacatataataaataatcatctaagacgacatattaattaattactccctttgcttt960
atattgtaaggtgttctaagttcatcttaagtcaaactttgtttaactactatcaaaata1020
tagaaaaacttagcaacatctctaacactatattaattttattaaaaccgccattaaata1080
ggagcagatctttatagtattttattaaaaattgacttgcatcaacttaattaatatact1140
actagcagtttcaaaaattgatacgctatctgtaaccaatgtaatttctacccatataac1200
agctactaatataggagtatatactactccgtccgtcccataatacaagagatcatggcc1260
ttcaaatttatcccgaaacgttagagatcttggtatcccgagacaatacttatttattcc1320
tcacccctaacttaaagcgagcagccaagctactgtagctaatggtagggcgcgtgcgac1380
agtggagtaaagtgaagcagcagcagagaagcagagaccatttccctcctccctcctctc1440
tcgccaaacacgacgacgtcgcctcggtttagtcgtcgtcggccggcagccgg1493
- 还没有人留言评论。精彩留言会获得点赞!
- CRISPR-Cas9特异性敲除猪SALL1基因的方法及用于特异性靶向SALL1基因的sgRNA的制作方法
- CRISPR-Cas9特异性敲除猪CMAH基因的方法及用于特异性靶向CMAH基因的sgRNA的制作方法
- CRISPR-Cas9特异性敲除猪SLA-2基因的方法及用于特异性靶向SLA-2基因的sgRNA的制作方法
- 一种安宁铗蠓的特异基因及其分子鉴定方法
- 一种蓝腹库蠓的特异基因及其分子鉴定方法
- 一种特异性抑制twist1基因表达的小干扰rna及其应用
- 一种特异性抑制magea1基因表达的小干扰rna及其应用
- 一种特异性抑制magea1基因表达的小干扰rna及其应用
- 一种特异性抑制twist1基因表达的小干扰rna及其应用
- 一种特异性抑制ctgf基因表达的小干扰rna及其应用