鉴定新型冠状病毒的引物探针及在三重荧光RPA的应用的制作方法
本发明属于应用生物技术领域,具体涉及筛查鉴定新型冠状病毒以及其他类sars冠状病毒的特异性快速筛查检测引物、探针、鉴定方法及鉴定试剂盒。
背景技术:
新型冠状病毒(sars-cov2)导致的肺炎疫情(covid-19)目前席卷全球,其对经济、社会、人民正常的生活影响巨大,而对新冠病毒病例的快速诊断就成为切断传染源、控制疫情传播的重要手段。尤其是当前国内疫情趋于平稳,国外疫情严峻,输入性病例增加,对核酸排查的精准性要求更高。
目前国家cdc和who均推荐了荧光定量pcr作为新型冠状病毒确诊方法,然而实际应用过程中时效性不是特别好,反转录荧光pcr耗时90min,还需要专门的荧光pcr仪进行数据分析。相比荧光定量pcr,荧光恒温rpa具有快速、准确、对仪器设备要求低等优势;此外,本发明三重rpa可用于鉴定区分新型冠状病毒与其他类sars病毒,这对疫病防控及筛查其他类似疫病有重大影响。
技术实现要素:
本发明提供了一组用于鉴定新型冠状病毒(sars-cov2)的引物和探针,所述的引物和探针包括第一套引物探针,所述第一套引物探针包括正向引物nf、反向引物nr和探针np,所述引物和探针的序列如下:
正向引物nf:
aagaccttaaattccctcgaggacaaggcgttc;
反向引物nr:
aggtagtagaaataccatcttggactgagatct3’;
探针np:
caccaatagcagtccagatgaccaaattggc/i6famdt/a/idsp//ibhq1dt/accgaagagctaccag/ispc3/。
其中,探针np的荧光标记为fam。
进一步的,上述一组用于鉴定新型冠状病毒(sars-cov2)的引物和探针还包括第二套引物探针,所述第二套引物探针包括正向引物ef、反向引物er和探针ep,所述引物和探针的序列如下:
正向引物ef:
gacaggtacgttaatagttaatagcgtacttct;
反向引物er:
agactcacgttaacaatattgcagcagtacgca;
探针ep:
ttcgtggtattcttgctagttacactagcca/ihexdt/c/idsp//ibhq1dt/tactgcgcttcgattg/ispc3/;
其中,探针ep的荧光标记为hex。
进一步的,上述一组用于鉴定新型冠状病毒(sars-cov2)的引物和探针还包括第三套引物探针,所述第三套引物探针包括正向引物sf、反向引物sr和探针sp,所述引物和探针的序列如下:
正向引物sf:
aaccattggtagatttgccaataggtattaacat;
反向引物sr:
cctaggttgaagataacccacataataagctgc;
探针sp:
tacatagaagttatttgactcctggtgattct/icy5dt/c/idsp//ibhq2dt/caggttggacagctg/ispc3/;
其中,探针sp的荧光标记为cy5。
另一方面,本发明还提供了上述引物和探针在鉴定sars-cov2病毒以及非sars-cov2冠状病毒中的应用。
进一步的,上述应用包括利用上述引物和探针对待测样本进行三重荧光rpa反应;如果探针np、探针ep和探针sp均为阳性,判定为新型冠状病毒;如果探针ep为阳性,探针np和探针sp为阴性,判定为非sars-cov2冠状病毒;如果探针np、探针ep和探针sp均为阴性,判定为非冠状病毒。
另一方面,本发明还提供了上述引物和探针在制备鉴定sars-cov2病毒以及非sars-cov2冠状病毒的试剂盒中的用途。
进一步的,上述试剂盒为三重荧光rpa反应试剂盒。
进一步的,可以根据反应结果判断待测样本的类型;具体而言,如果探针np、探针ep和探针sp均为阳性,判定为新型冠状病毒;如果探针ep为阳性,探针np和探针sp为阴性,判定为非sars-cov2冠状病毒;如果探针np、探针ep和探针sp均为阴性,判定为非冠状病毒。
进一步的,上述非sars-cov2冠状病毒包括sars病毒、mers病毒。
另一方面,本发明还提供了一种能用于新型冠状病毒(sars-cov2)以及其他冠状病毒快速筛查检测的特异性三重荧光rpa试剂盒,上述试剂盒包括rna提取试剂、以及上述引物和探针。
本发明提供的鉴定新型冠状病毒(sars-cov2)的引物和探针,检测灵敏度低,通过一个三重荧光rpa反应即可区分鉴别新型冠状病毒、除sars-cov2病毒外的其他类sars病毒,以及其他非相关病原,具有广泛的应用前景。
附图说明
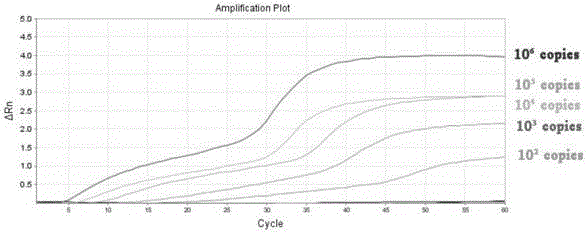
图1、三重荧光rpa检测新型冠状病毒敏感度试验第一套引物探针,靶标n基因。从左至右,共7孔,分别是1:106copies/reaction(n基因);2:105copies/reaction;3:104copies/reaction;4:103copies/reaction;5:102copies/reaction;6:101copies/reaction;7:negativecontrol。
图2、三重荧光rpa检测新型冠状病毒敏感度试验第二套引物探针,靶标e基因。从左至右,共7孔,分别是1:106copies/reaction(e基因);2:105copies/reaction;3:104copies/reaction;4:103copies/reaction;5:102copies/reaction;6:101copies/reaction;7:negativecontrol。
图3、三重荧光rpa检测新型冠状病毒敏感度试验第三套引物探针,靶标s基因。从左至右,共7孔,分别是1:106copies/reaction(s基因);2:105copies/reaction;3:104copies/reaction;4:103copies/reaction;5:102copies/reaction;6:101copies/reaction;7:negativecontrol。
图4、三重荧光rpa检测新型冠状病毒特异性试验。从左至右,共7孔,分别是1:pedv病毒核酸;2:tgev病毒核酸;3:pprv病毒核酸;4:fmdv病毒核酸;5:rv病毒核酸;6:ppv病毒核酸;7:阴性对照;8:阳性对照(ncov-cdna)。
图5、三重荧光rpa检测模拟sars病毒核酸。同时试验的还有三组,阳性对照、阴性对照,pedv。仅展示模拟sars病毒核酸检测结果,其他三组与图4结果类似,不再重复展示。
图6、三重荧光rpa临床样本检测结果(fam信号,n基因)。从左至右,共7孔,分别是1:临床样本2011;2:临床样本2012;3:临床样本2013;4:临床样本2014;5:临床样本2015;6:临床样本2016;7:阳性对照(ncov-cdna)。
图7、三重荧光rpa临床样本检测结果(hex信号,e基因)。从左至右,共7孔,分别是1:临床样本2011;2:临床样本2012;3:临床样本2013;4:临床样本2014;5:临床样本2015;6:临床样本2016;7:阳性对照(ncov-cdna)。
图8、三重荧光rpa临床样本检测结果(cy5信号,s基因)。从左至右,共7孔,分别是1:临床样本2011;2:临床样本2012;3:临床样本2013;4:临床样本2014;5:临床样本2015;6:临床样本2016;7:阳性对照(ncov-cdna)。
实施方式
下面结合实施例对本发明做进一步的说明,以下所述,仅是对本发明的较佳实施例而已,并非对本发明做其他形式的限制,任何熟悉本专业的技术人员可能利用上述揭示的技术内容加以变更为同等变化的等效实施例。凡是未脱离本发明方案内容,依据本发明的技术实质对以下实施例所做的任何简单修改或等同变化,均落在本发明的保护范围内。
实施例1、引物、探针序列的获得及阳性质粒的构建
根据新型冠状病毒(sars-cov2)全长核酸序列,进行比对分析,并与sars病毒、类sars病毒的全长序列做比对,找出sars-cov2病毒特异性序列s基因,病毒保守序列n基因,类sars病毒保守序列e基因,orf1ab基因,m基因,然后根据上述序列设计引物、探针;本申请所涉及的引物、探针如下表所示:
本申请通过构建标准质粒完成荧光rpa方法的敏感性检验。以puc57质粒为基础,合成目的基因并构建重组质粒。使用热激法转入大肠杆菌(escherichiacoli)感受态细胞内,涂布平板挑选单克隆菌落,将菌落扩繁培养并取菌液提取质粒。在应用nanodrop定量后,计算质粒浓度,然后分别稀释为5×106copies/μl,5×105copies/μl,5×104copies/μl,5×103copies/μl,5×102copies/μl,5×10copies/μl,5copies/μl。可用于后续敏感度试验。
实施例2、实际检测样品的处理及病毒rna基因组提取
检测样本包括但不限于人的血清、血浆、全血、粪便、咽喉拭子以及痰液等。样本处理:1g粪便或1支病人的咽喉拭子溶于1ml生理盐水中,振荡混匀,5000r/min离心10min,取上清液提取病毒rna。痰液加等量10g/l乙酰半胱氨酸,室温震荡1h,充分液化后提取病毒rna。血浆与全血应加抗凝剂(肝素等)。
异硫氰酸胍-玻璃粉法提取病毒rna:具体操作步骤如下:(1)在0.1ml标本液中加入异硫氰酸胍-玻璃粉裂解液(4.7mol/l异硫氰酸胍,20mmol/ledta,100mmol/ltris-hclph6.4,1%tritonx-100和玻璃粉10g)0.9ml,混匀,室温作用10min,6000×g离心1min。(2)弃上清,加异硫氰酸胍漂洗液(4.7mol/l异硫氰酸胍和100mmol/ltris-hclph6.4)1ml,混匀后6000×g离心1min。(3)弃上清,加70%乙醇1ml,混匀后6000×g离心1min。(4)弃上清,将塑料离心管倒置,37℃烤干10~15min。(5)加入depc处理的去离子水50μl洗脱rna,振荡混匀后6000×g离心1min,取上清即可作为荧光rpa的模板。
qiagen公司的试剂盒提取病毒rna(也可选用其他试剂公司的产品):操作按照说明书进行,具体操作步骤如下:(1)在1.5ml塑料离心管中加入avl560μl,然后加入标本液140μl,混匀后室温作用10min。(2)加入无水乙醇560μl。(3)混匀后分两次加入过滤柱中,每次加630μl,8000r/min离心1min。(4)加入aw1液500μl,8000r/min离心1min。(5)加入aw2液500μl,14000r/min离心3min。(6)最后加入60μlave液,8000r/min1min将rna洗脱下来作为模板用于pcr扩增。
实施例3、实施三重荧光rpa
三重荧光rpa反应包括配制体系、扩增及信号读取2个步骤。采用rna恒温快速扩增试剂盒(荧光型)推荐的50μl体系,以制备的rna或(dna质粒)为模板,使用的引物和探针序列见摘要,进行三重荧光rpa反应。荧光rpa反应体系(50μl):buffera29.4μl,上游引物nf、ef、sf各0.8μl(10μmol/l),下游引物nr、er、sr各0.8μl(10μmol/l),探针np、ep、sp各0.3μl(10μmol/l),核酸模板2μl,rnase-freewater10.2μl,rox染料0.2μl,bufferb2.5μl。反应条件设置为:42℃,20min,每30s收集一次荧光信号,共40个循环。仪器自动采集荧光信号,可实时观察荧光扩增信号,使用的abi的7500荧光pcr仪。
荧光rpa敏感度测试:体系50μl,与前述体系相同。同浓度dna质粒模板n基因、e基因及s基因各2μl(10倍稀释共六个浓度梯度,从5×106copies/μl到5copies/μl),阴性对照为rnase-freewater2μl。
荧光rpa特异性测试:反应体系(50μl),其中病毒核酸各2μl(核酸总量为50至100ng之间)。特异性检测包括6种病毒,其中两种冠状病毒pedv(猪流行性腹泻病毒)、tgev(传染性胃肠炎病毒),还有rna病毒pprv(小反刍兽疫病毒)、rna病毒fmdv(口蹄疫病毒)、rna病毒rv(轮状病毒)以及dna病毒ppv(猪细小病毒)。阳性对照为新冠病毒核酸反转录cdna,阴性对照为rnase-freewater。
检测区分sars冠状病毒(sars-cov)与新型冠状病毒(sars-cov2):反应体系(50μl)。人工合成sars冠状病毒的s基因全长序列以及sars病毒n基因全长,以puc57质粒为基础,分别构建对照质粒p-sars-s及p-sars-n。以质粒p-sars-s、p-sars-n和新冠病毒e基因作为模板,模拟sars病毒基因组,开展三重rpa检测区分新型冠状病毒以及其他类sars冠状病毒的实验。共有四组,分别是阳性对照新冠病毒核酸反转录cdna,阴性对照为rnase-freewater,其他冠状病毒pedv以及sars冠状病毒模拟核酸。
临床样本检测:参加上海市临床检验中心组织的新型冠状病毒核酸检测测量审核计划,取得灭活的临床样本6支,批号为2011、2012、2013、2014、2015以及2016,样本量为600μl/支。取50μl/支的样本量,按照前述方法提取rna核酸,用20μlrnase-freewater溶解核酸。rpa反应体系(50μl)同之前叙述,临床样本核酸各2μl(核酸总量为50至100ng之间)。阳性对照为新冠病毒核酸反转录cdna,阴性对照为rnase-freewater。
实施例4、检测结果:
对实施例1中涉及的引物和探针的灵敏度和特异性进行检验。在三重rpa反应(需要三套引物探针)中,所采用的引物探针组合选择如下:
首先,发明人对nf/nr/np、nf2/nr2/np2、orf/orr/orp、orf2/orr2/orp2、mf/mr/mp五组引物探针组合进行了分析比对,nf2/nr2/np2、mf/mr/mp、orf/orr/orp三组引物探针的组合敏感度均在103copies/reaction数量级,敏感度较低,而orf2/orr2/orp2引物探针组合阴性对照有非特异性扩增,因此三重rpa反应第一套引物探针选择nf/nr/np。
针对e基因设计了两组引物探针组合,经过试验,ef2/er2/ep2的探针组合的分析敏感度较低,仅能到达104copies/reaction,因此三重rpa反应第二套引物探针选择ef/er/ep;
针对s基因,选择sf/sr/sp引物探针组合,经过试验其敏感性、特异性良好,即为三重rpa反应第三套引物探针sf/sr/sp。
对于上述选定的三重rpa反应的三套引物探针(sf/sr/sp、ef/er/ep和nf/nr/np),三重荧光rpa检测方法灵敏度测试显示,其对n基因的检测限值(灵敏度)为102copies/reaction(图1),对e基因的检测限值(灵敏度)也为102copies/reaction(图2),对s基因的检测限值(灵敏度)在10copies以内(图3)。另外,上述引物探针的特异性良好,荧光rpa方法可检测新型冠状病毒,e基因、s基因和n基因全部阳性,且与pedv、tgev、pprv、fmdv、rv、ppv均无交叉反应(图4);检测sars冠状病毒模拟核酸,结果显示e基因阳性,而s基因和n基因阴性(图5),证实三重rpa检测方法可用于鉴定区分新冠病毒与类sars病毒;三重rpa的临床样本检测,n基因检测结果显示2012、2014与2015三个样本阳性(图6),e基因检测结果也显示2012、2014与2015三个样本阳性(图7),而s基因检测结果显示2012、2014、2015与2016四个样本阳性(图8),三重rpa方法中s基因检测结果符合率100%,获得上海市临床检验中心组织颁发的证书。
- 还没有人留言评论。精彩留言会获得点赞!
- 一种用于评估皮肤抗过敏情况的引物和探针及试剂盒的制作方法
- 一种用于评估皮肤防御情况的引物和探针及试剂盒的制作方法
- 一种荧光定量PCR检测猪delta冠状病毒的引物、探针、试剂盒及方法
- 一种快速区分HP-PRRS疫苗GDr180株与野毒株的引物、探针及方法
- 一种用于检测样品中猪凸隆病毒的荧光rt-pcr引物和探针和试剂盒及检测方法
- 一种阿胶中驴、马、牛和猪源性巢式荧光pcr检测引物、探针、试剂盒、检测方法及应用
- 一种用于评估皮肤防晒情况的引物和探针及试剂盒的制作方法
- 一种用于评估皮肤抗皱情况的引物和探针及试剂盒的制作方法
- 一种用于检测car-t转导效率的引物、探针和方法
- 用于微嵌合检测和个体识别的引物、探针、试剂盒及方法