RGDfK抑制PDL1的检测方法及其在制备抗PDL1药物中的应用与流程
本发明属于医药技术领域,具体涉及一种rgdfk抑制pdl1的检测方法及其在制备抗pdl1药物中的应用。
背景技术:
乳腺癌是一种恶性肿瘤,在女性群体中发病率很高。近年来,针对乳腺癌的治疗已经取得了显著的临床效果,治疗方式主要有手术、放疗和化疗,然后5年生存率普遍较低,特别是中晚期患者。随着肿瘤生物学和免疫学的发展,癌症免疫治疗已成为近年来肿瘤治疗领域的新研究热点,被喻为第四种肿瘤治疗模式,主要是指应用免疫学原理和方法,通过激活体内的免疫细胞和增强机体抗肿瘤免疫应答,特异性地清除肿瘤微小残留病灶、抑制肿瘤生长,打破免疫耐受的治疗方法。肿瘤免疫治疗就是要克服肿瘤免疫逃逸的机制,从而重新唤醒免疫细胞来清除癌细胞。一般地,肿瘤患者机体免疫反应处于抑制状态,一方面是由于体内细胞毒性t细胞相关抗原及辅助性t细胞不足,另一方面是肿瘤细胞产生的免疫抑制分子,导致免疫耐受。有研究显示,免疫检查点程序性死亡受体1(programmeddeath1,pd1)及其配体1(pdl1)参与形成肿瘤微环境,能显著抑制t细胞活性,促使肿瘤细胞逃避机体免疫系统的监视和杀伤。pd1是一种细胞表面受体,属于免疫球蛋白超家族,仅在活化的t淋巴细胞上表达。在结构上,成熟的pd1蛋白包含细胞外识别结构域、跨膜区以及细胞内尾部。功能上,pd1在抑制t细胞活性中起重要作用,具有两个磷酸化位点的尾部,分别是免疫受体酪氨酸抑制基序(immunoreceptortyrosine-basedinhibitionmotif,itim)和一个基于免疫受体酪氨酸的转换基序(immunoreceptortyrosine-basedswitchmotif,itsm),均负调节t细胞受体信号。
乳腺癌是危害女性身体健康最常见的恶性肿瘤,而转移是乳腺癌临床治疗失败的主要原因。上皮间质转化(epithelialmesenchymaltransformation,emt)是肿瘤转移的关键步骤,参与乳腺癌的发生、浸润等多个恶变过程。纤连蛋白(fibronectin,fn)是细胞外基质中一种功能性糖蛋白。临床数据研究表明,fn在正常成人乳腺组织中低表达,而在肿瘤基质中表达水平显著升高。整合素是一种位于细胞表明介导细胞内外信号传导的跨膜糖蛋白受体,fn可通过rgd位点与整合素受体结合调控细胞多种生理功能。
随着信号通路、细胞凋亡等分子生物学方法在肿瘤研究中的应用,乳腺癌分子靶点和靶向治疗逐渐成为抗乳腺癌研究的趋势和热点。鉴于传统治疗方法的局限性,免疫疗法以其高特异性和记忆性,对改善肿瘤患者的生存率和预后情况具有潜在作用。免疫检查点是阻碍机体免疫细胞抗肿瘤的主要原因,也是发生免疫逃逸的罪魁祸首。目前针对免疫检查点,主要是采用单克隆抗体抑制剂的方法来提高抗肿瘤的效果。pdl1和pdl2是目前肿瘤免疫治疗,特别是免疫检查点阻断疗法的核心靶点。抑制pdl1和pdl2功能可以激活t细胞的抗肿瘤免疫,杀伤肿瘤细胞。cyclo(-rgdfk)是整合素αvβ3高效选择性环肽类抑制剂,rgdfk的抗肿瘤作用已在多种肿瘤治疗中得到广泛开展,本发明旨在研究rgdfk在制备抗pd-l1药物中的应用,为cyclo-rgdfk的临床实践提供更多的理论依据。
技术实现要素:
本发明要解决的技术问题是提供一种rgdfk抑制pdl1的检测方法及其在制备抗pdl1药物中的应用,为cyclo-rgdfk的临床实践提供更多的理论依据。
为解决上述技术问题,本发明的实施例提供一种rgdfk抑制pdl1的检测方法,包括如下步骤:
(1)探究肿瘤细胞表面pdl1分子的表达调控机制:利用小分子抑制剂处理肿瘤细胞,分别通过基因和蛋白水平来表征pdl1的表达;
(2)检测肿瘤细胞中erk的磷酸化水平;
(3)验证rgdfk对肿瘤细胞pdl1的抑制作用:用rgdfk抑制剂处理肿瘤细胞后,用免疫荧光技术检测细胞中pdl1的蛋白表达水平。
其中,步骤(1)中,小分子抑制剂包括整合素αvβ3的抑制剂rgdfk。
其中,所述肿瘤细胞包括乳腺癌细胞系sum159和mda-mb-231。
其中,所述整合素αvβ3的抑制剂rgdfk的处理浓度为0、2和5μm。
其中,步骤(1)中采用westernblot方法和实时定量pcr方法检测pdl1蛋白水平和基因水平的表达。
其中,步骤(1)中利用小分子抑制剂处理肿瘤细胞的步骤为:
(1-1)复苏细胞:从-80℃中取出冻存管,直接浸入37℃温水中,摇动令其尽快融化;
(1-2)从37℃水浴中取出冻存管,加入1ml的完全培养基,混匀;
(1-3)1000rpm离心3min,弃去上清液;
(1-4)加入含10%fbs的dmem培养基重悬细胞,均匀接种于60mm的培养皿中,5%co2,37℃培养箱静置培养;次日更换一次培养液,继续培养;
(1-5)待细胞密度达到90%时,胰酶消化细胞,根据后续实验确定铺孔的数目;,继续培养;
(1-6)tak1抑制剂处理:5z7,选择处理的浓度依次为0,1,3μm,加药处理时间为24h。
其中,步骤(1)中蛋白质免疫印迹的步骤为:
(1-7)蛋白样品的制备:配制裂解缓冲液置于冰浴中备用;细胞经预冷pbs清洗后转移至灭菌离心管,离心后弃去上清;用含有pmsf的裂解液重悬细胞,冰浴上裂解30min;4℃,高速离心15min后完全吸取上清;蛋白与5×loadingbuffer混匀后,按4:1的比例吸取,95℃金属浴煮沸5min,置于-20℃储存;
(1-8)电泳跑胶及转膜显色:将蛋白样品105℃再次煮沸5min;按照蛋白胶的配方配制10%的分离胶,上层配制5%的浓缩胶,各孔加入10μl蛋白样品;调节电泳仪电压至80v,当溴酚蓝指示剂到达下层分离胶时再次调节电泳仪电压至120v;依据标准蛋白marker将待考察的样品区域胶割下;pvdf膜剪成与割离的蛋白胶相同大小,置于转膜buffer中平衡3min;按照如下叠放顺序:电源正极-滤纸-pvdf膜-凝胶-滤纸-电源负极,300ma湿转1h;pvdf膜置于5%脱脂奶粉中,封闭2h;tbst漂洗pvdf膜3min,加入牛奶或一抗稀释液稀释的一抗,4℃孵育过夜;次日tbst漂洗5min×3,加入适量的二抗,室温孵育2h;最后tbst漂洗10min×3,使用ecl试剂显色。
其中,步骤(3)中免疫荧光检测的步骤为:
(3-1)定量rt-pcr
(3-1-1)通过基因转录水平进行检测,分别设计了pdl1和pdl2的rt-pcr引物,分别在sum159和mda-mb-231细胞中验证;引物分别为:
pdl1-rt-f:gtagcactgacattcatcttc
pdl1-rt-r:ttccttcctcttgtcacgctc
pdl2-rt-f:catagccacagtgatagccct
pdl2-rt-r:ggctcccaagaccacaggttc;
(3-1-2)细胞总rna提取:利用trizol法从上述处理的细胞中提取总rna,具体如下:细胞弃去培养液,利用pbs清洗一次,加入胰酶消化细胞并收集在无rna酶的ep管中;加入1mlrnaisolater,室温放置5min;加入200μl氯仿,剧烈震荡15s,室温静置3min;12000r,4℃离心15min,分为三层,小心吸取上层至一个新的无rna酶的ep管中,加入0.5ml异丙醇,上下颠倒混匀,-20℃静置2h;12000r,4℃离心10min,管底有白色沉淀;弃上清,加入1ml预冷的75%乙醇。7500r,4℃离心5min,尽可能的弃去上清;在通风橱中干燥沉淀10-30min,加入30μl的depc水溶解rna,65℃水浴加热5min,测浓度后放置于-80℃保存;
(3-2)cdna的合成及qpcr检测:
把步骤(3-1-2)提取的rna按照qpcr试剂盒的说明书逆转合成cdna,具体如下:
(3-2-1)基因组去除,在rnase-free的离心管中配制如下混合液,模板rna1µg;4×gdnawipermix,4µl;rnase-freeddh2o补足至16μl,用移液器轻轻吹打混匀,42℃2min;
(3-2-2)配制逆转录反应体系,在步骤(3-2-1)的反应管中直接加入4µl的5×hiscriptiiqrtsupermixii;
(3-2-3)进行逆转录反应,50℃15min,85℃5s,产物加水稀释8倍,置于-20℃保存;随后利用定量pcr检测试剂盒检测pdl1和pdl2的基因表达水平;
(3-3)免疫荧光检测
(3-3-1)让细胞生长在放入24孔细胞培养板中的圆形盖玻片上,接种密度达到60%,加药处理细胞24h;
(3-3-2)每孔用500μl的pbs洗细胞3次,每次5min;之后每孔加200ul4%多聚甲醛,室温固定15min;
(3-3-3)去除多聚甲醛,每孔用500μlpbs洗细胞3次,每次5min;
(3-3-4)每孔加入500μl的1%bsa,室温封闭2h;
(3-3-5)去除封闭液,每孔加200μl一抗,4℃过夜;
(3-3-6)去除抗体,每孔用500μlpbs洗细胞3次,每次5min;
(3-3-7)每孔加200μl荧光二抗,室温孵育2h;
(3-3-8)去除二抗,每孔用500pbs洗细胞3次,每次5min;
(3-3-9)每孔加入hochest,室温10min,500μlpbs洗细胞3次,每次5min;
(3-3-10)载玻片上滴一小滴抗褪色剂,将盖玻片从孔中取出,面朝下盖到抗褪色剂上,使其接触到载玻片上;
(3-3-11)将玻片置于暗处5min使其晾干,此时即可在荧光显微镜下进行观察。
本发明还提供一种rgdfk在制备抗pdl1药物中的应用。
本发明的上述技术方案的有益效果如下:本发明采用整合素αvβ3的抑制剂rgdfk来抑制肿瘤细胞表达免疫检查点pdl1,有效削弱了pd1/pdl1抑制信号通路的功能,以此增加t细胞的抗肿瘤活性。利用小分子抑制剂来提高t细胞的细胞毒性相对于单克隆抗体有较多优点,如容易大规模生产,成本低;较易浸润到肿瘤组织内部,有效发挥抗肿瘤活性;小分子抑制剂还具有其他的抗肿瘤机制,能够起到联合抗肿瘤的效果。本发明采用的rgdfk是一种具有良好开发前景的潜在的抗肿瘤药物,在基因水平明显下调pdl1的表达,有望为临床上治疗乳腺癌提供可行性和理论依据。
附图说明
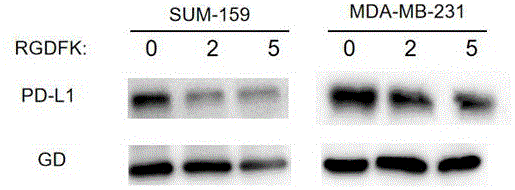
图1为本发明中rgdfk处理sum159和mda-mb-231细胞后wb检测pdl1的表达图;
图2为本发明中rgdfk处理sum159和mda-mb-231细胞后rt-pcr检测pdl1的表达图;
图3为本发明中rgdfk处理sum159和mda-mb-231细胞后wb检测p-erk的表达图;
图4为本发明中不同浓度的rgdfk处理sum159细胞后免疫荧光检测pd-l1的表达图;
图5为本发明中不同浓度的rgdfk处理mda-mb-231细胞后免疫荧光检测pd-l1的表达图。
具体实施方式
为使本发明要解决的技术问题、技术方案和优点更加清楚,下面将结合附图及具体实施例进行详细描述。
本发明提供一种rgdfk抑制pdl1的检测方法,包括如下步骤:
(1)探究肿瘤细胞表面pdl1分子的表达调控机制:利用小分子抑制剂处理肿瘤细胞,分别采用westernblot方法和实时定量pcr(rtpcr)方法检测pdl1蛋白水平和基因水平的表达;
本步骤中的小分子抑制剂优选整合素αvβ3的抑制剂rgdfk,所述整合素αvβ3的抑制剂rgdfk的处理浓度为0、2和5μm。
(2)检测肿瘤细胞中erk的磷酸化水平;
(3)验证rgdfk对肿瘤细胞pdl1的抑制作用:用rgdfk抑制剂处理肿瘤细胞后,用免疫荧光技术检测细胞中pdl1的蛋白表达水平。
所述肿瘤细胞包括乳腺癌细胞系sum159和mda-mb-231。
本发明还提供一种rgdfk在制备抗pdl1药物中的应用。
下面结合具体实施例详细阐述本发明的技术方案。
为了探究肿瘤细胞表面pdl1分子的表达调控机制,利用不同小分子抑制剂处理肿瘤细胞,分别通过基因和蛋白水平来表征pdl1的表达。研究发现,整合素αvβ3的抑制剂rgdfk处理乳腺癌细胞系sum159和mda-mb-231,pdl1和pdl2的表达显著下降。实验中,选择整合素αvβ3抑制剂rgdfk的处理浓度分别为0、2和5μm,通过westernblot方法和实时定量pcr(rtpcr)方法检测pdl1蛋白水平和基因水平的表达。
1、细胞处理
1.1、复苏细胞:从-80℃中取出冻存管,直接浸入37℃温水中,摇动令其尽快融化(慢冻速溶)。
1.2、从37℃水浴中取出冻存管,加入1ml的完全培养基,混匀。
1.3、1000rpm离心3min,弃去上清液。
1.4、加入含10%fbs的dmem培养基重悬细胞,均匀接种于60mm的培养皿中,5%co2,37℃培养箱静置培养;次日更换一次培养液,继续培养。
1.5、待细胞密度达到90%时,胰酶消化细胞,根据后续实验确定铺孔的数目(6孔板),继续培养。
1.6、tak1抑制剂处理:5z7,选择处理的浓度依次为0,1,3μm,加药处理时间为24h。
2、蛋白质免疫印迹(wb)
2.1、蛋白样品的制备:配制裂解缓冲液(含10μlpmsf与990μllysisbuffer)置于冰浴中备用;细胞经预冷pbs清洗后转移至灭菌离心管,离心后弃去上清;用含有pmsf的裂解液重悬细胞,冰浴上裂解30min(摇床);4℃,高速离心15min后完全吸取上清(蛋白)。蛋白与5×loadingbuffer混匀后,按4:1的比例吸取,95℃金属浴煮沸5min,置于-20℃储存。
2.2、电泳跑胶及转膜显色:将蛋白样品105℃再次煮沸5min;按照蛋白胶的配方配制10%的分离胶,上层配制5%的浓缩胶,各孔加入10μl蛋白样品;调节电泳仪电压至80v,当溴酚蓝指示剂到达下层分离胶时再次调节电泳仪电压至120v;依据标准蛋白marker将待考察的样品区域胶割下;pvdf膜剪成与割离的蛋白胶相同大小,置于转膜buffer中平衡3min;按照如下叠放顺序:电源正极-滤纸-pvdf膜-凝胶-滤纸-电源负极,300ma湿转1h;pvdf膜置于5%脱脂奶粉中,封闭2h;tbst漂洗pvdf膜3min,加入牛奶或一抗稀释液稀释的一抗(1:1000),4℃孵育过夜;次日tbst漂洗5min×3,加入适量的二抗(1:2000),室温孵育2h;最后tbst漂洗10min×3,使用ecl试剂显色。蛋白水平检测结果如图1所示,结果分析表明在sum159和mda-mb-231细胞中,rgdfk能够显著抑制pdl1蛋白的表达。前期结果表明,sum159和mda-mb-231细胞中pdl1和pdl2的表达,依赖肿瘤细胞中erk的激活。此外,在两种细胞中,rgdfk处理前后检测了erk的磷酸化水平,结果如图3所示,结果分析表明在sum159和mda-mb-231细胞中,rgdfk能够显著抑制erk的磷酸化水平。
3、定量rt-pcr
本发明通过基因转录水平进行检测,为此分别设计了pdl1和pdl2的rt-pcr引物,分别在sum159和mda-mb-231细胞中验证。引物分别为:
pdl1-rt-f:gtagcactgacattcatcttc
pdl1-rt-r:ttccttcctcttgtcacgctc
pdl2-rt-f:catagccacagtgatagccct
pdl2-rt-r:ggctcccaagaccacaggttc
细胞总rna提取:利用trizol法从上述处理的细胞中提取总rna,具体如下:细胞弃去培养液,利用pbs清洗一次,加入胰酶消化细胞并收集在无rna酶的ep管中;加入1mlrnaisolater(诺唯赞r401-01),室温放置5min;加入200μl氯仿,剧烈震荡15s,室温静置3min;12000r,4℃离心15min,分为三层,小心吸取上层至一个新的无rna酶的ep管中,加入0.5ml异丙醇,上下颠倒混匀,-20℃静置2h(增加沉淀);12000r,4℃离心10min,管底有白色沉淀;弃上清,加入1ml预冷的75%乙醇(depc水配制)。7500r,4℃离心5min,尽可能的弃去上清;在通风橱中干燥沉淀10-30min,加入30μl的depc水溶解rna,65水浴加热5min,测浓度后放置于-80℃保存。
cdna的合成及qpcr检测:
把上面测量后rna按照hiscript®iiqrtsupermixforqpcr(+gdnawiper)(诺唯赞r223-01)的说明书逆转合成cdna。具体如下:①基因组去除,在rnase-free的离心管中配制如下混合液,模板rna1µg;4×gdnawipermix,4µl;rnase-freeddh2o补足至16μl,用移液器轻轻吹打混匀,42℃2min。②配制逆转录反应体系,在第①步的反应管中直接加入4µl的5×hiscriptiiqrtsupermixii。③进行逆转录反应,50℃15min,85℃5s。产物加水稀释8倍,置于-20℃保存。随后利用aceq®qpcrsybrgreenmastermix(诺唯赞q111-02)试剂盒检测pdl1和pdl2的基因表达水平。
mrna水平检测结果如图2所示,结果分析表明在sum159和mda-mb-231细胞中,rgdfk能够显著抑制pdl1基因的转录。
为了进一步验证rgdfk对肿瘤细胞pdl1的抑制作用,用免疫荧光技术检测细胞中pdl1的蛋白表达水平。接着,利用免疫荧光技术在sum159和mda-mb-231细胞中检测pdl1的表达水平,实验中,选择rgdfk处理浓度分别为0、2和5μm。
4、免疫荧光
让细胞生长在放入24孔细胞培养板中的圆形盖玻片上,接种密度达到60%,加药处理细胞24h。每孔用500μl的pbs洗细胞3次,每次5min;之后每孔加200ul4%多聚甲醛,室温固定15min;去除多聚甲醛,每孔用500μlpbs洗细胞3次,每次5min;每孔加入500μl的1%bsa,室温封闭2h;去除封闭液,每孔加200μl一抗(bsa稀释),4℃过夜;去除抗体,每孔用500μlpbs洗细胞3次,每次5min;每孔加200μl荧光二抗,室温孵育2h;去除二抗,每孔用500pbs洗细胞3次,每次5min;每孔加入hochest(1:200pbs稀释),室温10min,500μlpbs洗细胞3次,每次5min;载玻片上滴一小滴抗褪色剂,将盖玻片从孔中取出,面朝下盖到抗褪色剂上,使其轻轻接触到载玻片上(小心气泡);将玻片置于暗处5min使其晾干,此时即可在荧光显微镜下进行观察。
sum159细胞的检测结果如图4所示,结果分析rgdfk处理sum159细胞以后,免疫荧光强度明显减弱,这表明pdl1蛋白水平显著下调。类似的实验结果在mda-mb-231细胞中也得到证实,试验结果如图5所示。
综上,整合素αvβ3的抑制剂rgdfk在乳腺癌细胞中能够显著抑制pdl1基因的表达,可能是通过减弱erk的磷酸化水平的方式来降低pdl1基因的转录,最终抑制了pdl1在肿瘤细胞中的表达。避免了乳腺癌的肿瘤免疫逃逸,因此,整合素αvβ3的抑制剂rgdfk可以增强t细胞在乳腺癌中的免疫治疗效果,有望为临床上治疗乳腺癌提供可行性和理论依据。
以上所述是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明所述原理的前提下,还可以作出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
序列表
<110>南通大学
<120>rgdfk抑制pdl1的检测方法及其在制备抗pdl1药物中的应用
<141>2020-12-14
<160>1
<170>siposequencelisting1.0
<210>1
<211>21
<212>prt
<213>人工合成(artificialsynthesis)
<400>1
glythralaglycysalacysthrglyalacysalathrthrcysala
151015
thrcysthrthrcys
20
- 还没有人留言评论。精彩留言会获得点赞!