抗微生物阳离子聚碳酸酯的制作方法与工艺
抗微生物阳离子聚碳酸酯联合研究协议的各方本发明是按照国际商业机器公司(InternationalBusinessMachinesCorporation)与新加坡科技研究局(AgencyForScience,TechnologyandResearch)之间的联合研究协议进行的。
背景技术:
本发明涉及抗微生物阳离子聚碳酸酯聚合物,且更具体地,涉及具有85摩尔%-100摩尔%阳离子碳酸酯重复单元的阳离子聚碳酸酯均聚物和无规共聚物。耐受抗生素的细菌的不断增加的存在已引起开发新的抗生素的迫切需要。抗微生物肽具有高的活性、生物相容性和优异的选择性。然而,尽管已确定了超过1000种抗微生物肽,但是仅四种肽成功地进入用于创伤愈合的III期临床试验。它们的极其有限的用途的主要原因由如下产生:具有挑战性的合成、高的构造成本和由于蛋白酶降解所致的体内不稳定性。合成阳离子聚合物提供缺乏酶识别的成本固有地较低的替代物。带有阳离子电荷的合成聚合物可通过可比较的静电相互作用而类似地与细菌膜缔合。而且,合成阳离子聚合物可被容易地合成为具有能够被结合(整合,integrate)在细菌膜内的疏水性区域。然而,提高疏水性以努力增加活性常常证明是有问题的,这是因为选择性损失,如由溶血活性和/或细胞毒性的急剧增加所证明的。因此,寻求具有提升的抗微生物活性而不牺牲微生物选择性的合成抗微生物聚合物。
技术实现要素:
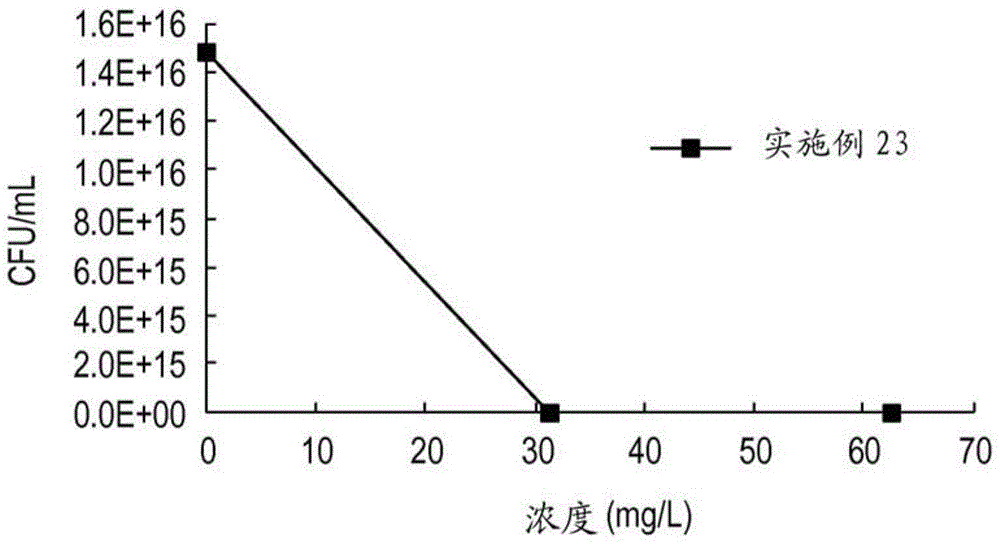
因此,公开具有根据式(12)的结构的抗微生物阳离子聚合物:Zc-Pb-C'-Pb-Zc(12),其中C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧、和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧、和硫,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的全部阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链。还公开式(14)的抗微生物阳离子聚合物:Zc-Pb-C”-Pb-Zc(14),其中C”为使各聚合物链Pb结合的二价连接基团,其中C”包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧、和硫,ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧、和硫,和iii)共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的化合物,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的C6-C25阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链基团,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链基团。进一步公开式(16)的抗微生物阳离子无规共聚物:Zc-Pc-C'-Pc-Zc(16),其中C'为使各聚合物链Pc结合的C2-C15二价连接基团,其中C'包含i):连接到第一聚合物链Pc的第一杂原子,其中所述第一杂原子选自氮、氧、和硫,和ii)连接到第二聚合物链Pc的第二杂原子,其中所述第二杂原子选自氮、氧、和硫,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各Pc为基本上由如下组成的聚合物链:I)约85摩尔%-99.9摩尔%的阳离子碳酸酯重复单元,和II)0.1摩尔%-约15摩尔%的包含共价结合形式的类固醇和/或维生素化合物的碳酸酯重复单元,其中i)所述阳离子聚合物具有约5-约45的重复单元总数量,ii)所述阳离子碳酸酯重复单元各自包含聚合物主链部分和连接到所述聚合物主链部分的C6-C25阳离子侧链部分,和iii)各阳离子侧链部分包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链基团,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链基团。另一抗微生物阳离子无规共聚物具有根据式(18)的结构:Yc-Pb-C'-Pb-Yd(18),其中C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧、和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧、和硫,Yc为独立的选自氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团的单价第一末端基团,Yd为独立的选自氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团的单价第二末端基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的全部阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链。还公开一种方法,其包括,通过环状碳酸酯单体的有机催化的开环聚合(ROP)形成聚碳酸酯,其中所述ROP通过选自如下的双亲核性(di-nucleophilic)化合物引发:类固醇、维生素、包含共价结合形式的前述类固醇和维生素的化合物、及其组合;任选地将所述聚碳酸酯封端;和用季化剂处理所述聚碳酸酯,从而形成抗微生物阳离子聚合物;和其中所述环状碳酸酯单体具有结构式(15):其中环原子编号为1-6地显示,t为具有0-2的值的正整数,t'为具有0-2的值的正整数,t和t'不能两者都为零,La为包含3个或更多个碳的二价连接基团,E'为能够反应以形成连接到La的阳离子部分(Q'(Ra)u')的基团,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,和各Ra为独立的具有1-3的化合价的基团,其中各Ra包含1个或更多个碳,各R'为独立的选自氢和甲基的单价基团,和R”为选自氢、甲基和乙基的单价基团。从下列详细描述、附图和所附权利要求,本发明的上述和其它特征和优点将被本领域技术人员领会和理解。附图说明图1A和1B分别为显示在与三种浓度的阳离子聚合物实施例13和实施例23一起进行18小时温育之后活的金黄色葡萄球菌(S.aureus)菌落形成单位(CFU)的数量的图。所述浓度为0、MIC、和2×MIC,其中MIC为约31mg/L的最小抑菌浓度。图2A-2C为显示作为阳离子聚合物实施例10、11、20、21(图2A),实施例8、9、18、19(图2B),以及实施例12、13、22、23(图2C)的浓度的函数的兔红细胞的溶血%的图。图3A-3F为显示用多种浓度的阳离子聚合物处理的人皮肤成纤维(HDF)细胞的细胞生存力%的图。图4为显示含有悬垂的α-生育酚基部分的实施例49-51的对于大鼠红细胞的溶血活性的图。图5为显示含有悬垂的维生素D2部分的实施例52-54对于大鼠红细胞的溶血活性的图。图6A和6B为显示在用多种浓度(0、0.5MIC、MIC、2MIC)的阳离子聚合物实施例51处理的细菌S.aureus(图6A)和大肠杆菌(E.coli)(图6B)的18小时的温育之后的活的细菌菌落形成单位(CFU)(作为杀灭的百分数)的柱状图。图7A和7B为绘制在用多种浓度(0、0.5MIC、MIC、2MIC)的阳离子聚合物实施例51处理的细菌S.aureus(图6A)和大肠杆菌(E.coli)(图6B)的18小时的温育期间的不同的时间点处的活的细菌菌落形成单位(CFU)的图。图8为显示作为实施例58、61和68-70的浓度的函数的大鼠血细胞的溶血%的图。图9为显示作为阳离子聚合物实施例58、61和68-70的浓度的函数的人皮肤成纤维细胞生存力(%)的图。图10为与异硫氰酸荧光素标记的(FITC标记的)葡聚糖一起在不存在实施例51的情况下(a)或者在存在实施例51的情况下温育10分钟(b)和20分钟(c)的S.aureaus(左侧)的共焦显微镜图像、以及与FITC标记的葡聚糖一起在不存在实施例51的情况下(d)或者在存在实施例51的情况下温育10分钟(e)和20分钟(f)的E.coli(右侧)的图像。比例尺:10微米。图11为S.aureaus(a1,a2)、E-coli(b1,b2)的在与阳离子聚合物实施例51一起进行2小时的温育之前和之后,以及白色念珠菌(C.albicans)(c1,c2)的在与阳离子聚合物实施例47一起进行2小时的温育之前和之后的一系列扫描电子显微镜(SEM)图像。所有实验是使用致死剂量(1.5×MIC)的各聚合物实施的。具体实施方式本发明基于其中重复单元的85%-100%为阳离子碳酸酯重复单元的抗微生物阳离子聚合物。所述阳离子聚合物总体上具有低的质量且对于革兰氏阳性菌、革兰氏阴性菌、和真菌是高度活性和选择性的。所述活性和/或选择性表现出受带正电荷的杂原子与主链的间隔、以及连接到所述带电荷的杂原子的取代基的大小和类型的相当大的影响。使用其中带正电荷的杂原子以不同的长度与主链隔开的阳离子重复单元的混合物也可有利地影响所述活性和/或选择性。聚合物末端基团的大小和类型也可对所述活性和/或选择性具有影响。所述阳离子聚合物优选使用包括一种或多种能够在聚合之后形成阳离子碳酸酯重复单元的环状碳酸酯单体的有机催化的开环聚合(ROP)的过程形成。所述聚合物可使用单亲核性引发剂和/或双亲核性(di-nucleophilic)引发剂形成。还公开抗微生物阳离子共聚物,其包括较少摩尔分数的包含共价结合形式的维生素的碳酸酯重复单元。优选地,这些重复单元是不带电荷的。所述阳离子聚合物可为可生物降解的。术语“可生物降解的”由美国材料与试验协会(theAmericanSocietyforTestingandMaterials)定义为由生物活性、尤其是通过酶促作用引起的降解,导致材料的化学结构的显著变化。为了本文中的目的,如果材料根据ASTMD6400在180天内经历60%的生物降解,则其是“可生物降解的”。在这里,如果材料可通过经由酶催化的反应而降解(例如,解聚),则其是“可酶促生物降解的”。所述阳离子聚合物可为生物相容的。“生物相容的”材料在本文中被定义为在特定的应用中能够以适当的宿主应答运行的材料。在本文中,维生素被定义为对于活体的正常的新陈代谢是少量地必需的且通常不能在所述活体中合成的一组有机化合物中的任意。示例性的维生素包括维生素A(视黄醇)、维生素B1(硫胺)、维生素B2(核黄素)、维生素B3(烟酸)、维生素B5(泛酸)、维生素B6(吡哆醇)、维生素B7(生物素)、维生素B9(叶酸)、维生素B12(钴胺素)、β-胡萝卜素、维生素C(抗坏血酸)、维生素D化合物(其包括维生素D1(钙化醇)、维生素D2(麦角钙化醇)、和/或维生素D3(胆钙化醇))、维生素E化合物(其包括α-生育酚、β-生育酚、γ-生育酚、δ-生育酚、α-生育三烯酚、β-生育三烯酚、γ-生育三烯酚和/或δ-生育三烯酚)、和维生素K1(叶绿醌)。所述阳离子重复单元的带正电荷的基团可在聚合之前或之后形成。具有一个聚合物链(单臂)的阳离子聚合物所述抗微生物阳离子聚合物可具有根据式(1)的结构:Z'-P'-Z”(1),其中Z'为单价C1-C15第一末端基团,其中Z'连接到P'的主链羰基基团,Z”为选自氢和C1-C15部分的单价第二末端基团,P'为基本上由阳离子碳酸酯重复单元组成的聚合物链,其中i)P'具有约5-约45的聚合度(DP),ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的C6-C25阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子碳酸酯重复单元的约25%-约100%(称为第一阳离子碳酸酯重复单元)具有包含13-约25个碳的阳离子侧链,和所述阳离子碳酸酯重复单元的约0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-12个碳的阳离子侧链。Z'可为任何合适的包含1-15个碳的末端基团。Z'包含连接到P'的主链羰基的氧、氮或硫杂原子,分别为碳酸酯、氨基甲酸酯或硫代碳酸酯基团的形式。Z'可为用于形成所述阳离子聚合物的开环聚合中使用的引发剂的残基。在一个实施方式中,Z'为共价结合形式的C1-C15化合物。在另一实施方式中,Z'为C1-C15烷氧基或芳氧基基团。Z"优选连接到P'的主链氧。当Z”为氢时,所述阳离子聚合物具有末端羟基基团。当Z”不为氢时,Z”可为任何合适的包含1-15个碳的末端基团。在一个实施方式中,Z”为共价结合形式的C1-C15化合物。在另一实施方式中,Z"为C1-C15酰基基团。所述第一阳离子碳酸酯重复单元优选包含具有13-约20个碳、甚至更优选15-约20个碳的阳离子侧链。在一个实施方式中,P'由25摩尔%-约75摩尔%的所述第一阳离子碳酸酯重复单元、和约75摩尔%-约25摩尔%的所述第二阳离子碳酸酯重复单元组成。在另一实施方式中,P'由25摩尔%-约50摩尔%的所述第一阳离子碳酸酯重复单元、和约75摩尔%-约25摩尔%的所述第二阳离子碳酸酯重复单元组成。所述阳离子碳酸酯重复单元可具有根据式(2)的结构:其中La-Q'(Ra)u'为包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,t为具有0-2的值的正整数,t'为具有0-2的值的正整数,t和t'不能两者都为零,和X'为带负电荷的离子。带星号的键为与聚合物结构的其它部分的连接点。在式(2)中,阳离子碳酸酯重复单元的聚合物主链原子标记为1-6。在这种情况下,阳离子侧链基团连接到所述重复单元的主链碳5。在一个实施方式中,t和t'两者都为1,各R'为氢,且R"为甲基或乙基。在其阳离子碳酸酯重复单元具有式(2)的式(1)的阳离子聚合物中,第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u'。第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。所述阳离子碳酸酯重复单元可具有根据式(3)的结构:其中Lb-Q'(Ra)u'为包含季铵基团和/或季基团的C5-C24阳离子部分,其中Lb为包含至少2个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,和X'为带负电荷的离子。在这种情况下,阳离子侧链基团为C(=O)O-Lb-Q'(Ra)u'且C(=O)O-Lb对应于式(2)的二价连接基团La。所述阳离子侧链连接到标记为5的主链碳。在其阳离子碳酸酯重复单元具有式(3)的式(1)的阳离子聚合物中,第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链C(=O)O-Lb-Q'(Ra)u'。第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链C(=O)O-Lb-Q'(Ra)u'。所述阳离子重复单元可具有根据式(4)的结构:其中Lc-Q'(Ra)u'为包含季铵基团和/或季基团的C5-C24阳离子部分,其中Lc为包含至少2个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,和各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,和X'为带负电荷的离子。在这种情况下,所述阳离子侧链为N(H)C(=O)O-Lc-Q'(Ra)u'且N(H)C(=O)O-Lc对应于式(2)的二价连接基团La。所述阳离子侧链连接到标记为5的主链碳。丝氨醇和/或苏氨醇提供用于形成式(4)的重复单元的有用的起始材料。在其阳离子碳酸酯重复单元具有式(4)的式(1)的阳离子聚合物中,第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链N(H)C(=O)O-Lc-Q'(Ra)u'。第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链N(H)C(=O)O-Lc-Q'(Ra)u'。使用式(2)的阳离子重复单元,式(1)的阳离子聚合物可具有根据式(5)的结构:其中:n'表示阳离子碳酸酯重复单元的数量,其中n'具有约5-约45的值,Z'为单价C1-C15第一末端基团,Z”为选自氢和C1-C15部分的单价第二末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。如式(5)中所示,聚合物链包含主链部分,所述主链部分包含在所述链的第一末端处的氧羰基基团(称作“羰基末端”)、以及在所述链的第二末端处的主链氧(称作“氧末端”)。所述阳离子碳酸酯重复单元的主链原子编号为1-6地显示。在式(5)中,所述第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共13-约25个碳。优选地,所述第一阳离子碳酸酯重复单元的La基团包含5-约12个碳、或更优选8-约12个碳。优选地,所述第一阳离子碳酸酯重复单元的Q'(Ra)u'包含3-约18个碳、更优选4-约18个碳。同样,式(5)的第二阳离子碳酸酯重复单元的La和Q'(Ra)u'可各自具有至少3个碳,条件是La-Q'(Ra)u'具有总共6-12个碳。在一个实施方式中,Z”为氢。在另一实施方式中,所述第一阳离子碳酸酯重复单元具有包含15-约20个碳的阳离子侧链La-Q'(Ra)u'。作为更具体的非限制性的实例,Z'可为苄氧基和/或4-甲基苄氧基,和Z”可为氢和/或乙酰基。末端基团Z'和/或Z”、以及下面描述的末端基团可提升抗微生物功效和或使所述阳离子聚合物免受由例如未封端的亲核性羟基末端基团引起的潜在的不想要的副反应(例如,链断裂)而稳定。体积较大的末端基团还可提供疏水性,其容许控制所述阳离子聚合物的两亲性质。所述抗微生物阳离子聚合物可具有根据式(6)的结构:其中n'表示阳离子碳酸酯重复单元的数量,且n'具有约5-约45的值,Y'为包含共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的生物活性的化合物的单价第一末端基团,Y”为选自氢和C1-C15部分的单价第二末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(6)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(6)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。所述生物活性的化合物可为立体专一性的(立体规整性的,stereospecific)或非立体专一性的(非立体规整性的)。在一个实施方式中,Y'包含共价结合形式的类固醇(例如,胆固醇),称为S'。所述类固醇基团可提升所述阳离子聚合物的生物相容性。在另一实施方式中,Y'包含共价结合形式的维生素(例如,α-生育酚(维生素E化合物)和/或麦角钙化醇(维生素D2))。Y'可具有结构S'-L'-*,其中S'为类固醇基团且L'为单键或任何合适的包含1-约10个碳的二价连接基团。在这种情况下,L'将S'连接到聚碳酸酯主链的羰基末端。所述抗微生物阳离子聚合物可具有根据式(7)的结构:其中n'表示阳离子碳酸酯重复单元的数量,且n'具有约5-约45的值,W'为单价C1-C15第一末端基团,W”为包含共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的生物活性的化合物的单价第二末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(7)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(7)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。W”可包含立体专一性或非立体专一性形式的所述生物活性的化合物。在一个实施方式中,W”包含共价结合形式的胆固醇、α-生育酚(维生素E化合物)、麦角钙化醇(维生素D2)、或其组合。W”可具有总的结构S'-L”-*,其中S'为类固醇基团且L”为单键或任何合适的包含1-约10个碳的二价连接基团。在这种情况下,L”将S'连接到聚碳酸酯主链的氧末端。所述抗微生物阳离子聚合物可为具有根据式(8)的结构的无规共聚物:Z'-P”-Z”(8),其中Z'为单价C1-C15第一末端基团,Z”为选自氢和C1-C15部分的单价第二末端基团,P”为基本上由如下组成的聚合物链:I)约85摩尔%-99.9摩尔%的阳离子碳酸酯重复单元、以及II)0.1摩尔%-约15摩尔%的包含共价结合形式的类固醇和/或维生素化合物的碳酸酯重复单元,其中i)P”具有约5-约45的聚合度(DP),ii)所述阳离子碳酸酯重复单元各自包含聚合物主链部分和连接到所述聚合物主链部分的阳离子侧链部分,和iii)各阳离子侧链部分包含季铵基团和/或季基团的带正电荷的杂原子,所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(8)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(8)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。式(8)的抗微生物阳离子聚合物可具有根据式(9)的结构:其中n'表示阳离子碳酸酯重复单元的数量,其中n'具有大于0的值,m'表示碳酸酯重复单元的数量,其中m'具有大于0的值,n'+m'具有约5-约45的值,m':n'的比率为约15:85-约0.1:99.9,Z'为单价C1-C15第一末端基团,Z”为选自氢和C1-C15部分的单价第二末端基团,各Ld为独立的选自单键和包含1-约10个碳的单价基团的二价连接基团,各H'为独立的包含共价结合形式的类固醇和/或维生素化合物的单价基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。在式(9)的方括号内的重复单元的垂直堆叠表示在聚合物链内的重复单元的无规分布。式(9)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(9)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。H'可包含共价结合形式的维生素E化合物、维生素D化合物、或其组合。优选地,所述维生素化合物为α-生育酚(维生素E化合物)、麦角钙化醇(维生素D2)、或其组合。随后的讨论适用于本文中所有公开的阳离子聚合物结构。示例性的非限制性的二价La基团包括:及其组合。在这些实例中,羰基和氨基甲酸酯氮的带星号的键连接到聚碳酸酯主链(例如,以上阳离子碳酸酯重复单元中的标记为5的主链碳),且亚甲基基团的带星号的键连接到Q'。La和Q'(Ra)u'一起形成季铵基团或季基团,意味着带正电荷的杂原子Q'键合到La的碳和最高达三个独立的Ra基团。各Ra包含至少一个碳。各Ra可为单价烃取代基(例如,甲基、乙基等),在该情况中u'为3。Ra可与Q'形成环,在该情况中所述环的Ra具有2的化合价。例如,Q'(Ra)u'可为:其中带星号的键连接到La,Q'为氮,且u'为2。在该实例中,第一Ra为二价亚丁基基团(*-(CH2)4-*),且第二Ra为甲基。Ra可与Q'形成多环部分。例如,Q'(Ra)u'可为:其中带星号的键连接到La,Q'为氮,u'为1,且Ra为具有3的化合价的片段Ra基团还可独立地包含氧、氮、硫、和/或另外的杂原子。在一个实施方式中,各Ra为独立的单价支化或未支化的烃取代基。示例性的非限制性的Ra基团包括甲基、乙基、正丙基、异丙基、正丁基、异丁基、正戊基、正己基、正庚基、正辛基、和苄基。所述Ra基团可组合使用。示例性的非限制性的Q'(Ra)u'基团包括:及其组合。在前述实例中,应理解,带正电荷的氮和磷是四价的,且带星号的键连接到La的碳。Q'基团可单独地或组合存在于所述阳离子聚合物中。示例性的带负电荷的离子X'包括卤根(例如,氯根、溴根、和碘根)、羧酸根(例如,乙酸根和苯甲酸根)、和/或磺酸根(例如,甲苯磺酸根)。所述X'离子可单独地或组合存在。示例性的非限制性的阳离子碳酸酯重复单元包括下列:及其组合,其中X-为带负电荷的离子。总的来说,所述阳离子聚合物的抗微生物活性通过如下促进:使所述阳离子碳酸酯重复单元的25摩尔%-100摩尔%(第一阳离子碳酸酯重复单元)中的带正电荷的杂原子Q'与聚碳酸酯主链隔开具有从聚合物主链起6个或更多个邻接连接的原子中心的最短路径。最短路径定义为将Q'结合到聚合物主链的邻接连接的原子中心的最低数量。邻接连接的原子中心应被理解为在聚碳酸酯主链和Q'之间。例如,如果La-Q'为:则从聚合物主链到Q'的最短路径具有如所编号的5个邻接连接的原子中心。所述最短路径不包括羰基氧。作为另一实例,如果La-Q'为则从聚合物主链到Q'的最短路径具有如所编号的6个邻接连接的原子中心。所述最短路径不包括酰胺氢和羰基氧。作为另一实例,如果La-Q'为则从聚合物主链到Q'的最短路径具有如所编号的8个邻接连接的原子中心。所述最短路径不包括芳族环的两个碳和羰基氧。作为另一实例,如果La-Q'为则从聚合物主链到Q'的最短路径具有如所编号的7个邻接连接的原子中心。所述最短路径不包括芳族环的三个碳和羰基氧。最后,作为另一实例,如果La-Q'为则从聚合物主链到Q'的最短路径具有如所编号的4个邻接连接的原子中心。所述最短路径不包括芳族环和羰基氧。优选地,所述第一碳酸酯重复单元的Q'与所述聚合物主链隔开具有6-约18个邻接连接的原子中心、且更优选8-约15个邻接连接的原子中心的最短路径。类固醇基团S'可源自天然存在的人类固醇、非人类固醇、和/或合成类固醇化合物。在这里,类固醇基团包含四环的环结构:其中环体系的17个碳如所显示地编号。所述类固醇基团可包含一个或多个额外的取代基,所述取代基连接到所编号的环位置的一个或多个。所述四环的环结构的各环可独立地包含一个或多个双键。示例性的类固醇基团包括在下面没有立体化学地显示的来自胆固醇的胆甾醇基:胆甾醇基的非限制性的立体专一性的结构包括其中标记了各立体专一性的非对称中心的R、S立体构型。额外的非限制性的类固醇基团包括来自睾丸激素的来自马烯雌酮的来自表雄酮的来自二氢睾酮的来自诺龙(nandrolone)的来自二氢孕酮的来自孕烯醇酮的来自马萘雌酮的来自脱氢表雄酮的来自醋酸皮质酮的来自醋酸去氧皮质酮的和来自雌素酮的带星号的键表示连接点。例如,以上类固醇基团各自的带星号的键可经由二价连接基团L'连接到聚碳酸酯主链的末端羰基基团。替代地,所述类固醇基团的带星号的键可直接连接到聚碳酸酯主链的末端羰基基团(即,L'可为单键)。本领域技术人员将认识到,所述类固醇基团的各非对称中心可作为R立体异构体、S立体异构体、或者作为R和S立体异构体的混合物存在。额外的类固醇基团S'包括以上结构的多种立体异构体。阳离子聚合物可包含作为单一的立体异构体或作为立体异构体的混合物的类固醇基团。在一个实施方式中,S'为胆甾醇基基团,其中所述胆甾醇基基团为下列异构体的混合物:其由结构表示。更具体的含有类固醇的阳离子聚合物具有根据式(10)的结构:其中n'表示阳离子碳酸酯重复单元的数量,且具有约5-约45的值,S'-L'为第一末端基团,其中L'为单键或包含1-约10个碳的二价连接基团,和S'包含共价结合形式的类固醇,Y”为选自氢和C1-C15部分的单价第二末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。在式(10)中,当L'为单键时,S'直接连接到聚碳酸酯主链的末端羰基基团。在一个实施方式中,L'为包括选自如下的亚烷基氧的二价连接基团:亚乙基氧(*-CH2CH2O-*)、亚丙基氧*-CH2CH2CH2O-*、和/或三(亚乙基氧)(*-CH2CH2OCH2CH2OCH2CH2O-*),其中氧的带星号的键连接到聚碳酸酯主链的末端羰基基团且碳的带星号的键连接到S'。式(10)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(10)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。含有类固醇的阳离子聚合物可包含以上进一步描述的阳离子碳酸酯重复单元的一种或组合。所述含有类固醇的阳离子聚合物可具有根据式(11)的结构:其中n'表示阳离子碳酸酯重复单元的数量,且具有约5-约45的值,Y'为单价C1-C15第一末端基团,S'-L”为第二末端基团,其中L”为单键或包含1-约10个碳的二价连接基团且S'包含共价结合形式的类固醇,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。基团S'-L”连接到聚碳酸酯主链的氧末端,且Y'连接到聚碳酸酯主链的羰基末端。式(11)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(11)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。具有两个阳离子聚合物链的阳离子聚合物(双臂阳离子聚合物)所述抗微生物阳离子聚合物可具有根据式(12)的结构:Zc-Pb-C'-Pb-Zc(12),其中C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的全部阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链。式(12)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(12)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。在一个实施方式中,各Zc为氢。在另一实施方式中,所述第一阳离子碳酸酯重复单元的带正电荷的杂原子Q'与所述主链部分隔开在Q'和所述主链部分之间具有6-约15个邻接连接的原子中心的最短路径。更具体的式(12)的阳离子聚合物具有根据式(13)的结构:其中n'表示所述阳离子聚合物的阳离子碳酸酯重复单元的总数量,且具有约5-约45的值,C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,聚合物链Pb基本上由所述阳离子碳酸酯重复单元组成,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(13)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(13)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。C'可为用于通过开环聚合制备阳离子聚合物的双亲核性引发剂的残基。在另一抗微生物聚合物中,连接两个阳离子聚合物链的片段包含共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的生物活性的化合物。这些抗微生物阳离子聚合物具有根据式(14)的结构:Zc-Pb-C”-Pb-Zc(14),其中C”为使各聚合物链Pb结合的二价连接基团,其中C”包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,和iii)共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的化合物,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的C6-C25阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链基团,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链基团。式(14)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(14)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链,且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链。所述第一阳离子碳酸酯重复单元的带正电荷的杂原子Q'可与所述主链部分隔开在Q'和所述主链部分之间具有6-约18个邻接连接的原子中心的最短路径。在一个实施方式中,C”包含共价结合形式的胆固醇。在另一实施方式中,C”包含共价结合形式的选自α-生育酚、麦角钙化醇、及其组合的维生素。更具体的式(14)的阳离子聚合物具有根据式(15)的结构:其中n'表示所述阳离子聚合物的阳离子碳酸酯重复单元的总数量,且具有约5-约45的值,C”为使各聚合物链Pb结合的二价连接基团,其中C”包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,和iii)共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的化合物,所述聚合物链Pb各自基本上由阳离子碳酸酯重复单元组成,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%(称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(15)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(15)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。所述抗微生物阳离子聚合物可具有根据式(16)的结构:Zc-Pc-C'-Pc-Zc(16),其中C'为使各聚合物链Pc结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pc的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pc的第二杂原子,其中所述第二杂原子选自氮、氧和硫,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各Pc为基本上由如下组成的聚合物链:I)约85摩尔%-99.9摩尔%的阳离子碳酸酯重复单元,和II)0.1摩尔%-约15摩尔%的包含共价结合形式的类固醇和/或维生素化合物的碳酸酯重复单元,其中i)所述阳离子聚合物具有约5-约45的重复单元总数量,ii)所述阳离子碳酸酯重复单元各自包含聚合物主链部分和连接到所述聚合物主链部分的C6-C25阳离子侧链部分,和iii)各阳离子侧链部分包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链基团,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%,称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链基团。式(16)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(16)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链,且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链。式(16)的阳离子聚合物可具有根据式(17)的结构:其中n'表示阳离子碳酸酯重复单元的总数量,其中n'具有大于0的值,m'表示碳酸酯重复单元的总数量,其中m'具有大于0的值,n'+m'具有约5-约45的值,和比率m':n'为约15:85-约0.1:99.9,C'为使各聚合物链Pc结合的C2-C15非聚合物型二价连接基团,其中C'包含:i)连接到第一聚合物链Pc的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pc的第二杂原子,其中所述第二杂原子选自氮、氧和硫,各Zc为独立的选自氢和C1-C15部分的单价末端基团,各Ld为独立的选自单键和包含1-约10个碳的单价基团的二价连接基团,各H'为独立的包含共价结合形式的类固醇和/或维生素化合物的单价基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%,称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(17)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(17)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。H'可包含共价结合形式的维生素E化合物、维生素D化合物、或其组合。在一个实施方式中,H'包含共价结合形式的选自如下的维生素化合物:α-生育酚(维生素E化合物)、麦角钙化醇(维生素D2)、及其组合。所述抗微生物阳离子聚合物可具有根据式(18)的结构:Yc-Pb-C'-Pb-Yd(18),其中C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,Yc为独立的选自如下的单价第一末端基团:氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团,Yd为独立的选自如下的单价第二末端基团:氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团,各聚合物链Pb基本上由阳离子碳酸酯重复单元组成,其中i)所述阳离子聚合物包含总共5-约45个阳离子碳酸酯重复单元,ii)所述阳离子碳酸酯重复单元各自包含所述聚合物链的主链部分和连接到所述主链部分的阳离子侧链,和iii)所述阳离子侧链包含季铵基团和/或季基团的带正电荷的杂原子Q',所述阳离子聚合物的全部阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链,和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%,称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链。式(18)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(18)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。Yc和/或Yd可包含共价结合形式的类固醇和/或维生素。更具体的式(18)的阳离子聚合物具有根据式(19)的结构:其中n'表示所述阳离子聚合物的阳离子碳酸酯重复单元的总数量,且具有约5-约45的值,C'为使各聚合物链Pb结合的C2-C15二价连接基团,其中C'包含:i)连接到第一聚合物链Pb的第一杂原子,其中所述第一杂原子选自氮、氧和硫,和ii)连接到第二聚合物链Pb的第二杂原子,其中所述第二杂原子选自氮、氧和硫,聚合物链Pb基本上由所述阳离子碳酸酯重复单元组成,Yc为独立的选自如下的单价末端基团:氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团,Yd为独立的选自如下的单价末端基团:氢、包含共价结合形式的类固醇的基团、和包含共价结合形式的维生素的基团,各La-Q'(Ra)u'为独立的包含季铵基团和/或季基团的C6-C25阳离子侧链,其中La为包含至少3个碳的二价连接基团,Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,且各Ra包含至少1个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,没有阳离子碳酸酯重复单元具有t=0和t'=0,和各X'为独立的带负电荷的离子;和其中所述阳离子聚合物的所述阳离子碳酸酯重复单元的约25%-100%(称为第一阳离子碳酸酯重复单元)具有包含10-约25个碳的阳离子侧链La-Q'(Ra)u',和所述阳离子聚合物的所述阳离子碳酸酯重复单元的0%-约75%,称为第二阳离子碳酸酯重复单元)具有包含6-9个碳的阳离子侧链La-Q'(Ra)u'。式(19)的第一阳离子碳酸酯重复单元的La和Q'(Ra)u'可单独地具有3-约22个碳,条件是La-Q'(Ra)u'具有总共10-约25个碳。在一个实施方式中,式(19)的第一阳离子碳酸酯重复单元具有包含13-约25个碳的阳离子侧链La-Q'(Ra)u',且第二阳离子碳酸酯重复单元具有包含6-12个碳的阳离子侧链La-Q'(Ra)u'。形成阳离子的环状碳酸酯单体制备所公开的阳离子聚合物的优选方法利用能够在聚合之前或之后形成阳离子部分的环状碳酸酯单体。这些称作形成阳离子的单体,其具有式(20):其中环原子编号为1-6地显示,La为包含至少3个碳的二价连接基团,E'为能够反应以产生连接到La的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含1个或多个碳,且Q'(Ra)u'和La总共包含6-约25个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,t为具有0-2的值的正整数,t'为具有0-2的值的正整数,和t和t'不能两者都为零。式(20)的形成阳离子的单体具有环取代基La-E'。该环取代基La-E'变成通过所述形成阳离子的单体的开环聚合形成的初始聚合物的侧链。E'可为亲电性和/或亲核性基团,只要侧链La-E'能够反应以产生所述阳离子聚合物的C6-C25阳离子侧链La-Q'(Ra)u'。优选地,E'为能够与叔胺反应以形成季铵基团、和/或与叔膦反应以形成季基团的离去基团。所述形成阳离子的单体可为立体专一性的或非立体专一性的。在一个实施方式中,式(20)的t和t'各自为1,在碳4处的各R'为氢,在碳6处的各R'为氢,且在碳5处的R”选自氢、甲基、和乙基。式(20)的形成阳离子的单体的开环聚合产生具有根据式(21)的重复单元的初始聚碳酸酯:其中主链原子编号为1-6地显示,La为包含至少3个碳的二价连接基团,E'为能够反应以产生连接到La的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,且Q'(Ra)u'和La总共包含6-约25个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,t为具有0-2的值的正整数,t'为具有0-2的值的正整数,和t和t'不能两者都为零。更具体的形成阳离子的单体具有式(22):其中环原子5被标记,Lb为包含至少2个碳的二价连接基团,E'为能够反应以产生连接到Lb的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,且Q'(Ra)u'和Lb总共包含5-约24个碳,和R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团。式(22)的形成阳离子的单体的开环聚合产生具有根据式(23)的重复单元的聚碳酸酯:其中主链原子5被标记,Lb为包含至少2个碳的二价连接基团,E'为能够反应以产生连接到Lb的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,且Q'(Ra)u'和Lb总共包含5-约24个碳,和R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团。所述形成阳离子的单体可具有式(24):其中环原子5被标记,Lc为包含至少2个碳的二价连接基团,E'为能够反应以产生连接到Lc的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,且Q'(Ra)u'和Lc总共包含5-约24个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,和R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团。式(24)的形成阳离子的单体的开环聚合产生具有根据式(25)的重复单元的初始聚碳酸酯:其中主链原子5被标记,Lc为包含至少2个碳的二价连接基团,E'为能够反应以产生连接到Lc的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含至少1个碳,且Q'(Ra)u'和Lc总共包含5-约24个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,和R”为选自氢、卤素、和包含1-6个碳的烷基基团的单价基团。示例性的形成阳离子的单体包括表1的环状碳酸酯单体。表1用于单臂阳离子聚合物的单亲核性引发剂用于ROP的亲核性引发剂通常包括醇、胺、和/或硫醇。对于以上描述的具有一个阳离子聚合物链的阳离子聚合物(单臂阳离子聚合物),ROP引发剂为单亲核性非聚合物型引发剂(例如,乙醇、正丁醇、苯甲醇等)。在一些情况下,所述ROP引发剂可包含共价结合形式的选自类固醇、非类固醇激素、维生素、和药物的生物活性的化合物。例如,单亲核性ROP引发剂包括胆固醇、α-生育酚、和麦角钙化醇。更具体的单亲核性ROP引发剂包含类固醇基团S'。所述引发剂可具有根据式(26)的结构:S'-Le(26),其中S'为类固醇基团且Le为单价基团,其包含:i)1-约10个碳和ii)用于ROP的亲核性引发基团。式(26)的ROP引发剂的非限制性的实例包括Chol-OPrOH:和Chol-OTEG-OH:在以上实例中,S'为胆甾醇基基团。使用以下描述的制备阳离子聚合物的优选方法,所述阳离子聚合物的S'-L'-*片段为当连接到聚碳酸酯主链的羰基末端时ROP引发剂的残基。得自Chol-OPrOH的S'-L'-*片段具有结构:得自Chol-OTEG-OH的S'-L'-*片段具有结构:所述ROP引发剂可单独地或者与不同的ROP引发剂(例如,具有不同的类固醇基团和/或不同的Le基团的引发剂)组合使用。所述ROP引发剂可为立体专一性的或非立体专一性的。用于双臂阳离子聚合物的双亲核性引发剂用于形成以上描述的具有两个聚合物链的阳离子聚合物(双臂阳离子聚合物)的ROP引发剂为双亲核性引发剂。示例性的双亲核性ROP引发剂包括乙二醇、丁二醇、1,4-苯二甲醇、和Bn-MPA:包含类固醇基团的示例性的双亲核性ROP引发剂为Chol-MPA:ROP聚合使用式(20)的环状碳酸酯单体来说明制造所公开的阳离子聚合物的方法,形成包含如下的反应混合物:式(20)的环状碳酸酯单体、催化剂、任选的加速剂、单亲核性ROP引发剂(任选地包含类固醇基团)、和溶剂。搅拌所述反应混合物形成初始聚合物。任选地可将所述初始聚合物封端以形成经封端的初始聚合物。所得聚合物具有根据式(27)的结构:其中n'表示阳离子碳酸酯重复单元的数量,其中n'具有约5-约45的值,Z'为单价C1-C15第一末端基团,Z”为选自氢和C1-C15部分的单价第二末端基团,La为包含至少3个碳的二价连接基团,E'为能够反应以产生连接到La的阳离子部分Q'(Ra)u'的取代基,其中Q'为四价的带正电荷的氮或磷,u'具有1-3的值,各Ra为独立的具有1-3的化合价的基团,其中各Ra包含1个或多个碳,且Q'(Ra)u'和La总共包含6-约25个碳,各R'为独立的选自氢、卤素、甲基和乙基的单价基团,各R”为独立的选自氢、卤素、和包含1-6个碳的烷基基团的单价基团,各t为独立的具有0-2的值的正整数,各t'为独立的具有0-2的值的正整数,和没有碳酸酯重复单元具有t=0和t'=0。Z'可为所述ROP引发剂的残基。在一个实施方式中,Z'为包含类固醇部分的S'-L'基团。在这种情况下,所述初始聚合物的各碳酸酯重复单元包含侧链E'基团。通过ROP形成的初始聚合物的活性末端(氧末端)具有反应性的羟基基团(第二末端基团Z”=H),其能够引发另外的ROP。所述活性末端可用封端剂处理,从而形成能够防止进一步的链增长和使所述聚合物对于不想要的副反应诸如链断裂稳定的第二末端基团Z”。所述聚合和封端可在相同的锅中在不分离所述初始聚合物的情况下发生。封端剂包括,例如,用于将末端羟基基团转化成酯的材料,诸如羧酸酐、羧酰氯、和反应性的酯(例如,对-硝基苯基酯)。在一个实施方式中,所述封端剂为酰化剂,且所述第二末端基团Z”为酰基基团。在另一实施方式中所述酰化剂为醋酸酐,且所述第二末端基团Z”为乙酰基基团。在另一实施方式中,所述封端剂包含共价结合形式的类固醇基团、维生素、或其组合。可对所述初始聚合物和/或经封端的初始聚合物进行化学、热、和/或光化学处理以将E'转化成带正电荷的Q'(Ra)u'基团,从而形成阳离子聚合物。例如,E'可为亲电性离去基团(例如,氯根、溴根、碘根、磺酸酯等),其能够经历与路易斯碱(例如,叔胺、三烷基膦)的亲核取代反应以形成季铵基团和/或基团。在一个实施方式中,E'为氯根、溴根、和/或碘根。在另一实施方式中,所述环状碳酸酯单体为式(22)的化合物且所述初始聚合物包含式(23)的重复单元。在另一实施方式中,所述环状碳酸酯单体为式(24)的化合物且所述初始聚合物包含式(25)的重复单元。还设想使用包含带正电荷的Q'基团的阳离子环状碳酸酯单体形成所述阳离子聚合物的方法。在这种情况下,ROP形成具有活性末端单元(即,能够引发随后的ROP的亲核性羟基末端基团)的初始阳离子聚合物。可将所述活性末端单元封端以防止不想要的副反应。用于通过与亲电性E'基团的亲核取代反应形成季胺的示例性的非限制性的叔胺包括三甲胺、三乙胺、三正丙胺、三异丙胺、三正丁胺、三正戊胺、二甲基乙基胺、二甲基丙基胺、二甲基-异丙基胺、二甲基丁基胺、二甲基戊基胺、二甲基苄基胺、二乙基甲基胺、二乙基戊基胺、二乙基丁基胺、N,N-二甲基环己基胺、N-甲基咪唑、N-乙基咪唑、N-(正丙基)咪唑、N-异丙基咪唑、N-(正丁基)咪唑、N,N-二乙基环己基胺、N,N-二甲基苯胺、N,N-二乙基苯胺、吡啶、及其组合。用于通过与亲电性E'基团的亲核取代反应形成季基团的示例性的非限制性的叔膦包括三甲基膦、三乙基膦、三丙基膦、三丁基膦、乙基二甲基膦、丙基二甲基膦、丁基二甲基膦、戊基二甲基膦、己基二甲基膦、庚基二甲基膦、辛基二甲基膦、甲基二乙基膦、丙基二乙基膦、丁基二乙基膦、戊基二乙基膦、己基二乙基膦、庚基二乙基膦、辛基二乙基膦、戊基二丙基膦、戊基二丁基膦、二戊基甲基膦、二戊基乙基膦、二戊基丙基膦、二戊基丁基膦、三戊基膦、己基二丙基膦、己基二丁基膦、环己基-二甲基膦、环己基二乙基膦、二己基甲基膦、二己基-乙基膦、二己基丙基膦、苄基二甲基膦、及其组合。示例性的非限制性的带有共价结合形式的类固醇或维生素的环状碳酸酯单体列于表2中。表2.所述开环聚合可在约环境温度或更高、更特别地15℃-200℃、和甚至更特别地20℃-80℃的温度下进行。优选地,所述ROP在环境温度下进行。反应时间随着溶剂、温度、搅拌速率、压力和设备而改变,但总的来说,所述聚合在1-100小时内完成。所述ROP反应优选地用溶剂进行。非限制性的溶剂包括二氯甲烷、氯仿、苯、甲苯、二甲苯、氯苯、二氯苯、三氟甲苯、石油醚、乙腈、戊烷、己烷、庚烷、2,2,4-三甲基戊烷、环己烷、二乙醚、叔丁基甲基醚、二异丙醚、二氧六环、四氢呋喃、或包含前述溶剂之一的组合。合适的单体浓度为约0.1-5摩尔/升、且更特别地约0.2-4摩尔/升。所述ROP聚合在惰性干燥气氛诸如氮气或氩气下在100MPa-500MPa(1atm-5atm)的压力下、更典型地在100MPa-200Mpa(1atm-2atm)的压力下进行。在所述反应完成时,可使用降低的压力除去溶剂。不太优选的用于ROP聚合的催化剂包括金属氧化物诸如四甲醇锆、四-异丙醇锆、四-异丁醇锆、四-正丁醇锆、四-叔丁醇锆、三乙醇铝、三-正丙醇铝、三-异丙醇铝、三-正丁醇铝、三-异丁醇铝、三-仲丁醇铝、单-仲丁醇-二-异丙醇铝、乙酰乙酸乙基铝二异丙酯(ethylacetoacetatealuminumdiisopropylate)、三(乙酰乙酸乙酯)铝、四乙醇钛、四-异丙醇钛、四-正丙醇钛、四-正丁醇钛、四-仲丁醇钛、四-叔丁醇钛、三-异丙醇镓、三-异丙醇锑、三-异丁醇锑、三甲醇硼、三乙醇硼、三-异丙醇硼、三-正丙醇硼、三-异丁醇硼、三-正丁醇硼、三-仲丁醇硼、三-叔丁醇硼、四甲醇锗、四乙醇锗、四-异丙醇锗、四-正丙醇锗、四-异丁醇锗、四-正丁醇锗、四-仲丁醇锗和四-叔丁醇锗;卤化化合物诸如五氯化锑、氯化锌、溴化锂、氯化锡(IV)、氯化镉和三氟化硼二乙醚;烷基铝诸如三甲基铝、三乙基铝、氯化二乙基铝、二氯化乙基铝和三-异丁基铝;烷基锌诸如二甲基锌、二乙基锌和二异丙基锌;杂多酸诸如磷钨酸、磷钼酸、硅钨酸和其碱金属盐;锆化合物诸如锆酰氯、辛酸锆、硬脂酸锆、和硝酸锆。优选地,用于所述开环聚合的催化剂的化学式不包括离子或非离子形式的选自如下的金属:铍、镁、钙、锶、钡、镭、铝、镓、铟、铊、锗、锡、铅、砷、锑、铋、碲、钋、以及周期表第3-12族的金属。所述周期表第3-12族的金属包括钪、钛、钒、铬、锰、铁、钴、镍、铜、锌、钇、锆、铌、钼、锝、钌、铑、钯、银、镉、镧、铈、镨、钕、钷、钐、铕、钆、铽、镝、钬、铒、铥、镱、镥、铪、钽、钨、铼、锇、铱、铂、金、汞、锕、钍、镤、铀、镎、钚、镅、锔、锫、锎、锿、镄、钔、锘、铹、和优选的催化剂为其化学式不含有以上金属的有机催化剂。用于开环聚合的有机催化剂的实例包括叔胺诸如三烯丙基胺、三乙胺、三-正辛基胺和苄基二甲基胺4-二甲基氨基吡啶、膦、N-杂环卡宾(NHC)、双官能氨基硫脲、磷腈、脒、和胍。更具体的有机催化剂为N-二(3,5-三氟甲基)苯基-N’-环己基硫脲(TU):其它的ROP有机催化剂包含至少一个1,1,1,3,3,3-六氟丙-2-醇-2-基(HFP)基团。贡献单个氢键的催化剂具有式(28):R2-C(CF3)2OH(28),其中R2表示氢或具有1-20个碳的单价基团例如烷基基团、取代的烷基基团、环烷基基团、取代的环烷基基团、杂环烷基基团、取代的杂环烷基基团、芳基基团、取代的芳基基团、或其组合。示例性的贡献单个氢键键合的催化剂列于表3中。表3.贡献两个氢键键合的催化剂具有两个HFP基团,由式(29)表示:其中R3为包含1-20个碳的二价基团桥接基团诸如亚烷基基团、取代的亚烷基基团、亚环烷基基团、取代的亚环烷基基团、亚杂环烷基基团、取代的亚杂环烷基基团、亚芳基基团、取代的亚芳基基团、及其组合。代表性的式(29)的双氢键键合催化剂包括列于表4中的那些。在具体的实施方式中,R2为亚芳基或取代的亚芳基基团,且HFP基团在芳族环上占据彼此的间位。表4.在一种实施方式中,所述催化剂选自4-HFA-St、4-HFA-Tol、HFTB、NFTB、HPIP、3,5-HFA-MA、3,5-HFA-St、1,3-HFAB、1,4-HFAB、及其组合。还设想包含结合到载体的含有HFP的基团的催化剂。在一种实施方式中,所述载体包括聚合物、交联聚合物珠、无机颗粒、或金属颗粒。含有HFP的聚合物可通过已知的方法形成,所述方法包括直接聚合含有HFP的单体(例如,甲基丙烯酸酯单体3,5-HFA-MA或苯乙烯基单体3,5-HFA-St)。可经历直接聚合(或与共聚单体的聚合)的含有HFP的单体中的官能团包括丙烯酸酯、甲基丙烯酸酯、α,α,α-三氟甲基丙烯酸酯、α-卤代甲基丙烯酸酯、丙烯酰胺基、甲基丙烯酰胺基、降冰片烯、乙烯基、乙烯基醚、和本领域中已知的其它基团。连接基团的实例包括C1-C12烷基、C1-C12杂烷基、醚基团、硫醚基团、氨基基团、酯基团、酰胺基团、或其组合。还设想如下催化剂:其包含带电的含有HFP的基团,通过离子缔合结合到聚合物或载体表面上的带相反电荷的位点。ROP反应混合物包含至少一种有机催化剂,且当适当时包含在一起的几种有机催化剂。ROP催化剂以相对于环状羰基单体的1/20-1/40,000摩尔的比例、且优选地以相对于环状羰基单体的1/1,000-1/20,000摩尔的比例添加。ROP加速剂ROP聚合可在任选的加速剂、特别是氮碱的存在下进行。示例性的氮碱加速剂在下面列出且包括表5中显示的吡啶(Py)、N,N-二甲基氨基环己烷(Me2NCy)、4-N,N-二甲基氨基吡啶(DMAP)、反式1,2-二(二甲基氨基)环己烷(TMCHD)、1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)、1,5,7-三氮杂双环[4.4.0]十二碳-5-烯(TBD)、7-甲基-1,5,7-三氮杂双环[4.4.0]十二碳-5-烯(MTBD)、(-)-金雀花碱、(Sp)1,3-二(2-丙基)-4,5-二甲基咪唑-2-亚基(Im-1)、1,3-二(2,4,6-三甲基苯基)咪唑-2-亚基(Im-2)、1,3-二(2,6-二-异丙基苯基)咪唑-2-亚基(Im-3)、1,3-二(1-金刚烷基)咪唑-2-亚基(Im-4)、1,3-二-异丙基咪唑-2-亚基(Im-5)、1,3-二叔丁基咪唑-2-亚基(Im-6)、1,3-二(2,4,6-三甲基苯基)-4,5-二氢咪唑-2-亚基(Im-7)、1,3-二(2,6-二-异丙基苯基)-4,5-二氢咪唑-2-亚基、1,3-二(2,6-二-异丙基苯基)-4,5-二氢咪唑-2-亚基(Im-8)、或其组合。表5.在一个实施方式中,所述加速剂具有两个或三个各自能够作为路易斯碱参与的氮,如例如在结构(-)-金雀花碱中那样。较强的碱通常改善聚合速率。所述催化剂和所述加速剂可为相同的材料。例如,一些开环聚合可使用单独的1,8-二氮杂双环[5.4.0]十一碳-7-烯(DBU)在不存在另外的催化剂或加速剂的情况下进行。基于环状羰基单体的总摩尔数,所述催化剂优选以约0.2-20摩尔%、0.5-10摩尔%、1-5摩尔%、或1-2.5摩尔%的量存在。所述氮碱加速剂,当使用时,优选以基于环状羰基单体的总摩尔数的0.1-5.0摩尔%、0.1-2.5摩尔%、0.1-1.0摩尔%、或0.2-0.5摩尔%的量存在。如上所述,在一些情况下,取决于具体的环状羰基单体,所述催化剂和所述氮碱加速剂可为相同的化合物。基于环状羰基单体的总摩尔数,引发剂组优选以0.001-10.0摩尔%、0.1-2.5摩尔%、0.1-1.0摩尔%、或0.2-0.5摩尔%的量存在。在特别的实施方式中,基于环状碳酸酯单体的总摩尔数,所述催化剂以约0.2-20摩尔%的量存在,所述氮碱加速剂以0.1-5.0摩尔%的量存在,和所述引发剂的亲核性引发剂组以0.1-5.0摩尔%的量存在。所述催化剂可通过选择性沉积、或者在固体担载的催化剂的情况下通过过滤除去。基于所述阳离子聚合物和残余的催化剂的总重量,催化剂可以0wt%(重量百分数)-约20wt%、优选0wt%(重量百分数)-约0.5wt%的量存在。所述阳离子聚合物优选不包含残余的催化剂。平均分子量所述阳离子聚合物具有约1500-约50,000、更特别地约1500-约30,000的如通过尺寸排阻色谱法测定的数均分子量(Mn)。所述阳离子聚合物的前体聚合物和/或所述阳离子聚合物优选具有1.01-约1.5、更特别地1.01-1.30、和甚至更特别地1.01-1.25的多分散指数(PDI)。在一些情况下,所述阳离子聚合物可在去离子水中自组装成纳米粒状胶束。所述阳离子聚合物可具有约15mg/L-约45mg/L的临界胶束浓度(CMC)。所述胶束可具有约7mg/L-约500mg/L的对于微生物生长的最小抑菌浓度(MIC)。在一些情况下,MIC低于CMC,意味着抗微生物活性不依赖于所述阳离子聚合物的自组装。进一步公开处理微生物的方法,包括使微生物与所公开的阳离子聚合物接触,从而杀灭所述微生物。对于下面的实施例,下列定义是可适用的。HC50定义为引起50%的哺乳动物红细胞经历溶血的阳离子聚合物的浓度(以mg/L为单位)。500mg/L或更高的HC50值是合乎需要的。HC20定义为引起20%的哺乳动物红细胞经历溶血的阳离子聚合物的浓度(以mg/L为单位)。500mg/L或更高的HC20值是合乎需要的。最小抑菌浓度(MIC)定义为抑制给定微生物的生长达24小时的时间所需的阳离子聚合物的最小浓度(以mg/L为单位)。小于500mg/L的MIC是合乎需要的。甚至更合乎需要的是250mg/L或更小的MIC。较低的MIC表明较高的抗微生物活性。最小杀菌浓度(MBC)定义为杀灭给定的微生物所需的阳离子聚合物的最小浓度(以mg/L为单位)。较低的MBC表明较高的抗微生物活性。HC50选择性定义为HC50/MIC的比率。3或更大的HC50选择性是合乎需要的。较高的HC50选择性值表明较大的对于微生物细胞的活性和较小的对于哺乳动物细胞的毒性。同样,HC20选择性定义为HC20/MIC的比率。3或更大的HC20选择性是合乎需要的。在下面的实施例中使用的非限制性的微生物包括革兰氏阳性表皮葡萄球菌(S.epidermidis)、革兰氏阳性金黄色葡萄球菌(S.aureus)、革兰氏阴性大肠杆菌(E.coli)、革兰氏阴性铜绿假单胞菌(P.aeruginosa)、革兰氏阳性真菌白色念珠菌(C.albicans)、革兰氏阳性耐甲氧苯青霉素金黄色葡萄球菌(MRSA)、革兰氏阳性耐万古霉素肠球菌(VRE)、革兰氏阴性鲍曼不动杆菌(A.baumannii)、革兰氏阳性酵母新型隐球菌(C.neoformans)、和革兰氏阴性克雷白氏肺炎杆菌(K.pneumoniae)。总的来说,其中阳离子碳酸酯重复单元的侧链La-Q'(Ra)u'基团的大于75%含有8个碳或更少的碳的具有5-约45的DP的阳离子聚合物对于革兰氏阴性和/或革兰氏阳性菌和真菌是弱活性的。而且,在低的DP(<10)下,所述阳离子聚合物的HC50和/或HC20值通常降低到低于500mg/L,表明朝向杀生物性质的趋势。约10-约45的DP通常促进较高的HC50和/或HC20值(500mg/L或更高)。更下面的实施例还显示,当阳离子碳酸酯重复单元的侧链基团的至少25%含有13个或更多个碳且DP为约10-约30时,阳离子聚合物对于革兰氏阴性和革兰氏阳性菌和真菌两者都是高度活性的(MIC<500mg/L),且具有500mg/L或更高的HC50值。使用类固醇末端基团Z'获得增加的抑制功效和较低的红细胞毒性(较高的HC50值)。溶血选择性(HC50/MIC)也增加。可使用基团Z'、Z”、Zc和C'进一步调节抗微生物活性、溶血选择性,或提供第二功能(例如,细胞辨识能力、细胞膜渗透性的提升等等)。实施例还显示,当阳离子碳酸酯重复单元的25%-100%包含10-25个碳时,10摩尔%或更少的包含α-生育酚基(维生素E化合物)和/或麦角钙化醇基(ergocalciferyl)(维生素D2)侧链部分的碳酸酯重复单元在降低MIC(即,增加对微生物的毒性)和/或增加HC50值(降低对哺乳动物红细胞的毒性)方面也是有效的。在一些情况下,与所述阳离子聚合物一起温育的人成纤维细胞的细胞生存力超过75%。低的平均质量、高的抗微生物活性、和低的细胞毒性使得这些阳离子聚合物对于包括如下的一系列医学和家庭用途是非常有吸引力的:创伤处理、感染的处理、抗生素药物、以及用于家庭和医院表面和医学仪器的消毒剂。在一个实施方式中,用于杀灭微生物的医药组合物包含所公开的阳离子聚合物的一种或多种。所述医药组合物可为溶液、粉末、丸剂、糊剂、或软膏剂的形式。所述医药组合物可包含水,其中所述阳离子聚合物的浓度低于所述阳离子聚合物的临界胶束浓度。所述医药组合物可局部地施用和/或注射。下列实施例展示阳离子聚合物的制备和性质。实施例在下列实施例中使用的材料列于表6中。表6.在这里,Mn为数均分子量,Mw为重均分子量,且MW为一个分子的分子量。除非具体提及,否则所有的材料购自Sigma-Aldrich、TCI或Merck。所有溶剂为分析级的,购自FisherScientific或J.T.Baker且如所收到地使用。在转移到手套箱中之前,单体和其它试剂(例如,引发剂、单体等)通过在高真空下冻干而彻底地干燥。N-二(3,5-三氟甲基)苯基-N'-环己基硫脲(TU)如由R.C.Pratt、B.G.G.Lohmeijer、D.A.Long、P.N.P.Lundberg、A.Dove,H.Li、C.G.Wade、R.M.Waymouth和J.L.Hedrick在Macromolecules,2006,39(23),7863-7871中报道地制备,并通过在CaH2上干燥的THF中搅拌而干燥,过滤,且在真空下除去溶剂。将1,8-二氮杂双环[5,4,0]十一碳-7-烯(DBU)在CaH2上搅拌并真空蒸馏,之后转移到手套箱中。临界胶束浓度(CMC)测量通过使用芘作为探针的荧光光谱法估算阳离子聚合物的各临界胶束浓度(CMC)。在含有10%体积/体积水的MHBII中以多种浓度(0.25-2000mg/L)制备一系列含有0.616微摩尔芘的聚合物溶液。在一整夜的温育之后,使用分光荧光计(HitachiF-2500)以390nm的发射波长和1nm的带宽在室温下从325到360nm记录所述溶液的激发光谱。绘制I339对I335的强度比率作为聚合物浓度的函数。CMC值取自曲线在拐点处的切线与在低浓度下的点的水平切线的交点。I.单体合成MTC-OH(MW160.1)的制备MTC-OH可通过R.C.Pratt,etal.,ChemicalCommunications,2008,114-116的方法制备。MTC-C6H5(MW326.2)的制备向100mL圆底烧瓶装入bis-MPA(5.00g,37mmol,MW134.1)、碳酸二-(五氟苯基)酯(PFC,31.00g,78mmol,MW394.1)、和CsF(2.5g,16.4mmol),用70mL四氢呋喃(THF)冲洗。最初,反应是非均相的,但在一小时之后,形成澄清的均相溶液,容许其搅拌20小时。在真空中除去溶剂且将残余物再溶解于二氯甲烷中。容许所述溶液静置大约10分钟,在该时间五氟苯酚副产物沉淀且可被定量地收取。该五氟苯酚副产物显示出在五氟苯酚的19FNMR中的3个特征峰和在GCMS中的单峰,且质量为184。将滤液用碳酸氢钠、水萃取并且用MgSO4干燥。将溶剂在真空中蒸发并将产物重结晶(乙酸乙酯/己烷混合物)以给出作为白色结晶粉末的MTC-C6F5。GCMS具有单峰且质量为326g/mol。C12H7F5O5的计算的分子量与所指认的结构一致。1H-NMR(400MHz,在CDCl3中):δ4.85(d,J=10.8Hz,2H,CHaHb),4.85(d,J=10.8Hz,2H,CHaHb),1.55(s,3H,CCH3)。MTC-BnCl(MW298.7)的制备向烧瓶装入MTC-C6F5(10g,30.6mmol)、对-氯甲基苯甲醇(4.8g,30.6mmol)、PROTONSPONGE(2g,9.3mmol)和THF(30mL)。将反应混合物搅拌12小时,然后直接添加到硅胶柱。使用二乙醚作为洗脱液对产物进行分离以给出7.45g(81%)白色结晶粉末。1HNMR(400MHz,CDCl3,22℃):δ7.40(dd,4H,C6H4),5.24(s,2H,-OCH2C6H4),4.73(d,2H,-CH2OCOO),4.60(s,2H,-CH2Cl),4.22(d,2H,-CH2OCOO),1.35(s,3H,-CH3)。MTC-PrCl(MW236.65)的制备使用标准程序以草酰氯将MTCOH(8.82g,55mmol)转化成MTCOCl。在装备有搅拌棒的干燥250mL圆底烧瓶中,将所形成的中间体溶解于150mL干燥二氯甲烷中。在氮气流下,安装滴液漏斗,将3-氯丙醇(4.94g,4.36mL,52.25mmol)、吡啶(3.95g,4.04mL,55mmol)、和干燥二氯甲烷(50mL)合并到所述滴液漏斗。使用冰浴将烧瓶冷却至0℃并在30分钟的时间期间逐滴添加顶部溶液。将所形成的溶液在移除冰浴之前搅拌额外的30分钟并将所述溶液在氮气下搅拌额外的16小时。将粗产物MTC-PrCl直接施加到硅胶柱上并通过用100%的二氯甲烷进行洗脱而对产物进行分离。取走产物级分并将溶剂蒸发,给出作为灰白色油的产物,其在静置时结晶。产率11g(85%)。1H-NMR(CDCl3)δ:4.63(d,2H,CH2),4.32(t,2H,CH2),4.16(d,2H,CH2),3.55(t,2H,CH2),2.09(m,2H,CH2),1.25(s,3H,CH3)。5-甲基-5-(3-溴丙基)氧羰基-1,3-二氧六环-2-酮(MTC-PrBr)(MW281.10)的制备使用3-溴-1-丙醇作为醇以45mmol的规模通过用于MTCOPrCl的程序制备MTCOPrBr。产物通过柱层析法纯化,且随后重结晶以给出白色晶体(6.3g,49%)。1HNMR(400MHz,CDCl3):δ4.69(d,2H;CH2OCOO),4.37(t,2H;OCH2),4.21(d,2H;CH2OCOO),3.45(t,2H;CH2Br),2.23(m,2H;CH2),1.33(s,3H;CH3)。13CNMR(100MHz,CDCl3):δ171.0,147.3,72.9,63.9,40.2,31.0,28.9,17.3。MTC-C6Cl(MW278.09)的制备向烧瓶装入MTC-C6F5(6.6g,20.1mmol)、6-氯-1-己醇(2.5g,18.3mmol)、PROTONSPONGE(3.9g,18.3mmol)和四氢呋喃(THF)(8mL)。将反应混合物搅拌12h并添加过量的乙酸铵。将反应混合物搅拌额外的3小时,然后直接添加到硅胶柱。使用己烷/乙酸乙酯作为洗脱液对产物进行分离以给出油(4.2g,57%)。1HNMR(400MHz,CDCl3,22℃):δ4.72(d,2H,-CH2OCOO),4.23(d,t4H,-CH2OCOO,-OCH2CH2),3.57(t,2H,-OCH2CH2CH2CH2CH2CH2Cl),1.84(m,2H,-OCH2CH2CH2CH2CH2CH2Cl),1.76(m,2H,-OCH2CH2CH2CH2CH2CH2Cl),1.45(m,2H,-OCH2CH2CH2CH2CH2CH2Cl),1.39(m,2H,-OCH2CH2CH2CH2CH2CH2Cl),1.35(s,3H,-CH3)。MTC-C8Cl(MW306.12)的制备向烧瓶装入MTC-C6F5(6.6g,20.1mmol)、6-氯-1-辛醇(2.5g,18.3mmol)、PROTONSPONGE(3.9g,18.3mmol)和THF(8mL)。将反应混合物搅拌12小时并添加过量的乙酸铵。将反应混合物搅拌额外的3小时,然后直接添加到硅胶柱。使用己烷/乙酸乙酯作为洗脱液对产物进行分离以给出油(4.2g,57%)。1HNMR(400MHz,CDCl3,22℃):δ4.72(d,2H,-CH2OCOO),4.23(d,t4H,-CH2OCOO,-OCH2CH2),3.57(t,2H,-OCH2CH2(CH2)3CH2CH2CH2Cl),1.84(m,2H,-OCH2CH2(CH2)3CH2CH2CH2Cl),1.76(m,2H,-OCH2CH2(CH2)3CH2CH2CH2Cl),1.45(m,2H,-OCH2CH2(CH2)3CH2CH2CH2Cl),1.35(br,9H,-CH3,OCH2CH2(CH2)3CH2CH2CH2Cl)。Chol-MTC的制备所述制备包括三个步骤:1)胆甾醇氯甲酸酯Chol-Cl与2-溴乙基胺氢溴酸盐在二氯甲烷和三乙胺(TEA)中反应以形成氨基甲酸酯Chol-Br;2)Chol-Br与酸二醇bis-MPA在二甲基甲酰胺(DMF)/KOH中进行碱催化的反应以形成二醇酯Chol-MPA,和3)对Chol-MPa进行三光气介导的环化以形成环状碳酸酯单体Chol-MTC,其中总产率为约26%。三个步骤各自的详细程序提供在下面。使用1H和13CNMR确认中间体和环状碳酸酯单体的结构。1)Chol-Br的制备.在装备有磁力搅拌棒的500mL圆底烧瓶中,将胆固醇氯甲酸酯(25.0g,55.7mmol,1.0当量)和2-溴乙基胺氢溴酸盐(12.9g,63.0mmol,1.1当量)悬浮于二氯甲烷(200mL)中并使悬浮液在冰浴中急冷。向该悬浮液,在1小时期间逐滴添加三乙胺(TEA)(18.0mL,13.06g,129.1mmol,2.3当量)在二氯甲烷(100mL)中的溶液。将反应混合物保持在该冰浴中额外的一小时并容许其温热至室温。然后容许反应进行另外的14h,此后在真空下除去二氯甲烷并将所得固体悬浮于乙酸乙酯和己烷的1:1混合物(300mL)中。将有机层用饱和盐水(100mL)和去离子水(50mL)的混合物洗涤2次,并用饱和盐水(100mL)洗涤1次。将有机层在硫酸钠上干燥并在真空下除去溶剂以给出浅黄色固体(29.1g,97.4%)。由于通过1HNMR测定粗产物具有令人满意的纯度,不进行进一步的纯化。1HNMR(400MHz,CDCl3,δ,ppm):5.38(胆固醇中的CH=C),5.03(侧链的NHCOO),4.50(胆固醇的CH-OCONH),3.58(BrCH2CH2NH),2.45-0.6(来自胆固醇的其余质子)。2)Chol-MPA的合成.在具有磁力搅拌棒的500mL圆底烧瓶中,将KOH(85%,2.0g,30.3mmol,1.1当量)、bis-MPA(4.20g,31.3mmol,1.1当量)和二甲基甲酰胺(DMF)(200mL)的混合物加热至100℃1.5小时。形成均相溶液,且将Chol-Br(15.0g,28.0mmol,1.0当量)添加到所述热的溶液。在加热的情况下继续搅拌16小时且在降低的压力下除去大部分的DMF,以得到油状的半固体,然后将其溶解于2:1乙酸乙酯:己烷混合物(300mL)中。将有机溶液用饱和盐水(100mL)和去离子水(100mL)混合物洗涤。将所得含水层用乙酸乙酯萃取(3×100mL)以收取在洗涤过程期间损失的Chol-MPA。将合并的有机层用饱和盐水(80mL)和去离子水(20mL)混合物洗涤。将合并的有机层用Na2SO4干燥并且在真空中除去溶剂以得到作为苍白色蜡状固体的粗产物(16.5g)。通过使用二氧化硅作为装填材料且使用己烷到乙酸乙酯的梯度作为洗脱液的快速柱层析法对粗产物进行纯化以产生作为蜡状白色固体的最终的产物Chol-MPA(10.7g,64.8%)。1HNMR(400MHz,CDCl3,δ,ppm):5.35(胆固醇中的CH=C和侧链的NHCOO),4.47(胆固醇的CH-OCONH),4.26(CH2CH2NHCOO),3.88和3.72(CH2OH)3.45(CH2CH2NHCOO),3.34(OH),2.50-0.60(来自胆固醇的其余质子和来自bis-MPA的CH3)。3)Chol-MTC的制备.在具有磁力搅拌棒的500mL圆底烧瓶中,将Chol-MPA(10.1g,17.1mmol,1.0当量)溶解于无水二氯甲烷(150mL)中。添加吡啶(8.2mL,8.0g,101.5mmol,5.9当量)并将溶液在干冰-丙酮浴(-78℃)中冷却。向该经冷却的反应混合物,在1小时期间逐滴添加三光气(2.69g,9.06mmol,基于三光气的官能当量的1.9当量)溶液(溶解于50mL二氯甲烷中)。在1小时之后,容许反应混合物从-78℃温热至室温,且在2小时之后,通过添加饱和氯化铵水溶液(50mL)使反应猝灭。将有机层用如下洗涤两次:1.0NHCl(20mL)和饱和盐水(80mL)的混合物,随后是饱和盐水(50mL)和饱和NaHCO3(50mL)的混合物,使用Na2SO4干燥。在真空中除去溶剂产生作为稍带黄色的固体的粗产物。将粗产物通过使用二氧化硅作为装填材料且使用氯仿到氯仿:乙酸乙酯(4:1)混合物的梯度作为洗脱液的快速柱层析法进一步纯化,以产生作为蜡状白色固体的最终的产物Chol-MTC(6.8g,65%)。1HNMR(400MHz,CDCl3,δ,ppm):5.35(胆固醇中的CH=C),4.95(NHCOO),4.86和4.27(CH2OCOOCH2),4.47(胆固醇的CH-OCONH),4.27(CH2CH2NHCOO),3.45(CH2CH2NHCOO),2.40-0.60(来自胆固醇的其余质子和环状碳酸酯单体中的CH3)。MTC-VitD2的制备将MTC-OH(3.08g,19.3mmol)溶解在具有几滴DMF的无水THF(50mL)中。然后逐滴添加草酰氯(3.3mL,39.4mmol)且将反应混合物在氮气流下搅拌1小时,之后在真空下除去挥发物。将所得灰白色固体加热至65℃2-3分钟以除去任何残余的试剂和溶剂,留下酰氯中间体MTC-Cl。将该固体再溶解于干燥二氯甲烷(50mL)中并使用冰浴使其急冷至0℃。随后在30分钟期间逐滴添加麦角钙化醇(维生素D2)(7.65g,19.3mmol)和干燥三乙胺(3mL,21.6mmol)在干燥二氯甲烷(50mL)中的溶液。容许混合物温热至环境温度并搅拌额外的18小时。在除去溶剂之后获得粗固体,并通过使用硅胶的柱层析法对其进行纯化。最初使用二氯甲烷作为洗脱液,之后逐渐增加极性到最后以5%乙酸乙酯结束。将所得固体用MeOH洗涤以获得高的纯度的作为白色固体的期望的产物(5.20g,50%)。1HNMR(400MHz,CDCl3):δ6.20(d,1H,J=11.2Hz,VitD2-C=CH2),6.01(d,1H,J=11.2Hz,VitD2-C=CH2),5.21(t,2H,J=6.0Hz,VitD2-C=CH),5.08(重叠的峰,宽的s,2H,VitD2-C=CH,CH(O-MTC)),4.86(s,1H,VitD2-C=CH),4.66(d,2H,J=12.4Hz,MTC-CH2),4.17(d,2H,J=12.8Hz,MTC-CH2),1.20-2.90(重叠的峰,24H,VitD2),1.02(d,3H,J=6.4Hz,VitD2-CH3),0.91(d,3H,J=6.8Hz,VitD2-CH3),0.84(t,6H,J=6.4Hz,VitD2-CH3),0.55(s,3H,MTC-CH3)。MTC-VitE单体的制备将MTC-OH(3.08g,19.3mmol)溶解于具有几滴DMF的无水THF(50mL)中。然后逐滴添加草酰氯(3.3mL,39.4mmol)并将反应混合物在氮气流下搅拌1h,之后在真空下除去挥发物。将所得灰白色固体加热至65℃2-3分钟以除去任何残余的试剂和溶剂,留下酰氯中间体MTC-Cl。将该固体再溶解于干燥二氯甲烷(50mL)中并使用冰浴使其急冷至0℃。随后在30分钟期间逐滴添加α-生育酚(8.30g,19.3mmol)和干燥三乙胺(3mL,21.6mmol)在干燥二氯甲烷(50mL)中的溶液。容许混合物温热至环境温度并搅拌额外的18小时。在除去溶剂之后获得粗固体,并通过使用硅胶的柱层析法对其进行纯化。最初使用己烷作为洗脱液,之后逐渐增加极性到最后以50%乙酸乙酯结束。使用二氯甲烷/乙酸乙酯(4:1)实施第二次层析法分离以获得高的纯度的作为白色固体的期望的产物(6.05g,53%)。1HNMR(400MHz,CDCl3):δ4.92(d,2H,J=10.8Hz,MTC-CH2),4.34(d,2H,J=10.8Hz,MTC-CH2),2.59(d,2H,J=6.7Hz,四氢吡喃基-CH2),2.09(s,3H,Ar-CH3),2.00(s,3H,Ar-CH3),1.96(s,3H,Ar-CH3),1.70-1.90(m,2H),1.00-1.60(重叠的峰,27H),0.80-0.90(m,12H,在疏水性尾部上的4×CH3)。II.引发剂合成Bn-MPA二醇引发剂的制备将2,2-二(羟甲基)丙酸(Bis-MPA)、KOH、DMF、和苄基溴(BnBr)在一起在100℃下加热15小时从而以62%的产率形成苄基酯Bn-MPA。Chol-OMes中间体(MW464.7)的制备将胆固醇(10g,25.8mmol,MW386.35)溶解于干燥氯仿(CHCl3)(15mL)和吡啶(15mL)中。然后将反应混合物用氮气吹扫且快速地搅拌。然后逐滴添加甲磺酰氯(3mL,38.8mmol)。将反应混合物在环境温度下搅拌4小时,随后沉淀到MeOH(600mL)中。经由真空过滤收集滤液以给出9.6g(80%)白色粉末。Chol-OPrOH(MW444.7)的制备将Chol-OMes(1g,2.15mmol)悬浮于1,4-二氧六环(10mL)和1,3-丙二醇(4g,53.8mmol)中。将反应混合物脱气,用氮气吹扫并加热至110℃。在1小时之后,容许反应混合物冷却至环境温度并沉淀到MeOH/H2O(4:1)中。使用柱层析法对产物进行进一步纯化产生0.72g(75%)蜡状灰白色材料。Chol-OTEG-OH(MW518.8)的制备将Chol-OMes(1g,2.15mmol)悬浮于1,4-二氧六环(10mL)和二缩三乙二醇(8g,53.8mmol)中。将反应混合物脱气,用氮气吹扫并加热至110℃。在1小时之后,容许反应混合物冷却至环境温度并沉淀到MeOH/H2O(4:1)中。使用柱层析法对产物进行进一步纯化产生0.92g(83%)蜡状浅棕色材料。III.开环聚合具有含有胆甾醇基的末端基团的阳离子聚合物的制备在随后的反应图示中,使用缩写Z1和Z2表示阳离子聚合物的下列类固醇残基:带星号的键表示与阳离子聚合物主链的连接点。Z1和Z2残基也是用于形成阳离子聚合物的引发剂的残基。实施例10的制备是代表性的。该阳离子聚合物根据方案1中的反应顺序制备。方案1.第1部分.在惰性手套箱中,向小瓶装入Chol-OPr-OH(0.179g,0.4mmol)、TU(0.04g,0.1mmol)、MTC-BnCl(0.6g,2mmol)、二氯甲烷(DCM)(3g)和搅拌棒。搅拌反应混合物且聚合通过添加DBU(20微升,0.15mmol)而开始。在15分钟之后,添加过量的乙酰氯以使反应猝灭和将IP-1末端乙酰化以形成IP-2。将乙酰化的中间体聚合物IP-2沉淀到异丙醇中给出0.73g(94%)白色蜡状聚合物。使用1HNMR(CDCl3)和GPC(THF,37℃)对所述聚合物进行表征。通过碳酸酯双重峰(2H,-OCOOCH2-,4.7ppm)的消失以及包括新形成的线型碳酸酯亚甲基(-CH2OCOOCH2-)和苄基酯两者的宽的多重峰(6H,4.2ppm)的相应出现证实完全的聚合。通过GPC证实分子量且发现分子量为2.6kDa,其中PDI为1.2。通过采用胆甾醇基甲基位移积分(3H,0.87ppm)相对于苄基氯信号(2H,5.0ppm)之比计算平均聚合度(DP),其与GPC值良好地相符。第2部分.用三甲胺(TMA)将IP-2季化以形成CP-1。向小瓶装入乙酰化的中间体聚合物IP-2(0.3g,0.15mmol)、乙腈(4mL)和搅拌棒。然后将反应混合物置于干冰/丙酮浴(-78℃)中且使过量的TMA气体鼓泡通过被搅拌的溶液。然后将小瓶密封并容许其在搅拌下温热至环境温度。在4小时之后,添加二乙醚(5mL)以使产物聚合物沉淀。然后将反应小瓶离心10分钟并将上清液倾析。将产物用过量的二乙醚洗涤并在高的真空下干燥以给出0.32g(94%)半透明蜡状材料。使用1HNMR证实季化。可归于季化的TMA的特征化学位移(9H,3.2ppm)出现且可相对于苄基铵信号(2H,5.0ppm)进行积分,证实完全的转化。用三甲基膦(TMP)将IP-2季化以形成实施例11是代表性的。向Schlenk管装入IP-2(0.3g,0.15mmol)、乙腈(4mL)和搅拌棒。然后将反应混合物经由3X冷冻/抽吸/解冻循环排气。使用不透气的注射器添加TMP(0.6mL)并将溶液在环境温度下搅拌。在4小时之后,将所述Schlenk管放置在真空罩(housevacuum)下以除去过量的TMP,随后添加醚(5mL)。收集沉淀物,将其用过量的醚洗涤并在高的真空下干燥以给出0.34g(95%)。使用1HNMR证实季化。可归于季化的TMP的特征化学位移(9H,3.3ppm)出现且可相对于苄基铵信号(2H,5.1ppm)进行积分,证实完全的转化。实施例1-27.使用作为用于ROP的类固醇引发剂的胆固醇(Chol-OH)、Chol-OPr-OH或Chol-OTEG-OH,作为环状碳酸酯单体的MTC-BnCl或MTC-PrCl,以及作为季化剂的TMA或TMP根据以上总的聚合和季化程序制备阳离子聚合物。表7列出使用基于胆甾醇基的引发剂制备的阳离子均聚物、它们通过1HNMR测量的聚合度(DP)n'、临界胶束浓度(CMC)、和阳离子重复单元的阳离子侧链的总碳。表7.B.用4-甲基苯甲醇引发剂制备的阳离子聚合物实施例28-41.使用作为引发剂的4-甲基苯甲醇(4-MeBnOH),作为环状碳酸酯单体的MTC-BnCl、MTC-PrCl或MTC-PrBr,以及多种胺季化剂根据以上总的聚合和季化程序制备阳离子聚合物。表8列出使用4-MeBnOH引发剂制备的阳离子均聚物、它们的聚合度(DP)、季化剂、CMC、和各阳离子重复单元的碳的总数。表8.a“无”意指聚碳酸酯链的末端羟基基团未被保护。bN.D.意指未测定。c实际的,如通过1HNMR分析测定的C.用具有侧链α-生育酚基部分的MTC-VitE制备的阳离子无规共聚物实施例42-50.使用用于阳离子碳酸酯重复单元的MTC-PrBr和MTC-BnCl前体、作为疏水性共聚单体的MTC-VitE、苯甲醇(BnOH)引发剂、和作为催化剂的DBU/硫脲制备无规阳离子共聚物。用三甲胺或N-取代的咪唑进行季化。反应顺序示于方案2中。方案2.实施例50是代表性的。在手套箱中的含有磁力搅拌棒的20mL小瓶中,将MTC-BnCl(608.8mg,2.04mmol,30当量)、MTC-VitE(40.0mg,68微摩尔,1.0当量)和TU(25.2mg,68微摩尔,1.0当量)溶解于二氯甲烷(3mL)中。向该溶液,添加BnOH(7.0微升,68微摩尔,1.0当量)且随后添加DBU(10.2微升,68微摩尔,1.0当量)以引发聚合。容许反应混合物在室温下搅拌20分钟并通过添加过量(~20mg)的苯甲酸而使反应混合物猝灭。然后将该混合物沉淀到冰冷的甲醇(50mL)中并在-5℃下离心30分钟。将所得半透明的油在真空下干燥直至获得泡沫似的白色固体。实施中间体的GPC分析并且聚合物在没有进一步纯化的情况下使用。随后将聚合物溶解于乙腈中,转移到可用特氟龙塞子密封的管中且使其急冷至0℃。添加三甲胺以开始季化过程。将反应混合物在密封的管中在室温下搅拌18小时。在反应过程期间观察到油状材料的沉淀。将混合物在真空下抽空至干燥并冷冻干燥以最后给出白色的脆的泡沫似的固体。通过1HNMR表征最终的聚合物以确定最终的组成和纯度。表9列出用MTC-VitE和BnOH引发剂制备的阳离子无规共聚物、它们的聚合度(DP)、季化剂、CMC、和各阳离子重复单元的碳的总数。表9.a“无”意指聚碳酸酯链的末端羟基基团未被保护。bN.D.意指未测定。c实际的,如通过1HNMR分析测定的表10列出使用MTC-VitE制备的阳离子无规共聚物的分析性质表10.a对预季化的聚合物进行GPCC.用具有侧链麦角钙化醇基部分(维生素D2)的MTC-VitD2制备的阳离子聚合物实施例52-54.实施例54是代表性的。在手套箱中的含有磁力搅拌棒的20mL小瓶中,将MTC-BnCl(500.0mg,1.67mmol,3.0当量)、MTC-VitD2(30.0mg,56微摩尔,1.0当量)和TU(20.6mg,56微摩尔,1.0当量)溶解于二氯甲烷(3mL)中。向该溶液,添加BnOH(5.8微升,56微摩尔,1.0当量)且随后添加DBU(8.3微升,56微摩尔,1.0当量)以引发聚合。容许反应混合物在室温下搅拌20分钟且通过添加过量(~30mg)的苯甲酸而使反应混合物猝灭。然后使混合物沉淀到冰冷的甲醇(50mL)中并在-5℃下离心30分钟。将所得的半透明的油在真空下干燥直至获得泡沫似的白色固体。实施中间体聚合物的GPC分析并且所述聚合物在没有进一步纯化的情况下使用。随后将所述聚合物溶解于乙腈中,转移到可用特氟龙塞子密封的管且使其急冷至0℃。添加三甲胺以开始季化过程。将反应混合物在该密封的管中在室温下搅拌18小时。在反应期间观察到油状材料的沉淀。将混合物在真空下抽空至干燥并冷冻干燥以最后给出白色的脆的泡沫似的固体。通过1HNMR表征最终的聚合物以确定最终组成和纯度。表11列出使用MTC-VitD2制备的阳离子无规共聚物、它们的聚合度(DP)、季化剂、CMC和各阳离子重复单元的碳的总数表11.a“无”意指聚碳酸酯链的末端羟基基团未被保护。bN.D.意指未测定。c实际的,如通过1HNMR分析测定的表12列出使用MTC-VitD2制备的阳离子无规共聚物的分析性质表12.a对预季化的聚合物进行GPC用二醇引发剂Bn-MPA制备的阳离子聚合物实施例55-63.使用Bn-MPA二醇引发剂制备一系列阳离子聚合物。实施例60的制备是代表性的。将MTCOPrCl(501mg,2.1mmol)、Bn-MPA(4.7mg,0.02mmol,引发剂)、和TU(37.2mg,0.1mmol)溶解于二氯甲烷(1mL)中,并将该溶液转移到含有DBU(15.2mg,0.1mmol)的小瓶以在室温下开始聚合([M]0/[I]0=100)。在2小时之后,将乙酸酐(72.4mg,0.71mmol)添加到混合物中并搅拌所述混合物48小时(转化~95%)。然后将溶液沉淀到冷的甲醇中两次并将沉淀物离心且在真空中干燥。产率:466mg(93%),GPC(THF):Mn12200g/mol,PDI1.17,1HNMR(400MHz,CDCl3):δ7.39-7.29(m,5H;Ph),5.16(s,2H;PhCH2),4.38-4.19(br,~350H;CH2OCOO,OCH2聚合物),3.64-3.55(m,~117H;CH2Cl聚合物),2.15-2.07(m,~114H;CH2聚合物),2.06(s,6H;OCH3乙酰基末端),1.27(br,~169H;CH3聚合物)。将初始聚合物添加到小瓶并溶解于MeCN中。然后将小瓶冷却至-78℃并添加TMA气体。然后将小瓶加热至50℃且容许其搅拌过夜或者直至反应完成。然后将反应混合物沉淀到二乙醚中。将聚合物再溶解和沉淀到二乙醚中。可用乙酰氯代替乙酸酐。表13列出使用Bn-MPA单体制备的阳离子共聚物、聚合度(DP)、季化剂、CMC和各阳离子重复单元的碳的总数。表13.a“无”意指聚碳酸酯链的末端羟基基团未被保护。bN.D.意指未观察到。c实际的,如通过1HNMR分析测定的;n'为两个聚碳酸酯链中的所有重复单元之和。IV.生物学测量最小抑菌浓度(MIC)测量。使表皮葡萄球菌(S.epidermidis)(ATCC编号12228)、金黄色葡萄球菌(S.aureus)(ATCC编号29737)、大肠杆菌(E.coli)(ATCC编号25922)、铜绿假单胞菌(P.aeruginosa)(ATCC编号9027)、和白色念珠菌(C.albicans,真菌)(ATCC编号10231)、耐甲氧苯青霉素金黄色葡萄球菌(MRSA)(临床分离的,由中国浙江大学的范伟民(WeiminFan)提供)、耐万古霉素肠球菌(VRE)(临床分离的,由中国浙江大学的范伟民提供)、鲍曼不动杆菌(A.baumannii)(临床分离的,由中国浙江大学的范伟民提供)、新型隐球菌(C.neoformans)(临床分离的,由中国浙江大学的范伟民提供)、和克雷白氏肺炎杆菌(K.pneumoniae)(临床分离的,由中国浙江大学的范伟民提供)从冻干的形式复原。将细菌样品在MuellerHintonII肉汤(MHBII)中在37℃下在300rpm的恒定摇动下进行培育。使用如先前报道的肉汤微量稀释方法测量聚合物的MIC。将100微升的含有多种浓度的聚合物的MHBII或胰蛋白酶大豆肉汤(TSB)置于96孔组织培养板的各孔中。将等体积的细菌悬浮液(3×105CFU/ml)(其中CFU意指菌落形成单位)添加到各孔中。在混合之前,首先将细菌样品接种过夜以进入其对数生长期。调节细菌溶液的浓度以在微孔板读数器(microplatereader)(TECAN,瑞士)上在600nm波长处给出大约0.07的初始光学密度(O.D.)读数,这对应于McFarland1溶液的浓度(3×108CFU/ml)。将细菌溶液进一步稀释1000倍以实现3×105CFU/ml的初始加样量。将96孔板在培育箱中在37℃下在300rpm的恒定摇动下保持18小时。MIC被取作在18小时温育结束时用肉眼和微孔板读数器(TECAN,瑞士)未观察到微生物生长的抗微生物聚合物的浓度。使用仅含有微生物细胞的肉汤作为阴性对照,且各测试以6次重复的实验实施。在下列表中,较低的MIC和较高的HC50(或HC20)值是合乎需要的。粗体的实施例表明在各系列中的对于微生物的一种或多种的最高的活性(最低的MIC值)以及对于红细胞的最低的毒性(高的HC50值)。标记为“总的阳离子侧链碳”的列为阳离子重复单元的带有季氮或季磷基团的阳离子侧链的碳的数量。表14列出胆甾醇基引发的阳离子聚合物(实施例1-27)对于S.epidermidis、S.aureus、E.coli、P.aeruginosa和C.albicans(真菌)的MIC(mg/L)和HC50(mg/L)值。表15列出4-甲基苯甲醇引发的阳离子聚合物(实施例28-41)对于S.epidermidis、S.aureus、E.coli、P.aeruginosa和C.albicans(真菌)的MIC和HC50值。表16为表14的(实施例28-41)的测试的继续,对于耐甲氧苯青霉素金黄色葡萄球菌(MRSA)、耐万古霉素肠球菌(VRE)、鲍曼不动杆菌(A.baumannii)、新型隐球菌(C.neoformans)和克雷白氏肺炎杆菌(K.pneumoniae)进行测试。表17列出用MTC-VitE共聚单体(具有α-生育酚基侧链部分的疏水性单体)制备的无规阳离子共聚物(实施例42-51)对于S.aureus、E.coli、P.aeruginosa、和C.albicans(真菌)的MIC和HC20值。表17还列出用MTC-VitD2共聚单体(具有维生素D2侧链部分的疏水性单体)制备的无规阳离子共聚物(实施例52-54)对于S.aureus和E.coli的MIC和HC20值。表18列出二醇引发的阳离子聚合物(实施例55-63)对于S.epidermidis、S.aureus、E.coli、P.aeruginosa和C.albicans(真菌)的MIC和HC50值。较低的MIC(500mg/L或更小)和较高的HC50或HC20(500mg/L或更大)代表优选的性能。HC20是比HC50更灵敏的红细胞毒性的度量。即,如果HC20值为1000,则HC50值将甚至更高。3或更大的HC选择性(HC50/MIC或HC20/MIC)值也是优选的。关于表14的含有胆甾醇基的“全阳离子”聚合物,其它特征相同时,用TMP季化剂形成的那些通常是比用TMA形成的阳离子聚合物更具活性的(例如,将实施例20与实施例21进行比较,和将实施例12与实施例13进行比较)。其它特征相同时,对于用环状碳酸酯单体MTC-BnCl形成的阳离子聚合物也观察到与用MTC-PrCl形成的阳离子聚合物相比更高的活性(例如,将实施例8与实施例10进行比较,和将实施例9与实施例11进行比较)。20-30的聚合度(DP)通常比5-10的DP有利。P.aeruginosa通常是耐受性的,但是对于具有胆甾醇基末端基团的具有20或30的DP的阳离子聚合物(实施例4-7,其用胆固醇引发)良好地响应。含有胆甾醇基的末端基团对抗微生物活性的积极影响通过将实施例4和6(表14)与实施例28和40(表15)以及实施例42和43(表17)进行比较而进一步证明。实施例28和40具有4-甲基苄氧基末端基团(由4-MeBnOH引发剂形成),且实施例42和43具有苄氧基末端基团(由BnOH引发剂形成)。表15的实施例显示,具有较小的末端基团(即,具有小于15个碳的末端基团)的阳离子聚合物的通常较弱的抗微生物活性可使用体积较大的Q'取代基(Ra基团)进行补偿。在这种情况下,Q'为氮。实施例37是代表性的。实施例37为用4-MeBnOH引发且用1:1摩尔比率的二甲基丁基胺(6个碳)和二甲基苄基胺(9个碳)的混合物季化的MTC-BnCl的均聚物。其它特征相同时,实施例37具有可与含有胆甾醇基的聚合物相比或者比其更好的高的活性和高的HC50(将实施例37与表14的实施例24进行比较)。实施例37的HC50选择性(HC50/MIC)也是优异的,从对于P.aeruginosa的>8到对于S.aureus的>128)。二甲基丁基胺/二甲基苄基胺混合物产生分别具有总共15和18个碳的阳离子碳酸酯重复单元。实施例37对于MRSA、VRE、A.baumannii、C.neoformans和K.pneumoniae也是高度活性的(表16)。较小的末端基团也可使用疏水性共聚单体和任选的大体积的季化剂(例如,其中季铵基团的Ra基团具有超过3个碳的总和的季化剂)进行补偿。这可通过将表17中的实施例42(MTC-PrCBr,DP30,无疏水性共聚单体)与实施例45、47和48(MTC-PrBr加约3摩尔%-约5摩尔%的MTC-VitE,DP30)进行比较而看出。对于MTC-BnCl在具有和不具有MTC-VitE或MTC-VitD的情况下显示出类似的趋势(将实施例43与实施例51和54进行比较)。α-生育酚的分子式为C29H50O2,且麦角钙化醇的分子式为C28H44O,表明疏水性共聚单体、特别是包含结合形式的包含20或更多个碳的生物活性/相容的材料的那些,可以小的量使用以控制抗微生物活性和/或红细胞毒性。含有胆甾醇基的聚合物的杀灭效率与MIC测试类似,将100微升的含有多种浓度(0、MIC和2.0MIC)的聚合物的MHBII置于96孔组织培养板的各孔中。将等体积的细菌悬浮液(3×105CFU/ml)(其中CFU意指菌落形成单位)添加到各孔中。在混合之前,首先将细菌样品接种过夜以进入其对数生长期。调节细菌溶液的浓度以在微孔板读数器(TECAN,瑞士)上在600nm波长处给出大约0.07的初始光学密度(O.D.)读数,这对应于McFarland1溶液的浓度(3×108CFU/ml)。将细菌溶液进一步稀释1000倍以实现3×105CFU/ml的初始加样量。将96孔板在培育箱中在37℃下在300rpm的恒定摇动下保持18小时。然后对各样品进行一系列十倍稀释并将其涂敷到溶原性肉汤(LB)琼脂平板上。然后将所述平板温育过夜并对菌落形成单位进行计数。使用以含有10%体积/体积水的肉汤处理的微生物的样品作为对照。图1A和1B为分别显示作为实施例13和实施例23(表14)的浓度的函数的S.aureusas的菌落形成单位/mL之间的关系的图。在两种情况下,在31mg/L的阳离子聚合物浓度下CFU计数都为零。含有胆甾醇基的聚合物的溶血活性测试用磷酸盐缓冲的盐水(PBS)对新鲜的兔血细胞或大鼠血细胞进行25×稀释以获得大约4%体积/体积悬浮液以用于该实验中。将红细胞悬浮液(300微升)添加到含有等体积(300微升)的在PBS中的聚合物溶液(具有范围3.9-500mg/L的最终聚合物浓度)的各管。然后将所述管在37℃下温育1小时,之后将它们以1000×g离心5分钟。将上清液的等分试样(100微升)转移到96孔板的各孔并使用微孔板读数器(TECAN,瑞士)在576nm处分析血红蛋白释放。使用与PBS一起温育的红细胞悬浮液作为阴性对照。使用以0.1%体积/体积TritonX-100溶解的红细胞的吸光度作为阳性对照且认为其是100%溶血的。使用下式计算溶血百分数:溶血(%)=[(经处理的样品的O.D.576nm-阴性对照的O.D.576nm)/(阳性对照的O.D.576nm-阴性对照的O.D.576nm)]×100。数据作为4次重复实验的平均值±标准偏差表示。图2A-2C为显示作为含有胆固醇的阳离子聚合物实施例10、11、20、21(图2A)、实施例8、9、18、19(图2B)、以及实施例12、13、22、23(图2C)的浓度(mg/L)的函数的兔红细胞的溶血%的图。较小的溶血%是优选的。具有DP5的阳离子聚合物的溶血%(图2A和2B)在3.9mg/L-62.5mg/L的浓度下小于25%。将在62.4mg/L下的图2A的实施例10、11、20和21进行比较,对于在引发剂残基中具有-OTEG-O-基团的阳离子聚合物观察到与在引发剂残基中具有-OPr-O-基团的阳离子聚合物相比更少的溶血。将图2A和2B与图2C进行比较,对于具有DP10的阳离子聚合物也观察到与具有DP5的阳离子聚合物相比更低的溶血%。对于DP10的阳离子聚合物,观察到小于约15%的溶血一直到约125mg/L的浓度(图2C)。在实施例12、13、22和23中将季化剂从TMA改变为TMP(图2C)未显著地改变阳离子聚合物的溶血活性。含有胆甾醇基的聚合物的细胞毒性测试将人皮肤成纤维(HDF)细胞保持在补加有10%胎牛血清(FBS)、丙酮酸钠、100U/mL青霉素和100mg/mL链霉素的DMEM生长培养基中并在37℃下在5%CO2和95%增湿的空气的气氛下培养。使用标准MTT试验方案研究聚合物的细胞毒性。将HDF细胞以1.5×104个细胞/孔的密度接种到96孔板上并容许其附着过夜。将聚合物首先溶解于高压液相色谱(HPLC)级水中并使用Dulbecco的改良伊格尔培养基(DMEM)生长培养基连续稀释以实现范围3.9-500mg/L的聚合物浓度,其中对于各条件,水浓度固定在10%体积/体积。将100微升的聚合物溶液添加到各孔中的细胞并容许所述板在37℃下温育18小时。随后,将100微升的生长培养基和10微升的MTT溶液(在PBS中5mg/ml)添加到各孔并根据制造商的指令将细胞在37℃下温育4小时。将在各孔中形成的所得甲晶体在除去生长培养基时使用150微升的二甲亚砜(DMSO)溶解并使用微孔板分光光度计在550nm和690nm的波长下测定吸光度。相对细胞生存力表示为[(A550-A690)样品/(A550-A690)对照]×100%。数据表示为每个聚合物浓度3-4次重复实验的平均值±标准偏差。图3A-3F为显示作为含有胆固醇的阳离子聚合物浓度的函数的HDF细胞的细胞生存力百分数的图。在给定的浓度下较高的细胞生存力百分数值是合乎需要的。将该系列中的各条曲线进行比较,可看出,通过使用TMA相对于使用TMP促进了细胞生存力(将图3A的实施例10与实施例11进行比较,将图3B中的实施例20与实施例21进行比较,和将图3D中的实施例18与实施例19进行比较)。通过使用Chol-OTEG-OH相对于使用Chol-OPr-OH也促进了较高的细胞生存力百分数。这可通过将实施例10(图3A)与实施例20(图3B)进行比较、和将实施例8(图3C)与实施例18(图3D)进行比较而看出。DP10相对于DP5也促进了较高的细胞生存力百分数。这可通过将实施例10(图3A)与实施例12(图3E)进行比较、和将实施例11(图3A)与实施例13(图3E)进行比较而看出。实施例20(图3B)和实施例18(图3D)在最宽的浓度范围内具有最高的细胞生存力(大于80%的生存力一直到分别约125mg/L和150mg/L。α-生育酚和麦角钙化醇(维生素D2)官能化的聚合物的抗微生物和溶血研究将包含维生素E部分(用MTC-VitE制备的)的阳离子聚合物如以上所显示地在溶液中对于多种细菌菌株进行测试。表17总结了抗微生物、选择性和溶血结果。总的来说,α-生育酚基部分的引入增加对于大部分细菌的抑制效率。对于用MTC-MTC-PrBr制备且用三甲胺(TMA)季化的阳离子共聚物,在添加MTC-VitE的情况下,对于S.aureus和E.coli的MIC值降低(将实施例42与实施例44-46进行比较)。如通过MIC/HC20值度量的实施例45对于S.aureus相对于大鼠红细胞(RBC)的选择性大于16(>1000/63)。当将季化剂从三甲胺变成甲基咪唑(实施例47)或乙基咪唑(实施例48)时,对于E.coli的MIC值(从1000,对于实施例42)降低至63mg/L。尽管与实施例47相比实施例48具有更高的对于哺乳动物RBC的溶血毒性,但是它在其治疗浓度下未引起显著的溶血。所有MTC-VitE聚合物均显示出对于C.albicans的显著活性,尤其是用甲基咪唑季化的实施例47。对于用MTC/VitE/MTC-BnCl制备的阳离子聚合物(实施例49-51)而言,对于S.aureus和E.coli的效力更显著。实施例49-51对于S.aureus的MIC为31mg/L,而对照聚合物(实施例43,无MTC-VitE)对于S.aureus具有125mg/L的MIC。在这种情况下,聚合度(DP)表面上不引起在细菌抑制方面的显著差异。然而,对于E-coli,实施例51(1:30的MTC-VitE/MTC-BnCl比率,MIC=31mg/L)比实施例49(1:10的MTC-VitE/MTC-BnCl比率,MIC=63mg/L)有效。与不具有维生素E部分的对照样品(实施例42)相比,对于用MTC-PrBr制备的含有维生素E的阳离子聚合物(实施例44-48)而言,对于真菌C.albicans的活性增加。然而,与不具有维生素E部分的对照样品(实施例43)相比,对于用MTC-BnCl制备的含有维生素E的阳离子聚合物(实施例49-51)而言,对于真菌C.albicans的活性降低。这可能是由于含有维生素E的聚合物在酵母肉汤中的有限的溶解性。否则,所述聚合物是对于S.aureus和E.coli的强力的抑制剂。所述聚合物的大部分还显示出良好的选择性。对于S.aureus和E.coli,HC20/MIC值在约4-约30范围内。(用MTC-BnCl制备的)含有维生素E的阳离子聚合物实施例49-51的溶血活性显示于图4(柱状图)中。利用使用大鼠RBC的溶血试验来研究在溶液中的这些阳离子抗微生物聚合物的毒性。毒性是低的,所有聚合物都具有大于500ppm的HC50值。因此,在表17中提供更相关的HC20值。如在表17中看出的,(用TMA季化的)用MTC-PrBr制备的阳离子聚合物显示出对于大鼠RBC可忽略的溶血毒性,而用MTC-BnCl制备的阳离子聚合物显示出更大的溶血。在两个系列的聚合物中,疏水性单体含量的增加通常引起溶血的增加。即,实施例44的溶血%>实施例45的溶血%>实施例46的溶血%(图中未示出),且实施例49的溶血%>实施例50的溶血%>实施例51的溶血%(图4)。在由MTC-PrBr制备且用咪唑季化的聚合物(实施例47和48,图中未示出)中也看到该趋势。(用甲基咪唑季化的)实施例47与其乙基类似物实施例48(图中未示出)相比毒性较低。该观察结果与其中增加的毒性与较高比例的疏水性有关的先前发现是一致的。含有悬垂的维生素D2部分的实施例52-54的溶血活性示于图5(柱状图)中。这些聚合物也是非溶血性的(HC20值为1000mg/L或更大)。维生素E官能化的聚合物的时间-杀灭研究用实施例51(1:30的MTC-VitE/MTC-BnCl比率)处理S.aureus和E.coli以研究抗微生物性质的机理。使用S.aureus和E.coli进行菌落计数试验。如可在图6A和图6B的柱状图中看到的,在18小时的处理之后,在MIC浓度下实现细菌菌株各自约100%的杀灭效率,这支持了杀菌机理。还进行时间-杀灭动力学实验以确认所述机理。将S.aureus和E.coli用磷酸盐缓冲盐水(PBS)或实施例51在MIC或2.0MIC浓度下进行处理。在18小时期间的不同的时间点处对活的菌落进行计数。如图7A和图7B的图中所示,在用实施例51在MIC浓度下处理18小时之后,活的S.aureus和E.coli菌落是很少的。在致死聚合物浓度(2.0MIC)下,对于S.aureus在6小时之后且对于E.coli在4小时之后未观察到活的菌落。这些结果表明,所述阳离子聚合物有效地杀灭细菌而不是抑制它们的生长。二醇引发的(BnMPA)阳离子聚合物的抗微生物和溶血活性关于使用双亲核性引发剂BnMPA形成的聚合物(表18),基于更加疏水性的MTC-C8Cl的阳离子聚合物(实施例55、57和58)总的来说呈现出更大的抗微生物活性但是更大的红细胞毒性(较低的HC50值)。基于较小疏水性的MTC-PrCl的阳离子聚合物(实施例56)具有较低的抗微生物活性和较低的溶血活性(较高的HC50值)。将使用MTC-C8Cl与MTC-PrCl的混合物制备的阳离子聚合物(实施例59-61)稀释导致与MTC-C8Cl均聚物(实施例57,表18)相比可比较的抗微生物活性和更高的HC50值甚至一直到75摩尔%MTC-PrCl。实施例59-61还呈现出相对于MTC-C8Cl均聚物较低的溶血活性(图8,曲线图)和较低的细胞毒性(图9,曲线图)。而且,对于S.epidermidis、S.aureus和E.coli,实施例59-61的MIC值低于CMC(表13)。该观察结果表明,CMC对于抗微生物活性不是必需的。平衡电荷和疏水性的该方法导致具有高的抗微生物活性和最小的哺乳动物细胞毒性的阳离子聚合物。抗微生物性质的机理通过使用共焦显微镜法和场发射扫描电子显微镜法(FE-SEM)进一步研究阳离子聚合物微生物毒性的机理。用阳离子聚合物实施例51(MTC-VitE/MTC-BnCl(1:30),用TMA季化)在FITC标记的100K葡聚糖的存在下对S.aureus和E.coli进行短期(0分钟、10分钟和20分钟)处理,然后在干燥之后通过使用共焦显微镜法进行观察。如图10的照片中所示,在不存在实施例51的情况下,在细菌细胞中未观察到绿色荧光。然而,在用所述阳离子聚合物处理10分钟之后,清楚地看到在S.aureus和E.coli细胞两者中的异硫氰酸荧光素标记的(FITC标记的)葡聚糖分子的吸收,表明在细菌膜中的孔形成。在20分钟的温育时,在S.aureus和E.coli细胞中FITC标记的葡聚糖的吸收更明显,这表明在与阳离子聚合物的延长的膜相互作用之后更严重的膜损坏。在用阳离子聚合物处理更长的时间尺度(2小时)之后,通过FE-SEM观察到细菌细胞的形态变化。如可在图11的扫描电子显微镜(SEM)图像中看到的,当与阴性PBS对照相比时,用致死浓度(100mg/L)的实施例51处理2小时导致对于S.aureus(图11左侧,a1和a2)和E.coli(图11中间,b1和b2)的显著的膜损坏。并且对于C.albicans(图11右侧,c1和c2)在用500mg/L实施例47(MTC-VitE/MTC-PrBr(1:30),用甲基咪唑季化)处理之后也观察到类似的现象。这些结果表明,阳离子聚合物与细菌和酵母细胞的膜通过形成孔进行相互作用且最终导致细菌和酵母膜的破坏。二醇引发的阳离子聚合物(Bn-MPA)与单醇(monol)引发的阳离子聚合物(BnOH和4-MeBnOH)的比较通过将在下面再现于表19中的实施例43(单醇引发剂BnOH,表17)以及实施例62和63(二醇引发剂Bn-MPA,表18)的性质进行比较可看出二醇引发剂对单醇引发剂、以及封端对用MTC-BnCl制备的阳离子聚合物的影响。分别由MTC-PrBr和MTC-PrCl制备的实施例42和56也再现于表19中。表19.a胰蛋白酶大豆肉汤。bDP基于进料。将实施例43和62进行比较,聚合物的其它特征相同时,与单醇(BnOH)引发的阳离子聚合物实施例43相比,二醇(Bn-MPA)引发的阳离子聚合物62对于S.aureus和E.coli更具活性。两种聚合物对于P.aeruginosa都不是有效的。这两种聚合物对于C.albicans是同等有效的。各聚合物对于红细胞是非毒性的。将仅在封端基团方面不同的阳离子聚合物(实施例62和63)进行比较,封端的聚合物实施例63不及未封端的聚合物实施例62对于S.aureus和E.coli有活性。两种聚合物对于P.aeruginosa都不是有效的。两种聚合物对于C.albicans是同等有效的。各聚合物对于红细胞是非毒性的。使用MTC-PrCl/Br制备的阳离子聚合物(实施例42和56)各自对于S.aureus、E.coli、P.aeruginosa和C.albicans是弱活性的或无活性的(对于各微生物的MIC为500mg/L或更大)且各阳离子聚合物对于红细胞是非毒性的(HC>1000mg/L)。在单醇和二醇引发的阳离子聚合物之间观察到另一关于RBC毒性对聚合度(DP)的依赖性的差异。使用MTC-C8Cl制备的二醇引发的阳离子聚合物呈现出随着DP的降低而增加的HC50值(降低的RBC毒性)。这可通过将表18的实施例55(HC50250-500,DP15)、实施例57(HC50250,DP30)、和实施例58(HC50125-250,DP60)进行比较而看出。这些二醇引发的聚合物的抗微生物活性未看起来对于DP是敏感的。通过比较,单醇引发的阳离子聚合物通常呈现出随着DP从5增加到30而增加的HC50值(较低的RBC毒性)。这可通过将表14的实施例10、12、14和16、以及表14的实施例20、22、24和26进行比较而看出。这些结果表明,引发剂片段的位置和类型对于阳离子聚合物的抗微生物和/或选择性性质具有影响,潜在地容许享有相同数量和类型的阳离子碳酸酯重复单元的单醇引发的和二醇引发的阳离子聚合物具有有用地截然不同的和有益的抗微生物性质。在本文中使用的术语仅为了描述具体实施方式的目的且不意图为对本发明的限制。如在本文中使用的,单数形式“一个(种)(a,an)”和“所述(该)”也意图包括复数形式,除非上下文清楚地另外指明。将进一步理解,术语“包含”和/或“包括”当用在本说明书中时,表明存在所陈述的特征、整体、步骤、操作、元件、和/或组分,但不排除存在或添加一种或多种另外的特征、整体、步骤、操作、元件、组分、和/或其集合。当一个范围被用于表示使用两个数值界限X和Y(例如,Xppm-Yppm的浓度)的可能的值时,除非另外说明,否则所述值可为X、Y、或在X与Y之间的任何数。已经为了说明和描述的目的提供了本发明的描述,但是其不意图为穷举性的或限于所公开的形式的发明。在不背离本发明的范围和精神的情况下,许多修饰和变型对于本领域普通技术人员来说将是明晰的。选择和描述实施方式以最好地说明本发明的原理和它们的实际应用,且使本领域的其他普通技术人员能够理解本发明。
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1