一种盐酸普萘洛尔药物组合物的制作方法
本发明属于医药及医药生产技术领域,具体涉及一种盐酸普萘洛尔片及其制备方法。
背景技术:
盐酸普萘洛尔是一种β型肾上腺素受体阻滞剂,能减慢心率,降低心肌收缩力,从而减少心排血量,延迟房室传导时间、降低心肌氧耗量、提高运动耐量和降低血压,用于治疗各种心律失常,心绞痛,对部分高血压患者有中度降压作用。分子式为C16H21NO2·HCl,化学名为1-异丙氨基-3-(1-萘氧基)-2-丙醇盐酸盐,其化学结构式如下:
本发明所解决的技术问题是提供一种盐酸普萘洛尔片及其制备方法,能避免盐酸普萘洛尔在湿润状态下发生氧化反应,提高盐酸普萘洛尔的生物利用度,保证临床用药的安全性。
技术实现要素:
本发明的目的在于提供一种盐酸普萘洛尔片及其制备方法,该制剂稳定性好,生物利用度高。
本发明所述一种盐酸普萘洛尔药物组合物,其特征在于,该药物组合物重量百分比计为:盐酸普萘洛尔10-30%,淀粉10-40%,糊精20-70%,酒石酸0-1%,硬脂酸镁0-2%。
进一步地,该药物组合物重量百分比计为:盐酸普萘洛尔10-20%,淀粉15-40%,糊精40-60%,酒石酸0-0.5%,硬脂酸镁0.5-1.5%。
进一步地,该药物组合物重量百分比计为:盐酸普萘洛尔13%,淀粉38%,糊精48%,酒石酸0.2%,硬脂酸镁0.8%。
本发明所述一种盐酸普萘洛尔药物组合物,该药物组合物制备方法包括如下步骤:
1)将处方量1/5-1/4淀粉制成10%的淀粉浆;
2)将余量淀粉与盐酸普萘洛尔、糊精混合均匀;
3)混合料置于搅拌机中,干搅5—10分钟,将酒石酸溶于蒸馏水中过滤,滤液与10%的淀粉浆混合成粘合剂,加入搅拌机中搅拌15—20分钟,制成软材,用16-20目尼龙筛制粒,于50—60℃温度通风干燥;
4)干粒用16-20目尼龙筛整粒,加入硬脂酸镁,混匀,用5.5mm浅凹冲模压片、包装。
本发明所述一种盐酸普萘洛尔药物组合物,该药物组合物制备方法干粒水分应控制在2.0%以下。
本发明的有益效果为:
本发明的一种盐酸普萘洛尔片的制备方法,加入酒石酸作为稳定剂,能避免盐酸普萘洛尔在湿润状态下发生氧化反应,可以起到保护作用,提高了片剂是生物利用度,从而保证临床用药的安全性和有效性。
附图说明:
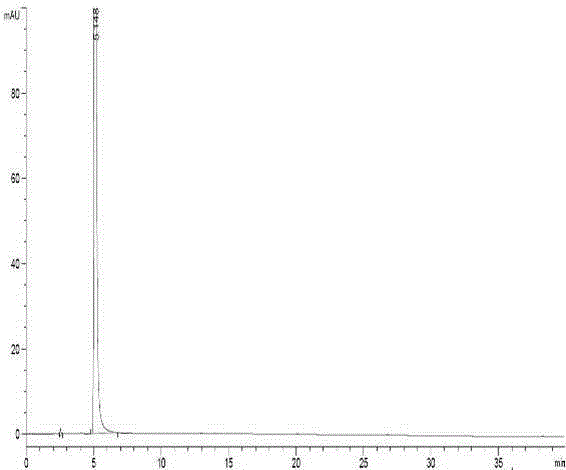
图1:盐酸普萘洛尔片辅料检查结果;
图2:盐酸普萘洛尔片 (加酒石酸)检查结果;
图3:普通盐酸普萘洛尔片 (未加酒石酸)检查结果。
具体实施方式
为了使本发明实现的技术手段、创作特征、达成目的与功效易于明白了解,下面结合具体实施例,进一步阐述本发明,但下述实施例仅仅为本发明的优选实施例,并非全部。基于实施方式中的实施例,本领域技术人员在没有做出创造性劳动的前提下所获得其他实施例,都属于本专利的保护范围。
实施例1
一、药品处方制成1000片:
主药:盐酸普萘洛尔 13g
辅料:淀粉 38g
糊精 48g
酒石酸 0.2g
硬脂酸镁 0.8g
二、制法:
1、将淀粉3—3.5g制成10%的淀粉浆。
2、将余量淀粉与盐酸普萘洛尔、糊精混合均匀。
3、混合料置于搅拌机中,干搅5—10分钟,将酒石酸溶于蒸馏水中过滤,滤液与10%的淀粉浆混合成粘合剂,加入搅拌机中搅拌15—20分钟,制成软材,用16目尼龙筛制粒,颗粒要求完整。于50—60℃温度通风干燥,干粒水分应控制在2.0%以下。
3、干粒用18目尼龙筛整粒,加入硬脂酸镁,混匀,计算片重。取样送检。
4、用5.5mm浅凹冲模压片。
5、包装。
实施例2
一、药品处方制成1000片:
主药:盐酸普萘洛尔 10g
辅料:淀粉 27g
糊精 38g
酒石酸 0.1g
硬脂酸镁 0.8g
二、制法:
1、将淀粉3—3.5g制成10%的淀粉浆。
2、将余量淀粉与盐酸普萘洛尔、糊精混合均匀。
3、混合料置于搅拌机中,干搅5—10分钟,将酒石酸溶于蒸馏水中过滤,滤液与10%的淀粉浆混合成粘合剂,加入搅拌机中搅拌15—20分钟,制成软材,用16目尼龙筛制粒,颗粒要求完整。于50—60℃温度通风干燥,干粒水分应控制在2.0%以下。
3、干粒用18目尼龙筛整粒,加入硬脂酸镁,混匀,计算片重。取样送检。
4、用5.5mm浅凹冲模压片。
5、包装。
实施例3
一、药品处方制成1000片:
主药:盐酸普萘洛尔 15g
辅料:淀粉 35g
糊精 23g
酒石酸 0.15g
硬脂酸镁 0.7g
二、制法:
1、将淀粉3—3.5g制成10%的淀粉浆。
2、将余量淀粉与盐酸普萘洛尔、糊精混合均匀。
3、混合料置于搅拌机中,干搅5—10分钟,将酒石酸溶于蒸馏水中过滤,滤液与10%的淀粉浆混合成粘合剂,加入搅拌机中搅拌15—20分钟,制成软材,用16目尼龙筛制粒,颗粒要求完整。于50—60℃温度通风干燥,干粒水分应控制在2.0%以下。
3、干粒用18目尼龙筛整粒,加入硬脂酸镁,混匀,计算片重。取样送检。
4、用5.5mm浅凹冲模压片。
5、包装。
实施例4
对比实施例1、2、3加速0月、1月、2月、3月、6月有关物质检查结果,结果见下表。
结果表明加酒石酸的各个盐酸普萘洛尔片处方有关物质均符合规定。
实施例5
将上述实施例1制得的盐酸普萘洛尔片(加酒石酸)与普通盐酸普萘洛尔片 (未加酒石酸)进行有关物质检查质量研究对比试验:
1.取本品盐酸普萘洛尔片 (加酒石酸)和普通盐酸普萘洛尔片 (未加酒石酸),分别照中国药典2010年版二部盐酸普萘洛尔质量标准有关物质检查项下方法检验。
2.盐酸普萘洛尔片辅料检查结果见图1;盐酸普萘洛尔片 (加酒石酸)检查结果见图2;普通盐酸普萘洛尔片 (未加酒石酸)检查结果见图3。
3.结果判断
根据中国药典2010年版二部盐酸普萘洛尔质量标准判断,供试品溶液的色谱图中如有杂质峰,单个杂质峰面积不得大于对照溶液主峰面积的0.5倍(0.1%),各杂质峰面积的和不得大于对照溶液主峰面积的2倍(0.4%)。结果表明,没加酒石酸的盐酸普萘洛尔片有关物质比加酒石酸的盐酸普萘洛尔片多,所以加酒石酸的盐酸普萘洛尔片 稳定性好,生物利用度更高,疗效更好。
以上显示和描述了本发明的基本原理、主要特征和本发明的优点。本行业的技术人员应该了解,本发明不受上述实施例的限制,上述实施例和说明书中描述的仅为本发明的优选例,并不用来限制本发明,在不调理本发明精神和范围的前提下,本发明还会有各种变化和改进,这些变化和改进都落入要求保护的本发明范围内。本发明要求保护范围由所付的权利要求书及其等效物界定。
- 还没有人留言评论。精彩留言会获得点赞!