一种干细胞制剂及其制备方法和应用与流程
本发明涉及生物治疗领域,特别涉及一种干细胞制剂及其制备方法和应用。
背景技术:
间充质干细胞是多能干细胞的一种,具有多向分化的潜能,在体外诱导的条件下可以分化为肌肉、神经、骨、软骨、脂肪、心肌和类肝组织等多种组织和细胞。在长期传代后仍然具有增殖复制能力,是一种理想的组织器官工程的种子细胞。目前在临床上也有越来越多的人使用间充质干细胞应用于组织器官的修复和免疫系统调节。
现有技术采用静脉注射培养的间充质干细胞来治疗急性肝损伤,现有技术的缺点是,单靠间充质干细胞治疗肝损伤效果较差,因为不同患者对间充质干细胞的反应会有显著差异,加上间充质干细胞是经过培养的细胞,很容易被机体清除掉。因此,研究一种对肝损伤具有良好疗效的间充质干细胞治疗方法或制剂是本领域技术人员需要解决的技术问题。
技术实现要素:
有鉴于此,本发明公开了一种干细胞制剂及其制备方法和应用,所述干细胞制剂对肝损伤有良好的疗效。
本发明公开了一种干细胞制剂,包括:间充质干细胞、白蛋白、人参皂苷和溶剂。
在本发明的一些具体实施方案中,所述间充质干细胞的含量为3×105~5×106/ml。优选地,所述间充质干细胞的含量为1×106个/ml。
在本发明的一些具体实施方案中,所述白蛋白的含量为1%~10%(w/v)。优选地,所述白蛋白的含量为3%。
在本发明的一些具体实施方案中,所述人参皂苷的含量为20ng/ml~120ng/ml。优选地,所述人参皂苷的含量为60ng/ml。
优选地,所述溶剂为生理盐水。
本发明还公开了所述干细胞制剂的制备方法,包括以下步骤:
a)、间充质干细胞、白蛋白、人参皂苷和溶剂混合,得到干细胞制剂。
优选地,所述间充质干细胞按照以下步骤获得:
b1)、将骨髓进行离心分离,得到原代间充质干细胞;
b2)、重悬所述原代间充质干细胞,进行培养;
b3)、换液除去未贴壁细胞,加入培养基继续对所述原代间充质干细胞进行培养,所述培养基包括灵芝三萜类化合物;
b4)、对培养的细胞进行消化,得到间充质干细胞。
本发明还公开了所述干细胞制剂或所述制备方法制得的干细胞制剂在制备治疗肝损伤药物中的应用。
本发明通过在间充质干细胞培养时加入灵芝三萜类化合物,并在干细胞制剂中加入人参皂苷,可以显著抑制患者体内的免疫反应,并且增强间充质干细胞的修复能力,提高治疗效果。
综上所述,本发明公开了一种干细胞制剂及其制备方法和应用,该干细胞制剂可以抑制患者体内的免疫反应,使间充质干细胞免受患者体内免疫系统的攻击,增加细胞在体内的生存时间,而且对肝损伤具有良好的疗效。
附图说明
图1示1周后实验组、对照组和对比例组的血清学检测结果;
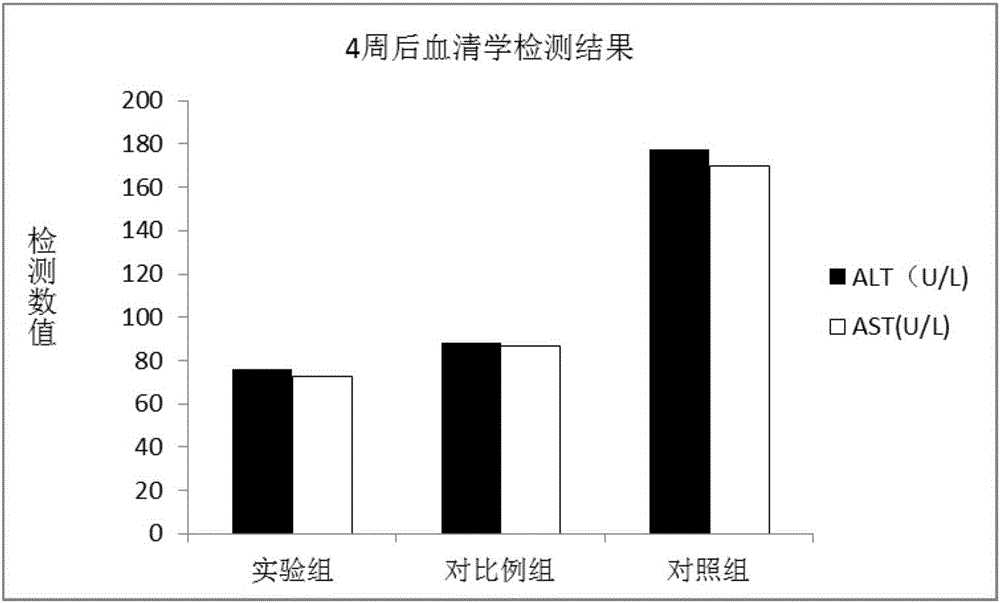
图2示4周后实验组、对照组和对比例组的血清学检测结果;
图3示8周后实验组、对照组和对比例组的血清学检测结果。
具体实施方式
本发明公开了一种干细胞制剂及其制备方法和应用,该干细胞制剂能抑制患者体内的免疫反应,对肝损伤具有良好的疗效。本领域技术人员可以借鉴本文内容,适当改进工艺参数实现。特别需要指出的是,所有类似的替换和改动对本领域技术人员来说是显而易见的,它们都被视为包括在本发明。本发明的方法及应用已经通过较佳实施例进行了描述,相关人员明显能在不脱离本发明内容、精神和范围内对本文所述的方法和应用进行改动或适当变更与组合,来实现和应用本发明技术。
本发明中所涉及原料均可由市场购得。其中,白蛋白购买自郑州莱士,人参皂苷购买自上海阿拉丁生化科技股份有限公司,灵芝三萜类化合物购买自大连美仑生物技术有限公司。
下面结合实施例,进一步阐述本发明。
实施例1间充质干细胞的分离培养和干细胞制剂的制备
1、取无菌条件下抽取的小鼠骨髓10ml,加入等体积的DMEM-LG培养基稀释混匀后,1000r/min离心5min,去除上层的脂肪及上清;
2、用含10%FBS和1×双抗的DMEM-F12培养基重悬细胞,并调整细胞密度为5×105/ml接种到15cm培养皿中,转移至5%CO2、37℃、饱和湿度为95%的CO2培养箱中培养;
3、培养48h后换液除去未贴壁杂细胞,同时培养基中加入50ng/ml的灵芝三萜类化合物,此后每隔2~3d换液1次,同样加入50ng/ml的灵芝三萜类化合物;
4、待细胞数达到1×108个后弃去培养基,生理盐水清洗3次,加入8ml0.25%(质量体积比)的胰酶(购买自gibco公司)消化细胞;
5、待细胞变圆松动后,加入两倍于胰酶体积的含10%FBS的DMEM-LG培养基终止消化;
6、倒出细胞悬液,离心弃去上清,生理盐水清洗2遍,得到用于制备干细胞制剂的间充质干细胞(CD90>95%,CD105>95%,CD74>95%,CD34<2%,CD45<2%,HLADR<2%)。
7、用含有3%白蛋白和60ng/ml人参皂苷的生理盐水重悬制得的间充质干细胞,使细胞密度为1×106个/ml,制成干细胞制剂注射液。
对比例间充质干细胞的分离培养和干细胞制剂的制备
1、取无菌条件下抽取的小鼠骨髓10ml,加入DMEM-LG培养基等倍稀释混匀后,1000r/min离心5min,去除上层的脂肪及上清;
2、用含10%FBS和1×双抗的DMEM-F12培养基重悬细胞,并调整细胞密度为5×105/ml接种到15cm培养皿,转移至5%CO2、37℃、饱和湿度为95%的CO2培养箱中培养。
3、培养48h后换液除去未贴壁杂细胞,此后每隔2~3d换液1次;
4、待细胞数达到1×108cell后弃去培养基,生理盐水清洗3次,加入8ml胰酶消化细胞;
5、待细胞变圆松动后,加入两倍于胰酶体积的含10%FBS的DMEM-LG培养基终止消化。
6、倒出细胞悬液,离心弃去上清,生理盐水清洗2遍,得到用于制备干细胞制剂的间充质干细胞;
7、用含有3%人血白蛋白的生理盐水重悬间充质干细胞,使细胞密度为1×106个/ml,制成注射液。
实施例3动物试验
将购买自广东省医学动物实验中心的急性肝损伤模型的12只昆明小鼠分为三组,组1为试验组,注射实施例1制备的干细胞制剂;组2为对照组,注射与试验组等量的生理盐水;组3为对比例组,注射对比例制备的干细胞制剂。注射方式均为尾静脉注射,每天一次,注射体积为3ml,连续注射3天。
于1周、4周、8周后检测相应数据。
在治疗后1周、4周、8周每组各随机选取2只小鼠,抽血通过Elisa试剂盒检测AST、ALT指标(试剂盒购买自南京金益柏生物科技有限公司)。
1周后血清学检测结果见表1、图1;4周后血清学检测结果见表2、图2;8周后血清学检测结果见表3、图3。
表1
ALT和AST是检测肝功能的两项指标,数值的正常范围在0-40之间,在肝功能受损的情况下数值会升高,并且数值越高,表明肝功能受损越严重。从数据中可以得出实验组的肝功能水平要好于对照组合对比例组,而对比例组又要好于对照组,具有显著差异(P<0.05)。
表2
从数据中可以得出实验组的肝功能水平要好于对照组合对比例组,而对比例组又要好于对照组,具有显著差异(P<0.05)。
表3
从数据中可以得出实验组的肝功能水平要好于对照组合对比例组,而对比例组又要好于对照组,具有显著差异(P<0.05)。
以上所述仅是本发明的优选实施方式,应当指出,对于本技术领域的普通技术人员来说,在不脱离本发明原理的前提下,还可以做出若干改进和润饰,这些改进和润饰也应视为本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!