一种拉莫三嗪干混悬剂及其制备方法与流程
本发明具体涉及一种拉莫三嗪干混悬剂及其制备方法,属于药品制剂领域。
背景技术:
拉莫三嗪药品在美国的商品名是Lamictal,是葛兰素史克公司的产品。主要治疗儿童和成人的癫痫疾病。
目前,美国食品和药品管理局批准了三种不同剂型的Lamictal上市,分别为普通片、咀嚼片和口腔崩解片。市场上没有拉莫三嗪液体制剂,因此医院在使用时往往需要粉碎拉莫三嗪片剂来配置液体试剂,方便儿童患者和吞咽困难的患者服用。
拉莫三嗪难溶于水,当把粉碎后的拉莫三嗪片剂加入水中时,药物会快速沉降并且不易散开,这样就可能影响到给药剂量的准确性。
中国专利CN201510288845.X和CN201510350210.8公开了拉莫三嗪口服溶剂的处方和制备方法,但该制剂浓度较低(小于2mg/ml),无法满足临床需求;如需高浓度的处方,则需要加入有机溶剂,不利于儿童服用。
另外液体制剂也不理想,申请人在制备拉莫三嗪液体混悬剂(10mg/ml)时,储存过程中会有方形晶体生成,生成的晶体很难分开,出现了溶液浑浊的情况,影响到给药剂量的准确性。另外申请人在进行拉莫三嗪液体混悬剂加速试验检测时,拉莫三嗪液体混悬剂在两年有效期内会产生超出限度的杂质。
因此目前拉莫三嗪制剂,存在患者给药剂量不易准确,且液体混悬剂的物理和化学性质稳定性不好等问题。
技术实现要素:
为了解决上述技术难题,本发明提供了一种拉莫三嗪干混悬剂,所述拉莫三嗪干混悬剂由药用活性成分和药用级辅料组成,所述药用活性成分为拉莫三嗪30-200重量份;所述药用级辅料由10-1000重量份的填充剂、10-100重量份的助悬剂、10-100重量份的缓冲剂、5-50重量份的甜味剂、1-20重量份的风味剂和1-10重量份的助流剂组成。
优选地,本发明进一步提供了一种拉莫三嗪干混悬剂,所述拉莫三嗪干混悬剂由药用活性成分和药用级辅料组成,所述药用活性成分为拉莫三嗪50-150重量份,所述药用级辅料由50-800重量份的填充剂、10-50重量份的助悬剂、10-50重量份的缓冲剂、5-20重量份的甜味剂、1-10重量份的风味剂和1-8重量份的助流剂组成。
更优选地,本发明进一步提供了一种拉莫三嗪干混悬剂,所述拉莫三嗪干混悬剂由药用活性成分和药用级辅料组成,所述药用活性成分为拉莫三嗪100重量份,所述药用级辅料由100-600重量份的填充剂、15-40重量份的助悬剂、10-30重量份的缓冲剂、5-10重量份的甜味剂、1-6重量份的风味剂和1-5重量份的助流剂组成。
其中拉莫三嗪为无水拉莫三嗪,粒径D90优选5μm-150μm。更优选10μm-120μm,最优选30μm-90μm,所述D90指的是颗粒直径小于所述粒径的颗粒占90%。
D90的选择,申请人在筛选试验过程中发现,当拉莫三嗪超过150μm,则在配制为湿混悬剂时,如在服用剂量较低时(如1ml),取样会不均匀,当拉莫三嗪低于5μm时,首先制备的干混悬剂的质量与所选5μm-150μm的质量无显著差别,且制备非常困难。浪费人力和财力,不具备实用性。
本发明中的助悬剂为黄原胶,这是本发明的一个重要辅料。以拉莫三嗪100重量份计,黄原胶用量为10-50重量份,优选15-40重量份,更优选18-25重量份,在最优选实施例中,以拉莫三嗪100重量份计,黄原胶用量为20重量份。
发明人首先进行了液体混悬剂的研究,制备了两种拉莫三嗪液体混悬剂,分别为处方20160304-1和20160323-2,具体处方见表1。
表1液体混悬剂
本发明提供的处方20160304-1、20160323-2拉莫三嗪液体混悬剂制备方法包括以下步骤:
1、在搅拌状态下,依次将处方量的一水磷酸二氢钠、聚乙二醇、三氯蔗糖、草莓香精、山梨酸钾和麦芽糖醇加入处方量80%的纯化水中,搅拌桨速度为300rpm至500rpm。
2、待上述辅料全部溶解后,缓慢加入处方量的卡拉胶(加入过快,卡拉胶会结块),在加入过程中,随着混悬剂粘度增加,逐渐增加搅拌桨转速,使液体一直保持成涡旋状,待卡拉胶加完后,继续搅拌水合1小时,搅拌桨转速为500rpm至1100rpm。
3、卡拉胶水合完后,逐渐加入处方量的拉莫三嗪,加完后继续搅拌30分钟,装瓶即可,搅拌桨转速为800rpm至1100rpm。
将液体拉莫三嗪混悬剂装入250ml药用级PET塑料瓶中,密封后,置于40℃、RH75%(相对湿度)条件下的恒温恒湿箱中考察加速条件下液体混悬剂的稳定性,结果见表2。
表2拉莫三嗪液体混悬剂加速试验
由表2可知,处方20160323-2(浓度10mg/ml)在加速试验中,40℃、RH75%下产生的杂质C为处方20160304-1(浓度5mg/ml的一半。杂质C为拉莫三嗪的主要降解产物,美国药典中规定拉莫三嗪普通片的杂质C的限量为0.50%,拉莫三嗪咀嚼分散片杂质C的限量为0.30%,由加速试验结果可以推知,即使选择浓度为10mg/ml液体混悬剂也不能达到常温下储存两年的要求。
有文献报道,拉莫三嗪杂质C为其储存过程中产生的氧化产物,因此本发明还考察了不同抗氧化剂对拉莫三嗪液体混悬剂稳定性的影响。分别进行了丁香羟基茴香醚(BHA)、二丁基羟基甲苯(BHT)、没食子酸丙酯的抗氧化剂对本制剂杂质C的影响研究,发现3种抗氧化剂对抑制拉莫三嗪液体混悬剂在储存过程中产生的杂质C都没有明显的效果。
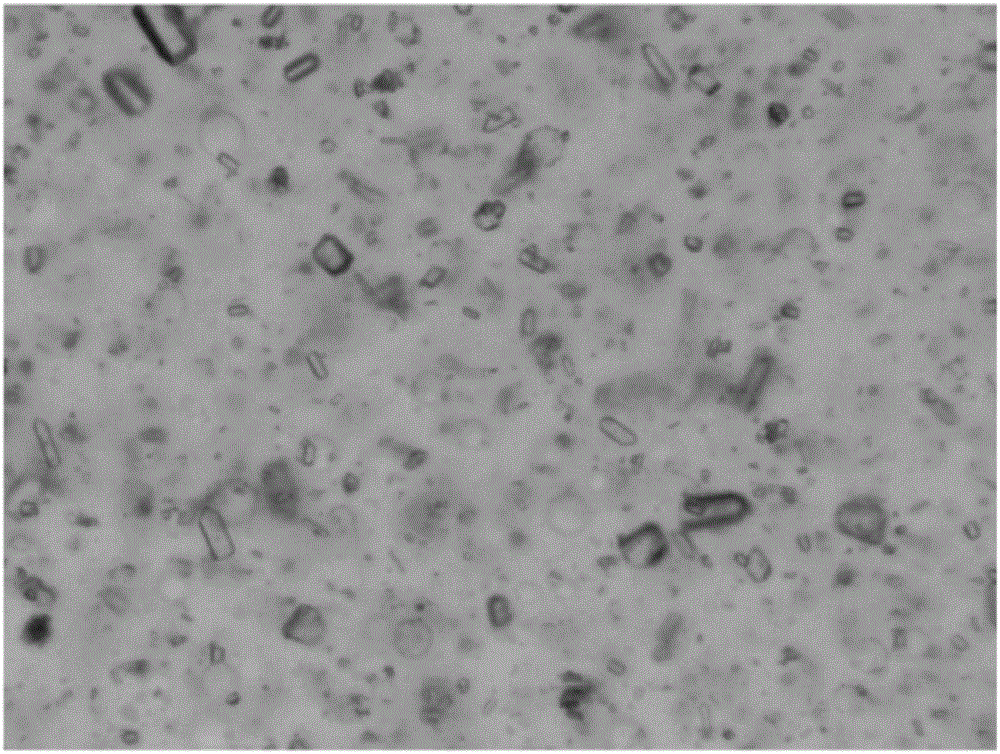
本发明还观察常温下拉莫三嗪液体混悬剂的物理稳定性,具体结果见图1和图2。由显微镜图片可知,拉莫三嗪液体混悬剂在刚制备好时未观察到块状晶体,而在常温下放置3天后,有大量块状晶体出现,并且随着时间增加,晶体有变大的趋势。由文献报道可知,这种块状晶体可能是拉莫三嗪在水中形成的水合物。拉莫三嗪液体混悬剂在储存过程中会产生块状晶体,不仅影响液体混悬剂的外观,而且结块的晶体不容易重新分散开,影响用药剂量的准确性。
由于拉莫三嗪液体混悬剂的物理稳定性和化学稳定性较差,且该技术问题难以解决。申请人进行了拉莫三嗪干混悬剂的研发。然而国内外未见有拉莫三嗪干混悬剂的上市和报道,因此申请人对于拉莫三嗪干混悬剂制剂辅料需要进行一系列的筛选。
特别进行了助悬剂的筛选:分别筛选了黄原胶、卡拉胶、羧甲基纤维素钠、羟丙基甲基纤维素K4M、卡波姆934P的筛选。
表3助悬剂的筛选
通过混悬剂分散时间试验进行评价,(加入等量水后,配制湿混悬剂振摇分散的时间,以时间短为佳)和沉降体积比(中国药典2015版规定沉降体积比应不低于0.90)来筛选助悬剂。
表4检测结果
检测结果见表4,其中选择黄原胶为最优选助悬剂,优点为分散时间快,混悬剂沉降体积比高,药物在使用过程中不会沉降。
本发明还对黄原胶的用量进行了考察。见表5
表5黄原胶用量筛选
表6检测结果
检查结果见表,最终选择黄原胶为20重量份,因为增加处方黄原胶用量后,分散时间明显增加,减少处方黄原胶用量后分散时间变化不大,考虑到厂家不同批次的黄原胶粘度会有差异,若某批次黄原胶粘度偏小,低用量黄原胶的处方粘度也会偏小,处方沉降体积比可能会低于0.90而影响产品质量,而当黄原胶用量大于100重量份时,所述拉莫三嗪溶液配置时,粘度会增大,分散时间会过于长,不易分散,因此所述黄原胶的用量,在拉莫三嗪为100重量份的条件下,不宜超过100重量份,而在这个条件下,黄原胶优选20重量份。
本发明提供了一种拉莫三嗪干混悬剂的处方,见表7
表7拉莫三嗪干混悬剂配方
本发明还提供了20160810-1的湿法制粒方法:
1、将拉莫三嗪原料药以及处方中的所有辅料分别过1016微米的筛网;
2、称取处方量的拉莫三嗪原料药以及内向辅料在合适体积的湿法制粒机中混合5分钟后,加适量水制粒。湿法制粒机搅拌剪切速度均为300-500rpm,制粒时间为3-5分钟;
3、用6350微米的筛网湿整粒后,用流化床在50℃条件下干燥至LOD<2%。LOD为制粒的含水量指标,当达到LOD<2%,可以认为湿法制粒中的水分已经被除去;
4、用1016um筛网干整粒,并与处方量的外向辅料至于合适体积的混合仪中,以20转/分钟的速度混合10分钟;
5、使用自动包装机对制备好的拉莫三嗪干混悬剂进行包装。
处方20160815-1与处方20160810-1所用辅料种类和用量相同,制备工艺采用干粉混合。见表8。
表8
本发明提供的处方20160815-1拉莫三嗪干混悬剂制备方法包括以下步骤:
1、将拉莫三嗪原料药以及处方中的所有辅料分别过1016微米的筛网;
2、称取处方量的拉莫三嗪原料药以及所有辅料,放在大小适合的混合仪中,以20-50转/分钟的速度混合10-20分钟;
3、使用自动包装机对制备好的拉莫三嗪干混悬剂进行包装。
处方20160815-1拉莫三嗪干混悬剂各项指标(如含量、含量均匀度、装量、分散时间、溶出)检测合格,采用干粉混合,工艺简单。
所有辅料必须过1016微米的筛网目的是:有些辅料在储存过程中会结块(如空气潮湿吸水所致),过筛网的目的是将其打散,且便于后续的混合均匀。
处方20160822-1拉莫三嗪干混悬剂中不含有黄原胶,具体见表9。设计此处方的目的是用于研究黄原胶在抑制拉莫三嗪水合物形成方面的作用。处方20160822-1的工艺流程与处方20160815-1相同。
表9
将处方20160815-1和20160822-1干混悬剂分别用水制备成10mg/ml的液体混悬剂,并且分别在2、4、8和24小时取样,离心后,得到的液体混悬剂中的混悬剂溶质样品粉末。然后对拉莫三嗪原料药以及得到的样品进行粉末X射线衍射实验。具体结果见X射线衍射图谱图3到图6。
从粉末X射线衍射结果,我们发现处方20160815-1中拉莫三嗪在2、4、8、24小时与拉莫三嗪原料药具有相同的晶形,而不含黄原胶的处方20160822-1中的拉莫三嗪晶型在8小时后就开始变化。由美国专利US7390807B2和US8486927B2可知,新形成的晶型是拉莫三嗪的水合物。
上述结果令人诧异,因为通常认为拉莫三嗪无水物一接触水就会开始形成水合物。也有文献报道拉莫三嗪在水溶液中很容易形成水合物。但是,本发明发现使用少量的助悬剂(本发明中为黄原胶),有抑制拉莫三嗪水合物形成的作用。
拉莫三嗪水合物具有不同的晶型,而加入黄原胶后,即将20160815-1处方配置成液体混悬液后,在24小时内,形成拉莫三嗪水合物的速度会显著降低,表现为晶型转化会变慢。这在病人使用干混悬剂配置成液体混悬液时,在质量稳定性上具有重要意义,保证了干混悬剂配置成液体混悬剂在24小时内质量相比未加入黄原胶时更稳定。
本发明进一步提供一种拉莫三嗪干混悬剂,所述填充剂为蔗糖、甘露醇、乳糖的一种或多种组合。
优选蔗糖,原因是,既可以作为甜味剂还可以作为填充剂,填充剂用量大,选择蔗糖因为其安全,使用广。
蔗糖粒径D90为50μm-400μm,优选50μm-300μm,更优选50μm-180μm。原因是蔗糖为处方中的填充剂,在处方中的用量大(约80%),其粒径若太小,粉末流动性差,会使药物含量不均匀,粉末包装难度也会加大,其粒径若太大,则会与其它原辅料粒径(粒径均小于180μm)相差太大,也会导致药物含量不均匀,因此蔗糖的粒径应该控制在一个范围内。优点是蔗糖粒径D90选择为50μm-180μm,既可以使药物混合更均匀,也可以改善粉末的流动性,便于粉末包装。
本发明进一步提供一种拉莫三嗪干混悬剂,所述缓冲剂为柠檬酸钠、柠檬酸、磷酸二氢钠、磷酸氢二钠的一种或多种组合;所述风味剂为草莓味、香蕉味、甜橙味、薄荷味香精之一;所述甜味剂为蔗糖、三氯蔗糖、阿斯巴甜、糖精钠的一种或者多种组合。
所述缓冲剂应有足够的缓冲能力,使混悬剂pH保持在所需的pH范围内,优选磷酸氢二钠。pH优选5-6.
本发明优选甜橙味香精。
本发明进一步提供一种拉莫三嗪干混悬剂,所述助流剂为二氧化硅、硬脂酸镁、滑石粉、硬脂酸富马酸钠的之一。
本发明提供了拉莫三嗪干混悬剂的制备方法,所述制备方法为干粉混合、湿法制粒、干法制粒的一种。
干粉混合工艺简单,重现性好。
拉莫三嗪干混悬剂可以包装在药用级塑料瓶或者玻璃瓶中供多次使用,也可以包装在小袋中供单次使用。
拉莫三嗪干混悬剂可以由药剂师或者病人父母或者其他成年人按照说明书的要求用水配制成特定浓度,优选10mg/ml的液体混悬剂用于病人口服。依据说明书上病人体重与服药量关系的表格计算病人此次服药体积,通过使用配套的1ml或者10ml口服注射器吸取准确体积的混悬剂直接注射于病人的口中。
本发明的创新点:
本发明中的拉莫三嗪干混悬剂,相比其片剂,可以快速均匀混悬于水中,改善了药物口感,服用更简单,给药剂量更准确;相比液体混悬剂(液体混悬剂也叫湿混悬剂),具有更好的化学稳定性,在有效期内仅有极少量的杂质产生。另外,本发明中助悬剂黄原胶,不仅助悬效果好,分散时间快,而且配置成为拉莫三嗪液体混悬剂时,晶型转化显著变慢,抑制拉莫三嗪水合物的形成,液体混悬剂物理稳定性更好,这些优点使得本发明中拉莫三嗪干混悬剂具有很好的病人依从性。
附图说明
图1处方20160304-1刚制备好后显微镜(放大100倍)下照片;
图2处方20160304-1制备后放置3天后显微镜(放大100倍)下照片;
图3拉莫三嗪活性成分、处方20160815-1和20160822-1在2小时的粉末X射线衍射图(纵坐标为强度计数,横坐标为2θ角,API为原料药);
图4拉莫三嗪活性成分、处方20160815-1和20160822-1在4小时的粉末X射线衍射图(纵坐标为强度计数,横坐标为2θ角,API为原料药);
图5拉莫三嗪活性成分、处方20160815-1和20160822-1在8小时的粉末X射线衍射图(纵坐标为强度计数,横坐标为2θ角,API为原料药);
图6拉莫三嗪活性成分、处方20160815-1和20160822-1在24小时的粉末X射线衍射图(纵坐标为强度计数,横坐标为2θ角,API为原料药)。
具体实施方式
下面的实施例仅用于进一步说明本发明但不限于本发明。凡基于本发明上述内容所实现的技术均属于本发明范围。
实施例1
处方1
干粉混合,具体步骤为:
1、将拉莫三嗪原料药以及处方中的所有辅料分别过1016微米的筛网。
2、称取处方量的拉莫三嗪原料药以及所有辅料,放在大小适合的混合仪中,以20转/分钟的速度混合10分钟。
3、使用自动包装机对制备好的拉莫三嗪干混悬剂进行包装。得到所述拉莫三嗪干混悬剂。
实施例2
采用实施例1的处方1,使用湿法制粒。
具体步骤为:
1、将拉莫三嗪原料药以及处方中的所有辅料分别过1016微米的筛网。
2、称取处方量的拉莫三嗪原料药以及内向辅料在合适体积的湿法制粒机中混合5分钟后,加适量水制粒。湿法制粒机搅拌剪切速度均为300rpm,制粒时间为5分钟。
3、用6350微米的筛网湿整粒后,用流化床在50℃条件下干燥至LOD<2%。
4、用1016um筛网干整粒,并与处方量的外向辅料至于合适体积的混合仪中,以20转/分钟的速度混合10分钟。
5、使用自动包装机对制备好的拉莫三嗪干混悬剂进行包装。得到所述拉莫三嗪干混悬剂。
实施例3
处方2
采用实施例1干粉混合方法制备。
实施例4
处方为实施例3的处方2,制备方法为实施例2的湿法制粒。
实施例5
处方3
采用实施例1干粉混合方法制备。
实施例6
处方为实施例5的处方3,制备方法为实施例2的湿法制粒。
实施例7
处方4
采用实施例1干粉混合方法制备。
实施例8
处方为实施例7的处方4,制备方法为实施例2的湿法制粒。
实施例9
处方5
采用实施例1干粉混合方法制备。
实施例10
处方6
制备方法与实施例1方法相同
实施例11
处方与实施例1中处方1其他辅料相同,拉莫三嗪为30mg
制备方法与实施例1方法相同。
实施例12
处方与实施例9中处方5其他原辅料相同,黄原胶为10mg
制备方法与实施例9方法相同。
实施例13
处方与实施例9中处方5其他原辅料相同,黄原胶为15mg
制备方法与实施例9方法相同。
实施例14
处方与实施例9中处方5其他原辅料相同,黄原胶为18mg
制备方法与实施例9方法相同。
实施例15
处方与实施例9中处方5其他原辅料相同,黄原胶为20mg
制备方法与实施例9方法相同。
实施例16
处方与实施例9中处方5其他原辅料相同,黄原胶为50mg
制备方法与实施例9方法相同。
本发明中的助悬剂为黄原胶,这是本发明的一个重要辅料。以拉莫三嗪100重量份计,黄原胶用量为10-50重量份,优选15-40重量份,更优选18-25重量份,根据技术效果评估,最优选实施例为,以拉莫三嗪100重量份计,黄原胶用量为20重量份。
其中拉莫三嗪为无水拉莫三嗪,粒径D90优选5μm-150μm。更优选10μm-120μm,最优选30μm-90μm,所述D90指的是颗粒直径小于所述粒径的颗粒占90%。
蔗糖粒径D90为50μm-400μm,优选50μm-300μm,更优选50μm-180μm。
以上所述实施例仅表达了本发明的几种实施方式,其描述较为具体和详细,但并不能因此而理解为对本发明专利范围的限制,应当指出的是,对于本领域的技术人员来说,在不脱离本发明构思的前提下,还可以做出若干变形和改造,这些都属于本发明的保护范围,因此,本发明专利的保护范围以所附权利要求为准。
- 还没有人留言评论。精彩留言会获得点赞!