医药组合物用于制备促发炎细胞介素抑制剂的用途的制作方法
本发明涉及一种用于降低个体中的促发炎细胞介素量的手段。具体而言,本发明是涉及一种医药组合物用于制备促发炎细胞介素抑制剂及制备治疗细胞介素释放症候群的药品的用途。
背景技术:
过去,癌症的治疗药物主要为小分子化学药物或大分子抗体。现在,治疗方法已经达到细胞疗法水平。然而,嵌合抗原受体t细胞免疫疗法(car-t)已得到广泛研究。它具有特异性受体并靶向识别特异性的细胞诸如肿瘤细胞。目前,世界上有两家制药公司novartis及gilead,它们已被fda批准进行car-t细胞疗法。临床试验表明,所述疗法具有高缓解率及延长的总体存活期。
尽管car-t细胞疗法为临床上有效的,但亦有一些副作用,甚至死亡。最普遍的不良反应为细胞介素释放症候群(cytokinereleasesyndrome,crs)。当将car-t细胞注射至患者体内时,t细胞杀死癌细胞,然后引起包括tnf-α、ifn-γ、il-10及il-6的细胞介素的释放,导致患者发烧、低血压、呼吸衰竭。因此,如何控制由car-t细胞回输引起的这些免疫风暴为car-t疗法的挑战。
技术实现要素:
在数次药物筛选及测试之后,申请人发现多种化合物或组成物,诸如吩噻嗪衍生物(phenothiazinederivatives)、石莲花(graptopetalumparaguayense)提取物、红景天(rhodiolarosea)提取物及组蛋白去乙酰酶(histonedeacetylase,hdac)抑制剂,可以抑制促发炎细胞介素的产生,因此提供了一种用于治疗患者的免疫反应的新方法,同时避免了由降低抗肿瘤功效的潜在风险引起的不必要的免疫抑制。
如上文所述,本发明提供了一种新的用于降低个体中的促发炎细胞介素表现量的方法;该方法包含向有需要的个体给予治疗有效量的医药组合物,该医药组成物包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种。
另外,本发明还提供一种治疗由car-t细胞疗法引起的细胞介素释放症候群或由促发炎细胞介素的产生过量介导的病症的方法;该方法包含向有需要的个体投予治疗有效量的医药组合物,该医药组成物包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种。
即,本发明可以提供一种医药组合物用于制备个体促发炎细胞介素抑制剂的用途,所述医药组合物包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种。
根据本发明的一个实施例,促发炎细胞介素(proinflammatorycytokine)为选自由tnf-α、ifn-γ、il-10、及il-6中的至少一种。
根据本发明的一个实施例,吩噻嗪衍生物为三氟拉嗪(trifluoperazine)或硫利达嗪(thioridazine)。
根据本发明的一个实施例,组蛋白去乙酰酶(hdac)抑制剂为辛二酰苯胺异羟肟酸(suberoylanilidehydroxamicacid)。
根据本发明的一个实施例,其中在投予含硫利达嗪的医药组合物后6小时,细胞中的ifn-γ含量降低了至少18.6%;在投予含硫利达嗪的医药组合物后24小时,细胞中的ifn-γ含量降低了至少28.2%。
根据本发明的一个实施例,其中在投予含石莲花提取物的医药组合物后6小时,细胞中的ifn-γ含量降低了至少72.5%;在投予含石莲花提取物的医药组合物后24小时,细胞中的ifn-γ含量降低了至少77.7%。
根据本发明的一个实施例,其中在投予含红景天提取物的医药组合物后6小时,细胞中的ifn-γ含量降低了至少36.3%;在投予含红景天提取物的医药组合物后24小时,细胞中的ifn-γ含量降低了至少62.9%。
根据本发明的一个实施例,其中在投予含硫利达嗪的医药组合物后6小时,细胞中的il-6含量降低了至少20.7%;在投予含硫利达嗪的医药组合物后24小时,细胞中的il-6含量降低了至少39.5%。
根据本发明的一个实施例,其中在投予含石莲花提取物的医药组合物后6小时,细胞中的il-6含量降低了至少37.5%;在投予含石莲花提取物的医药组合物后24小时,细胞中的il-6含量降低了至少19.4%。
根据本发明的一个实施例,其中在投予含红景天提取物的医药组合物后6小时,细胞中的il-6含量降低了至少35.2%;在投予含红景天提取物的医药组合物后24小时,细胞中的il-6含量降低了至少24.3%。
本发明的另一实施方式是关于一种医药组合物用于制备治疗细胞介素释放症候群的药物的用途,所述医药组合物包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种。
根据本发明的一个实施例,细胞介素释放症候群是由car-t细胞疗法引起的,并且医药组合物是在car-t细胞疗法期间或在car-t细胞疗法之后投予。
根据本发明的一个实施例,细胞介素释放症候群是关于一或多种促发炎细胞介素的产生过量。
本发明的另一实施方式是关于一种医药组合物用于制备治疗由细胞介素的产生过量介导的病症的药品的用途,所述病症诸如发炎、自体免疫疾病、糖尿病、动脉粥样硬化及癌症。
另外,本发明还可以提供一种医药组合物,其包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种;该医药组合物是用以降低个体中促发炎细胞介素表现量,并且能够进一步治疗由car-t细胞疗法引起的细胞介素释放症候群或由促发炎细胞介素的产生过量介导的病症。
以下,详细描述本发明的一或多个实施例。经由以下详细描述及所附申请专利范围,将使得本发明的前述特征变得更加明显。应当理解的是,前述一般描述及以下详细描述的意旨是只用于说明性目的而具有例示性;而且并不用于限制本发明的范畴的意图。
附图说明
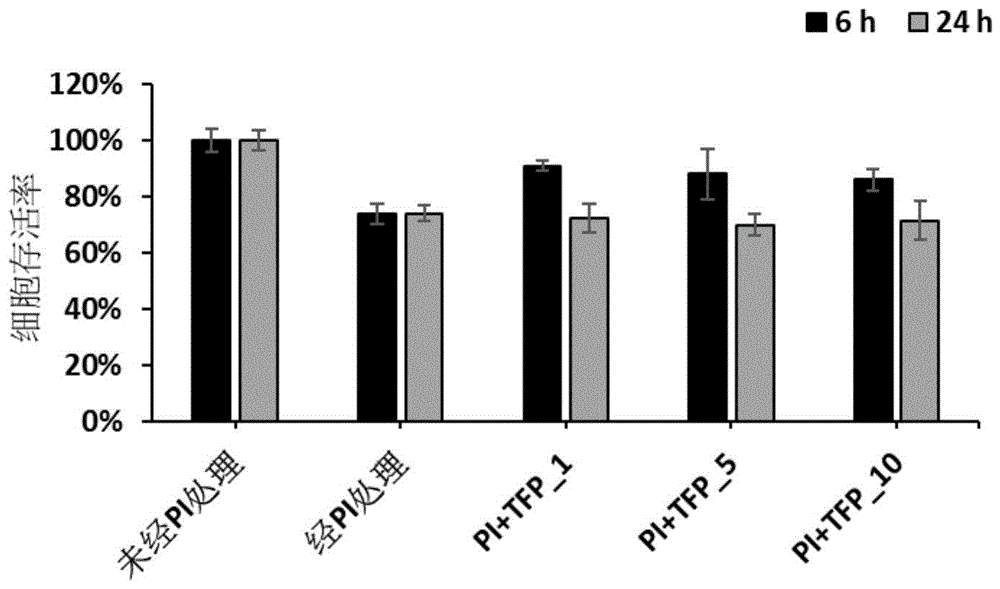
图1a为本发明的实施例1中的三氟拉嗪(tfp)的细胞存活率测试结果图。
图1b为本发明的实施例1中的三氟拉嗪(tfp)的细胞介素释放测试结果图。
图2a为本发明的实施例1中的硫利达嗪(thz)的细胞存活率测试结果图。
图2b为本发明的实施例1中的硫利达嗪(thz)的细胞介素释放测试结果图。
图3a为本发明的实施例1中的石莲花提取物(hh-f3)的细胞存活率测试结果图。
图3b为本发明的实施例1中的石莲花提取物(hh-f3)的细胞介素释放测试结果图。
图4a为本发明的实施例1中的红景天提取物(rr-etoh)的细胞存活率测试结果图。
图4b为本发明的实施例1中的红景天(rhodiolarosea)提取物(rr-etoh)的细胞介素释放测试结果图。
图5a为本发明的实施例1中的辛二酰苯胺异羟肟酸(saha)的细胞存活率测试结果图。
图5b为本发明的实施例1中的辛二酰苯胺异羟肟酸(saha)的细胞介素释放测试结果图。
图6a为本发明的实施例2中的三氟拉嗪(tfp)的细胞存活率测试结果图。
图6b为本发明的实施例2中的三氟拉嗪(tfp)的细胞介素释放测试结果图。
图7a为本发明的实施例2中的硫利达嗪(thz)的细胞存活率测试结果图。
图7b为本发明的实施例2中的硫利达嗪(thz)的细胞介素释放测试结果图。
图8a为本发明的实施例2中的石莲花提取物(hh-f3)的细胞存活率测试结果图。
图8b为本发明的实施例2中的石莲花提取物(hh-f3)的细胞介素释放测试结果图。
图9a为本发明的实施例2中的红景天提取物(rr-etoh)的细胞存活率测试结果图。
图9b为本发明的实施例2中的红景天(rhodiolarosea)提取物(rr-etoh)的细胞介素释放测试结果图。
图10a为本发明的实施例3中的硫利达嗪(thz)的细胞存活率测试结果图。
图10b为本发明的实施例3中的硫利达嗪(thz)的细胞介素释放测试结果图。
图11a为本发明的实施例4中的石莲花提取物(hh-f3)的细胞存活率测试结果图。
图11b为本发明的实施例4中的石莲花提取物(hh-f3)的细胞介素释放测试结果图。
具体实施方式
在本文中,本文所用的所有技术及科学术语均具有与本发明所属领域中的普通技术人员通常理解的含义相同的含义。另外,除非上下文有另外指示,否则本文所用的单数术语应包括复数,且复数术语应包括单数。
除非本文另外定义,否则术语“治疗(treat/treating/treatment)”意谓向患有特定疾病或病症的患者投予的动作,其中所述动作可以减轻患者的疾病或病症、或降低一种或多种症状的严重性、或减慢或延迟疾病或病症的进展。
在本文中,术语“有效量”意谓向患者直接或间接投予(administered/administration)的医疗药物在适当的给药期后可达成降低促发炎细胞介素表现量的作用的特定量。
在本文中,术语“个体”或“患者”可以彼此互换使用。术语“个体”或“患者”是指分别可借由化合物及/或方法治疗的动物,包括但不限于例如狗、猫、马、绵羊、猪、牛及其类似动物以及人类、非人类灵长类动物。除非另外指定,否则“个体”或“患者”可包括男性及女性。另外,其亦包括适合接受本发明的医药组合物及/或方法治疗的个体或患者,较佳为人类。
尽管阐述本发明的广泛范畴的数值范围及参数为近似值,但在特定实例中所阐述的数值尽可能精确地加以报告。然而,任何数值本身均含有由其各自测试量测中存在的标准偏差必然引起的某些误差。在本文中,术语“约”通常意谓实际值在特定值或范围以上或以下10%、5%、1%或0.5%之内。替代地,术语“约”指示当由本领域中的普通技术人员考虑时,实际值落在平均值的可接受的标准误差内。除在实例中或另外有明确指示的以外,本文所用的所有范围、量、值及百分比(例如,用于描述材料的量、时间、温度、操作条件、量比率及其类似者)应理解为借由词“约”进行修饰。因此,除非有相反的明确说明,否则本说明书及所附权利要求书中所公开的数值参数全部为近似值,并且如果需要,可以改变。无论如何,各数值参数应至少依照报告的有效数位的数值且借由应用普通的舍入技术来解释。
在本发明的一个实施方式中,本发明提供一种用于降低个体中的促发炎细胞介素表现量的方法,其借由向有需要的个体投予治疗有效量的医药组合物来进行,所述医药组合物包含选自吩噻嗪衍生物、石莲花提取物、红景天提取物、及组蛋白去乙酰酶(hdac)抑制剂中的至少一种。
根据上文,所公开的医药组合物可借由众所所周知的制药制程制备。在本发明的一个实施方式中,本发明中所公开的医药组合物可借由任何适当的给药途径投予,例如借由以胶囊、悬液剂或糖衣锭的口服投予或者借由例如以肌内注射、静脉内注射、皮下注射或腹膜内注射的肠胃外投予的全身投予模式。此外,在一些实施例中,本发明中所公开的医药组合物亦可通过透黏膜或透皮手段进行投予,例如局部皮肤应用、或者支气管、鼻或口服吸入、或者呈滴鼻剂的滴注;且亦可经直肠投予。
对于口服投予,本发明中所公开的医药组合物可以与赋形剂一起投予或可以不与赋形剂一起投予。同样,本发明的医药组合物亦可调配成呈固体剂型的糖衣锭,其中含有各种助剂、崩解剂、颗粒状黏合剂或润滑剂。另外,在一个实例中,亦可使用乳糖或高分子量聚乙二醇。此外,视情况,任何药物活性成分的释放速率可用包衣或包层例如肠溶衣经进一步改善。在其他实例中,本发明的医药组合物亦可调配成脂质体结构或仿生细胞外基质是统结构,或者可填充至硬质及软质明胶胶囊中,或者可封装至套组中的可生物降解的颗粒中。
同样,在本发明中,医药上可接受的赋形剂意谓与医药调配物的其他成分相容并且与有机体相容的赋形剂,例如封装材料或各种添加剂诸如吸收增强剂、抗氧化剂、黏合剂、缓冲液、包衣剂、着色剂、稀释剂、崩解剂、乳化剂、补充剂、填充剂、调味剂、保湿剂、润滑剂、香料、防腐剂、推进剂、脱模剂、杀菌剂、甜味剂、增溶剂、润湿剂及其混合物。
适用于本发明的助剂的实例可为例如微晶纤维素、碳酸钙、磷酸氢钙或甘胺酸。适用于本发明的崩解剂的实例可为例如淀粉、藻酸或某些硅酸盐。适用于本发明的颗粒状黏合剂的实例可为例如聚乙烯吡咯啶酮、蔗糖、明胶或阿拉伯胶。适用于本发明的颗粒状黏合剂的实例可为例如硬脂酸镁、月桂基硫酸钠或滑石。适用于本发明的赋形剂的实例可为例如乳糖、蔗糖、甘露醇、山梨糖醇、玉米淀粉、小麦淀粉、米淀粉、马铃薯淀粉、明胶或黄蓍胶。
在一些实施例中,本发明的医药组合物经调配成适合口服投予的液体剂型,例如口服悬液剂、乳剂、微乳剂及/或酏剂。对于此一液体剂型,本发明的医药组合物的活性成分可进一步与各种甜味剂或调味剂、着色剂或染料一起调配,如果需要,则添加乳化剂及/或助悬剂、或稀释剂诸如水、酒精、丙二醇或甘油、或用于维持ph值的缓冲液。
同样,在其他实施例中,将含有本发明的医药组合物的液体调配物制成无菌可注射溶液或悬液剂;例如,制成适于借由静脉内、肌内、皮下或腹膜内注射投予的溶液。
在一些实施例中,本发明中所公开的医药组合物可以用作另外的辅助治疗剂,以改善癌症的主要治疗方法如手术、放射疗法或化学疗法的治疗效果。本发明中所公开的医药组合物可以单独应用或与已知医药上可接受的助剂组合应用,并且例如可以口服或与食物一起向个体投予。
在一些实施例中,本发明的方法进一步包括在向个体投予本发明的医药组合物之前、期间或之后,另外向个体应用癌症的另一主要治疗手段诸如手术、放射疗法或化学疗法,以便改善个体中的癌症的治疗效果。
为了更全面且完整地描述本发明,以下对本发明的实施方式及具体实例进行说明性的描述。然而,此等并无代表本发明的具体实例中可实践或可利用的唯一形式的意图。实施例中涵盖了多个具体实例的特征和构造;以及操作这些具体实例的过程步骤及顺序。然而,在其他实例中,亦可借由相同或等效的功能及步骤顺序来完成。
首先,描述本发明的实例中的测试的标准操作过程。
<细胞培养及试剂>
本实施例中所选用的人类jurkatt细胞株(clonee6-1,atcctib152)及人类白血病细胞株thp-1,购自中国台湾生物资源保存及研究中心(bioresourcecollectionandresearchcentre;bcrc)。将细胞维持在具有2mml-麸酰胺的rpmi1640培养基(gibco,carlsbad,ca,usa)中,所述培养基经调整成含有1.5g/l碳酸氢钠、4.5g/l葡萄糖、10mmhepes、1.0mm丙酮酸钠、1%(v/v)青霉素-链霉素(hyclone,logan,ut)及10%(v/v)胎牛血清(fbs;hyclone)。将细胞在37℃下保存在具有5%co2的培养箱中。当细胞進行传代时,每毫升细胞密度不允许超过3×106个细胞数。
<试剂及药物>
此实施例中所用的离子霉素(ionomycin)、佛波醇12-肉豆蔻酸酯13-乙酸酯(phorbol12-myristate13-acetate,pma)、脂多醣(lipopolysaccharide,lps)、三氟拉嗪(trifluoperazine,tfp)、硫利达嗪(thioridazine,thz)及辛二酰苯胺异羟肟酸(suberoylanilidehydroxamicacid,saha)购自sigma-aldrich(st.louis,mo,usa)。
根据制造商的说明,用于细胞毒性检定的3-(4,5-二甲基噻唑-2-基)-5(3-羧基甲氧基苯基)-2-(4-磺苯基)-2h-四唑(3-(4,5-dimethylthiazol-2-yl)-5(3-carboxymethoxyphenyl)-2-(4-sulfophenyl)-2h-tetrazolium,mts)购自celltilter
可借由美国专利第8686030号中所示的方法制备石莲花提取物及红景天提取物,所述专利所公开的内容以全文引用的方式并入本文。
即,将石莲花(称为gp)的叶子研磨并在-20℃下冻干成粉末,且在提取前在25℃下储存于防潮箱(moisturebuster)中。首先,将1.5ggp粉末与10ml100%甲醇(meoh)震荡5分钟,然后以1500g离心5分钟。去除上清液后,将10ml水、100%丙酮、100%甲醇、100%乙醇、70%乙醇、50%乙醇、100%dmso及30%dmso添加至各沉淀物中以使其重新悬浮以得到各提取物。将悬浮液藉由震荡5分钟进行混合,以1500g离心5分钟两次,再次以9300g离心5分钟并在室温下使用0.45μm滤器进行层流过滤。
然后,借由sephadexlh-20管柱将30%dmso上清液分级成四个流份(hh-f1、hh-f2、hh-f3、hh-f4),并且借由具有uv侦测器的高效液相层析法(hplc)进一步分析各流份。本发明中较佳选择hh-f3。
类似地,将红景天(称为rs)的植物冻干成粉末,且在提取前在25℃下储存于防潮箱中。将1.5公克的rs粉末溶解在10mlh2o中,然后以1500g离心5分钟,接着在室温下使用0.45μm滤器进行层流过滤。将样品在-20℃下呈150mg/ml储液进行储存且在本发明中命名为rr-etoh。
<t细胞的活化建模及细胞介素量测>
将jurkat细胞以每毫升5.0×105个细胞数的密度接种在48孔培养盘中的培养基中。为了促进干扰素γ(ifn-γ;ifng)产生,在培养基中分别使用含有pma与离子霉素或不含有pma与离子霉素的组合刺激细胞。另外,thp-1细胞则是分别使用含有促进il-6产生的lps的培养基或不含有lps的培养基进行培养。
借由离心收集培养上清液,并-20℃下储存以供细胞介素分析。借由elisa套组(invitrogen,carlsbad,ca,usa)根据制造商的说明测量ifn-γ及il-6的浓度。
<细胞存活率检定>
使用mts试剂(promega)确定细胞存活率。在37℃、5%co2下借由向各孔中添加mts达3小时进行检定。甲瓒的转化量取决于活细胞数量,然后用96孔盘读取器记录在490nm处的吸光度。
此后,将借由参考附图解释本发明的较佳实施例来详细描述本发明。
《实施例1》
为了诱导ifn-γ产生,将jurkatt细胞如上文所述进行培养并用pma加上离子霉素刺激24小时,之后分别用如表1中所示的候选药物进行培育。6小时及24小时后,收集上清液以供细胞存活率分析及细胞介素分析。采用人类ifn-γelisa套组(invitrogen)根据制造商的说明量测细胞介素的浓度,并将所测得的ifn-γ浓度与细胞存活率相除(ifn-γ/细胞存活率),进而获得用细胞存活率正规化的ifn-γ浓度。
表1中列出了细胞存活率结果及用细胞存活率正规化的ifn-γ浓度。并且结果亦显示在图1a、图1b、图2a、图2b、图3a、图3b、图4a、图4b、图5a及图5b中。
表1
关于细胞存活率,从以上表1中可以看出,在用pma加上离子霉素预培养24小时后,jurkatt细胞的细胞存活率降低至约80~90%。并且在药物处理6小时及24小时后,细胞存活率的下降小于30%,表明上述药物不对细胞造成严重损伤。此外,hh-f3能够恢复由pma及离子霉素引起的细胞损伤,从而增加细胞存活率。
此外,关于ifn-γ含量,从以上表1可以看出,在存在pma加上离子霉素的情况下,jurkatt细胞可经刺激以产生ifn-γ。并且在药物处理6小时及24小时后,jurkatt细胞中的ifn-γ含量能够降低。在它们当中,与tfp及saha相比,硫利达嗪(thz)、hh-f3及rr-etoh对细胞的作用更强。随着这三种药物浓度及培养时间的增加,ifn-γ含量逐渐降低。
更特定而言的,当所述医药组合物仅包含硫利达嗪时,在投予分别含有1μm、5μm及10μm硫利达嗪的医药组合物6小时后,细胞中的ifn-γ含量分别降低了18.6%、23.7%及36.2%;在投予分别含有1μm、5μm及10μm的硫利达嗪的医药组合物24小时后,细胞中的ifn-γ含量分别降低了28.2%、57.7%及52.2%。
当所述医药组合物仅包含石莲花提取物(hh-f3)时,在投予分别含有10μg/ml、20μg/ml及40μg/ml的石莲花提取物(hh-f3)的医药组合物6小时后,细胞中的ifn-γ含量分别降低了72.5%、80.8%及90.8%;在投予分别含有10μg/ml、20μg/ml及40μg/ml的石莲花提取物(hh-f3)的医药组合物24小时后,细胞中的ifn-γ含量分别降低了77.7%、87.1%及94.4%。
当所述医药组合物仅包含红景天提取物(rr-etoh)时,在投予分别含有10μg/ml、20μg/ml及40μg/ml的红景天提取物(rr-etoh)的医药组合物6小时后,细胞中的ifn-γ含量分别降低了36.3%、57.2%及60.9%;在投予分别含有10μg/ml、20μg/ml和40μg/ml的红景天提取物(rr-etoh)的医药组合物24小时后,细胞中的ifn-γ含量分别降低了62.9%、67.0%及76.6%。
《实施例2》
为了诱导il-6产生,将thp-1细胞如上文所述进行培养并用lps刺激16小时,之后分别用如表2中所示的候选药物进行培育。6小时及24小时后,收集上清液以供细胞存活率分析及细胞介素分析。借由il-6elisa套组(invitrogen)根据制造商的说明量测细胞介素的浓度,并将所测得的il-6浓度与细胞存活率相除(ifn-γ/细胞存活率),进而而获得用细胞存活率正规化的ifn-γ浓度。
表2中列出了细胞存活率结果及用细胞存活率正规化的il-6浓度。并且结果亦显示在图6a、图6b、图7a、图7b、图8a、图8b、图9a及图9b中。
表2
关于il-6含量,从以上表2可以看出,在存在pma加上离子霉素的情况下,jurkatt细胞可经刺激以产生il-6。并且在药物处理6小时及24小时后,jurkatt细胞中的il-6含量能够降低。在它们当中,与tfp相比,硫利达嗪(thz)、hh-f3及rr-etoh对细胞的作用更强。随着这三种药物浓度及培养时间的增加,il-6含量逐渐降低。
更特定言的,当所述医药组合物仅包含硫利达嗪时,在投予分别含有1μm、5μm及10μm的硫利达嗪的医药组合物6小时后,细胞中的il-6含量分别降低了20.7%、37.1%及45.9%;在投予分别含有1μm、5μm及10μm的硫利达嗪的医药组合物24小时后,细胞中的il-6含量分别降低了39.5%、51.8%及65.2%。
当所述医药组合物仅包含石莲花提取物(hh-f3)时,在投予分别含10μg/ml、20μg/ml及40μg/ml的石莲花提取物(hh-f3)的医药组合物6小时后,细胞中的il-6含量分别降低了39.2%、37.5%及38.5%;在投予分别含有10μg/ml、20μg/ml及40μg/ml的石莲花提取物(hh-f3)的医药组合物24小时后,细胞中的il-6含量分别降低了26.3%、19.4%及22.3%。
当所述医药组合物仅包含红景天提取物(rr-etoh)时,在投予分别含有10μg/ml、20μg/ml及40μg/ml的红景天提取物(rr-etoh)的医药组合物6小时后,细胞中的il-6含量分别降低了35.2%、47.5%及44.6%;在投予分别含有10μg/ml、20μg/ml和40μg/ml的红景天提取物(rr-etoh)的医药组合物24小时后,细胞中的il-6含量分别降低了24.3%、24.9%及24.5%。
《实施例3》
在所述实施例中,将jurkat细胞以每毫升5.0×105个细胞数的密度接种于48孔培养盘中的不同培养基中,并且各培养基含有以下文表3中所示的比例的pma、离子霉素及thz。
24小时及48小时后,收集上清液以供细胞存活率分析及细胞介素分析。借由人类ifn-γelisa套组(invitrogen)根据制造商的说明量测细胞介素的浓度。表3中列出了细胞存活率结果及用细胞存活率正规化的ifn-γ浓度。并且结果亦显示在图10a及图10b中。
表3
*ifn-γ/细胞存活率:用细胞存活率正规化的ifn-γ浓度
从以上表3中列出的结果中清楚知道,在培育24小时及48小时后,第3组的ifn-γ数值正规化后分别为34.9pg/ml及32.6pg/ml,比第2组降低46.5%及18.7%;在培育24小时及48小时后,第4组的ifn-γ数值正规化后分别为35.7pg/ml及39.7pg/ml,比第2组降低45.3%及1.0%。thz及pma加上离子霉素的共处理显著减弱了jurkat细胞中的细胞介素诱导。结果表明可在car-t细胞疗法期间向个体投予药物,以阻止细胞介素产生。
此外,第2组、第3组与第4组的间的细胞存活率没有显著差异,因此可清楚地知道,thz不影响细胞存活率。
《实施例4》
在所述实施例中,将jurkat细胞以每毫升5.0×105个细胞数的密度接种于48孔培养盘中的不同培养基中,并且各培养基含有以下文表4中所示的比例的pma、离子霉素及hh-f3。
24小时、30小时及48小时后,收集上清液以供细胞存活率分析及细胞介素分析。借由人类ifn-γelisa套组(invitrogen)根据制造商的说明量测细胞介素的浓度。表4中列出了细胞存活率结果及用细胞存活率正规化的ifn-γ浓度。并且结果亦显示于图11a及图11b中。
表4
*用细胞存活率正规化的ifn-γ浓度(pg/ml)
从以上表4中列出的结果中可清楚知道,在培育24小时、30小时及48小时后,第3组的ifn-γ数值正规化后分别为39.5pg/ml、24.9pg/ml及23.7pg/ml,比第2组降低39.5%、50.4%及35.4%;在培育24小时、30小时及48小时后,第4组的ifn-γ数值正规化后分别为29.0pg/ml、19.1pg/ml及20.5pg/ml,比第2组降低55.6%、62.0%及44.1%;在培育24小时、30小时及48小时后,第5组的ifn-γ数值正规化后分别为24.2pg/ml、13.9pg/ml及18.2pg/ml,比第2组降低62.9%、72.3%、50.4%。hh-f3及pma加上离子霉素的共处理显著减弱了jurkat细胞中的细胞介素诱导。结果表明可在car-t细胞疗法期间向个体投予药物,以阻止细胞介素产生。
此外,关于细胞存活率,第3组至第5组的细胞存活率高于第2组,这表明hh-f3可恢复由pma及离子霉素引起的细胞损伤,然后增加细胞存活率。
本发明显示以下内容:抗精神病药物硫利达嗪(thz)显著降低了产生ifn-γ的细胞中的ifn-γ的表现量。经研究中草药hh-f3及rr-etoh的处理对减少ifn-γ分泌量有显著作用,并且亦影响了t细胞中的il-6分泌。此外,采取处理后细胞的存活率几乎不受影响。结果表明,候选药物硫利达嗪(thz)、hh-f3及rr-etoh可能具有免疫抑制作用,并提供了细胞介素释放症候群的潜在疗法。
此外,借由使用药物共处理方法,hh-f3及硫利达嗪亦能够减少细胞介素产生。结果表明,hh-f3及硫利达嗪在car-t细胞抗癌疗法中预防细胞介素释放症候群。
上文所述的具体实施例仅用于说明本发明的特征和效果,且不旨在限制本发明的实施方案范畴。在不脱离本发明的精神及技术范畴的情况下,基于本发明中所公开的内容进行的任何等效改变及修改仍落在所描述的专利范畴内。
- 还没有人留言评论。精彩留言会获得点赞!