具有探针竞争物的扩增分析的制作方法
在先申请的交叉引用
本申请基于35u.s.c.§119(e)要求美国临时申请62/174,279的优先权,该临时申请的申请日为2015年6月11日,以上全文以引用的方式并入本文中用于所有目的。
其他材料的交叉引用
本申请通过引用结合以下材料的全文用于所有目的:2006年5月9日授权的美国专利7,041,481;2010年7月8日公布的公布号为2010/0173394a1的美国专利申请;2011年9月8日公布的公布号为2011/0217712a1的美国专利申请;2012年6月21日公布的公布号为2012/0152369a1的美国专利申请;2013年2月14日公布的公布号为2013/0040841a1的美国专利申请;2014年6月26日公布的公布号为2014/178889a1的美国专利申请;2014年8月7日公布的公布号为2014/0221238a1的美国专利申请;以及josephr.lakowicz的《萤光光谱学原理》(principlesoffluorescencespectroscopy)(第2版,1999)。
介绍
数字分析通常依赖于样品中分析物个体副本的存在和活性的检测能力。在典型的数字分析中,样品被分离成通常等量的一组分解部分。如果分析物副本在各分解部分中随机分布并且分析物经过充分稀释,一些分解部分应该不含副本,其他仅含一个副本,并且,如果这些分解部分的数量足够大,仍有其他分解部分包含两个副本、三个副本甚至更高数量的副本。基于分析物在各分解部分中给定的平均浓度,在一个分解部分中发现恰好为0、1、2、3或更多副本的概率可通过泊松分布进行描述。相反的,分析物在各分解部分中(因而在样品中)的浓度可通过在各分解部分中发现给定数量的副本的概率进行评估。
未发现副本和发现一个或多个副本的概率的评估可通过数字分析进行测量。可测试每个分解部分以确定该分解部分是包含至少一个分析物副本的阳性分解部分,还是不包含分析物副本的阴性分解部分。在分解部分中未发现副本的概率可通过测试为阴性的分解部分的数量分数(阴性分数)进行估计,且发现至少一份副本的概率可通过测试为阳性的分解部分的数量分数(阳性分数)进行估计。阳性分数或者等效的阴性分数可用于通过泊松统计确定各分解部分中分析物的浓度。
扩增分析,例如数字分析的那些,可用于测试不同等位基因的存在。例如,通过使用特异性结合突变型(相对于野生型而言)的“突变”探针,可区分目标序列的突变型和对应的野生型。然而,该方法通常需要使用不同的突变探针检测每种不同的突变型的存在,这可能是昂贵的、耗时的且不切实际的。另外,如果突变型在样品中数量很少,突变型假阳性的频率可能使真阳性频率无用,使得测试样品中突变序列存在的分析不可靠。
需要新方法,允许在扩增分析中使用相同探针测试不同的变异序列和/或增加测试少量突变序列的灵敏度。
技术实现要素:
本发明提供用于检测扩增分析中的目标的等位形式的方法和组合物,其可为数字分析。在示例性方法中,可形成多个分解部分,其都包含目标的至少一种第一等位形式(例如一种或多种变异形式)和一第二等位形式(例如野生型)。每个分解部分可包含(i)能够特异性结合至目标的每一种第一和第二等位形式的相同探针和(ii)配置成选择性结合相对于至少一种第一等位形式而言的第二等位形式并配置成阻断探针与第二等位形式的结合的竞争物。该目标的至少一种第一等位形式在各分解部分中可以扩增。当该些分解部分包含标签时,可从探针的标签检测到信号。基于信号可确定对于至少一种第一等位形式是阳性的分解部分的数量,或者对于至少一种第一等位形式是阴性的分解部分的数量。可基于确定数量计算该至少一种第一等位形式的水平。
附图说明
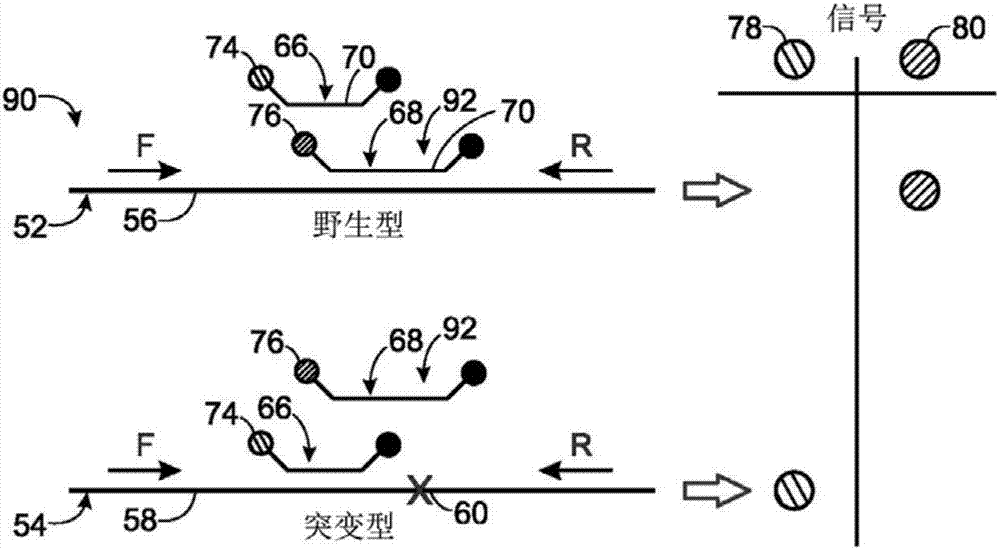
图1是用于检测变异和野生型目标的数字扩增分析的示意图,其中该分析在不含竞争物时进行。
图2是用于检测变异和野生型目标的典型扩增的示意图,其中该分析在具有结合至不同标签的探针和竞争物的条件下进行,其根据本发明公开内容的各方面。
图3是用于检测变异和野生型目标的典型扩增分析的另一示意图,其中根据本发明公开内容的各方面,该分析在具有结合至不同量的相同标签的探针和竞争物的条件下进行。
图4是用于检测变异和野生型目标的典型扩增分析的另一示意图,其中根据本发明公开内容的各方面,该分析具有未标记竞争物和可区分标记探针,用于检测变异目标以及非目标参照。
图5是根据本发明公开内容的各方面,在具有探针和竞争物的数字扩增分析中可进行的典型步骤的流程图。
图6是根据本发明公开内容的各方面,用于阐明检测人egf受体(egfr)的外显子19中的突变的数字扩增分析的典型实施方式各方面的一套排列序列。
图7是荧光信号检测图,根据本发明公开内容的各方面,根据图2的配置,在存在fam标记探针和hex标记竞争物的液滴中的目标经过扩增后,从共同包含外显子19egfr目标的突变型和野生型的液滴进行荧光信号检测。
图8是根据本发明公开内容的各方面的液滴荧光信号检测图,该液体与图7的相比,除了仅包含野生型目标,其他相同。
具体实施方式
本发明提供用于检测扩增分析中的目标的等位形式的方法和组合物,其可为数字分析。在示例性方法中,可形成多个分解部分,其共同包含目标的至少一种第一等位形式(例如一种或多种变异形式)和一第二等位形式(例如野生型)。每个分解部分可包含(i)能够特异性结合至目标的每一种第一和第二等位形式的相同探针和(ii)配置成选择性结合相对于至少一种第一等位形式而言的第二等位形式并配置成阻断探针与第二等位形式的结合的竞争物。该目标的至少一种第一等位形式在各分解部分中可以扩增。当该些分解部分包含标签时,可从探针的标签检测到信号。基于该信号可确定对于至少一种第一等位形式是阳性的分解部分的数量,或者对于至少一种第一等位形式是阴性的分解部分的数量。可基于确定数量计算该至少一种第一等位形式的水平。
本发明的方法和组合物相对于其他检测等位序列如目标的一种或多种变异型和/或野生型的方法相比具有实质性优势。更具体而言,竞争物通过阻断探针与野生型目标的结合,当给定分解部分仅存在野生型时,可降低从该分解部分中的探针标签检测到的信号水平。该降低的信号可显著减少变异型的假阳性的分解部分的数量分数,以提供更高灵敏度的变异检测。而且,该方法和组合物能检测破坏与竞争物杂交但不破坏探针与变异型杂交的任何变异型目标。相应的,可能发生于基因局部突变热点的各种删除、插入和/或取代,每种扰乱竞争物与目标结合但未扰乱探针与目标结合的突变都可用相同扩增分析进行检测。
本发明公开内容的其他方面呈现在下列部分:(i)典型分析配置,(ii)变异型目标的定量方法,(iii)组合物,和(iv)实例。
i.典型分析配置
该部分提供了典型扩增分析配置的概述,其在具有或不含竞争物的条件下进行,并设计成检测和定量样品中目标的等位形式(例如至少一种变异型(例如至少一种突变型));见图1-4。
等位基因是相同基因或其他染色体区域的不同形式。野生型等位基因是生物群体(例如人类种群)中的基因或其他染色体区域的最普遍形式。变异型等位基因是野生型等位基因的序列变异。该变异型等位基因可以低于野生型等位基因频率的任意频率出现。在一些情形下,变异型等位基因的存在频率可低于1%,在该情形下,变异型等位基因可描述为突变型等位基因。目标(也称目标序列)可以是基因或其他染色体区域的任何合适区域,并可具有来源于至少一种第一等位基因(例如基因的一种或多种变异/突变型等位基因)的至少一种第一等位形式,以及来源于第二等位基因(例如基因的野生型等位基因)的第二等位形式。目标可具有任意合适长度,例如至少约30、40、50、75或100个核苷酸等。
图1-4显示了用于进行扩增分析优选进行各分解部分(如液体)数字分析的典型目标、引物、探针和竞争物配置的图示。每种引物置于上部并与目标末端区域进行垂直排列,每种引物在该区域通过杂交进行特异性结合。每种探针置于上部并与目标(或参照(见图4))的某个区域进行垂直排列,在不存在竞争物的情况下,探针通过杂交特异性结合至该目标的至少一种形式(例如野生型)(若存在)的该区域。每种竞争物置于上部并与目标的某个区域进行垂直排列,竞争物通过杂交结合至目标的至少一种形式(例如野生型)的该区域。每种形式的目标和每种探针或竞争物之间的垂直分离表明了(用于探针的)结合是否被竞争物阻断和/或结合是否被目标序列中的变异(例如突变)破坏。特别的,在扩增中和/或扩增后能够特异性结合且与给定形式的目标的结合未被阻断的每种探针或竞争物与对应的引物水平向排列。相反,在扩增中和/或扩增后不能特异性结合和/或与给定形式的目标的结合被阻止的每种探针或竞争物从引物垂直偏移并且与给定形式目标的间隔比结合发生时更远。
图1显示了用于检测数字扩增分析中的变异和野生型目标的数字扩增系统50的示意图。系统50不包含竞争物,并包括与使用竞争物(见图2-4)的其他系统的比较。系统50的任意合适方面可存在于图2-4中的基于竞争物的系统。
图1左部显示了由待分析样品提供的多核苷酸对或模板对52,54的部分视图。模板52,54源于相同基因或染色体区域的不同等位基因。模板包括相同目标(也称为目标序列或序列)的不同形式,例如野生型56和至少一种变异型,例如至少一种突变型58。类型56、58在序列变异60的至少一个位点不同(在突变型58中用“x”表示),其可以为多态性或突变(例如删除、插入、取代或其组合)等等。野生型56和突变型58的序列在其他方面可以相同。删除、插入或取代可移除(删除)、添加(插入)或替换(取代)任意合适数量的核苷酸,例如至少1个、2个、3个、4个或5个等等。
目标的类型56、58可以用包含在各分解部分中的一种或多种引物进行扩增。例如,在描述的实施方式中,相同的引物对(例如寡核苷酸引物),即正向引物62(“f”)和反向引物64(“r”)相互配合以准备好每种形式目标的扩增。该扩增产生了每种形式目标的副本,也称为扩增目标或每种目标形式的扩增子。引物可限定端点并因此限定每种目标形式的尺寸,且可结合至目标的各自的另一端。在一些实施方式中,目标的每种形式可用相同的引物进行扩增,其同时作为正向和反向引物。相同的引物可引导扩增,例如,模板52、54的每个末端都结合至相同连接子。
可通过一个或多个包含在各分解部分中的探针的存在检测扩增。在描述的实施方式中,一对探针66、68允许包含突变型58的分解部分与那些包含野生型56的区分开。
每个探针66、68可具有序列识别部分70,其能够特异性结合(例如杂交)至至少一种形式的目标的某区域。部分70可通过寡核苷酸或其类似物提供。探针66的部分70并非类型特异性的,且能够与目标的任意形式杂交。探针68的部分70是野生型特异性的,不与突变型目标杂交。
每个探针66、68可以为标记探针,其包括提供可检测信号的标签72。每个标签可连接至序列识别部分70(例如共轭或非共价连接)。探针的标签可相互区分。例如,在描述的实施方式中,每个标签72是不同结构的光致发光体74、76,例如荧光团,发出光谱可区分信号78或80。每个探针和/或序列识别部分70还可以与能量传递伴侣,例如淬灭子82或第二光学发光体关联(例如共轭)。通过光致发光能量共振转移,淬灭子82可减少从每个光致发光体以邻近依赖方式检测的光致发光量。相应的,在一些实施方式中,在扩增过程中通过聚合酶催化的探针剪切(例如水解)可从淬灭子中分离光致发光体从而增加信号。在其他实施方式中(例如具有分子信标探针),将探针结合至扩增目标产生的探针构象改变引起信号增加。作为能量受体的第二光致发光体如果存在于探针中,也可发出可检测信号并因而可被描述为标签。
在每种目标形式扩增后检测到的信号78、80图示于图1的右部。最初包含至少一个野生型56副本的部分在扩增目标中提供与探针66和68的结合位点,并因而对于从每个探针的标签(此处为光致发光体74或76)检测的信号78、80呈阳性。相反,最初包含至少一个突变型58副本但不含野生型56的副本的部分在扩增目标中仅提供探针66的结合位点,并因而仅对从探针66的标签(光致发光体74)检测到的信号78呈阳性。
显示于图1中的分析配置可能具有某些缺陷。首先,仅基于一个信号(即信号80)的强度来区分野生型和突变型56、58。相应的,一旦野生型的信号80波动至阈值以下,野生型会被错误鉴定为突变型,突变型的假阳性比例可能很高。因此,在一些情形下,计算的突变型数量可能被高估。第二,接收两种目标形式的副本的每个分解部分产生与仅包含野生型的分解部分相同的信号构型,造成错过一些突变型的副本。因此,在一些情形下,计算的突变型数量可能被低估。通过高度稀释样品最大限度减少在相同个体分解部分共占两种目标形式形成的分解部分可避免这种低估,但是该更高稀释度使得分析效率更低。第三,分析系统50不能被有效用于主体相的动力学分析(例如,实时pcr),相反需要数字实现来定量突变型。
图2-4显示了基于竞争物的系统,其克服了一些或所有上述系统50的缺陷。相应的,图2-4的每个系统可用于实现主体相的动力学分析或者分解部分中的数字分析。
图2显示了用于检测变异和野生型目标56、58的另一扩增系统90的示意图。系统90可具有上述系统50的合适的元件和特征组合。例如,系统90利用非类型特异性的探针66和系统50中的野生型特异性探针68。(探针66可与每种目标形式(例如与各种形式杂交时具有相同融化温度)同等互补,和/或至少与每种目标形式部分互补或完全互补。)然而,野生型探针68配置成竞争物92(也被称为探针竞争物),其与探针66竞争与野生型56至少部分重叠区域的结合。竞争物92配置成在于野生型56结合中战胜探针66,使得探针66和野生型的结合实质性减少,本文描述为被阻断。探针68/竞争物92可以至少部分或全部与野生型56(或其他等位形式)互补。
竞争物92和探针66可形成探针的结合层级,竞争物92(探针68)相比探针66占优势。在一些实施方式中,可引入一种或多种另外的探针,以形成三种或更多种探针结合野生型的相互重叠区域的层级制度。具有三种或更多种探针,在分析中可分析更大的区域(例如更大的突变热点)和/或突变可更精准的定位。
与探针66和野生型结合相比,竞争物92可更稳定的结合至野生型56。换而言之,竞争物92与野生型杂交时可具有比与野生型杂交的探针66更高的熔解温度。相应的,竞争物92的序列识别部分70(例如寡核苷酸)可由比探针66的部分70更多的核苷酸组成,可富含更多gc,可具有不同的碱基结构(例如肽核酸),或者其组合,等等。
在野生型56中的竞争物92和探针66的各自结合位点可重叠任意数量的核苷酸,例如至少3、4、5、7或10个核苷酸,等等。在一些实施方式中,竞争物92的部分70的至少四分之一、三分之一或二分之一的核苷酸可结合至野生型56上探针66结合的相同区域。在一些实施方式中,探针66具有至少5、7或10个按顺序排列的连贯的核苷酸,这也出现于竞争物92中。
探针66和竞争物92都具有合适的熔解温度,以与一种目标形式杂交。根据使用的探针类型和/或进行信号检测的温度,熔解温度可高于或低于退火温度和/或目标进行扩增的延伸温度。例如,通过扩增过程修饰(例如降解或延伸)的探针可具有一熔解温度,用于与一种目标形式杂交,该温度高于目标扩增的退火/延伸温度。相反,未通过扩增过程修饰的探针(分子信标探针)可具有一熔解温度,用于与一种目标形式杂交,该温度低于目标扩增的退火/延伸温度。
从分析系统90检测的信号图示于图2的右边,应该与图1的那些进行对比。由于探针66和竞争物92与每种目标形式的结合是相互专一的,每种目标形式的扩增提升了两种标签(光致发光体74和76)中的仅一种的信号。如果野生型56扩增了,信号80会增强。如果野生型58扩增了,信号78会增强。如果在各分解部分中进行分析,包含56和58形式的分解部分将具有增强的两种信号并将与仅包含野生型56或仅包含变异型58的分解部分区分开。相对于系统50的系统90可具有变异型假阳性的更低比例并可允许在更高浓度目标的条件下进行分析并且需要更少的分解部分获得相同或更精确结果。
可分析信号78、80以确定包含(或不包含)突变型目标的各分解部分的第一数量以及包含(或不含)野生型目标的各分解部分的第二数量。目标的一种或两种形式的水平可基于第一数量和/或第二数量进行计算。在一些实施方式中,基于第一数量和第二数量,可计算突变型目标和野生型目标的相对副本数量。例如,可计算第一和第二数量的比例作为相对副本数量。在其他情形下,两种数量的一种可为算法的输入值,例如泊松算法,其计算一种或两种目标的水平,然后计算突变型的相对副本数量,作为突变型和野生型目标的水平的比例。
图3显示了用于检测变异和野生型目标56、58的另一扩增系统110的示意图。系统110可具有上述系统50和90的合适的元件和特征组合。系统110与系统90相同,除了相同标签、光致发光体74用于探针66和竞争物92中(探针68)。然而,当56、58型目标在各自分解部分扩增时,探针68配置成形成比探针66更强的信号78。例如,探针68分子相对于探针66的更大百分率可用光致发光体进行标记。或者,或另外,存在的探针68可超过探针66,使得探针66更加限制信号形成。在任何情况下,基于信号80的强度,仅包含野生型56的分解部分可与仅包含突变型58的分解部分区分开。包含两种形式的分解部分也可与仅包含一种形式的分解部分区分开。基于信号强度的多路复用分析的更多方面描述于上列交叉引用部分的文献中,其通过引用结合至本文,尤其是2013年2月14日公布的2013/0040841a1号美国专利公布文件;2014年6月26题公布的2014/178889a1号美国专利申请公布文件;以及2014年8月7日公布的2014/0221238a1号美国专利申请公布文件。
图4显示了用于检测变异和野生型目标56、58的另一扩增系统130的示意图。系统130可具有上述系统50、90和110的合适的元件和特征组合。然而,系统130可使用未标记竞争物92以阻断探针66与野生型56的结合。竞争物92仅具有序列识别部分70。另外,系统包括模板132,其提供另一目标,即参照目标,其被称为参照134。野生型和突变型目标56、58可用相同的正向和反向引物对扩增,如上所述,其在描述的实施方式中确定为f1和r1。参照134可用不同的正向和反向引物对f2和r2进行扩增。参照134的扩增可用探针136进行标记,例如包含光致发光体76的探针,而突变型58的扩增用携带光致发光体74的探针66进行检测,如上述图2所示。
作为每种目标扩增结果检测的信号78、80图示于图4的右边。突变型58和存在和扩增通过信号78报告,参照134的通过信号80报告。
野生型56的存在和扩增不通过任意信号报告。因此,分析可在野生型56扩增或未扩增情形下进行。在一些实施方式中,竞争物92可配置成相对于突变型58,选择性阻断野生型56的扩增。例如,竞争物92可抵抗用于扩增的聚合酶的降解,因而允许竞争物阻止引物f1的延伸。竞争物因而可为降解的标准寡核苷酸,或者抵抗降解的肽核酸或锁核酸,等等。
相同样品可提供参照134和56、58型目标,且可存在于相同基因组副本中。该参照可与56、58型目标没有重复,使得引物f1和r1、探针66、和竞争物92不会特异性结合至参照。该参照可通过与目标不同(或相同)的基因提供,且样品的每个基因组可具有已知或假定的副本数量。因此,突变型58的相对副本数量可相对参照134进行计算,其允许确定每个基因组的突变型58的副本数量。
可使用相同组的各分解部分(或未分割的相同体相)检测突变型58和野生型56(或参照134),如上所述。另外,相同样品的各分解部分可配置成两组不同的分解部分(或者两个不同的体相)。突变型58可用其中一组(或体相中的一个)进行分析,野生型56或参照134用另一组(或其他体相)进行分析。使用不同组分解部分(或不同体相)允许在各组之间改变样品的稀释度,以增加稀少突变的灵敏度。
ii.定量目标变异型的方法
该部分描述了在扩增分析中定量变异型(或其他等位形式)目标的典型方法,其可为在各分解部分例如液滴中或者在体相中进行的数字分析;见图5的流程图140。在该部分描述的步骤可以任意合适的顺序和组合进行,具有本文其他部分描述的任意分析配置、组分和特征,例如部分i、iii和iv中描述的。
反应混合物制备。可制备包含至少一种探针、竞争物(其可以是或不是探针)和相同目标的等位形式的反应混合物,如142所示。目标的等位形式可包括相同目标的野生型和至少一种变异型(例如至少一种突变型)。该反应混合物可以是扩增混合物,配置成支持每种目标形式的扩增并因而可包含通过存在于反应混合物中的样品提供的模板进行目标扩增所需的所有试剂。该反应混合物也可包含另一目标(即参照)扩增所需的所有试剂(见图4)。该试剂在下文进行详细描述,其可例如包括一种或多种引物、多种dntp和/或ntp,多聚酶(例如rna聚合酶或dna聚合酶,任意一种可以是或非热稳定的)、缓冲液、水、表面活性剂,等。
在反应混合物中的聚核苷酸作为目标/参照扩增的最初模板,并可具有任意合适的结构和特征。在目标/参照扩增前的反应混合物中,每种模板可至少为主要单链或至少为主要双链,等。例如,每种模板可至少主要为dna(例如基因组dna、线粒体dna或cdna),至少主要为rna(例如基因组rna、转录rna、信使rna、trna、核糖体rna等),其组合(例如dna-rna混合物)等等。每种模板的分子可以是长度一致(例如通过限制性酶消化或全长使用),或者尺寸不同(例如通过随机破碎,例如用非特异性核酸酶剪切、消化等)。可通过核酸样品提供模板,该核酸样品是不同核酸(不同多核苷酸)的复合混合物,具有用于目标/参照扩增的少量模板。核算样品可主要由基因组dna、线粒体dna、基因组rna、总rna、核rna、细胞质rna、信使rna或其任意组合,等等。
反应混合物也可包括一种或多种引物,该引物与野生型和变异型模板以及每种目标互补并结合至其上(可选的,一种或多种引物与参照互补并结合至其上)。当结合至模板(和/或目标/参照)分子形成反应产物,例如扩增目标/参照副本的至少一部分(例如一种互补链),也被称为扩增产物,引物可在反应混合物中通过聚合酶延伸。引物可包括用于目标扩增的正向和反向引物,其可以是相同引物或不同引物。该正向引物和反向引物可限定每种目标形式的末端。不同正向和反向引物对可限定扩增的参照的末端(见图4)。在一些实例中,目标引物对变异型和野生型模板与每种目标形式具有相同量的互补性,使得引物不能区分变异型和野生型模板和/或变异型和野生型目标形式。本文公开的任何引物可以为任何合适长度的寡核苷酸,例如至少10、15或20个核苷酸,等等。
反应混合物的制备可包括或被描述为制备样品。制备样品可包括任何合适的样品处理,包括采集、稀释、浓缩、纯化、裂解、冷冻、提取,与一种或多种分析试剂混合,至少进行一个预反应以制备用于分析中的一个或多个反应的样品,或其任意组合,等等。制备样品可包括使得样品能够进行后续的一个或多个反应,例如一个或多个酶催化反应和/或结合反应。
在一些实施方式中,制备样品可包括混合样品与用于扩增的试剂以及一种或多种报告子(也被称为信号试剂)用于报告扩增是否发生。用于扩增的试剂可包括一种或多种用于合成扩增的目标/参照的引物、多种dntp和/或多种ntp、至少一种酶(例如聚合酶、连接酶、反转录酶、限制性酶或其组合,每种可以是或不是热稳定的),等。因此,制备样品可使得样品(或其部分)能够扩增样品中的每种目标形式和/或参照(或其部分)(若存在)。用于报告的试剂可包括(a)同时特异性结合至变异型和野生型目标的标记探针,(b)特异性结合野生型目标(相对于变异型目标)的标记探针,和/或(c)特异性结合参照的标记探针。制备用于报告的样品可使得样品能够报告,或者进行分析用于确定变异型目标、野生型目标和/或参照是否发生扩增,以及可选的,确定该任意扩增的程度。每种探针可包括用于特异性结合目标/参照的序列识别部分(例如寡核苷酸)和结合至序列识别部分的可检测标签。例如,该标签可被光学检测,例如通过检测涉及标签的发光、吸收、散射、极化、能量转移,等等。在示例性实施方式中,标签可以是光致发光的(即光致发光部分),例如荧光团。
术语“发光”是指不仅仅归因于发光体温度的发光。示例形式的发光包括光致发光、化学发光、电致发光等。“发光体”是任何原子、相关原子团、基团、分子或能够发光的相关分子团。光致发光是响应于激发光辐射而产生的任何发光,包括荧光、磷光等。相应的,发光体可以是光致发光体,例如荧光团或磷光团,等等。
报告子可具有任何合适的结构和特性。每个报告子可以是特异性结合至核苷酸序列的探针。该探针可包括核酸。例如,探针可包括寡核苷酸和与寡核苷酸关联的发光体(例如,发光体共价结合至寡核苷酸),以标记寡核苷酸。该探针也可以包括或不包括发光体的能量转移搭档或以其他方式与其关联,例如淬灭子,其可以或不可以发光。该探针可能够特异性结合至目标(包括扩增目标)或者参照(包括扩增的参照)。该探针可作为或不作为扩增引物,其形成分析中产物(扩增子)的一部分。示例性标记探针包括
在一些情形下,至少一个报告子可以是通用报告子,例如荧光染料,其结合并标记相对非特异性的核酸。例如,荧光染料可未共价结合至提供重要序列结合特异性的寡核苷酸。荧光染料可为大沟接合子、小沟接合子、嵌入剂、或外部接合子等。相对于单链核酸,荧光染料可优先结合至双链核酸和/或当结合至双链核酸时可展示出相对于单链核酸的光致发光特性(密度)的更大改变。合适的示例性染料包括发光蓝色素、菲啶、吖啶、吲哚、咪唑等,例如dapi、
反应混合物的形成可包括形成包含目标/参照扩增所需的所有组件的连续相或主体相。或者,或另外,反应混合物的形成可包括在孔中融合各分解部分,例如液滴(见下文)或流体,以混合反应混合物的各组件。
反应混合物可作为主体相(可互称为连续相)进一步进行处理。另外,反应混合物可形成为分散相,其由通过固相(例如容器壁)、液相(例如乳液的载体相)、气相或其组合分离的多个部分组成。
目标可交替的称为分析物、目标序列或在一些情形下,称为参照。
分解部分形成可形成提供目标/参照模板的反应混合物和/或样品的各分解部分,(也称为“创建”),在144中有所指出。用另一种方式陈述,该反应混合物和/或样品可分成多个分解部分以形成分离的液体体积,每体积液体包含分解部分反应混合物和/或样品。
形成的各分解部分可在“局部占据”中包含该目标的至少一种变异型(变异目标形式)、野生型目标(野生型目标形式)和/或参考,这意味着各分解部分的子集(一个或多个)不包含目标形式/参照的副本且各分解部分的剩余分解部分包含目标形式/参照的至少一个副本。例如,各分解部分的另外子集(一个或多个)可包含目标形式/参照的单个副本(仅一个副本),且可选的,除其外的各分解部分的另外子集(一个或多个)可包含两个或更多个目标形式/参照副本。术语“局部占据”允许但非必须稀释提供目标形式/参照的样品/反应混合物,并不局限于在任意分解部分中仅含一个目标形式/参照的情形。相应的,当形成分区时,局部占据中包含目标形式/参照的各分解部分可在每分解部分中包含平均数量多于或少于目标形式/参照的约1个副本、2个副本、或3个副本等。目标形式/参照(和模板)的副本可在各分解部分中随机分布,其可描述为泊松分布。
分解部分的形成可涉及将包含多至所有样品/反应混合物的任意合适部分分布至各分解部分中。每个分解部分从其他分解部分空间上分离,且可以是和/或包括与其他分解部分液体体积分离的液体体积。可通过流体/液体相,如乳液的连续相,通过固相,例如至少一容器壁或其组合等,将各分解部分进行分离。在一些实施方式中,各分解部分可以是置于连续相中的液滴,使得液滴和连续相共同形成乳液。
各分解部分可由任意合适的程序通过任意合适的方式形成,具有任意合适的特性。例如,各分解部分可通过以下方式形成:通过流体分配器,例如移液器,至少一个液滴生成器,其具有孔口和/或通道交叉(在该处形成液滴),通过搅动样品/反应混合物(例如摇动、搅动、超声等)等等。相应的,各分解部分可连续、并行或分批形成。各分解部分可具有任意合适的体积。各分解部分可具有相同或不同体积。具有相同体积的示例性分解部分是单分散的液滴。各分解部分的示例性体积包括平均体积少于约100、10或1μl,少于约100、10或1nl,或少于约100、10或1pl,等。
能够进行每种目标形式和/或参照的扩增的各分解部分可直接由包含目标和/或参照的副本的主体相形成,或通过多个步骤形成。在一些情形下,形成分解部分的步骤可包括将主体相分成单独的流体体积(例如液滴)其在局部占据中包含至少一种突变目标形式和/或野生型形式。流体体积可以是各分解部分本身或者组成各分解部分。例如,流体体积可以是第一组流体体积,形成各分解部分的步骤可包括将第一组单个的流体体积与第二组的单个流体体积混合。第二组可包括一种或多种用于扩增一种或多种目标的试剂,例如至少一种用于扩增至少一种目标、探针等的引物。混合步骤可包括单独将第一组流体体积与第二组流体体积融合,例如将包含模板的液滴与包含用于从模板扩增一种或多种目标的引物的液体融合。
目标扩增。当竞争物阻断探针与野生型目标结合时,变异型目标可进行扩增,如146所示。扩增的变异型可以是多种不同的变异形式,其通过分析不能进行区分。扩增步骤也可扩增野生型形式和/或参照。在一些实施方式中,野生型形式的扩增可被竞争物(见图3)特异性阻断,例如当竞争物设计为抵抗聚合酶的降解。
可在各分解部分(分散相)或连续相中进行扩增,例如在未形成分解部分的反应混合物中。如果在个分解部分中进行,每种目标型和/或参照的扩增可仅发生于各分解部分的子集中,例如少于各分解部分的约四分之三、二分之一、四分之一或十分之一等。每种目标形式和/或参照的扩增可仅发生于包含至少一种目标形式/参照(即包含至少一种对应于目标形式/参照的模板副本)的分解部分中。
扩增可以在或不在等温条件下进行。在一些情形下,各分解部分中的扩增可受热循环激励,即将各分解部分置于多个加热和冷却循环中。各分解部分可在变性温度(例如大于约90摄氏度)、退火温度(例如,约50-75摄氏度)和/或延伸温度(例如约60-80摄氏度)下培养一个或多个循环。在一些实例中,各分解部分可进行热循环以促进聚合酶链反应和/或连接酶链反应。合适的示例性恒温扩增方法包括基于核酸序列扩增、转录介导扩增、多重置换扩增、链置换扩增、滚环扩增、dna环介导扩增、解旋酶依赖扩增、单引物扩增,等等。
信号检测。信号可通过探针标签检测,如148所示。如果未形成分解部分,信号可从主体相进行检测。例如,信号可在多循环过程中的动力学分析(实时)中进行检测以确定扩增突变型至阈值(例如最大量的一半)所需的循环数。使用各分解部分,信号可从完整的各分解部分进行检测,而标签包含在各分解部分中,可选的在端点分析中。更具体而言,可从分析中的每个报告子/探针的至少一个标签检测信号以收集代表在主体相或单独分解部分中的一个或多个目标形式和/或参照的扩增的数据。
信号可代表任意检测形式的能量,例如电磁的、电动的、磁力的等。在示例性实施方式中,信号代表检测到的可见光、紫外光和/或红外光的性能。
至少部分对探针发光体的光依赖可被检测到。可直接通过发光体发光,或者可通过发光体的能量转移搭档发光。光检测可描述为扩增数据收集。可通过检测由单独的完整分解部分或主体相反应混合物发出的光收集数据。可通过响应于各分解部分或反应混合物的激发光辐射而发光,用于发光体或其能量转移搭档。可从各分解部分或反应混合物收集某个光域(一种光通道)、两个不同光域(两种光通道)(例如每一种用于一种目标/探针)等的发光数据。不同的光域由相互不同波长和/或波段定义。
光通道可代表特定的发光和测光的检测区域。检测区域可通过用于检测发射光的波长/波段(即波长区域)表征。如果脉冲激发光用于检测区域以诱导光发射,检测区域可通过激发光来发光的波长或波段和/或一时间间隔表征,在该时间间隔内检测与每个光脉冲相关的光发射。相应的,不同的光通道可与激发光的波长/波段不同,与检测到的发射光的波长/波段不同,和/或与时间间隔不同,在该时间间隔内,相对于激发光的每个脉冲的发射光被检测,等等。
数据收集可包括从反映混合物的各自分解部分检测一种或多种信号。该信号可代表光性能,例如密度、极化或光寿命等。可选的,信号可包括在两种或更多不同的光通道中(例如在不同波长/波长范围(波段)和/或颜色区域)从用于相同和/不同目标的探针/报告子收集的数据。从每个探针/报告子检测的光可以是通过发光体(例如荧光体)发射的光。在给定光通道中检测的光可以备检测,使得从不同探针/报告子的光被叠加或积累而不归因于特定探针/报告子。因此,给定通道的信号可以是复合信号,其代表两种、三种、四种或更多种目标或目标形式。在其他情形下,用于目标和/或目标形式的信号可在不同光通道中被检测。
信号可代表从各分解部分中的一种或多种探针/报告子发射的被检测光。该一种或多种探针/报告子可报告由信号代表的两种或更多种特定扩增反应中的至少一种是否在一分解部分中发生,并因此报告对应两种或更多种特定扩增反应的两种或更多种特定目标或目标形式的至少一种的至少一个副本是否存在于该分解部分中。对应于报告子的信号的水平或幅度可被分析以确定至少一种特定扩增反应是否已发生并且特定目标或目标形式的一种的至少一个副本是否存在。信号的水平或幅度可在各分解部分中不同,其根据至少一种特定扩增反应是否发生以及至少一种特定目标或目标形式是否存在于每个分解部分中。例如,对特定目标或目标形式测试为阳性的分解部分仅可产生在给定阈值以上和/或给定范围内的信号值。可在任意合适的时间分析各分解部分并检测信号。示例性时间包括在分析的反应相的末期(端点分析),当反应进行完成且数据不再变化时,或者在某个更早的时间,只要数据充分、可靠的分离。
可在任意合适的条件下,从多个分解部分(即仅子集或所有分解部分)中收集数据。所有的数据可在大约相同温度下,从多个分解部分中进行收集,例如在低于每个扩增子的熔解温度以下的温度,和/或低于约50摄氏度,等等。
获得分割信号值。从每种标签或每种光通道检测的信号(例如在每种波长或波长区域)可被处理以获得用于每个分解部分的信号值。例如,信号可被解析以确定对应于每个分解部分的信号分解部分。然后,该分解部分的信号值可从该信号分解部分获得,例如通过整合信号分解部分,提取信号分解部分中的信号的最大值或平均值。在任何事件中,每个分解部分可被分配一信号值用于每个标签和/或光学通道。与每个分解部分关联的信号值的大小用于确定该分解部分是否包含目标的变异型,以及可选的,该分解部分是否包含野生型和/或参照。
列举分解部分。多个包含至少一种变异型目标的分解部分可通过从标签检测的信号确定,如150所示。包含野生型目标的多个分解部分和/或包含参照的多个分解部分可被确定,其基于从相同标签和/或至少一种其他标签检测的一种或多种信号(例如,见图2-4)。
每种数量的分解部分可基于从一个或多个信号获得的该分解部分信号值确定。例如,每个分解部分的一个或多个信号值可与至少一种阈值(和/或范围)比较以确定该分解部分是否包含给定目标形式或参照。
用于每种目标形式和/或参照的分解部分的数量可通过相同组分解部分确定。或者,可利用不同组的分解部分确定包含野生型目标和/或参照的分解部分的数量。例如,样品在一组分解部分中的更低稀释度提供稀有突变型的检测灵敏度,而相同样品在另一组分解部分中可提供更精确的确定野生型/参照的水平。
对一种或多种目标形式和/或目标测试为阴性或阳性的分解部分总体(交替称为簇或带)可基于其信号值进行鉴定。鉴定可通过使用算法的数据处理器(例如鉴定数据中的模式(例如部分簇)的算法),通过用户,或其组合进行。在一些情形下,数据处理器可产生或输出(例如展示)信号值绘图(例如线形图、2d散布图、柱状图等)。用户然后可基于图限定每种群体的范围,例如通过图形用户界面限定群体的范围,和/或通过输入值(例如代表信号值的阈值/范围)限定每种群体的范围。每种群体范围可通过一种或多种范围值、围绕群体的几何图形(多边形、椭圆形等)等限定。算法可用于用或不用用户输入来限定群体范围。
各分解部分群体的鉴定可包括将每分解部分分配给多个预定箱中的一个,每个箱对应具有不同目标形式/目标内容的不同分解部分群体。该预定箱可代表用于目标形式/目标的阴性和阳性的所有组合。
计算变异型数量。可计算至少一种变异型的数量,如152所示。计算可基于确定含有变异型的分解部分的数量(如果分析通过各分解部分进行),或者基于从探针标签检测到的信号(如果分析在主体相中进行)。
数量可以是变异型的绝对或相对水平。绝对水平可例如是变异型的多个分子/副本,或变异型的浓度(例如每分解部分或每单元体积),等。相对水平可例如是变异型相对于野生型或参照目标的相对副本数量,等。相对水平或者也可以是每个基因组、每份质量的核酸(例如每份质量的基因组dna)等表达的变异型的相对数量。
可计算相对副本数量,在一些情形下,通过直接比较(例如取一比例)包含变异型的分解部分数量和包含野生型或参照目标的分解部分的数量。在其他情形下,各分解部分包含的每种目标形式和/或参照的分子或副本数量(或每分解部分的分子/副本平均数量)可从包含目标形式/参照的分解部分的数量进行计算,下文将详细描述。然后,分子或副本数量(或每分解部分的平均数量)可进行比较(例如作为一比例)以计算相对副本数量。
该水平可代表扩增前存在的目标或目标形式的水平。水平的确定可(或可以不)基于在各分解部分中具有泊松分布的每种目标或目标形式。例如,每种水平可以是代表对于目标或目标型呈阳性(或阴性)的分解部分的总量,或者浓度值,例如代表每分解部分或单元体积的目标或目标型的平均副本数量的值,等。该分解部分的数据可进一步用于(例如直接和/或作为浓度数据)通过任意合适算法评估样品的样品副本数量(cn)和变异副本数量(cnv)或其他性能。
每种目标(或目标形式)的水平(例如浓度)可用泊松统计确定。该浓度可表述为相对于各分解部分(或反应混合物)和/或相对于提供目标的样品。目标在分解部分中的浓度可从阳性分解部分分数(或等效的,阴性分解部分分数)计算,通过假定目标副本(在扩增前)在分解部分中具有泊松分布。根据该假设,具有k模板副本的分解部分的分数f(k)通过以下方程给出:
此处,λ是分解部分中目标的浓度,表述为每分解部分中目标副本的平均数量(扩增前)。简化的泊松方程(也称为算法)可来源于上述更多的通用方程,且可用于从阳性分解部分的分数确定目标浓度。可用的示例性泊松方程如下:
其中n+是对给定目标呈阳性的分解部分的数量(即分解部分计数),且ntot是对目标呈阳性或阴性的分解部分的总数量。ntot等于下述的总和:(a)目标的n+和(b)对目标呈阴性的分解部分的数量或n–。n+/ntot(或n+/(n++n–))等于f+,其为对模板呈阳性的分解部分的分数(即f+=f(1)+f(2)+f(3)+…)(见方程1),且其为具有至少一个模板副本的分解部分的测量的概率估值。可用的另一示例性泊松方程如下:
其中n–和ntot如上所定义。n–/ntot等于f–,阴极分解部分的分数(或1–f+),且是不含目标副本的分解部分的测量的概率估值,且λ是如上所描述的目标浓度。
上述方程2和3可以被重新排列以获得以下:
λ=ln(ntot)-ln(ntot-n+)(4)
λ=ln(ntot)-ln(n-)(5)
在分析中的每种目标的浓度能够用方程2-5任意一种用获得的ntot和n–值或等效的,n+值(即分解部分计数)确定,用于每种目标。在一些情形下,用于ntot的值(总的分解部分计数)对于每种目标可以是相同的。在其他情形下,用于ntot的值可以是不同的,例如如果由于群体重叠导致一些群体从总计数中排除。在一些实施方式中,ntot可以等于所有群体的混合,即鉴定的所有群体的总的分解部分计数。
在一些实施方式中,目标(和/或模板)的水平估值可直接从阳性分数获得,无需使用泊松统计。特别的,阳性分数和浓度(每分解部分的副本)随着浓度降低收敛。例如,阳性分数为0.1,用方程2确定的浓度为约0.105,差异仅为5%;阳性分数为0.01,浓度确定为约0.01005,十分之一的较小差异仅为0.5%。然而,使用泊松统计可提供更精确的浓度估值,尤其是具有相对较高的阳性分数,因为泊松统计考虑了相同分解部分中的相同目标(或目标形式)/模板的多个副本的产生。
可适合于本发明的系统的样品制备、分解部分形成、扩增、信号检测、信号处理、获得分解部分计数和计算水平/数量等的其他方面可在本发明中其他地方和交叉引用中的参考文献中进行描述,通过引用进行结合。
ⅲ.组合物
该分解部分提供本发明的示例性组合物。每种组合物可包含或不含扩增核酸目标(例如通过pcr)所需的所有试剂。
该组合物可包括至少一体积的流体或共同包含野生型和至少一种变异型目标的多个分离的分解部分。目标的变异型(且可选的,野生型)可存在于各分解部分中的部分占据中。该体积的流体和/或每个分解部分可包含能够特异性结合每种形式目标的探针。该探针可被标记,例如具有光致发光体和/或淬灭子。该体积的流体和/或每个分解部分也可包含配置成特异性结合野生型(相对于变异型)且阻断探针与野生型结合的竞争物。竞争物也可为标记的探针。
该体积的流体和/或每个分解部分进一步可包含扩增变异型目标的试剂。该试剂可包含至少一种或相同对引物以扩增每种形式的目标。该试剂也可包括聚合酶,例如热稳定聚合酶,和多个dntp,等。
这些分解部分可通过连续相进行相互分离,例如与各分解部分不相溶的液相。液相可包括油和优选的表面活性剂。
iv.实例
下述实例表述了用于用竞争物进行的变异测定的扩增分析的选择的方面和实施方式。这些方面和实施方式用于阐明目的并不限制本发明的整个范围。
实例1egfr外显子19突变型的数字分析
该实例描述了示例性数字扩增分析,用于检测表皮生长因子受体(egfr)的外显子19的突变的存在,参见图6-8。
图6显示了垂直排列的序列组((seqidnos:1-17),阐明了用于检测人egfr外显子19中的突变的扩增分析的示例性实施方式。顶部的序列(seqidno:1)是存在于人野生型egfr的外显子19中的60个核苷酸的序列,且包含用于删除的热点。
用于分析的竞争物(seqidno:2)和探针(seqidno:3)的核苷酸序列列于野生型序列下方。竞争物和探针可用不同荧光体标记。例如,对于该实例中存在的数据,竞争物在5’末端用hex荧光染料标记,且探针在5’用fam荧光染料标记,每种染料共轭至相应寡核苷酸的核苷酸的5’末端。每种竞争物和探针也可共轭至3’的iowa
竞争物长度为28个核苷酸(12/28g或c),而探针长度仅为18个核苷酸(8/18g或c)。因此,当其每一种结合至野生型序列时,竞争物具有比探针显著更高的熔解温度。该探针和竞争物具有12个核苷酸的重叠,其小于竞争物长度的一半且大于探针长度的一半。
egfr的外显子19是促进癌变的突变热点。已鉴定的14个外显子19删除突变列于图6中,为seqidnos:4-17。相对于野生型被删除的核苷酸用虚线识别,插入核苷酸包括在括号中。每种删除移除野生型序列的10-19个核苷酸。竞争物显著覆盖了热点;与竞争物序列互补的野生型序列的最小的10个核苷酸从每种删除情形中移除,其有效清除了竞争物与每种相对于野生型的突变的结合。因此,显示的每种删除可在扩增分子中用本文列举的相同探针和竞争物检测。在某些情形下,更小的删除或者甚至是点突变也可被检测,但是本文显示的删除大小是用本文配置的分析更有效和更可信的检测到的。
92个核苷酸的egfr序列(seqidno:18)的扩增通过pcr在液滴中用taqdna聚合酶进行。19和20个核苷酸长度的正向引物(seqidno:19)和反向引物(seqidno:20)分别引导扩增。一连串液滴流过荧光检测器,从fam荧光染料和vic荧光染料在不同波长测定液滴的荧光,以提供随时间测量的fam染料信号和vic染料信号。对各自液滴获得的fam和vic值(任意单位(arb.))进行作图,获得图7和8的散布图,其中每个液滴的两个信号值(fam和vic)由散布图中的点位置表示。
图7显示了在液滴中的目标扩增后,从包含突变型和野生型外显子19egfr目标的液滴检测的液滴信号值的作图。突变型是149_egfr_l747_a750>p(seqidno:9)。两者均不含(阴性)、仅含突变型(突变)、仅含野生型(野生型)以及含两种形式的液滴集群在图中进行鉴定。
图8显示了从液滴检测的滴液信号值的作图,该液滴与图7相同但仅含野生型目标。在虚线椭圆鉴定的突变区域内没有假阳性液滴是可检测的(对比图7和图8)。突变型假阳性比例测定为仅约1/105液滴,这允许检测样品中的稀有突变。
实例2选定的实施方式
该实例描述了本发明选定的实施方式,呈现为一系列索引自然段。
第a1段。一种检测等位形式目标的方法,该方法包括:(a)形成共同包含至少一种第一等位形式和第二等位形式目标的多个分解部分,每分解部分包含(i)能够特异性结合第一和第二等位形式目标的相同探针和(ii)配置成选择性结合至相对于该至少一种等位形式的第二等位形式且阻断探针与第二等位形式结合的竞争物;(b)在各分解部分中扩增该至少一种第一等位形式目标;(c)当标签包含在各分解部分中时从探针标签检测信号;以及(d)基于该信号,确定对于该至少一种第一等位形式呈阳性的分解部分数量或者对该至少一种第一等位形式呈阴性的分解部分数量。
第a2段。根据第a1段所述的方法,其中探针和竞争物配置成与第二等位形式目标的部分重叠区域杂交。
第a3段。根据a1或a2段的方法,其中至少一种第一等位形式包括在与竞争物互补的区域内具有两个或更多个核苷酸删除的相对于第二等位形式的第一等位形式。
第a4段。根据a1-a3段任意一项的方法,进一步包含基于测定的数量计算该至少一种第一等位形式的水平。
第a5段。根据第a4段所述的方法,其中计算步骤包括计算该至少一种第一等位形式的相对副本数量。
第a6段。根据第a5段所述的方法,其中相对副本数量是相对于第二等位形式或非目标形式的参照进行计算。
第a7段。根据a5段所述的方法,其中各分解部分是由包含一分解部分样品的第一混合物形成的第一组分解部分,该样品包括每一种等位目标形式,该方法进一步包含从含分解部分样品的第二混合物形成第二组分解部分的步骤,其中该数量从第一组确定,其中计算步骤基于第一组确定的数量,以及对第二等位形式或参照呈阳性的第二组分解部分数量或对第二等位形式或参照呈阴性的第二组分解部分的数量。
第a8段。根据第a7段所述的方法,其中该至少第一等位形式是一种或多种变异型目标,其中第二等位形式是野生型目标,且其中样品在第二组分解部分中比在第一组分解部分中具有更高的稀释度。
第a9段。根据a1-a6段任一项所述的方法,探针是第一探针,其中竞争物是第二探针,其中检测信号的步骤包括从第一探针标签和第二探针标签检测一种或更多种信号,进一步包含基于该一种或多种信号中的至少一种确定对第二等位形式呈阳性的分解部分数量,或者对第二等位形式呈阴性的分解部分数量。
第a10段。根据第a9段所述的方法,进一步包含基于确定的第二等位形式的数量计算第二等位形式水平。
第a11段。根据a10段所述的方法,其中计算步骤包括基于确定的两种数量,确定该至少一种第一等位形式相对于第二等位形式的副本数量。
第12段。根据第a11段所述的方法,其中确定该至少一种第一等位形式的副本数量的步骤包括计算对该至少一种第一等位形式呈阳性的分解部分的数量与对第二等位形式呈阳性的分解部分的数量的比例。
第a13段。根据第a10段所述的方法,其中确定该至少一种第一等位形式的相对副本数量的步骤包括基于泊松算法计算该至少一种第一等位形式的水平和第二等位形式的水平的步骤,以及计算该至少第一等位形式水平和第二等位形式水平的比例的步骤。
第a14段。第a9-a13段中任一项所述的方法,其中第一探针和第二探针每一种用相互不同的光致发光体标记。
第a15段。a1-a14段中任一项所述的方法,其中与目标第二等位形式杂交的竞争物的熔解温度大于与目标第二等位形式杂交的探针的熔解温度。
第a16段。根据a1-a15中任一项所述的方法,其中每个分解部分形成时包含的竞争物摩尔数比探针多。
第a17段。根据第a1-a6和a9-a16中任一项所述的方法,其中目标的每种等位形式由包含非目标的参照的样品提供,其中扩增步骤包括扩增参照的步骤,该方法进一步包含计算该至少一种第一等位形式相对于参照的相对副本数量。
第a18段。根据第a1-a17段中任一项所述的方法,其中扩增步骤包括用相同引物对扩增目标的每种等位形式的步骤。
第a19段。根据第a1-a18段中任一项所述的方法,其中各分解部分是液滴。
第a20段。根据a1-a19中任一项所述的方法,其中扩增步骤降解了至少一摩尔分数的探针。
第a21段。根据第a1-a20段中任一项所述的方法,其中扩增步骤降解了至少一摩尔分数的竞争物。
第a22段。根据第a21段所述的方法,其中当扩增步骤结束时竞争物的摩尔分数没有变化。
第a23段。根据第a1-a22段中任一项所述的方法,其中扩增步骤通过聚合酶催化,该聚合酶在扩增步骤中催化了至少一摩尔分数的探针的降解,且其中竞争物抵抗由聚合酶催化的降解,使得等位形式目标的扩增被竞争物阻断。
第a24段。根据第a1-a23段中任一项所述的方法,其中探针能够在熔解温度以下(另称为杂交温度)特异性结合至每一种第一和第二等位形式目标。
第a25段。根据第24段所述的方法,其中扩增步骤在至少部分低于熔解温度下进行。
第a26段。根据第a24或a25所述的方法,其中扩增步骤包括使至少一种引物退火至第一和第二等位形式目标的步骤和在退火后延伸该至少一种引物的步骤,且其中退火步骤在低于熔解温度下进行。
第a27段。根据第a24-a26段中任一项所述的方法,其中扩增步骤包括延伸至少一种杂交至第一和第二等位形式目标的引物的步骤,以及其中该延伸步骤在低于熔解温度条件下进行。
第28段。根据第a24-a27段中任一项所述的方法,其中检测步骤在各分解部分低于熔解温度条件下进行。
第29段。根据第a24段所述的方法,其中扩增步骤在整体高于熔解温度条件下进行。
第a30段。根据第a29段所述的方法,其中扩增步骤包括通过多个热循环使各分解部分热循环的步骤,且其中各分解部分在每个热循环的整个过程高于熔解温度。
第b1段。一种检测等位形式目标的方法,该方法包括:(a)制备混合物,所述混合物包含(i)至少一种第一等位形式目标和一第二等位形式目标,(ii)能够特异性结合每种第一和第二等位形式目标的相同探针,以及(iii)配置成选择性结合至相对于该至少一种第一等位形式的第二等位形式且阻断探针与第二等位形式结合的竞争物;(b)分离至少一分解部分混合物至各分解部分中,其中仅各分解部分的子集的每分解部分包含该至少一种第一等位形式目标;(c)在各分解部分中扩增该至少一种第一等位形式目标;(d)当标签包含在各分解部分中时从探针标签检测信号;以及(e)基于该信号,确定对于该至少一种第一等位形式呈阳性的分解部分数量或者对该至少一种第一等位形式呈阴性的分解部分数量。
第c1段。一种检测等位形式目标的方法,该方法包括:(a)制备反应混合物,所述混合物包含(i)至少一种第一等位形式目标和一第二等位形式目标,(ii)能够特异性结合每种等位形式目标的相同探针,以及(iii)配置成选择性结合至相对于第二等位形式的该至少一种第一等位形式并且阻断探针与第二等位形式结合;(b)在至少一分解部分反应混合物中扩增该至少一种第一等位形式;(c)从探针标签检测信号;和(d)基于该信号确定至少一种第一等位形式的水平。
第c2段。根据第c2段所述的方法,其中检测信号的步骤包括在扩增完成前检测信号的步骤。
第c3段。根据c2段所述的方法,其中扩增步骤包括将反应混合物暴露于多个热循环的步骤,以及其中检测信号的步骤在两个或多个热循环的每一个当中和/或之后进行。
第c4段。根据c3段所述的方法,其中确定水平的步骤基于信号和进行的热循环数量之间的关系。
第c5段。根据第c1-c4段中任一项所述的方法,其中扩增、检测和确定步骤包括实时pcr分析。
第c6段。根据c1-c5段中任一项所述的方法,其中探针能够在熔解温度(又称为杂交温度)以下特异性结合至每种第一和第二等位形式目标。
第c7段。根据c6段所述的方法,其中扩增步骤在至少部分低于熔解温度条件下进行。
第c8段。根据第c6或c7段所述的方法,其中扩增步骤包括使至少一种引物退火至第一和第二等位形式目标的步骤,以及在退火步骤后延伸该至少一种引物的步骤,以及其中退火步骤在低于熔解温度条件下进行。
第c9段。根据c6-c8段中任一项所述的方法,其中扩增步骤包括延伸至少一种杂交至第一和第二等位形式目标的引物的步骤,以及其中延伸步骤在低于熔解温度的条件下进行。
第c10段。根据c6-c9段中任一项所述的方法,其中检测步骤在至少一部分反应混合物在低于熔解温度条件下进行。
第c11段。根据c6段所述的方法,其中扩增步骤在整体高于熔解温度条件下进行。
第c12段。根据c11所述的方法,其中扩增步骤包括通过多个热循环使各分解部分热循环的步骤,且其中各分解部分在每个热循环的整个过程中高于熔解温度。
第d1段。一种组合物,包含:共同包含至少一种第一等位形式和一第二等位形式目标的多个分离的分解部分,每分解部分包含(a)能够特异性结合每种第一和第二等位形式目标的相同探针,(b)配置成选择性结合至相对于该至少一种第一等位形式的第二等位形式,并阻断探针与第二等位形式的结合的竞争物,以及(c)扩增该至少一种第一等位形式目标的试剂。
第d2段。根据第d1段所述的组合物,其中试剂包括引导每种等位形式目标扩增的相同引物对。
第d3段。根据d1或d2段所述的组合物,其中多个分解部分的每个分解部分不含该至少一种第一等位形式目标。
第d4段。根据d1-d3中任一项所述的组合物,其中多个分解部分的每个分解部分不含任意形式目标。
第d5段。根据d1-d4段中任一项所述的组合物,其中多个分解部分的每个分解部分包含该至少一种第一等位形式的至少一个副本以及该第二等位形式的至少一个副本。
第d6段。根据d1-d5段中任一项所述的组合物,其中探针和竞争物每种用光致发光体标记。
第d7段。根据d6段所述的组合物,其中光致发光体是荧光体。
第d8段。根据d6或d7段所述的组合物,其中探针和竞争物每种用相同光致发光体标记。
第d9段。根据d6或d7段所述的组合物,其中探针和竞争物用相互不同的光致发光体标记。
第d10段。根据d1-d9任一项所述的组合物,其中每个分解部分包含一聚合酶。
第d11段。根据d10段所述的组合物,其中聚合物是热稳定聚合酶。
第d12段。根据d1-d11任一项所述的组合物,其中各分解部分是置于不相溶载体流体中的液滴。
此处公开的内容可包括多种独立使用的不同发明。尽管这些发明的每一种以其优选形式公开,本文公开和阐述的具体实施方式并非认为是限制的意思,因为多种变形是可能的。本发明的主题包括本文公开的各种元件、特征、功能和/或性能的所有新型的和非显而易见的组合和次组合。下述权利要求特别的指出被认为是新型的和非显而易见的某些组合和次组合。特征、功能、元件和/或性能在其他组合和次组合中被具体化的发明可要求在要求本申请或相关申请的优先权的申请中获得保护。这些权利要求,不管针对不同发明或相同发明,且不管范围比原始权利要求更宽、更窄、相同或不同,都被视为包含在本发明主题中。另外,用于鉴定元件的次序标号,例如第一、第二、第三,用于区分各元件,并不指示这些元件的特定位置或顺序,除非另有说明。
序列表
<110>生物辐射实验室股份有限公司(bio-radlaboratories,inc.)
s·库珀(cooper,samantha)
<120>具有探针竞争物的扩增分析
<130>qli387pct
<150>us62/174,279
<151>2015-06-11
<160>20
<170>siposequencelisting1.0
<210>1
<211>60
<212>dna
<213>智人(homosapiens)
<400>1
aagttaaaattcccgtcgctatcaaggaattaagagaagcaacatctccgaaagccaaca60
<210>2
<211>28
<212>dna
<213>智人(homosapiens)
<400>2
cgtcgctatcaaggaattaagagaagca28
<210>3
<211>18
<212>dna
<213>智人(homosapiens)
<400>3
aattcccgtcgctatcaa18
<210>4
<211>45
<212>dna
<213>智人(homosapiens)
<400>4
aagttaaaattcccgtcgctatcaaaacatctccgaaagccaaca45
<210>5
<211>45
<212>dna
<213>智人(homosapiens)
<400>5
aagttaaaattcccgtcgctatcaaaatatctccgaaagccaaca45
<210>6
<211>45
<212>dna
<213>智人(homosapiens)
<400>6
aagttaaaattcccgtcgctatcaagacatctccgaaagccaaca45
<210>7
<211>42
<212>dna
<213>智人(homosapiens)
<400>7
aagttaaaattcccgtcgctatcaaggttccgaaagccaaca42
<210>8
<211>42
<212>dna
<213>智人(homosapiens)
<400>8
aagttaaaattcccgtcgctatcaaggatccgaaagccaaca42
<210>9
<211>51
<212>dna
<213>智人(homosapiens)
<400>9
aagttaaaattcccgtcgctatcaaggagccaacatctccgaaagccaaca51
<210>10
<211>48
<212>dna
<213>智人(homosapiens)
<400>10
aagttaaaattcccgtcgctatcaaggagcaatctccgaaagccaaca48
<210>11
<211>45
<212>dna
<213>智人(homosapiens)
<400>11
aagttaaaattcccgtcgctatcaaggaatctccgaaagccaaca45
<210>12
<211>42
<212>dna
<213>智人(homosapiens)
<400>12
aagttaaaattcccgtcgctatcaaggaaccgaaagccaaca42
<210>13
<211>51
<212>dna
<213>智人(homosapiens)
<400>13
aagttaaaattcccgtcgctatcaaggaaccaacatctccgaaagccaaca51
<210>14
<211>48
<212>dna
<213>智人(homosapiens)
<400>14
aagttaaaattcccgtcgctatcaaggaaccatctccgaaagccaaca48
<210>15
<211>42
<212>dna
<213>智人(homosapiens)
<400>15
aagttaaaattcccgtcgctatcaaggaacagaaagccaaca42
<210>16
<211>45
<212>dna
<213>智人(homosapiens)
<400>16
aagttaaaattcccgtcgctatcaaggaatctccgaaagccaaca45
<210>17
<211>42
<212>dna
<213>智人(homosapiens)
<400>17
aagttaaaattcccgtcgctatcaaggaatcgaaagccaaca42
<210>18
<211>92
<212>dna
<213>智人(homosapiens)
<400>18
ggatcccagaaggtgagaaagttaaaattcccgtcgctatcaaggaattaagagaagcaa60
catctccgaaagccaacaaggaaatcctcgat92
<210>19
<211>17
<212>dna
<213>智人(homosapiens)
<400>19
ggatcccagaaggtgag17
<210>20
<211>19
<212>dna
<213>智人(homosapiens)
<400>20
atcgaggatttccttgttg19
- 还没有人留言评论。精彩留言会获得点赞!
- 用于检测CYP2C19基因多态性的引物、探针及检测试剂盒的制造方法与工艺
- 分子信标探针及引物对、GC基因SNPs位点检测方法与流程
- 一种表面修饰分子印迹固相微萃取探针及其制备与应用的制造方法与工艺
- 一种木瑚菌属食用菌鉴别用分子标记及引物和探针的制造方法与工艺
- 一种用于检测样品中牛凸隆病毒的荧光RT-PCR引物、探针和试剂盒及检测方法与制造工艺
- CYP2C19基因多态性检测引物、探针及试剂盒的制造方法与工艺
- 检测CYP2C9和VKORC1基因多态性的引物、探针和试剂盒的制造方法与工艺
- 一种用于检验临床样本中活菌体的荧光PCR引物探针组及试剂盒的制造方法与工艺
- 含反义碱基的探针法实时荧光PCR的制造方法与工艺
- PCR反应管及包含其的固相载具的制造方法与工艺