一种改良型HCVRNA检测试剂盒的制作方法
技术领域:本发明属于一种生物技术分子诊断领域,特别是涉及一种丙型肝炎病毒的核酸检测试剂及其使用方法。
背景技术:
:
丙型肝炎是一种主要经血液传播的疾病,丙型肝炎病毒慢性感染可导致肝脏慢性炎症坏死和纤维化,部分患者可发展为肝硬化甚至肝细胞癌,对患者的健康和生命危害极大,已成为严重的社会和公共卫生问题。
丙型肝炎呈全球性流行,是欧美及日本等国家终末期肝病的最主要原因。据世界卫生组织2014年统计,全球约1.85亿人感染hcv,其中约1.5亿为慢性感染,每年有35万~50万人死于丙肝并发症,每年新发感染病例约300万~400万例。
hcv1b和2a基因型在我国较为常见,其中以1b型为主;某些地区有1a、2b和3b型报道;6型主要见于香港和澳门地区,在南方边境省份也可见此基因型。
hcv属于黄病毒科(flaviviridae),其基因组为单股正链rna,易变异,目前可分为6个基因型及50多种不同亚型,按照国际通行的方法,以阿拉伯数字表示hcv基因型,以小写的英文字母表示基因亚型(如1a、2b、3c等)。基因1型呈全球性分布,占所有hcv感染的70%以上。hcv基因组含有一个开放读框(openreadingframe,orf),编码10余种结构和非结构(ns)蛋白,ns3蛋白是一种多功能蛋白,氨基端具有蛋白酶活性,羧基端具有螺旋酶/三磷酸核苷酶活性;ns5b蛋白是rna依赖的rna聚合酶,为hcv复制所必需,是抗病毒治疗的重要靶位,其末端具有核苷酸转移酶活性,但由于rna酶缺乏矫正功能不能修正错配,多次复制后易导致hcv多种变异产生。
hcvrna定量检测方法包括实时荧光逆转录聚合酶链反应(qrt-pcr)、分枝dna(bdna)等。本发明所指的hcvrna定量试剂是指利用qrt-pcr方法的核酸检测技术,以hcv基因序列为检测靶标,对人血清、血浆及其他人体样本中的hcvrna进行体外定量检测的试剂,可作为hcv现症感染的证据和抗病毒疗效评估的观察指标。
现有hcvrna定量试剂的设计为:生物信息学分析、保守区的靶标选择,合成引物对靶标的扩增与检测,一般为5’ncr区,由于病毒基因组突变规律存在较大随机性的原因,有些设计者针对同一靶标采用兼并引物或多条引物避免漏检的方法。
然而,由于基因突变的普遍性,碱基置换、移码(包括缺失、插入、重复)的发生往往是随机的,构成了病毒的准种突变的复杂性。对hcvrna病毒来讲,其逆转录酶缺乏校正功能,尤其容易自发突变。基因库中的病毒序列再多,也无法覆盖真实样本中的所有病毒序列,更何况有得研究者,压根不上传有意义的病毒分离株的测序结果。分子诊断试剂研发者只能根据文献及基因库中的现有序列,通过序列比对,分析保守区及其中碱基的突变概率,估算错配发生率及带来的漏检风险等一系列概率统计,设计出相对优秀的引物探针,兼顾检测灵敏度及亚型覆盖率。经实践验证其可行性,在随后的临床试验中扩大样本量验证其适用性。引物探针设计属于分子诊断试剂的核心思想,
关系到试剂的灵敏度、特异性等基本性能。没有一种试剂可以宣称不漏检,只能尽量覆盖所检测病毒的基因型、基因亚型,其设计思想是不漏检全球的主要流行株、使用国家或地区的优势地域株。
本发明是针对上述分子诊断试剂的种种不足,创新设计双靶标的检测,以最大限度地避免漏检,理论上,双保守区在一次检测中的漏检概率是两个单保守区漏检率的乘机,设计见图1-1,双区域靶标设计,引物对①②、引物对③④可对靶标有效扩增,引物对①④也可参与扩增。意外地,本发明还大大提高了灵敏度,推测为双区域扩增的协同作用,尤其是双区域rt引物解决了一步法rt-pcr的rt效率低的通病。常规一步法rt-pcr检测病毒时,使用一条或多条针对一个区域靶标的特异性引物为逆转录引物,出于方便性的考虑,或出于企业不同产品采用相同rt-pcr程序的考虑,通常使用一种rt温度如50度或55度,然而众所周知,病毒基因组不同区域的gc%含量不同,导致指定温度下二级结构未处于完全打开状态而严重影响逆转录效率,虽然扩增试剂中可以使用熟知的一些技巧如二甲亚砜、甘油、甲酰胺、甜菜碱等变性剂,但带来负面的影响却难以预期。通过设计,双区域的rt引物可使病毒基因组二级结构打开更充分,两条rt引物在逆转录酶牵引下两个独立位点开始启动,容易发生协同作用,在一种rt温度下实现高效的逆转录效率。
双区扩增的产物本身多于单区扩增是毋庸置疑的,而外侧的一条引物还可能组成一对扩增组合,使得双区扩增可能在双区全漏检的情况下还有一种横跨双区的长片段组合不漏检,这原本是设计中的副产物,但在极端条件下仍可避免漏检,且有可能增加产物量,对提升灵敏度有贡献。
当然,双区域扩增也存在一个缺点,当设计的引物或探针存在交叉时,或者其他一些未知的原因,或特殊干扰核酸的存在时,可能会有非特异反应。但是,通过优选引物探针总是可以排除。研究者都应深知,任何pcr软件设计出来的引物探针并不总是很好地胜任工作,而是必须通过具体实验等实践活动来最终筛选出合格的双靶标的引物及探针。这一点与单靶标引物探针的设计并没有什么不同,只是多了一项特异性检测。
附图说明:
图1-1是本发明双区域靶标设计原理示意图
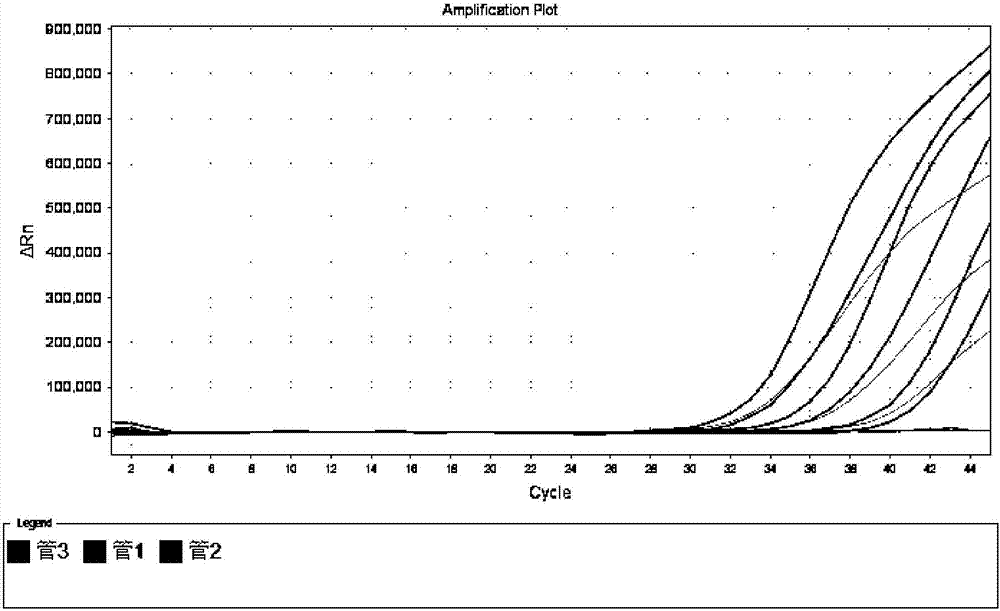
图2-1是本发明双区域靶标设计和单区域靶标设计对不同浓度hcvrna样品进行hcvrna病毒检测的荧光pcr结果对比图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图2-2是本发明双区域靶标设计和单区域靶标设计对阴性以及低浓度hcvrna样品进行hcvrna病毒检测的荧光pcr结果对比图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图3-1是本发明双区域靶标设计对hcvrna样品中加入内标和不加入内标进行hcvrna病毒检测的荧光pcr结果对比图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
图3-2是本发明双区域靶标设计对hcvrna样品中加入内标样品进行内标检测的荧光pcr结果图,横坐标代表扩增循环数,纵坐标代表荧光值强度。
实施案例1
设计针对hcv5’ncr前端约110bp的一对引物探针:正向引物kl034,反向引物kl037,taqman探针kl101,序列委托takara合成,要求page或hplc纯化,为冻干粉。用纯水复溶至100μm。
kl001:5’-ctgtgaggaactwctgtcttcacg-3’
kl002:5’-ccgcagaccactatggctct-3’
kl101:5’-fam-ctagccatggcgttagtaygagtgtcg-bhq1-3’
设计针对hcv5’ncr后端及c区前端约90bp的一对引物探针:正向引物nc201、nc202,反向引物nc203,taqman探针nc204,序列委托takara合成,要求page或hplc纯化,为冻干粉。用纯水复溶至100μm。
nc201:5’-gagtagtgttgggtcgcgaa-3’
nc202:5’-gagtagcgttgggttgcgaa-3’
nc203:5’-ggtgcacggtctacgagrcct-3’
nc204:5'-fam-tcgcaagcrccctatcaggcag-bhq1-3’
使用上海纽思格生物科技有限公司的rt-pcrmix(50μl扩增体系中15μl每个检测)及enzymemix(50μl扩增体系中10μl每个检测),也可使用thermofisher旗下invitrogen的同类产品。
rt-pcr反应液的配制方法如下:
管1-3均按每孔30μl分装至pcr管,加上不同浓度的hcvrna模板(来自上海纽思格生物磁珠法提取系统对阴性血、hcv50iu/ml,1000iu/ml,10000iu/ml浓度的阳性血进行提取后的产物,0.2ml上样,0.1ml洗脱;也可使用与之相当效果的凯杰生物的柱膜式提取试剂盒)20μl,上abi7500,扩增程序设置为50-60℃10-15分钟,95℃2-5分钟,95℃5-10秒、60℃30-40秒,循环45次,60℃末读取荧光fam,试验结果如图2-1。由图2-1可见,双靶标扩增使检测ct提前,对漏检的预防尚难通过有限数量的实验室标本观察到,但对检测灵敏度的提高是立竿见影的。为验证该结论,我们对阴性、15iu/mlhcvrna、50iu/mlhcvrna的标本各重复检测10次,结果如图2-2。由图2-2可见,只有双靶标设计的管3可以检测50iu/mlhcvrna(10/10)和15iu/mlhcvrna(10/10)为阳性。
实施案例2在前述实施案例中的双区扩增体系中(管3)增加非竞争性内对照的引物及探针,并在核酸提取时,裂解液中加入外源性假病毒颗粒,或者不加外源性内标,使用内源性持家基因的mrna,实施管内质控,要求内质控必须为阳性。
设计一对内源性内参引物探针如下hbdf、hbdr、hbdp,序列委托life合成,要求page或hplc纯化,为100μm液体。
hbdf:5’-agtcctttggggatctgtc-3’
hbdr:5’-gcttgtcacagtgcagctc-3’
hbdp:vic-tcctgatgctgttatgggcaacc-bhq1
rt-pcr反应液的配制方法如下:
我们对阴性、25iu/mlhcvrna的标本各重复检测20次,管3和管4的检测结果一致。试验结果如图3-1、3-2。由图3-1、3-2可见阴性无数值,阳性均检出,管4的内参ct也检出。管4的优点是可以监控假阴性事件的发生,一旦内参为阴性,说明标本提取过程出了问题或者加样错误、或者实时扩增仪该扩增孔出了问题。
以上所述例子仅为本发明的较佳实施例而已,并不用以限制本发明,凡在本发明的精神和原则之内所作的任何修改、等同替换和改进等,均应包含在本发明的保护范围之内。
kl001:5’-ctgtgaggaactwctgtcttcacg-3’
kl002:5’-ccgcagaccactatggctct-3’
kl101:5’-fam-ctagccatggcgttagtaygagtgtcg-bhq1-3’
nc201:5’-gagtagtgttgggtcgcgaa-3’
nc202:5’-gagtagcgttgggttgcgaa-3’
nc203:5’-ggtgcacggtctacgagrcct-3’
nc204:5'-fam-tcgcaagcrccctatcaggcag-bhq1-3’
- 还没有人留言评论。精彩留言会获得点赞!
- 一种用于检测犬副流感病毒试剂盒的制造方法与工艺
- 腹泻相关病毒多重基因检测体系及其试剂盒和应用的制造方法与工艺
- 基于POCKIT Micro荧光PCR平台的禽流感病毒H7亚型检测试剂及应用的制造方法与工艺
- 一种流行性乙型脑炎的重组酶常温扩增核酸(RT‑RPA)试纸条检测试剂盒及应用的制造方法与工艺
- 一种腺苷高半胱氨酸酶基因启动子区甲基化程度检测试剂盒及测定方法与流程
- 一种检测心肌梗死的试剂及其应用的制造方法与工艺
- 用于检测CDKN2B基因变异的试剂盒及CDKN2B基因变异率的定量检测方法与流程
- 一种CYP2C19*3基因型检测试剂盒及其检测方法与流程
- 一种CYP2C19*2基因型检测试剂盒及其检测方法与流程
- 基于高通量测序法的人类多基因突变检测试剂盒的制造方法与工艺