志贺菌荧光PCR检测试剂盒的制作方法
本发明涉及一种采用实时荧光pcr方法特异性检测样品中志贺菌核酸的试剂盒,属于志贺菌的体外诊断领域。
背景技术:
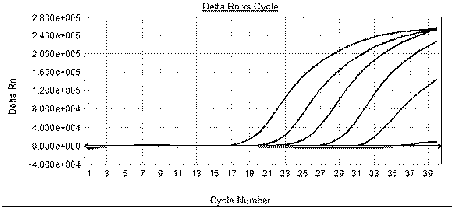
:志贺菌(shigella)为革兰氏阴性菌,杆菌,无鞭毛,有菌毛,属于肠杆菌志贺菌属。志贺菌属的细菌,通称痢疾杆菌,是人类细菌性痢疾的病原菌。根据其抗原构造的不同,可分为a、b、c、d四个群,即痢疾志贺菌、福氏志贺菌、鲍氏志贺菌和宋内志贺菌四群。志贺菌传染源是病人和带菌者,传播途径主要为粪-口途径。人类对志贺氏菌较易感,痢疾志贺菌引起病情较重;宋内志贺菌多引起轻型感染;福氏志贺细菌性痢疾是最常见的肠道传染病,夏秋两季患者最多。致病物质主要是侵袭力和内毒素,有的菌株还产生外毒素。临床感染类型为(1)急性菌痢:局部症状有脓血便,腹痛,里急后重。急性中毒性菌痢,以小儿多见,无明显的消化道症状,主要表现全身严重的中毒症状,各型志贺菌都有可能引起,临床症状主要有高热,神志障碍,休克,病死率较高;(2)慢性菌痢:病程大于2个月,迁延不愈,局部症状为主。在检测中,pcr法由于其快速简便的特点逐渐呈现出要替代以细菌培养和血清学检测为主的传统检测方法的趋势。而对于pcr方法来说,引物的特异性是其检测的特异性和敏感性的基础。本发明针对志贺菌基因序列的保守区域特异的靶序列设计引物和mgb探针,利用real-timepcr的方法,用来快速检测样品中是否存在志贺菌的核酸。技术实现要素:本发明主要解决的技术问题是快速准确地检测样品中是否存在志贺菌,提供一种特异性检测志贺菌的荧光pcr试剂盒。本发明所要解决的技术问题是通过以下技术方案来实现的:一种特异性检测样品中志贺菌核酸的试剂盒,其组分包括pcr反应液、酶混合液、阴性质控品和阳性质控品,其中pcr反应液主要含有相关的引物和探针、反应缓冲液、mg2+和dntp等,酶混合液主要含有热启动taq酶,阴性质控品为无rnase和dnase水,阳性质控品为含有志贺菌检测靶序列的重组质粒。其中pcr反应液中用于核酸扩增的引物为p1和p2,p1和p2为针对志贺菌基因组群特异性保守序列设计并经预实验筛选出的特异性引物;pcr反应液中用于荧光信号监测的寡核苷酸探针为probe1,probe1为针对志贺菌基因组群特异性保守序列设计并经预实验筛选出的特异性探针,其中荧光报告基团x1为hex,荧光淬灭基团y1为mgb(见表1)。表1检测志贺菌的引物和探针序列名称序列p15`-gtgtcgcgctcacatgga-3`p25`-cgccggtatcattatcgaaaa-3`probe15`-x1-ctggtccatcaggc-y1-3`本发明的另一个目的是提供本荧光pcr检测试剂盒在检测志贺菌的应用方法,包括:试剂盒选用的pcr反应体系为20µl,包括2×pcr缓冲液10µl、10mmol/ldntp1.0µl、25µmol/l引物各0.5µl、10µmol/l探针0.2µl、热启动taq酶混合液0.4µl、样品dna2µl,加灭菌水至终体系20µl。试剂盒的pcr反应循环参数为94℃,2min;进入循环阶段:94℃变性10s,56℃退火50s,72℃延伸15s,共反应40个循环。质量控制:每次实验应设立阴、阳性对照,阴性对照无ct值(或ct值为0),阳性对照ct值≤30,否则实验结果不成立。结果判读:阳性:出现“s”型扩增曲线,ct值≤35;可疑:出现“s”型扩增曲线,但ct值>35;阴性:没有出现“s”型扩增曲线,或者曲线虽然超过了阈值,但不呈“s”型;对可疑结果,应重复实验,如果重复实验还是出现“s”型扩增曲线,阴性对照没有污染,可判断为阳性。样本要求:临床样本类型包括括患者粪便、肛拭子、呕吐物和分离培养物;临床样本采集后应带冰运输,-20℃保存,不能反复冻融;从临床样本提取dna,建议采用性能稳定可靠的商品化试剂盒,具体方法参见相应商品化试剂盒说明书,提取的dna应立即检测,否则,应将dna分装后-80℃~-20℃保存。本发明提供的试剂盒具有很好的特异性,可以检出志贺菌,但不能检出非志贺菌病原体的核酸;对志贺菌核酸的检测下限为10拷贝每反应体系;只需要2小时即可完成检测,可为志贺菌的疾病监测和临床诊断提供实验依据。附图说明图1为单重实时荧光pcr检测志贺菌阳性标准品的扩增曲线图。从左至右的5条曲线分别为志贺菌dna梯度稀释后(2×106-2×102copies/µl)扩增结果。横坐标为反应循环数,纵坐标为不同循环数荧光检测信号的δrn值。图2为单重实时荧光pcr检测体系检测10种细菌基因组dna的扩增曲线图。10种细菌包括:志贺菌和9种阴性对照微生物。志贺菌出现s型扩增曲线,而其他9种病原微生物未出现s型扩增曲线。具体实施方式下面结合具体实施例详细说明本发明的优选实施方式。需要指出的是,这里列出的实施例仅仅为示例性说明的目的,而不应将其解释为对本发明范围的任何限制。其中使用的试剂盒、缓冲液等试剂仅仅为该具体实施例中具体选择的试剂,应理解,本领域技术人员可根据需要选择其他公司的相应试剂以实现本发明的目的。1、引物和taqman探针的设计与合成利用blast工具对genbank和国内外文献中的志贺菌基因组序列进行分析,分别选择其稳定的保守区域作为检测靶序列,并针对检测靶序列设计和合成引物和探针(见表1)。引物和探针均由日本takara大连宝生物公司合成,志贺菌的检测探针5’端标记hex荧光基团;3’端标记mgb荧光淬灭基团。2、检测菌种的准备本实施例中所使用的志贺菌以及其他阴性对照菌株(副溶血弧菌,蜡样芽孢杆菌,小肠结肠炎耶尔森菌,金黄色葡萄球菌,弯曲菌,大肠杆菌,变形杆菌,沙门氏菌,霍乱弧菌)均购买于中国药品生物制品检定所。3、菌株dna的抽提选用qiagen公司qiaampdnaminikit(货号:51306)提取菌株dna。具体步骤试剂盒参考操作说明书。4、引物和探针的筛选采用设计的引物和探针检测提取的志贺菌和阴性对照菌株的基因组dna,经反复实验,筛选出灵敏度、特异性和重复性最佳的引物探针组合(见序列表,志贺菌正向引物p1、反向引物p2和探针probe1)。5、标准品的构建与制备利用p1和p2引物扩增志贺菌基因组dna,将pcr产物克隆至pmd-18t载体,转化dh5α大肠杆菌,利用碱裂解法提取阳性克隆质粒,利用紫外可见分光光度计分别测定在波长260nm处、280nm处dna的吸光率,然后计算质粒浓度与纯度。然后10倍梯度稀释至200拷贝每微升,制备志贺菌的阳性标准品。6、反应条件优化对引物、探针、酶等要素逐一优化,确定的反应体系为:2×pcr缓冲液10µl、10mmol/ldntp1.0µl、25µmol/l引物各0.5µl、10µmol/l探针0.2µl、takara聚合酶混合物0.4µl、模板2µl,加灭菌水至终体系20µl。根据扩增片段长短、引物和探针的退火温度以及酶的特性,主要对反应的退火温度和延伸时间进行了优化,最终确定循环参数为:94℃,2min;进入循环阶段:94℃变性10s,56℃退火50s,72℃延伸15s,40个循环,每个循环在退火阶段采集荧光信号。在扩增结束后按同一条件分析数据,确定各样品的ct值。7、检测限的评价以上述5中的阳性标准品评价本发明提供的试剂盒的检测限,阳性标准品浓度为:2×106copies/µl、2×105copies/µl、2×104copies/µl、2×103copies/µl、2×102copies/µl,本发明提供的试剂盒对志贺菌核酸的检测下限为10拷贝每反应体系。8、检测特异性的评价以上述菌株dna为模板评价了本试剂盒的特异性。对志贺菌dna进行检测时均可见明确扩增曲线,对上述9种其他肠道常见病原微生物dna检测时,未产生阳性扩增曲线,说明我们使用的探针和引物与我们选定的其他菌株之间不存在交叉反应。尽管上文中以优选的方式,通过具体实施例示例性说明了本发明的某些实施方式,但是本领域技术人员应了解,本发明并不限于上面所公开的实施方式,而是可以根据本发明所属
技术领域:
的知识对其进行修改,所作修改不会超出本发明要求保护的范围。例如,本发明所使用的荧光实时pcr也可以根据需要采用说明书中所列出的实施例中指出的荧光报告基团和荧光淬灭基团以外的标记物质,如tet、hex、tamra、rox、cy3、txrd、joe等标记物;或使用taqman技术之外的其他标记体系,例如mgb探针、分子信标mb探针、蝎形探针、荧光双杂交探针等荧光探针标记技术;或使用染料嵌合法如sybrgreeni等不饱和染料与lcgreen等饱和染料,只要其使用了本发明所述的特异性引物序列,即可定性或定量检测目的基因的存在,进而特异性地检测志贺菌的存在。所以,这些本领域技术人员所了解的改变和惯用手段的替换也落入本发明的保护范围内。本发明的保护范围应由所附的权利要求书限定。序列表<110>江苏和创生物科技有限公司<120>志贺菌荧光pcr检测试剂盒<160>3<170>siposequencelisting1.0<210>1<211>18<212>dna<213>志贺菌(shigella)<400>1gtgtcgcgctcacatgga18<210>2<211>21<212>dna<213>志贺菌(shigella)<400>2cgccggtatcattatcgaaaa21<210>3<211>14<212>dna<213>志贺菌(shigella)<400>3ctggtccatcaggc14当前第1页12
相关技术
网友询问留言
已有0条留言
- 还没有人留言评论。精彩留言会获得点赞!
1