正极活性物质以及电池的制作方法
本公开涉及电池用正极活性物质以及电池。
背景技术:
专利文献1公开了一种正极活性物质,其具有属于空间群fm-3m的晶体结构,且由式li1+xnbymezapo2(me是含有fe和/或mn的过渡金属元素,0<x<1,0<y<0.5,0.25≤z<1,a是除了nb、me以外的元素,0≤p≤0.2)表示。
在先技术文献
专利文献
专利文献1:国际公开第2014/156153号
技术实现要素:
针对现有技术,期望实现高能量密度的电池。
本公开的一种方式中的正极活性物质,包含具有属于空间群fm-3m的晶体结构、且由下述组成式(1)表示的化合物。
lixmeyo2…式(1)
在此,前述me为mn,或者为选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和mn,或者为选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和ni以及mn,或者为选自ni、co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素,
并且,满足下述条件:0.5≤x/y≤3.0、1.5≤x+y≤2.3。
通过本公开,能够实现高能量密度的电池。
附图说明
图1是表示作为实施方式2中的电池的一例的电池10的概略构成的截面图。
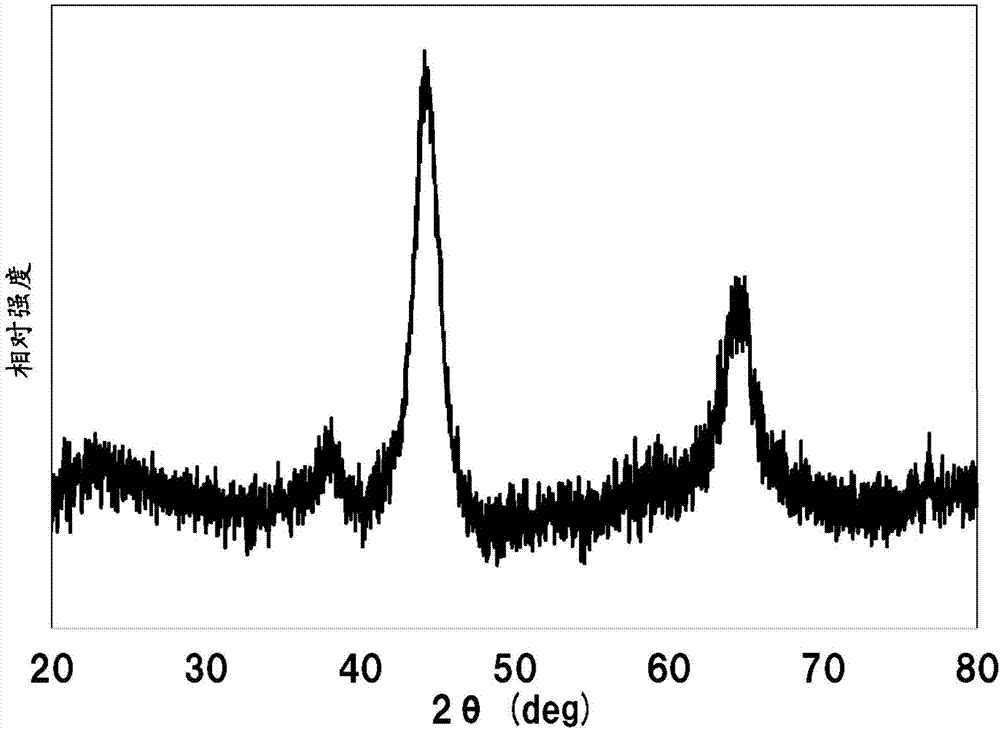
图2是表示实施例1的正极活性物质的粉末x射线衍射图的图。
附图标记说明
10电池
11外壳
12正极集电体
13正极活性物质层
14隔板
15封口板
16负极集电体
17负极活性物质层
18密封垫
21正极
22负极
具体实施方式
下面对本公开的实施方式进行说明。
(实施方式1)
实施方式1中的正极活性物质,包含具有属于空间群fm-3m的晶体结构、且由下述组成式(1)表示的化合物。
lixmeyo2…式(1)
在此,前述me为mn,或者为选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和mn,或者为选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和ni以及mn,或者为选自ni、co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素。
并且,在实施方式1中的正极活性物质中,上述化合物在组成式(1)中满足下述条件:0.5≤x/y≤3.0、1.5≤x+y≤2.3。
根据上述构成,能够实现高能量密度且高容量的电池。
在使用包含上述化合物的正极活性物质来构成例如锂离子电池的情况下,具有3.3v左右的氧化还原电位(li/li+基准)。
对于上述化合物而言,在组成式(1)中,x/y小于0.5的情况下,可以利用的li的量变少。另外,li的扩散路径被阻碍。因此,容量变得不充分。
另外,对于上述化合物而言,在组成式(1)中,x/y大于3.0的情况下,在充电时的li脱离时晶体结构不稳定化,放电时的li嵌入效率下降。因此,容量变得不充分。
另外,对于上述化合物而言,在组成式(1)中,x+y小于1.5的情况下,在合成时发生分相,会较多地生成杂质。因此,容量变得不充分。
另外,对于上述化合物而言,在组成式(1)中,x+y大于2.3的情况下,成为阴离子欠缺的结构,在充电时的li脱离时晶体结构不稳定化,放电时的li嵌入效率下降。因此,容量变得不充分。
对于由组成式(1)表示的化合物而言,可以认为li和me位于相同的位点(site)。
因此,由组成式(1)表示的化合物,例如,与作为以往的正极活性物质的limno2相比,能够相对于1个me原子使更多的li嵌入和脱离。
因此,实施方式1中的正极活性物质适于实现高容量的锂离子电池。
在此,作为比较例,可举出包含具有属于空间群fm-3m的晶体结构、在me中包含nb或ti的由组成式(1)表示的化合物的正极活性物质。
在该比较例中,由于作为me使用了有效核电荷低的元素nb或ti,因此工作电压下降。另外,nb在电子状态上难以发生氧化还原反应。因此,nb不会直接参与充放电。因此,能量密度变低。
另一方面,在实施方式1中的正极活性物质中,作为组成式(1)中的me,使用有效核电荷比nb和ti高、且在充放电时能够发生氧化还原反应的元素(即,选自mn、ni、co、fe、sn、cu、bi、v、cr中的一种或两种以上的元素)。由此,能够提高工作电压。因此,适于实现高能量密度且高容量的锂离子电池。
再者,在实施方式1中的正极活性物质中,me可以是选自mn、ni、co、fe、sn、cu、bi、v、cr中的一种元素的单质。
或者,在实施方式1中的正极活性物质中,me可以是由选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和mn形成的固溶体。或者,me可以是由选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和ni以及mn形成的固溶体。或者,me可以是由选自ni、co、fe、sn、cu、mo、bi、v、cr中的两种以上的元素形成的固溶体。
另外,在实施方式1中的正极活性物质中,在上述lixmeyo2中,li的一部分可以被na、k等碱金属置换。
另外,实施方式1中的正极活性物质,可以包含上述化合物作为主成分。
即,实施方式1中的正极活性物质可以包含50%重量以上的上述化合物。
根据上述构成,能够实现高能量密度且高容量的电池。
再者,实施方式1的正极活性物质,可以包含上述化合物作为主成分,而且含有不可避免的杂质、或者在合成上述化合物时所使用的起始原料以及副产物和分解产物等。
另外,实施方式1的正极活性物质,可以包含例如除了不可避免地混入的杂质以外的、90~100重量%的上述化合物。
根据上述构成,能够实现更高能量密度且更高容量的电池。
另外,在实施方式1中的正极活性物质中,me可以包含mn。
即,me可以为mn。或者,me可以是由选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和mn形成的固溶体。或者,me可以是由选自co、fe、sn、cu、mo、bi、v、cr中的一种或两种以上的元素、和ni以及mn形成的固溶体。
根据上述构成,能够实现更高能量密度且更高容量的电池。
另外,在实施方式1中的正极活性物质中,上述化合物可以是在组成式(1)中满足1.5≤x/y≤2.0的化合物。
根据上述构成,能够实现更高能量密度且更高容量的电池。
另外,在实施方式1中的正极活性物质中,上述化合物可以是在组成式(1)中满足1.9≤x+y≤2.0的化合物。
根据上述构成,能够实现更高能量密度且更高容量的电池。
<化合物的制作方法>
以下对实施方式1的正极活性物质中所包含的上述化合物的制造方法的一例进行说明。
由组成式(1)表示的化合物例如可以通过下述方法制作。
准备含有li的原料、含有o的原料、以及含有me的原料。例如,作为含有li的原料,可举出li2o、li2o2等氧化物,li2co3、lioh等盐类、limeo2、lime2o4等锂过渡金属复合氧化物等。作为含有me的原料,可举出me2o3等各种氧化状态的氧化物、meco3、meno3等盐类、me(oh)2、meooh等氢氧化物、limeo2、lime2o4等锂过渡金属复合氧化物等。例如,在me为mn的情况下,作为含有mn的原料,可举出mn2o3等各种氧化状态的氧化锰、mnco3、mnno3等盐类、mn(oh)2、mnooh等氢氧化物,limno2、limn2o4等锂过渡金属复合氧化物等。
称量这些原料,使得原料达到由组成式(1)表示的摩尔比。
由此,可以使组成式(1)中的x和y在由组成式(1)表示的范围内变化。
将称量好的原料采用例如干式法或湿式法进行混合,使其进行10小时以上的机械化学反应,由此能够得到由组成式(1)表示的化合物。例如,可以使用球磨机等混合装置。
通过调整使用的原料、以及原料混合物的混合条件,能够实质性地得到由组成式(1)表示的化合物。
通过作为前驱体使用锂过渡金属复合氧化物,能够使各种元素的混合所需的能量进一步下降。由此,可获得纯度更高的由组成式(1)表示的化合物。
所得到的由组成式(1)表示的化合物的组成,例如,可以通过icp发射光谱分析法和惰性气体熔融-红外线吸收法来确定。
另外,通过采用粉末x射线分析来确定晶体结构的空间群,能够鉴定由组成式(1)表示的化合物。
如上所述,实施方式1的一个方式中的正极活性物质的制造方法,包括准备原料的工序(a)、和通过使原料进行机械化学反应而得到正极活性物质的工序(b)。
另外,上述工序(a)可以包含下述工序:使含有li的原料和含有me的原料以li相对于me为0.5以上且3.0以下的摩尔比的比例进行混合,来制备混合原料。
此时,上述的工序(a)可以包含利用公知的方法制作作为原料的锂过渡金属复合氧化物的工序。
另外,在上述的工序(a)中,可以包含以li相对于me为1.5以上且2.0以下的摩尔比的比例进行混合,来制备混合原料的工序。
另外,在上述的工序(b)中,可以包含使用球磨机来使原料进行机械化学反应的工序。
如上所述,由组成式(1)表示的化合物可以通过使用行星型球磨机,使前驱体(例如,li2o、过渡金属氧化物、锂过渡金属复合氧化物等)发生机械化学反应来合成。
此时,可通过调整前驱体的混合比来包含更多的li原子。
(实施方式2)
以下对实施方式2进行说明。再者,与上述实施方式1重复的说明被适当地省略。
实施方式2中的电池,具备包含上述实施方式1中的正极活性物质的正极、负极和电解质。
根据上述构成,能够实现高能量密度且高容量的电池。
即,如在上述的实施方式1中所说明的那样,在正极活性物质中,相对于1个me原子包含较多的li原子。因此,能够实现高容量的电池。
实施方式2中的电池,可以作为例如锂离子二次电池、非水电解质二次电池、全固体二次电池等来构成。
在实施方式2中的电池中,正极可以具备正极活性物质层。此时,正极活性物质层可以包含上述实施方式1中的正极活性物质(上述实施方式1中的化合物)作为主成分(即,以相对于正极活性物质层总体的重量比例计为50%以上(50重量%以上))。
根据上述构成,能够实现更高能量密度且更高容量的电池。
或者,在实施方式2中的电池中,正极活性物质层可以包含以相对于正极活性物质层总体的重量比例计为70%以上(70重量%以上)的上述实施方式1中的正极活性物质(上述实施方式1中的化合物)。
根据上述构成,能够实现更高能量密度且更高容量的电池。
或者,在实施方式2中的电池中,正极活性物质层可以包含以相对于正极活性物质层总体的重量比例计为90%以上(90重量%以上)的上述实施方式1中的正极活性物质(上述实施方式1中的化合物)。。
根据上述构成,能够实现更高能量密度且更高容量的电池。
另外,在实施方式2中的电池中,例如,负极可以含有能够吸藏和释放锂的负极活性物质(例如,具有吸藏和释放锂的特性的负极活性物质)。
另外,在实施方式2中的电池中,例如,电解质可以是非水电解质(例如非水电解液)或固体电解质。
图1是表示作为实施方式2中的电池的一例的电池10的概略构成的截面图。
如图1所示,电池10具备正极21、负极22、隔板14、外壳11、封口板15和密封垫18。
隔板14配置于正极21和负极22之间。
在正极21、负极22和隔板14中浸渗有非水电解质(例如,非水电解液)。
采用正极21、负极22和隔板14来形成了电极群。
电极群被收纳在外壳11中。
外壳11被密封垫18和封口板15封闭。
正极21具备正极集电体12、和配置在正极集电体12上的正极活性物质层13。
正极集电体12例如由金属材料(铝、不锈钢、铝合金等)制成。
再者,也可以省略正极集电体12而将外壳11作为正极集电体使用。
正极活性物质层13包含上述实施方式1中的正极活性物质。
正极活性物质层13可以根据需要包含例如添加剂(导电剂、离子传导辅助剂、粘合剂等)。另外,正极活性物质层13可以包含与上述实施方式1中的正极活性物质不同的、一般所公知的二次电池用正极活性物质(例如,nca系活性物质等)。
负极22具备负极集电体16、和配置在负极集电体16下方的负极活性物质层17。
负极集电体16例如由金属材料(铝、不锈钢、铝合金等)制成。
再者,也可以省略负极集电体16而将封口板15作为负极集电体使用。
负极活性物质层17包含负极活性物质。
负极活性物质层17可以根据需要包含例如添加剂(导电剂、离子传导辅助剂、粘合剂等)。
作为负极活性物质,可以使用一般所公知的二次电池用负极活性物质(例如,金属材料、碳材料、氧化物、氮化物、锡化合物、硅化合物等)。
金属材料可以为单质的金属。或者,金属材料可以为合金。作为金属材料的例子,可举出锂金属、锂合金等。
作为碳材料的例子,可举出天然石墨、焦炭、石墨化途中碳、碳纤维、球状碳、人造石墨、无定形碳等。
从容量密度的观点来看,可以优选地使用硅(si)、锡(sn)、硅化合物、锡化合物。硅化合物和锡化合物分别可以是合金或者固溶体。
作为硅化合物的例子,可举出siox(其中,0.05<x<1.95)。另外,也可以使用通过将siox的一部分硅用其它的元素置换而得到的化合物(合金或者固溶体)。在这里,其它的元素是选自硼、镁、镍、钛、钼、钴、钙、铬、铜、铁、锰、铌、钽、钒、钨、锌、碳、氮和锡中的至少一种。
作为锡化合物的例子,可举出ni2sn4、mg2sn、snox(其中,0<x<2)、sno2、snsio3等。可以单独使用选自这些锡化合物中的一种锡化合物。或者,也可以使用选自这些锡化合物中的两种以上的锡化合物的组合。
另外,负极活性物质的形状无特别限定。作为负极活性物质,可以使用具有公知的形状(粒子状、纤维状等)的负极活性物质。
另外,用于将锂填充(吸藏)到负极活性物质层17中的方法不特别限定。具体而言,有:(a)通过真空蒸镀法等气相法将锂沉积在负极活性物质层17上的方法;(b)使锂金属箔与负极活性物质层17接触并将两者加热的方法。不论在哪一种方法中,都能够利用热使锂扩散到负极活性物质层17中。另外,也有使负极活性物质层17电化学性地吸藏锂的方法。具体而言,使用不具有锂的负极22和锂金属箔(正极)来组装电池。然后,将该电池充电,使得在负极22中吸藏锂。
作为正极21以及负极22的粘合剂,可以使用聚偏二氟乙烯、聚四氟乙烯、聚乙烯、聚丙烯、芳族聚酰胺(aramid)树脂、聚酰胺、聚酰亚胺、聚酰胺酰亚胺、聚丙烯腈、聚丙烯酸、聚丙烯酸甲酯、聚丙烯酸乙酯、聚丙烯酸己酯、聚甲基丙烯酸、聚甲基丙烯酸甲酯、聚甲基丙烯酸乙酯、聚甲基丙烯酸己酯、聚乙酸乙烯酯、聚乙烯吡咯烷酮、聚醚、聚醚砜、六氟聚丙烯、苯乙烯-丁二烯橡胶、羧甲基纤维素等。或者,作为粘合剂,可以使用选自四氟乙烯、六氟乙烯、六氟丙烯、全氟烷基乙烯基醚、偏二氟乙烯、氯代三氟乙烯、乙烯、丙烯、五氟丙烯、氟代甲基乙烯基醚、丙烯酸、己二烯中的两种以上的材料的共聚物。进而,也可以将选自上述材料中的两种以上的材料的混合物作为粘合剂使用。
作为正极21以及负极22的导电剂,可以使用石墨、炭黑、导电性纤维、氟化石墨、金属粉末、导电性晶须、导电性金属氧化物、有机导电性材料等。作为石墨的例子,可举出天然石墨和人造石墨。作为炭黑的例子,可举出乙炔黑、科琴黑(ケッチェンブラック,注册商标)、槽法炭黑、炉法炭黑、灯黑、热裂法炭黑等。作为金属粉末的例子,可举出铝粉末。作为导电性晶须的例子,可举出氧化锌晶须和钛酸钾晶须。作为导电性金属氧化物的例子,可举出氧化钛。作为有机导电性材料的例子,可举出亚苯基衍生物。
作为隔板14,可以使用具有大的离子透过度和充分的机械强度的材料。作为这样的材料的例子,可举出微多孔性薄膜、织布、无纺布等。具体而言,优选隔板14是由聚丙烯、聚乙烯等聚烯烃制成的。由聚烯烃制成的隔板14不仅具有优异的耐久性,而且在被过度加热时能够发挥关闭功能。隔板14的厚度在例如10~300μm(或者10~40μm)的范围。隔板14可以是由一种材料构成的单层膜。或者,隔板14也可以是由两种以上的材料构成的复合膜(或多层膜)。隔板14的孔隙率在例如30~70%(或者35~60%)的范围。所谓“孔隙率”,意指孔隙的体积占隔板14总体体积的比例。“孔隙率”可以采用例如压汞法进行测定。
非水电解液包含非水溶剂、和溶解在非水溶剂中的锂盐。
非水溶剂可以使用环状碳酸酯溶剂、链状碳酸酯溶剂、环状醚溶剂、链状醚溶剂、环状酯溶剂、链状酯溶剂、氟溶剂等。
作为环状碳酸酯溶剂的例子,可举出碳酸亚乙酯、碳酸亚丙酯、碳酸亚丁酯等。
作为链状碳酸酯溶剂的例子,可举出碳酸二甲酯、碳酸甲乙酯、碳酸二乙酯等。
作为环状醚溶剂的例子,可举出四氢呋喃、1,4–二
作为链状醚溶剂,可举出1,2-二甲氧基乙烷、1,2-二乙氧基乙烷等。
作为环状酯溶剂的例子,可举出γ-丁内酯等。
作为链状酯溶剂的例子,可举出乙酸甲酯等。
作为氟溶剂的例子,可举出氟代碳酸亚乙酯、氟代丙酸甲酯、氟苯、氟代碳酸甲乙酯、氟代碳酸二甲酯、氟腈等。
作为非水溶剂,可以单独使用选自这些溶剂中的一种非水溶剂。或者,作为非水溶剂,可以使用选自这些溶剂中的两种以上的非水溶剂的组合。
在非水电解液中可以含有选自氟代碳酸亚乙酯、氟代丙酸甲酯、氟苯、氟代碳酸甲乙酯、氟代碳酸二甲酯中的至少一种氟溶剂。
如果非水电解液含有这些氟溶剂,则非水电解液的抗氧化性提高。
其结果,在以高电压对电池10进行充电的情况下也能够使电池10稳定地工作。
作为锂盐,可以使用lipf6、libf4、lisbf6、liasf6、liso3cf3、lin(so2cf3)2、lin(so2c2f5)2、lin(so2cf3)(so2c4f9)、lic(so2cf3)3等。作为锂盐,可以单独使用选自这些锂盐中的一种锂盐。或者,作为锂盐,可以使用选自这些锂盐中的两种以上的锂盐的混合物。锂盐的浓度在例如0.5~2mol/l范围。
作为固体电解质,可以使用有机聚合物固体电解质、氧化物固体电解质、硫化物固体电解质等。
作为有机聚合物固体电解质,例如,可以使用高分子化合物与锂盐形成的化合物。
高分子化合物可以具有环氧乙烷型结构。通过具有环氧乙烷型结构,能够较多地含有锂盐,能够进一步提高离子导电率。
作为氧化物固体电解质,例如,可以使用以liti2(po4)3及其元素置换体为代表的nasicon型固体电解质、(lali)tio3系钙钛矿型固体电解质、以li14znge4o16、li4sio4、ligeo4及其元素置换体为代表的lisicon型固体电解质、以li7la3zr2o12及其元素置换体为代表的石榴石型固体电解质、li3n及其h置换体,li3po4及其n置换体等。
作为硫化物固体电解质,例如,可以使用li2s-p2s5、li2s-sis2、li2s-b2s3、li2s-ges2、li3.25ge0.25p0.75s4、li10gep2s12等。另外,可以向这些物质中添加lix(x可为f、cl、br、i)、mop、liqmop(m:p、si、ge、b、al、ga、in中的任意的元素)(p、q:自然数)等。
在这些电解质中,特别是硫化物固体电解质富有成形性,离子传导性高。因此,通过作为固体电解质30使用硫化物固体电解质,能够实现更高能量密度的电池。
另外,在硫化物固体电解质中,li2s-p2s5的电化学稳定性高,离子传导性更高。因此,如果作为固体电解质30使用li2s-p2s5,则能够实现更高能量密度的电池。
再者,实施方式2中的电池可以作为硬币型、圆筒型、方型、片型、钮扣型、扁平型、层叠型等各种形状的电池来构成。
实施例
<实施例1>
[正极活性物质的制作]
利用公知的方法得到锂锰复合氧化物(li2mno3)。
将获得的li2mno3、和coo以li2mno3/coo=3/1的摩尔比分别称量。
将得到的原料与适量的ф3mm的氧化锆制球一起放入45cc的氧化锆制容器内,在充氩手套箱内密闭。
从充氩手套箱中取出,采用行星型球磨机以600rpm进行了30小时的处理。
对获得的化合物实施了粉末x射线衍射测定。
测定的结果如图2所示。
获得的化合物的空间群为fm-3m。
另外,利用icp发射光谱分析法和惰性气体熔融-红外线吸收法求出了所得到的化合物的组成。
其结果,所得到的化合物的组成为li1.2mn0.6co0.2o2。
[电池的制作]
接下来,将70质量份的上述化合物、20质量份的导电剂、10质量份的聚偏二氟乙烯(pvdf)、以及适量的2-甲基吡咯烷酮(nmp)混合。由此,得到了正极合剂浆料。
在厚度20μm的铝箔形成的正极集电体的一面上涂敷了正极合剂浆料。
通过将正极合剂浆料干燥并进行轧制,获得了具有正极活性物质层的厚度为60μm的正极板。
通过将获得的正极板冲裁成直径为12.5mm的圆形而得到了正极。
另外,通过将厚度300μm的锂金属箔冲裁成直径为14.0mm的圆形而得到了负极。
另外,将氟代碳酸亚乙酯(fec)和碳酸亚乙酯(ec)以及碳酸甲乙酯(emc)以1:1:6的体积比进行混合,从而得到了非水溶剂。
通过使lipf6以1.0mol/l的浓度溶解于该非水溶剂中,得到了非水电解液。
使所得到的非水电解液浸渗到隔板(セルガード公司制,型号2320,厚度为25μm)中。
セルガード(注册商标)2320是由聚丙烯层、聚乙烯层和聚丙烯层形成的3层隔板。
使用上述正极、负极和隔板,在露点被控制为-50℃的干燥箱中制作了cr2032规格的硬币型电池。
<实施例2~16>
针对上述实施例1,分别改变了前驱体。
表1示出制造实施例2~16的正极活性物质时的前驱体和合成了的正极活性物质的组成比。
除此以外,与上述实施例1同样地进行,从而合成了实施例2~16的正极活性物质。
再者,实施例2~16的各前驱体,与实施例1同样地以化学计量比来称量并混合。例如,如果是实施例7,则以li2o/mno2/mn2o3/bi2o3=6/4/1/1的摩尔比分别称量各前驱体并混合。
另外,作为实施例2~16的正极活性物质而得到的化合物的空间群均为fm-3m。
另外,使用实施例2~16的各自的正极活性物质,与上述实施例1同样地进行,来制作出实施例2~16的硬币型电池。
<比较例1>
以li2co3/mn2o3/nb2o5=0.6/0.3/0.1的摩尔比分别称量了li2co3、mn2o3和nb2o5。
将得到的原料与适量的ф3mm的氧化锆制球一起放入45cc的氧化锆制容器内,在充氩手套箱内密闭。
从充氩手套箱中取出,利用行星型球磨机以300rpm进行了10小时的处理。
将所得到的混合物在氩气流中、950℃下进行10小时的烧成,从而得到了化合物。
对获得的化合物实施了粉末x射线衍射测定。
得到的化合物的空间群为fm-3m。
另外,利用icp发射光谱分析法和惰性气体熔融-红外线吸收法求出了所得到的化合物的组成。
其结果,获得的化合物的组成为li1.2mn0.6nb0.2o2。
另外,使用所得到的化合物作为正极活性物质,与上述实施例1同样地进行,来制作出硬币型电池。
<电池的评价>
将相对于正极的电流密度设定为1.0ma/cm2,对实施例1的电池充电直到电压达到5.2v为止。
然后,将放电终止电压设定为2.0v,以1.0ma/cm2的电流密度使实施例1的电池放电。
实施例1的电池的初次能量密度为841mwh/g。
将相对于正极的电流密度设定为1.0ma/cm2,对比较例1的电池充电直到电压达到5.2v为止。
然后,将放电终止电压设定为2.0v,以1.0ma/cm2的电流密度使比较例1的电池放电。
比较例1的电池的初次能量密度为580mwh/g。
另外,与实施例1同样地进行,来测定了实施例2~16的硬币型电池的能量密度。
将以上结果示于表1中。
表1
如表1所示,实施例1~16的电池的初次能量密度值大于580mwh/g。
即,实施例1~16的电池的初次能量密度高于比较例1的电池能量密度。
作为其原因,可以认为是因为:在实施例1~16中,使有效核电荷比nb高、且在充放电时能够进行氧化还原反应的元素进行了固溶。由此,可以认为,通过放电工作电压变高、且成为高容量,从而能量密度优良化。
另外,如表1所示,实施例2~11的电池的初次能量密度低于实施例1的电池的初次能量密度。
作为其原因,可以认为是因为:co的有效核电荷最高,,因此放电工作电压变得更高。由此,可以认为能量密度优良化。
另外,如表1所示,实施例2的电池的初次能量密度显示出与实施例1的电池的初次能量密度大致同等的值。
作为其原因,可以认为是因为:mn与co相比虽然有效核电荷低,但在费米能级附近mn与氧轨道适当地重叠,从而与co相比更能够利用氧的氧化还原反应。由此,可以认为,通过放电容量变高,从而能量密度显示出与实施例1同等的值。
另外,如图1所示,实施例3的电池的初次能量密度比实施例2的电池的初次能量密度高。
作为其原因,可以认为是因为:通过利用有效核电荷高的ni进行置换从而放电工作电压变高。由此,可以认为能量密度提高。
另外,如表1所示,实施例11的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例11中,li/mn比为1,因此不能适当地确保li的渗流路径,li离子扩散性下降。由此,可以认为能量密度下降了。
另外,如表1所示,实施例12的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例12的电池的初次充电中,过度地拉拢晶体结构内的li,从而晶体结构不稳定化,因此在放电中嵌入的li的量下降。由此,可以认为能量密度下降了。
另外,如表1所示,实施例13的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例13中,因合成时的li欠缺,因此mn规则地排列,从而不能充分地确保li离子的渗流路径,li离子扩散性下降。由此,可以认为能量密度下降了。
另外,如表1所示,实施例14的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例14中,由于初期结构的阴离子缺陷,导致充电时进行氧脱离,晶体结构不稳定化。由此,可以认为能量密度下降了。
另外,如表1所示,实施例15的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例15的电池的初次充电中,过度地拉拢晶体结构内的li,从而晶体结构不稳定化,因此放电时嵌入的li量下降。由此,可以认为能量密度下降了。
另外,如表1所示,实施例16的电池的初次能量密度比实施例2的电池的初次能量密度低。
作为其原因,可以认为是因为:在实施例16中,因合成时的li欠缺,因此mn规则地排列,从而不能充分地确保li离子的渗流路径,li离子扩散性下降。由此,可以认为能量密度下降了。
从以上的实施例2和实施例11~16的结果可知,通过在组成式lixmnyo2中满足1.9≤x+y≤2.0且1.5≤x/y≤2.0,能够更加提高初次能量密度。对于该结果,可以推定:即使在将组成式lixmnyo2的mn的一部分替换成其它的元素的情况下也能得到同样的效果。
产业上的可利用性
本公开的正极活性物质,可以很好地利用作为二次电池等电池的正极活性物质。
- 还没有人留言评论。精彩留言会获得点赞!