一种抗C5全人源单链抗体C5B3及其应用的制作方法
本发明属于生物工程领域,涉及一种抗c5全人源单链抗体c5b3及其应用。
背景技术
c5是补体很重要的成分,补体系统包括30余种成分,广泛存在于血清、组织液和细胞膜表面,补体不仅是机体固有免疫防御体系的重要组成部分,也是抗体发挥免疫效应的重要机制之一,并在不同环节参与适应性免疫应答及其调节。在炎症反应过程中c5转化酶将c5分解成c5a和c5b,c5a游离于液相,是重要的炎症介质,c5b经过一系列补体反应形成膜攻击复合物(mac),导致细胞裂解死亡。
补体激活是一种高度有序的级联反应,从而发挥广泛的生物学效应。正常情况下,补体激活及其末端效应均处于严密的调控之下,从而有效地维持机体的自稳功能,但是在免疫功能紊乱或不受控制的补体被激活时会对自身组织造成伤害。这与很多疾病的发生和发展密切相关,比如系统性红斑狼疮、类风湿关节炎、阵发性睡眠性血红蛋白尿、视神经脊髓炎等。因此,有关c5方面的治疗方法对很对疾病的治疗和预后有很大关系。
kohler和milstein于1975年创立了杂交瘤技术,第一次获得了专一识别抗原单一表位并与之特异性结合的单克隆抗体,开创了抗体广泛地作为治疗药物的新时代。单克隆抗体与多克隆抗体相比,单克隆抗体具有高特异性、高亲和力、副作用小等优点,大量的鼠单抗被研发应用并快速用于临床实验。然而在众多临床试验中却发现,鼠单克隆抗体因其对人体来说具有异源性,引起患者强烈的人抗鼠抗体反应(hama),无法多次使用;并且完整的抗体分子量较大,到达靶器官或者靶组织的药物很少。因此,从氨基酸残基序列的源头上对它们进行分子改造。抗体的人源化技术带来了治疗用基因工程抗体免疫原性的大大下降,但即使是人源化程度非常高的鼠单抗的人源化抗体,其中依然至少含有1%-5%的异源成分,依然可能引起患者的抗抗体反应。虽然人源化抗体目前在临床应用的抗体中独占鳌头,但随着人们在全人源抗体技术方面的进步,全人源抗体正逐步后来居上,占据了新抗体药物研发的主导位置。
目前关于阻断c5补体效应的单抗主要是鼠来源进行人源化改造获得的,人源化过程也较为复杂,而且人源化后依然存在hama反应,该反应影响抗体的治疗效果,可能对患者造成二次伤害,比如过敏反应、肾损害等,严重时可能危及生命。因此,人源抗体以其特有的优势越来越成为抗体研发的主流趋势。本发明基于以上研究背景,目前噬菌体展示技术在单抗筛选方面得到了广泛的应用,但针对不同的靶向目标及不同的噬菌体抗体库,有所不同。
技术实现要素:
针对现有技术中的缺陷和不足,本发明的第一个目的是提供一种抗c5全人源单链抗体c5b3,能够明显的抑制炎症反应过程中膜攻击复合物的形成,从而减少炎症反应过程中的损伤,可能对自身免疫性疾病及补体相关为特征的疾病提供了基于抗体的疗法。
本发明的第二个目的是提供c5全人源单链抗体c5b3在制备治疗自身免疫性疾病和/或补体为相关特征的疾病药物中的应用。
为达到上述目的,本发明采取的技术方案包括:
一种抗c5全人源单链抗体c5b3,所述的抗c5全人源单链抗体c5b3的dna序列选自以下一种的序列:seqidno:1所示序列;与seqidno.1具有90%以上同源性的序列。
可选的,所述的抗c5全人源单链抗体c5b3的氨基酸序列选自以下一种蛋白的编码序列:seqidno:2所示的序列;与seqidno.2具有90%以上同源性的蛋白序列。
可选的,所述的抗c5全人源单链抗体c5b3的重链可变区vhcdr1的氨基酸序列如seqidno:3所示;重链可变区vhcdr2的氨基酸序列如seqidno:4所示;重链可变区vhcdr3的氨基酸序列如seqidno:5所示;
抗c5全人源单链抗体c5b3的轻链可变区vlcdr1的氨基酸序列如seqidno:6所示,轻链可变区vlcdr2的氨基酸序列如seqidno:7所示,轻链可变区vlcdr3的氨基酸序列如seqidno:8所示。
一种含有抗c5全人源单链抗体c5b3的载体,该载体为pet30a,该载体上插入所述的抗c5全人源单链抗体c5b3。
一种重组宿主细胞bl21,所述的重组宿主细胞bl21含有所述的载体。
所述的抗c5全人源单链抗体c5b3在制备治疗自身免疫性疾病和/或c5补体为相关特征的疾病药物中的应用。
所述的抗c5全人源单链抗体c5b3在制备治疗炎症反应过程中膜攻击复合物的形成引起的自身免疫性疾病和/或c5补体为相关特征的疾病药物中的应用。
可选的,所述的自身免疫性疾病包括视神经脊髓炎、多发性硬化、系统性红斑狼疮和重症肌无力。
可选的,所述的c5补体为相关特征的疾病包括阵发性睡眠性血红蛋白尿、非典型溶血毒症综合征、外伤引起的炎症。
本发明的有益效果:
本发明的单链抗体针对补体c5,能够明显的抑制炎症反应过程中膜攻击复合物的形成,从而减少炎症反应过程中的损伤,可能对自身免疫性疾病及补体相关为特征的疾病提供了基于抗体的疗法。
附图说明
附图是用来提供对本公开的进一步理解,并且构成说明书的一部分,与下面的具体实施方式一起用于解释本公开,但并不构成对本公开的限制。在附图中:
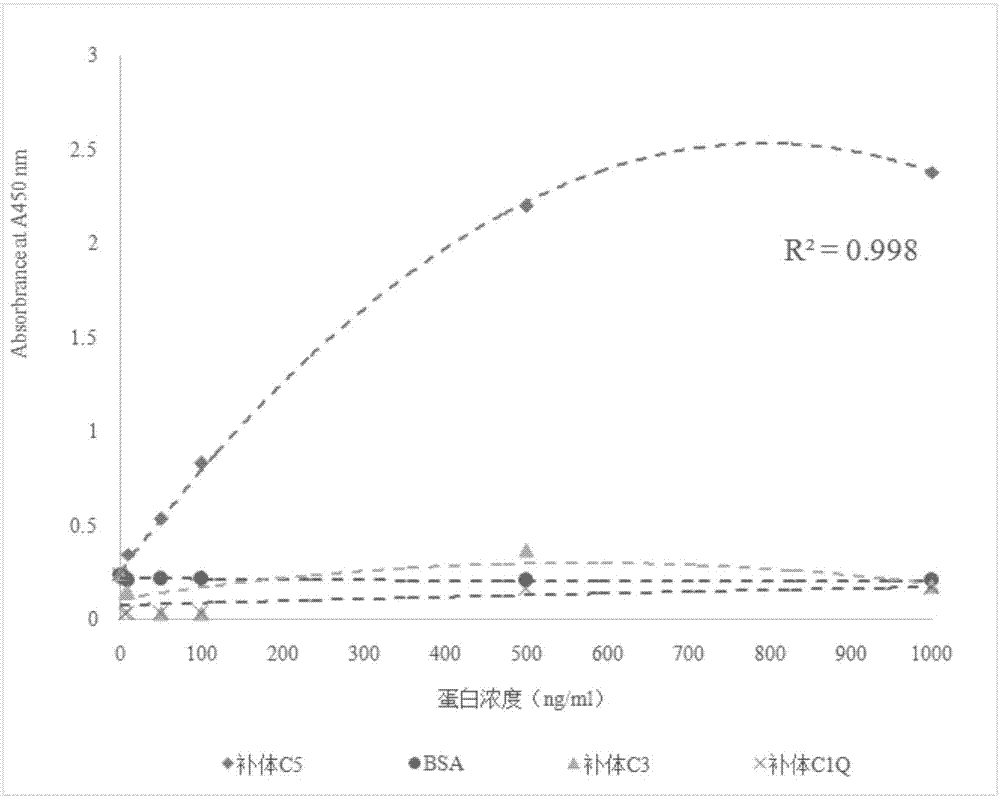
图1为elisa检测噬菌体c5b3抗体的特异性;
图2为重组的表达载体pet30a-c5b3结构示意图;
图3为纯化的c5b3单链抗体,大小约30kd;
图4为(左)c5b3减少补体沉积,(右)是减少补体沉积统计图;
图5为该发明单链抗体的功能验证,左图为阴性对照;右图为加了该单链抗体,死细胞(红色)明显减少;
图6为该抗发明c5单链抗体功能验证的量效关系,随着加入该发明单链抗体的量的增加,死细胞的数量也随之减少;
图7为该发明抗体体内实验验证结果,加入c5b3mab组有明显的保护作用,病灶明显较小;
图8为体内实验数据的统计分析图;
具体实施方法
以下结合附图对本公开的具体实施方式进行详细说明。应当理解的是,此处所描述的具体实施方式仅用于说明和解释本公开,并不用于限制本公开。
本发明基于全人源scfv单链抗体库,通过噬菌体展示的方法筛选得到全人源的抗c5的单链抗体,避免了hama反应,且已对进行了功能验证;与以往的抗c5的单链抗体的cdr区进行比较,差别较大,是全新的单抗药物。本发明为单链抗体,大小约30kd,蛋白分子量小,更易进去病灶部位起效,尤其是对脑部疾病,可以通过血脑屏障,缩短了到达病灶的时间,可起到更好的治疗效果。
全人源抗补体c5单链抗体c5b3,所述全人源抗补体c5单链抗体c5b3的dna序列如下所示:
atggccgaggtgcagctgttggagtctgggggaggcttggtacagcctggggggtccctgagactctcctgtgcagcctctggattcactttctctatgtatgatatgagctgggtccgccaggctccagggaaggggctggagtgggtctcaagttcttcttctggtggcattacttcgtacgcagactccgtgaagggccggttcaccatctccagagacaattccaagaacacgctgtatctgcaaatgaacagcctgagagccgaggacacggccgtatattactgtgcgaaaacgacgcggttttttgactactggggccagggaaccctggtcaccgtctcgagcggtggaggcggttcaggcggaggtggcagcggcggtggcgggtcgacggacatccagatgacccagtctccatcctccctgtctgcatctgtaggagacagagtcaccatcacttgccgggcaagtggctcgaacatcggaagtaatattttaaattggtatcagcagaaaccagggaaagcccctaagctcctgatctataatgaccatcgtttgcaaagtggggtcccatcaaggttcagtggcagtggatctgggacagatttcactctcaccatcagcagtctgcaacctgaagattttgcaacttactactgtcaacaggctcggactagtccttctacgttcggccaagggaccaaggtggaaatcaaacgg。
所述全人源抗补体c5单链抗体c5b3的氨基酸序列如下所示:maevqllesggglvqpggslrlscaasgftfsmydmswvrqapgkglewvsssssggitsyadsvkgrftisrdnskntlylqmnslraedtavyycakttrffdywgqgtlvtvssggggsggggsggggstdiqmtqspsslsasvgdrvtitcrasgsnigsnilnwyqqkpgkapklliyndhrlqsgvpsrfsgsgsgtdftltisslqpedfatyycqqartspstfgqgtkveikr。
该全人源抗补体c5单链抗体c5b3含有完整的抗体重链可变区vh和轻链可变区vl,其重链可变区vhcdr1的氨基酸序列为:gftfsmyd,重链可变区vhcdr2的氨基酸序列为:sssggit,重链可变区vhcdr3的氨基酸序列为:akttrffdy;其轻链可变区vlcdr1的氨基酸序列为:gsnigsni,轻链可变区vlcdr2的氨基酸序列为:ndh,轻链可变区vlcdr3的氨基酸序列为:qqartspst。
本发明基于pet30a重组了一种表达载体pet30a-c5b3,含有(3)所述的完整核酸序列,且转化进入bl21能大量可溶性表达c5b3。
自身免疫性疾病和/或补体相关为特征的疾病,其中,自身免疫性疾病包括视神经脊髓炎、多发性硬化、系统性红斑狼疮、重症肌无力等自身免疫性疾病,c5补体相关特征的疾病包括阵发性睡眠性血红蛋白尿(pnh)、非典型溶血毒症综合征(ahu)、外伤引起的炎症。
1.术语解释:
抗体(antibody),又称免疫球蛋白(immunoglobulins,ig),是机体免疫细胞被抗原激活后,b细胞分化成熟为浆细胞后所合成、分泌的一类能与相应抗原特异性结合的具有免疫功能的球蛋白。ig分子的基本结构是由四条多肽链组成的。即由两条相同的相对分子质量较大的肽链(称为重链,heavychain,h链)和两条相同的相对分子质量较小的肽链(称为轻链,lightchain,l链)组成,l链和h链的v区分别称为vl和vh。在vl和vh中某些局部区域的氨基酸组成和排列顺序具有更高的变化程度,且为抗体抗原结合的地方,因此称为互补决定区(complementarity-determiningregion,cdr),包括三个不同的部位cdr1,cdr2和cdr3,一般cdr3可变程度更高。超变区也是ig分子独特性决定簇(idiotypicdeterminants)主要存在的部位。在大多数情况下h链在与抗原结合中起更重要的作用。在v区中非cdr部位的氨基酸组成和排列相对比较保守,称为骨架区(frameworkregion,fr)。vl中的超变区有三个fr1、fr2、fr3。
鼠源性单克隆抗体:早期的治疗性抗体大多数是通过b淋巴细胞杂交瘤技术制备的、只针对一种抗原决定簇的鼠源性单克隆抗体。鼠源性单克隆抗体由于人鼠之间遗传背景的差异,在人体内使用小鼠抗体时会因为外源性的蛋白抗原而引起人抗鼠抗体反应,并充分激活人的效应功能,这极大地限制了单克隆抗体在疾病治疗上的应用和发展。相对而言,鼠源性单克隆抗体治疗剂一般难以获得成功。鼠源性抗体用于人体后抗体分子的半衰期较短,需重复应用,而反复大量应用后又会产生hama应答,导致鼠源性抗体被人体清除而药效降低。
人源化单克隆抗体:人源化抗体包括改形抗体和镶面抗体等,其特点是降低hama反应,在血中半衰期也相对较长。改形抗体也称cdr移植抗体(cdrgraftingantibody),是将鼠单抗的cdr移植到人单抗的框架区,使人单抗获得与鼠单抗一样的抗原特异性,并可以最大限度地降低鼠单抗的异源性。与嵌合抗体相比,改形抗体进一步减少了抗体中鼠源部分的比例,降低了hama反应。
全人源抗体:尽管人源化抗体的小鼠成分含量明显减少,但人源化抗体的免疫原性并不能达到令人满意的结果,其免疫原性还不能够被忽视,有的甚至达到无法忍受的程度。因此,全人源抗体的研究自然成为当前的发展趋势,全人源抗体可以通过使用人杂交瘤细胞、转基因动物,以及噬菌体抗体库等途径得以实现。噬菌体展示技术、转基因鼠以及其他分子生物学技术的利用,使得全人源单克隆抗体的研究得到快速发展。
2.噬菌体展示
(1)利用固相淘选方法对抗体噬菌体文库进行抗原特异性淘选,具体操作如下:
复苏噬菌体文库(来自于creactivebiolabs)于2ml的2*ty培养基中,于37℃摇床中培养至od=0.4,接种至50ml培养基扩大培养2h。加入m13ko7辅助性噬菌体(invitrogen);37℃静置孵育30-60min,摇床孵育30-60min,离心4500r/min5-10min,弃上清,用含有100ug/ml氨苄青霉素和50ug/ml卡那霉素的培养基重悬细胞,并于30℃摇床中过夜培养;离心8000r/min3-5min沉淀噬菌体文库,转移上清至干净的50ml离心管,25ml/管。向每只离心管内加入1/5上清体积的peg/nacl(20%peg-8000,2.5mol/lnacl,下同),混合均匀,置于冰上至少2h,离心,12000r/min,20min,弃上清;用2ml无菌pbs重悬噬菌体,离心,5000r/min,10min,除去剩余的细胞碎片。
具体筛选过程如下:
(1)将补体c5用0.1mol/lph9.6碳酸钠碳酸氢钠溶液做一定量稀释后包被96孔板,每轮包被的抗原量为300-800ng,包被体系每孔50~100μl,4℃过夜;
(2)次日洗去板中未吸附的抗原,用2%bsa(pbs)或用5%脱脂奶粉(pbs)于常温封闭1-2h;
(3)弃封闭液,在每孔加入50~70μl噬菌体抗体库,第一轮和第二轮常温孵育2h。第三轮孵育1h,第四轮及第五轮孵育40min,较少孵育时间,较少非特异性吸附及亲和能力弱的噬菌体抗体,弃孔中未结合噬菌体,用0.1%pbst缓冲液(1*pbs中加入0.1%tween-20)和pbs洗液洗每一孔,共洗6-8次,之后几轮依次增加次数提高筛选严格度,充分洗去非特异性吸附噬菌体;
(4)每孔加入ph值2.2的甘氨酸盐酸洗脱缓冲液50μl,第一轮、第二轮及第三轮室温孵育10min用于扩增,第三轮筛选后已有部分有亲和力及特异性的克隆,第四轮及第五轮先用甘氨酸预洗脱5min,弃去洗脱液,再加入50ul甘氨酸洗脱15min。期间用移液器反复吹打几次,但注意勿吹出过多气泡。加入2mol/ltris-hclph8.8,使溶液的ph值在7.0左右,以中和洗脱下来的噬菌体溶液;
(5)将洗脱液立即加入3ml新鲜制备的od600=0.6左右的e.colitg1菌,37℃孵育1-2h。加入100ug/ml氨苄青霉素及2%葡萄糖37℃220r/min过夜;
(6)加入1012pfu的辅助噬菌体m13ko7,37℃1-2h。4500r10min弃上清,加入100ug/ml氨苄青霉素及卡那霉素50μg/ml,37℃振荡培养过夜;
(7)8000r/min5min收集上清,加入peg/nacl冰上2-4h,12000r20-30min收集噬菌体,弃上清加入1ml无菌pbs溶解噬菌体,用于下一轮筛选,加入20%甘油-80℃可长期保存。本发明进行了5轮筛选;
(8)经5轮富集筛选后,将洗脱下来的噬菌体感染新鲜制备的tg1菌,37℃过夜培养后,随机挑265个克隆摇菌,加入辅助性噬菌体,获得噬菌体抗体上请,用于elisa检测。
3.elisa分析及测序分析
用碳酸盐包被液(ph9.6)稀释补体c5,每个反应孔中加50ul,4℃包被过夜;弃去反应孔中的液体,用1*pbs缓冲液洗涤3次,每孔加200ul2%的bsa封闭液,室温下封闭1-2h;用1*pbs缓冲液洗涤3次;加入含scfv抗体的噬菌体上清和阴性对照50ul/孔,室温孵育1-2h,用1*pbs缓冲液洗涤5次;加入封闭缓冲液稀释(1:1000)的anti-m13(hrp)单抗50ul/孔(creativediagnostics),室温孵育1h,用1*pbs缓冲液洗涤5次,;在每个反应孔里加入tmb底物溶液(50ul/孔)反应5-10min;加入终止溶液(2m硫酸,50ul/孔)终止反应;用酶标仪读取450nm的吸光值;重复elisa,根据elisa的结果,选取亲和力较高50个克隆测序,测序结果进行同源性分析,共包括9个序列,其中c5b3,c5a6,c5b35,c5a102出现的频率较高,c5b3出现的频率最高,共9个克隆为c5b3,且elisa呈强阳性且有很好的特异性(图1)。
4.c5b3质粒的构建和转染
抗补体c5的单链抗体c5b3,c5a6,c5b35基因以噬菌体载体的形式扩增,以c5b3为例进行说明,酶切位点选用bamhi及noti,设计上游物bamhi-r:aggatccgccgaggtgcagctgttg下游引物noti-f:tgcggccgcccgtttgatttccacctt,pcr扩增得到c5b3单链抗体基因。用bamhi、noti(takara)酶切目的片段及pet28a、pgex-4t载体,将目的片段及载体用t4dna连接酶连接,按照外源基因与载体dna的分子摩尔比为3:1配制连接反应体系:10×t4dnaligasebuffer(takara)1μldna片段约5ul载体dna约2ult4dnaligase1μl4℃连接过夜连接,将连接产物加入e.colidh5α感受态(thermo),37℃孵箱过夜待菌落出现,行菌落pcr鉴定,pcr鉴定阳性的结果测序,测序结果正确的转入表达菌e.colibl21(de3),pet28a-c5b3、pgex-4t-c5b3均不能表达。尝试单链抗体c5b3基因与pet-30a载体相连接,形成pet30a-c5b3(图2),转化进入e.colibl21(de3)。转化产物涂布平板,阳性克隆在含有卡那霉素70μg/ml的lb平板中挑取出来并测序。用dnaman比对测序结果,将构建成功的克隆转入e.colibl21(de3)菌。
随机挑选出转入了pet30a-c5b3的重组宿主菌bl21(de3)克隆扩大培养。在10ml含70μg/ml卡那霉素的lb培养基中接种测序正确的高表达单克隆,37℃下,220rpm培养一夜。次日,将菌液平均加至两瓶500ml含70ug/ml卡那霉素的lb培养基中,相同条件下摇至od600值达0.6左右。添加1m的iptg至终浓度0.2mm,16℃,180rpm低温诱导20h。诱导表达结束后,将菌液转移至50ml离心管。8000rpm,4℃下冷冻离心5min,多次收集。用10ml预冷pbs重悬沉淀菌体。超声波破碎菌体,参数为:功率400w,工作时间5s,间歇6s,每次循环99次,重复4次。4℃下10000rpm离心30min,将上清过0.22um滤膜除菌过滤,即获得单链抗体蛋白粗液。先用双蒸水冲洗镍柱10min,再用pbs平衡柱子10min,冲洗的流速为2ml/min。将单链抗体蛋白粗液上柱,控制流速为2ml/min。收集流出液,再次上样,结束后再用20mlpbs平衡镍柱。接着,分别用含有25mm,100mm,300mm,600mm咪唑的洗脱缓冲液洗脱镍柱上的蛋白,每个浓度梯度收满6ml管。每管50ul进行变性sds-page电泳,分离胶浓度为12%,选择蛋白纯度最高的进行后续实验(图3)。最后用双蒸水冲洗镍柱10min,保存在4℃环境中20%乙醇内。
5.功能验证
体外实验验证:将cho细胞(表达m23-aqp4)以20,000个细胞的密度接种在96孔微量培养板(corning,usa)上并在37℃下在5%co2的潮湿气氛中生长。细胞用pbs洗涤并在室温下用20%热失活的nmo血清温育30min。将2%混合的正常人补体血清(innovativeresearch,usa)和c5mab的溶液孵育30min,然后加入到cho细胞中。在添加人补体,热灭活的nmo血清和c5b3后,然后将cho细胞在27℃温育60min。通过细胞荧光c5b-9显示形成膜攻击复合物的量,加了c5b3mab的实验组膜攻击复合物明显减少(图4);用活细胞/死细胞染色试剂盒(invitrogen,usa)标记死细胞和活细胞,死细胞(红色)和活细胞(绿色)被计数。与对照组相比,c5a6、c5b35无保护作用,c5b3实验组有对该视神经脊髓炎模型明显的保护作用(图5、图6)。可能对多发性硬化、系统性红斑狼疮、重症肌无力等自身免疫性疾病和/或阵发性睡眠性血红蛋白尿(pnh)、非典型溶血毒症综合征(ahu)、外伤引起的炎症均起到保护作用。
体内实验验证:动物模型的诱导:将体重相匹配的雌性c57bl/6(8-12周龄)小鼠用10%水合氯醛(3ml/kg,腹膜内)麻醉,并置于立体定向框架(rwdlifescience,shenzhen,china)上。中线头皮切口被暴露前囟。对于实质内注射(脑内注射视神经脊髓炎免疫球蛋白g和人补体在小鼠脑实质中产生视神经脊髓损伤),在前囟右侧2mm的颅骨位置处用直径0.7mm的毛刺孔高速钻头(rwd)。将连接到25-ll气密玻璃注射器(hamilton,reno,nv)的33-g针插入3mm深以注入6ulnm0-igg,4ul人补体(含或不含)100ugc5b3mab总体积为15ul(1ul/分钟)。麻醉期间保证小鼠直肠温度保持在37-38℃。消毒表面后,将头皮缝合。7天后,将小鼠麻醉(10%水合氯醛)并用磷酸盐缓冲盐水(pbs)心脏灌注,然后用4%多聚甲醛(pfa)通过左心室灌注。将脑在4%pfa中后固定过夜,用30%的蔗糖溶液脱水,然后用包埋剂包埋成冷冻切片。
选择穿过针道的冷冻切片(6mm)。将冷冻切片用冷丙酮渗透并封闭(5%bsa),然后在4℃下用以下一级抗体免疫染色过夜:兔多克隆抗水通道蛋白aqp4(1:100,santacruzbiotechnology),山羊多克隆抗星形胶质细胞gfap(1:1000,abcam),大鼠抗髓磷脂碱性蛋白(mbp)(1:200,aa82-87,millipore),pbs洗一抗5遍,接着是合适的alexafluor二抗(1:1000,invitrogen)。用leicadm6000b显微镜检查组织切片。7天后,脑内注射igg-nmo和人补体产生gfap,aqp4和mbp的显着损失。加入c5b3mab的实验组,小鼠注射部位周围的gfap,aqp4和mbp明显减少(图7,图8),明显减小了视神经脊髓炎自身抗体与补体造成的病灶,可能对多发性硬化、系统性红斑狼疮、重症肌无力等自身免疫性疾病和/或阵发性睡眠性血红蛋白尿(pnh)、非典型溶血毒症综合征(ahu)、外伤引起的炎症均起到保护作用。
以上结合附图详细描述了本公开的优选实施方式,但是,本公开并不限于上述实施方式中的具体细节,在本公开的技术构思范围内,可以对本公开的技术方案进行多种简单变型,这些简单变型均属于本公开的保护范围。
另外需要说明的是,在上述具体实施方式中所描述的各个具体技术特征,在不矛盾的情况下,可以通过任何合适的方式进行组合。为了避免不必要的重复,本公开对各种可能的组合方式不再另行说明。
此外,本公开的各种不同的实施方式之间也可以进行任意组合,只要其不违背本公开的思想,其同样应当视为本公开所公开的内容。
核苷酸序列表电子文件
<110>陕西师范大学
<120>一种抗c5全人源单链抗体c5b3及其应用
<160>10
<210>1
<211>729
<212>dna
<213>全人源
<220>全人源抗补体c5单链抗体c5b3
<400>1
atggccgaggtgcagctgttggagtctgggggaggcttggtacagcctggggggtccctgagactctcctgtgcagcct
ctggattcactttctctatgtatgatatgagctgggtccgccaggctccagggaaggggctggagtgggtctcaagttc
ttcttctggtggcattacttcgtacgcagactccgtgaagggccggttcaccatctccagagacaattccaagaacacg
ctgtatctgcaaatgaacagcctgagagccgaggacacggccgtatattactgtgcgaaaacgacgcggttttttgact
actggggccagggaaccctggtcaccgtctcgagcggtggaggcggttcaggcggaggtggcagcggcggtggcgggtc
gacggacatccagatgacccagtctccatcctccctgtctgcatctgtaggagacagagtcaccatcacttgccgggca
agtggctcgaacatcggaagtaatattttaaattggtatcagcagaaaccagggaaagcccctaagctcctgatctata
atgaccatcgtttgcaaagtggggtcccatcaaggttcagtggcagtggatctgggacagatttcactctcaccatcag
cagtctgcaacctgaagattttgcaacttactactgtcaacaggctcggactagtccttctacgttcggccaagggacc
aaggtggaaatcaaacgg
<210>2
<211>243
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3的氨基酸序列
<400>2
maevqllesggglvqpggslrlscaasgftfsmydmswvrqapgkglewvsssssggitsyadsvkgrftisrdnsknt
lylqmnslraedtavyycakttrffdywgqgtlvtvssggggsggggsggggstdiqmtqspsslsasvgdrvtitcra
sgsnigsnilnwyqqkpgkapklliyndhrlqsgvpsrfsgsgsgtdftltisslqpedfatyycqqartspstfgqgt
kveikr
<210>3
<211>8
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3重链可变区vhcdr1的氨基酸序列
<400>3
gftfsmyd
<210>4
<211>7
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3重链可变区vhcdr2的氨基酸序列
<400>4
sssggit
<210>5
<211>9
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3重链可变区vhcdr3的氨基酸序列
<400>5
akttrffdy
<210>6
<211>8
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3轻链可变区vlcdr1的氨基酸序列
<400>6
gsnigsni
<210>7
<211>3
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3轻链可变区vlcdr2的氨基酸序列
<400>7
ndh
<210>8
<211>9
<212>prt
<213>全人源
<220>全人源抗补体c5单链抗体c5b3轻链可变区vlcdr3的氨基酸序列
<400>8
qqartspst
<210>9
<211>25
<212>dna
<213>全人源
<220>上游物bamhi-r
<400>9
aggatccgccgaggtgcagctgttg
<210>10
<211>27
<212>dna
<213>全人源
<220>下游引物noti-f
<400>10
tgcggccgcccgtttgatttccacctt
- 还没有人留言评论。精彩留言会获得点赞!