一种镇痛药物组合物的制作方法
本发明涉及一种镇痛药物组合物,属于医药技术领域。
背景技术:
疼痛是临床上最常见的症状,也是当今困扰人类健康的严重问题之一。据美国医学研究报告,在美国大约30%人群经历着慢性疼痛,这个比例超过了心脏病、癌症、糖尿病患者的总和。我国尚缺乏大规模的疼痛流行病学调查,据局部地区流行病学报告,北京市朝阳区慢性疼痛发生率为53.0%。另外我国已成为癌症发病和死亡大国。据全国肿瘤登记中心统计显示,2015年中国癌症新增429万例,死亡281万例,在这些癌症患者中高达60%的患者伴有不同程度的慢性疼痛。据此估计,我国患有慢性疼痛的人群数量非常惊人。慢性疼痛会给患者带来持久、难以忍受的痛苦,是致病、致残、致死的重要原因之一。由于慢性疼痛具有复杂性、长期性和对治疗的抵抗性,其治疗要远比急性疼痛棘手。目前临床上使用的镇痛药物主要是非甾体解热镇痛药和阿片类镇痛药,其中阿片类药物是治疗急性锐痛和中、重度疼痛最有效的药物。然而,在临床用药过程中,长期慢性使用阿片类镇痛药如吗啡、可待因、芬太尼等会产生呼吸抑制,耐受性,依赖性甚至成瘾等许多严重的不良反应。这些不良反应大大限制了阿片类药物在临床上的广泛应用。
实际上,尽管目前临床上可以使用的镇痛药物有很多种,但这些药物对于最大的疼痛患者群体即各种慢性疼痛患者的镇痛效果并不尽如人意。在镇痛药物研究领域,探索具有强效镇痛作用而滥用和成瘾潜力较低的药物一直是重要的研究方向之一。目前开发新型镇痛药物一条重要策略就是将两种及以上的药物组合形成新型制剂,希望药物组合后能够增强现有药物的镇痛效果,通过减少给药剂量而减少其副作用,以及预防和减少药物耐受性以及成瘾性的发生。
青藤碱(sinomenine)是从防已科植物青风藤的根茎中提取出来的一种生物碱,结构类似吗啡,文献报道其具有抗炎、免疫抑制、镇痛以及抗肿瘤等多种药理作用,在临床上已有相关制剂用于治疗风湿性关节炎等疾病。青藤碱的化学结构式如式(ⅰ)所示:
青藤碱的镇痛作用研究可追溯到上世纪70-80年代,研究发现青藤碱对急性疼痛具有一定的镇痛活性,且无成瘾性,与吗啡无交叉耐受性。近年来研究发现青藤碱对慢性疼痛模型具有良好镇痛效应,例如青藤碱对炎症性疼痛以及光化学性坐骨神经损伤导致的神经病理性疼痛动物模型,部分坐骨神经损伤(ssni)神经源性疼痛大鼠模型,坐骨神经慢性压榨性损伤(cci)神经病理疼痛大鼠模型,以及完全弗氏佐剂(cfa)注射引起的慢性炎症疼痛小鼠模型均具有镇痛作用。另外,青藤碱对急性疼痛如手术后痛也有良好镇痛效应。
中国专利cn1078467c公开了青藤碱在制备治疗术后疼痛的药物中的应用。cn104257658b公开了青藤碱在制备治疗慢性疼痛伴抑郁行为药物中的应用。cn101073621b公开了一种治疗风湿疼痛的药物组合物,该组合物由盐酸青藤碱与祖师麻组成。cn102813924b公开了一种基于青藤碱的用于镇痛的药物组合产品,专利中报道青藤碱单独使用对神经疼痛没有镇痛作用,但与gaba类药物加巴喷丁以及与扑热息痛的联用有显著的协同镇痛作用。cn103083401b公开了一种川芎提取物和青风藤提取物组成的复方药物组合物,用于治疗坐骨神经痛,手术后疼痛,癌症疼痛。其中青风藤提取物选自含有青藤碱50%以上的提取物。cn106333950a公开了一种治疗癌侵袭引起的镜像痛的药物,其活性成分中包含青藤碱与川芎嗪。以上专利显示了青藤碱单独应用或者与其它药物组合产品可以用于治疗临床上各种疼痛,但是现有各种技术资料显示这些青藤碱的相关产品的镇痛活性要远远低于阿片类镇痛药物,如果在针对临床顽固的慢性疼痛患者的治疗时,可能会在较大剂量时镇痛效果仍然不理想,一旦超过临床常规剂量又会引起许多不良反应。
技术实现要素:
本发明的目的是解决现有技术中阿片类药物及青藤碱作为镇痛药物时存在的不足,提供一种镇痛药物组合物,其对各种急慢性疼痛具有良好的镇痛作用,且长期用药不产生耐受性与成瘾性。
技术方案
本发明采用大鼠坐骨神经慢性压迫性损伤(chronicconstrictioninjury,cci)神经病理性疼痛模型和大鼠后足注射完全弗氏佐剂(cfa)致炎症疼痛模型,将青藤碱和阿片类药物(吗啡)先分别单独用药,然后再将其按不同比例进行联合用药,与各自单独用药结果进行比较,发现青藤碱和阿片类药物在镇痛方面有显著的协同增强作用,而且长期用药不产生耐受性与成瘾性。
具体方案如下:
一种镇痛药物组合物,包括青藤碱类药物和阿片类药物,青藤碱类药物和阿片类药物的重量比为10:1到300:1;
所述青藤碱类药物选自青藤碱、青藤碱盐酸盐、青藤碱硫酸盐或青藤碱磷酸盐中的任意一种;
所述阿片类药物选自吗啡、可待因、芬太尼或它们的盐酸盐、硫酸盐、磷酸盐、醋酸盐中的任意一种。
进一步,优选青藤碱类药物和阿片类药物的重量比为60:1到300:1。
进一步,所述青藤碱类药物优选为青藤碱。
进一步,所述阿片类药物优选为吗啡。
进一步,所述镇痛药物组合物还可以包括药用辅料,如药用赋形剂、稀释剂和/或载体等。
上述镇痛药物组合物的制备方法:将青藤碱类药物和阿片类药物混合均匀,即得,可以采用本领域常规制备方法制备成医学药剂学上常用的药物制剂,所述的药物制剂可以为汤剂、颗粒剂、片剂、丸剂或者液体制剂等。
本发明的药物制剂通常以皮下注射方式使用,当然也可以采用其它给药方式。较优的是大鼠cfa造模后给药用量为青藤碱13.1mg/kg+吗啡0.07mg/kg或者青藤碱8.7mg/kg+吗啡0.14mg/kg。大鼠cci造模后给药用量为青藤碱9.0mg/kg+吗啡0.095mg/kg,或者青藤碱6.8mg/kg+吗啡0.024mg/kg。
本发明的有益效果:本发明的镇痛药物组合物有显著的镇痛作用,单次急性给药以及慢性长期给药均能够有效减轻cci神经病理性疼痛以及cfa炎症性疼痛,而且长期用药不产生耐受性与成瘾性,适用于临床上各种顽固性疼痛的药物治疗,尤其是神经病理性疼痛以及炎症疼痛。本发明的镇痛药物组合物用量低,阿片类药物的用量仅为临床常规剂量的1/6到1/40甚至更低,青藤碱的用量可使用临床常规剂量或降低到常规剂量的1/2到1/3。正是由于减少了给药剂量而减少药物副作用,从而预防了阿片类药物耐受性以及成瘾性的发生。
所述神经病理性疼痛是指由于外周或中枢躯体感觉神经系统的损伤或疾病而直接造成的疼痛,表现为自发性、痛觉过敏、异常疼痛或感觉异常等临床特征。本发明所述的cci神经痛模型已被国际上普遍接受为代表性的神经病理性疼痛模型。本发明所述的“炎症性疼痛”,是指由于创伤、细菌或病毒性感染以及外科手术引起外周组织损伤导致炎症时所发生的疼痛。cfa致炎症模型被普遍接受为代表性的佐剂关节炎症性疼痛模型,可模拟临床上的自身免疫性炎症疾病如风湿关节炎的疼痛。慢性疼痛是指由于组织损伤、疾病相关或者自发性引起的疼痛持续或反复发作超过12周或者超过组织愈合所需的时间。慢性疼痛最典型的两种类型即为神经病理性疼痛与炎症性疼痛。而癌症性痛,在此特指癌症直接引起的疼痛,例如骨肿瘤或骨转移所致的骨痛,肺癌侵及胸膜引起的胸痛,脑肿瘤压迫引起头痛及脑神经痛等。癌性疼痛是一种复杂性慢性疼痛,目前认为其主要机制涉及到神经病理性疼痛与炎症性疼痛。
对于本领域的技术人员而言,由于青藤碱和阿片类药物(吗啡)各自单独应用对临床各种急慢性疼痛均有效,所以显而易见的是本发明镇痛药物组合物所针对的临床上疼痛类型应不仅限于本发明中所述的炎症性疼痛(如关节炎痛和腰背痛)和神经病理性疼痛(如神经和脊髓损伤痛、脑卒中后痛等),应还包括临床上其他类型的疼痛,包括癌症疼痛、术后疼痛及严重内脏疼痛等等。
附图说明
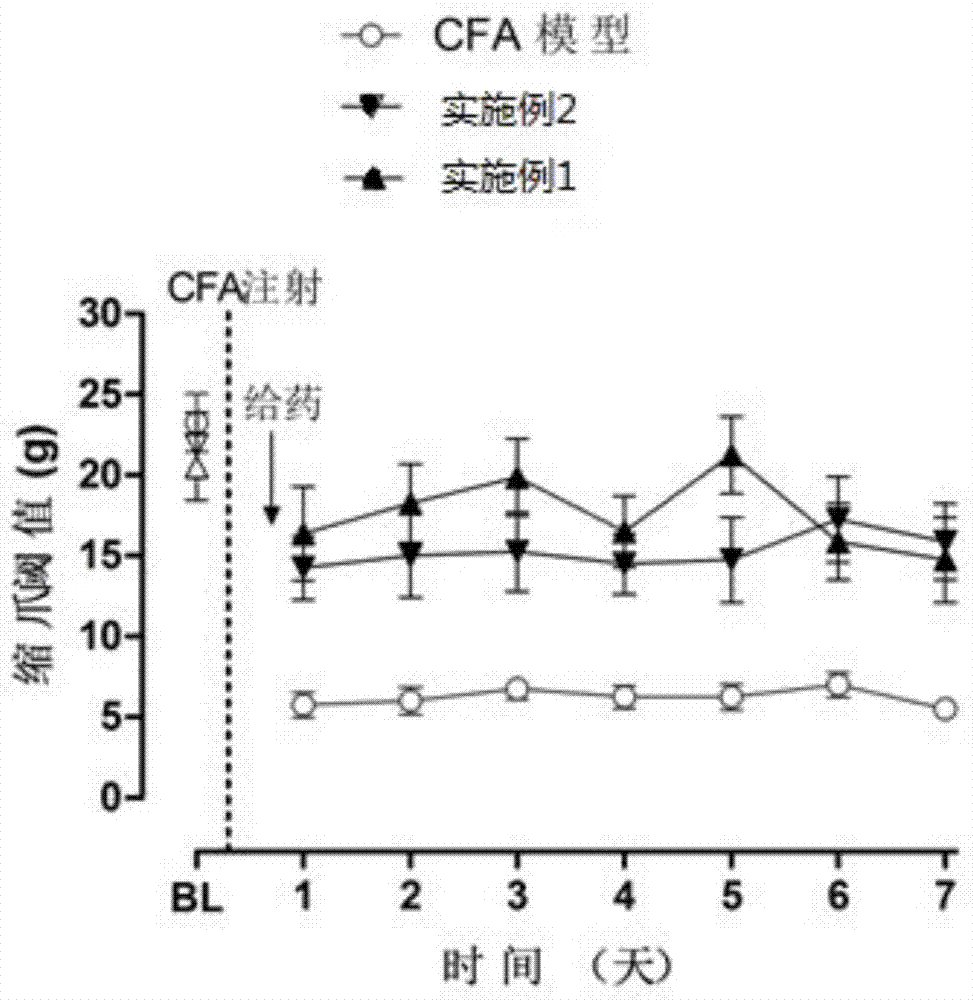
图1是实施例1-2的镇痛药物组合物单次给药对cfa炎症疼痛的镇痛效应曲线图;
图2是实施例1-2的镇痛药物组合物反复多次给药对cfa炎症疼痛的慢性镇痛效应曲线图;
图3是实施例3-4的镇痛药物组合物对cci神经病理性疼痛的镇痛效应曲线图;
图4是实施例3-4的镇痛药物组合物多次给药对cci神经病理性疼痛的慢性镇痛效应曲线图。
具体实施方式
下面结合附图和实施例对本发明作进一步说明。以下实施例是在以本发明技术方案为前提下进行实施,给出了详细的实施方式,但本发明的保护范围不限于下述的实施例。值得说明的是,下述实施例中,涉及药物剂量时,如无特别说明,其单位“mg/kg”是指每kg受试对象的体重所对应的药物剂量(mg)。以下实施例所用的青藤碱,购自阿拉丁公司(aladdinindustrialinc.),实验室用,也可市购,使用生理盐水配置成10mg/ml储备液,储存于4℃备用。所使用吗啡为盐酸吗啡注射液(10mg/ml),经卫生行政部门批准购于当地医院,并于当地公安局备案。
实施例1
取8.7份的青藤碱和0.14份的吗啡(青藤碱:吗啡=62:1),将二者混合均匀,即得镇痛药物组合物。
实施例2
取13.1份的青藤碱和0.07份的吗啡(青藤碱:吗啡=187:1),将二者混合均匀,即得镇痛药物组合物。
实施例3
取9.0份的青藤碱和0.095份的吗啡(青藤碱:吗啡=95:1),将二者混合均匀,即得镇痛药物组合物。
实施例4
取6.8份的青藤碱和0.024份的吗啡(青藤碱:吗啡=283:1),将二者混合均匀,即得镇痛药物组合物。
性能测试
将实施例制得的镇痛药物组合物进行单次给药对cfa炎症疼痛的镇痛效应、反复多次给药对cfa炎症疼痛的慢性镇痛效应、单次给药对cci神经病理性疼痛的镇痛效应和反复多次给药对cci神经病理性疼痛的慢性镇痛效应的测试,并与单独用药的青藤碱和吗啡进行对比,试验方法和测试结果如下。
1.单次给药对cfa炎症疼痛的镇痛效应
(1)cfa致炎症模型的制备方法:大鼠用异氟烷短暂麻醉后,右后爪底用酒精消毒片消毒,然后50微升cfa注射入足底皮下。注射结束后2小时以及随后每隔24h测定机械痛阈值(pwt)。机械痛阈值测定方法具体为:使用von-frey纤维丝测量套装(stoelting有限责任公司,美国),选用其中7种强度的von-frey细丝进行测定,按照大约对数型增加弯曲力度(等效于2,4,6,8,10,15,26g),测量手术侧(右侧)后爪在不同强度细丝刺激下的缩爪阈值作为其机械性痛阈值。测量时,大鼠单独放在置于金属筛网上的有机玻璃格子内,适应环境至少15分钟,von-frey细丝从2g开始,垂直刺激大鼠右后肢的爪底(以细丝稍弯曲作为完全受力的标准),持续时间≤4s,若出现缩爪视为阳性反应,否则为阴性。每个强度的纤维细丝均连续测定3次,若有2次或2次以上的反应则视为pwt。最大力度为26g,大于此值时仍记为26g。最小的力度记为2g,pwt越低说明机械痛敏越严重。
(2)动物分组与实验设计:取sd大鼠40只(由南通大学实验动物中心提供),标准体重200±20g,将其分成5组,每组8只;即cfa模型组(阴性对照,给予生理盐水),青藤碱20mg/kg单独用药组,吗啡1.0mg/kg单独用药组,以及本发明实施例1(青藤碱8.7mg/kg+吗啡0.14mg/kg)与实施例2(青藤碱13.1mg/kg+吗啡0.07mg/kg)给药组,均采用皮下注射给药。各组大鼠在造模前测定其pwt基线值(bl),然后全部给予cfa造模,24h后先测试各组给药前的pwt值,然后于给药后0.5、1、1.5、2、2.5、3、3.5、4h测定其pwt。测定pwt方法同前述。
(3)实验结果:实施例1-2的镇痛药物组合物及青藤碱与吗啡单独用药对cfa炎症疼痛的镇痛效果比较如图1所示。cfa模型组在测试期间的4h内,重复测量的疼痛阈值都稳定保持在最低水平。统计结果表明青藤碱20mg/kg组在2.5h达最大效应,并有明显镇痛效应(p<0.05);吗啡1.0mg/kg组在1-1.5h时间段有明显镇痛效应,在1.5h达最大效应(p<0.05);实施例1组在1-2h时间段有明显镇痛效应,在1.5h达最大效应(p<0.05);实施例2组在1.5-2.5h时间段有明显镇痛效应,在2h达最大效应(p<0.05)。
将实施例1和2与青藤碱及吗啡各自单独用药时的最大镇痛效应以及效应维持时间进行对比。给药后最大镇痛效应百分率计算公式为:%mpe=(给药后pwt-给药前pwt)/(cfa造模前pwt基线值-给药前pwt)×100。所得结果见表1:
表1.实施例1-2的镇痛药物组合物与青藤碱及吗啡各自单独用药时的镇痛效应比较
从表1中可以看出,在实施例1中青藤碱剂量为8.7mg/kg,远低于青藤碱单独用药剂量(20mg/kg),同时吗啡剂量为0.14mg/kg,也远低于吗啡单独用药剂量(1mg/kg)。但是其最大镇痛效应达81.1%,远高于青藤碱单独用药(46.6%)以及吗啡单独用药(61.4%),而且效应维持时间也要长于单独用药。在实施例2中青藤碱剂量为13.1mg/kg,吗啡剂量为0.07mg/kg,虽都远低于青藤碱及吗啡各自单独用药剂量,但是其最大镇痛效应(65.8%)以及效应维持时间均比青藤碱及吗啡单独用药时要强。
结果说明实施例1和2的镇痛药物组合物在急性给药下,对cfa炎症疼痛产生明显镇痛作用,与青藤碱以及吗啡各自单独用药时相比,镇痛效应明显得到增强。
在此实施方式中,与青藤碱协同作用的吗啡的单次镇痛剂量为0.07~0.14mg/kg大鼠体重,相当于约0.7~1.4mg的人剂量(根据体表面积法进行估算,标准体重60kg成人的剂量(mg)约为大鼠每公斤体重剂量(mg/kg)的10倍左右,算法下同),远低于吗啡作为镇痛药物在临床上单独注射时的一般成人剂量(单次5~15mg);青藤碱剂量使用8.7~13.1mg/kg大鼠体重,相当于约87~131mg的人剂量。而临床报导的青藤碱常规剂量为50~150mg/单次,200~240mg/日,没有超过临床常规推荐剂量。
2.反复多次给药对cfa炎症疼痛的慢性镇痛效应
(1)动物分组与实验设计:取sd大鼠24只,标准体重200±20g,分成3组,每组8只。即为cfa模型对照组,实施例1(青藤碱8.7mg/kg+吗啡0.14mg/kg)与实施例2(青藤碱13.1mg/kg+吗啡0.07mg/kg)组。cfa造模方法同前述,实施例1与2均采用皮下注射给药,cfa模型对照组给予注射生理盐水。各组大鼠在造模前测定其pwt基线值(bl),然后全部给予cfa造模,24h后于开始给药,每天给药2次,连续给药7天,于每天给药后1.5h测定其pwt。测定pwt方法同前述。
(2)实验结果:实施例1-2的镇痛药物组合物反复多次给药对cfa炎症疼痛的慢性镇痛效应结果如图2所示。cfa模型组在测试期间的7天内,重复测量的疼痛阈值都稳定保持在最低水平。统计分析显示实施例1与2反复多次给药,在7天内均能显著提高大鼠的机械疼痛阈值(p<0.05)。结果表明,实施例1与2连续用药7天,产生持续显著镇痛作用,未见到药物耐受性产生。在长期给药实验完毕后进行突然停药,连续3天未观察到大鼠有任何异常的停药反应,说明其无明显成瘾性。
在此实施方式中,实施例1与2中的吗啡的慢性使用剂量为0.14~0.28mg/kg大鼠体重,相当于约1.4~2.8mg的人剂量,远低于吗啡作为镇痛药物在临床上每日常规使用剂量(15~40mg/日);青藤碱慢性剂量使用17.4~26.1mg/kg大鼠体重,相当于约174~261mg的人剂量。而临床报导的青藤碱常规剂量为200~240mg/日,故在临床实际中,不超过临床常规推荐剂量即可。
3.对cci神经病理性疼痛的镇痛效应
(1)cci神经病理性疼痛模型的制备方法:大鼠采用异氟烷麻醉后,手术暴露右侧坐骨神经,在该神经主干部位,用4.0铬制羊肠线松结扎4道,每根羊肠线间隔1-2mm,逐层缝合肌肉及皮肤,术后将大鼠置于安静、温暖、避强光环境喂养。cci手术结束后2小时以及随后每隔24h测定pwt值。pwt测定方法同前。
(2)动物分组与实验设计:取sd大鼠40只(由南通大学实验动物中心提供),标准体重200±20g,将其分成5组,每组8只;即cci模型组(阴性对照,给予生理盐水),青藤碱20mg/kg单独用药组,吗啡1.0mg/kg单独用药组,以及本发明实施例3(青藤碱9.0mg/kg+吗啡0.095mg/kg)与实施例4(青藤碱6.8mg/kg+吗啡0.024mg/kg)组,均采用皮下注射给药。各组大鼠在造模前测定其pwt基线值(bl),然后全部给予cci手术造模,24h后先测试各组给药前的pwt值,然后于给药后0.5、1、1.5、2、2.5、3、3.5、4h测定其pwt。测定pwt方法同前述。
(3)实验结果:实施例3-4的镇痛药物组合物及青藤碱与吗啡单独用药对cci神经病理性疼痛的镇痛效果比较如图3所示。cci模型组在测试期间的4h内,重复测量的疼痛阈值都稳定保持在最低水平。统计结果表明青藤碱20mg/kg组在1.5~2h时间段有明显镇痛效应,2h达最大效应(p<0.05);吗啡1.0mg/kg组在0.5~2.5h时间段有明显镇痛效应,1.5h达最大效应(p<0.05);实施例3组在0.5~3.5h时间段有明显镇痛效应,2.5h达最大效应(p<0.05);实施例4组在0.5~3h时间段有明显镇痛效应,1h达最大效应(p<0.05)。
我们将实施例3和4与青藤碱及吗啡各自单独用药时的最大镇痛效应以及效应维持时间进行对比。给药后最大镇痛效应百分率计算公式为:%mpe=(给药后pwt-给药前pwt)/(cfa造模前pwt基线值-给药前pwt)×100。所得结果见表2:
表2.实施例3-4的镇痛药物组合物与青藤碱及吗啡各自单独用药时的镇痛效应比较
从表2中可以看出,在实施例3中青藤碱剂量为9mg/kg,远低于青藤碱单独用药剂量(20mg/kg),同时吗啡剂量为0.095mg/kg,也远低于吗啡单独用药剂量(1mg/kg)。但是其最大镇痛效应达94.3%,高于青藤碱单独用药(71.5%)以及吗啡单独用药(87.5%),而且效应维持时间也要长于各自单独用药。在实施例4中青藤碱剂量为6.8mg/kg,吗啡剂量为0.024mg/kg,虽都远低于青藤碱及吗啡各自单独用药剂量,但是其最大镇痛效应(93.8%)以及效应维持时间均比青藤碱及吗啡单独用药时要强。
结果说明实施例3和4急性给药下,对cci神经病理性疼痛产生明显镇痛作用,与青藤碱以及吗啡各自单独用药时相比,镇痛效应明显得到增强。
在此实施方式中,与青藤碱协同作用的吗啡的单次镇痛剂量为0.024~0.095mg/kg大鼠体重,相当于约0.24~0.95mg的人剂量,远低于吗啡作为镇痛药物在临床上单独注射时的一般成人剂量(单次5~15mg);青藤碱剂量使用6.8~9.0mg/kg大鼠体重,相当于约68~90mg的人剂量。而临床报导的青藤碱常规剂量为50~150mg/单次,没有超过临床常规推荐剂量。
4.多次给药对cci神经病理性疼痛的慢性镇痛效应
(1)动物分组与实验设计:取sd大鼠24只,标准体重200±20g,分成3组,每组8只。即为cci模型对照组,实施例3(青藤碱9.0mg/kg+吗啡0.095mg/kg)与实施例4(青藤碱6.8mg/kg+吗啡0.024mg/kg)组。cci造模方法同前述,实施例3与4均采用皮下注射给药,cci模型对照组给予注射生理盐水。各组大鼠在造模前测定其pwt基线值(bl),然后全部行cci手术造模,24h后于开始给药,每天给药2次,连续给药7天,于每天给药后1.5h测定其pwt。测定pwt方法同前述。
(2)实验结果:实施例3-4的镇痛药物组合物反复多次给药对cci神经病理性疼痛的慢性镇痛效应结果如图4所示。cfa模型组在测试期间的7天内,重复测量的pwt值都稳定保持在最低水平。统计分析显示实施例3与4反复多次给药,在7天内均能显著提高大鼠的pwt值(p<0.05)。结果表明,实施例3与4连续用药7天,产生持续显著镇痛作用,未见到药物耐受性产生。在长期给药实验完毕后进行突然停药,连续3天未观察到大鼠有任何异常的停药反应,说明其无明显成瘾性。
在此实施方式中,实施例3与4中的吗啡的慢性使用剂量为0.048~0.19mg/kg大鼠体重,相当于约0.48~1.9mg的人剂量,远低于吗啡作为镇痛药物在临床上每日常规使用剂量(15~40mg/日);青藤碱慢性剂量使用13.6~18.0mg/kg大鼠体重,相当于约136~180mg的人剂量,要低于临床报导的青藤碱临床推荐剂量200~240mg/日。
综上,本发明的用于治疗、改善和缓解受试对象的疼痛的药物组合物能够使用明显低于日常剂量的常规镇痛药来实现镇痛效果。事实证明,在单独使用镇痛药物,如青藤碱大剂量也有可能达不到有效的镇痛效果而且还产生副作用时,或者使用大剂量阿片类药物如吗啡时易产生耐受性以及成瘾性等副作用时,上述药物的小剂量的特定组合,可产生非常有效的镇痛作用,且无副作用的发生。
上述实施例为本发明较佳的实施方式,但本发明的实施方式不受上述实施例的限制。其他任何不脱离本发明之精神和原理下所作的变形,均应认为是本发明的保护范围。
- 还没有人留言评论。精彩留言会获得点赞!