一种紫外荧光分子探针的合成及其对亚硝酸根的检测的制作方法
本发明涉及的是一种紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的合成及其对亚硝酸根的检测,属于有机发光材料领域。
背景技术:
亚硝酸盐主要指亚硝酸钠(nano2)和亚硝酸钾(kno2),为白色或微黄色结晶或颗粒状粉末,称为工业食盐。由于对肉质食品有护色、抑菌、增强肉质风味的作用,因此亚硝酸盐被当作发色剂、防腐剂而应用于肉类制品中,但是亚硝酸盐具有较强的氧化性,大量摄入可使血红蛋白(fe2+)变成高铁血红蛋白(fe3+),失去输氧能力,导致组织缺氧,并对周围血管有扩张作用;另外硝酸盐是高致癌n-亚硝基化合物产生的重要前体物质,n-亚硝基化合物包括亚硝胺和亚硝酰胺,前者在体内经酶激活后成为致癌物,后者不需任何代谢激活即能在胃中直接诱发肿瘤。同时,no2-的过量摄入会引起诸如流产,婴儿高铁血红蛋白症,新生儿中枢神经缺陷,食道癌等诸多疾病,是威胁人类健康的重大隐患。目前,格里斯试剂(griess)比色法和2,3-二氨基萘试剂荧光法是检测亚硝酸根离子最常用的两种方法。但是这两种方法检测亚硝酸根离子时,都需要多种试剂组合,其中格里斯方法的试剂是由对氨基苯磺酰胺水溶液和萘乙二胺的磷酸溶液混合制得,需要避光冷藏储存,半小时内用完,并且试剂储存困难,检测步骤繁琐、复杂,耗时长。因此建立一种简便、高灵敏度检测亚硝酸根的方法对于保障人体生命安全具有重要的应用价值。
技术实现要素:
发明内容
鉴于上述,本发明的目的是一种紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的合成。
本发明的另一目的是该紫外荧光分子探针对亚硝酸根的检测。
本发明的目的是通过以下技术方案来实现:
一种紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺合成
a.将20ml甲苯、25ml乙醇、6ml超纯水加入到150ml的圆底烧瓶中混合摇匀,将混合溶剂在-70摄氏度的液氮中冷冻,抽真空至真空度0.08mpa,将圆底烧瓶放在室温下,置换氩气,解冻,溶剂溶解后再次放入液氮中冷冻,抽真空,置换氩气,上述步骤再重复一次,将溶剂中的溶解氧除净,溶液保存在氩气氛围下,作为下一步反应的溶剂;
b.向带有回流冷凝管装置250ml的两口圆底烧瓶中加入3-溴-4-氨基-n-丙基-1,8-萘二甲酸亚胺,碳酸钾,3-(n,n-二甲基氨基)苯基硼酸盐酸盐,在催化剂四三苯基膦钯条件下,密封接口处,氩气保护,将上述除净氧的溶剂用注射器注入烧瓶,90摄氏度回流36h,反应结束后,将体系冷却至室温,减压浓缩溶剂得到粗产品,粗产品通过硅胶柱柱层析,层析液二氯甲烷和甲醇体积比为50:1,洗脱,分离得到紫外荧光分子探针——3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺。
紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的合成结构式如下:
紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的理化性质:
3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺(c24h25n3o2)是易溶于水的黄色固体,其分子量为387.1947,熔点为158-166摄氏度。
紫外荧光分子探针测定亚硝酸根的机理。
在酸性条件下,亚硝酸根进攻3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的氨基位点,发生消去反应,消去水分子,生成11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮。探针的荧光发射产生波长产生60nm的斯托克斯位移,通过体系荧光信号的改变与亚硝酸根离子浓度间的线性关系,实现对实际样品中的亚硝酸根的快速定性定量检测。同时,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣作用后,生成了11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮,其颜色变为紫色,说明3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺探针可以通过颜色变化对no2﹣实现定性的识别。
本发明的优点和产生的有益效果:
本发明克服了现有技术的不足之处。利用3-溴-4-氨基-n-丙基-1,8-萘二甲酸亚胺,碳酸钾,3-(n,n-二甲基氨基)苯基硼酸盐酸盐合成了紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺。探针与亚硝酸根反应后生成11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮,其紫外吸收最大波长为550nm处,最强荧光发射在600nm处。本发明用于各类水和肉类样品的亚硝酸根的含量测定,可以检测出水和肉类样品中的亚硝酸根的含量,最低检测限分别为390nm和52nm,探针响应速度快,1分钟内可达响应平衡,对于保障人体健康产生积极的作用。本发明合成的紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺光学性质稳定,储存时间长,特异性好,灵敏度高,响应迅速,是一种快捷的检测亚硝酸根的方法。
附图说明
图1为所合成的3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的1h谱。
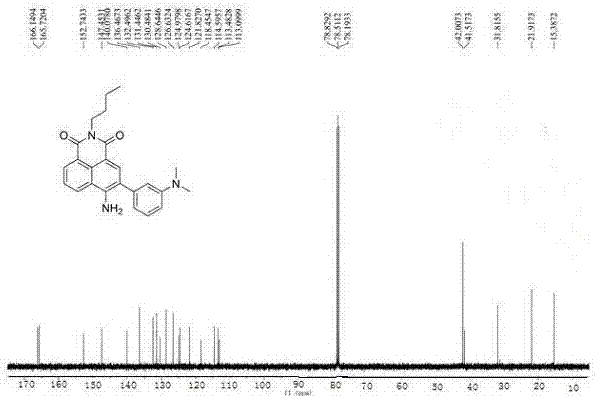
图2为所合成的3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的13c谱。
图3为所合成的3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的高分辨质谱图。谱图中388.2016[m+h+]为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的分子离子峰。
图4为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与亚硝酸根反应后产物的高分辨质谱图,谱图中399.1814[m+h+]为11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的分子离子峰。
图5为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的紫外吸收光谱
图6为11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的紫外吸收光谱(b)
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl。
图7为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的荧光发射光谱
图8为11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的荧光发射光谱
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl。
图9为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣在不同作用时间下的荧光强度变化
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl。
图10为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与各种被分析物作用的紫外吸收光谱
图11为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与各种被分析物作用的荧光发射光谱
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl。
图12为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与不同浓度的no2﹣作用后的紫外-可见吸收光谱变化
图13为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与不同浓度的no2﹣作用后的紫外最大吸收强度与no2﹣浓度的线性关系
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl,no2﹣:0,2.0,4.0,6.0,8.0,10,12,14,16,18,20,22,24,26,28,30,35,40μm。
图14为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与不同浓度的no2﹣作用后的荧光发射光谱变化
图15为3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与不同浓度的no2﹣作用后的最大荧光强度与no2﹣浓度的线性关系
测试体系为20μm3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,20μmnano2,1mol/lhcl,no2﹣:0,2.0,4.0,6.0,8.0,10,12,14,16,18,20,22,24,26,28,30,35,40μm。
具体实施方式
下面结合附图和实施例及实验例对本发明技术方案再做进一步说明:
实施例1
将20ml甲苯、25ml乙醇、6ml超纯水加入到150ml的圆底烧瓶中混合摇匀,将混合溶剂在-70摄氏度的液氮中冷冻,抽真空至真空度0.08ppm,将圆底烧瓶放在室温下,置换氩气,解冻,溶剂溶解后再次放入液氮中冷冻,抽真空,置换氩气,上述步骤再重复一次,将溶剂中的溶解氧除净,溶液保存在氩气氛围下,作为下一步反应的溶剂;
向带有回流冷凝管装置250ml的两口圆底烧瓶中加入0.2805g3-溴-4-氨基-n-丙基-1,8-萘二甲酸亚胺,0.7015g碳酸钾,0.5081g3-(n,n-二甲基氨基)苯基硼酸盐酸盐,在5%四三苯基膦钯催化下,密封接口处,氩气保护,将上述除净氧的溶剂用注射器注入烧瓶,90摄氏度回流36h,反应结束后,将体系冷却至室温,减压浓缩溶剂得到粗产品,粗产品通过硅胶柱柱层析,层析液二氯甲烷和甲醇体积比为50:1,洗脱,分离得到紫外荧光分子探针——3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,产率为75%,该分子化学性质稳定,可长期储存不变质。
将探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,溶于1mol/l的盐酸溶液,向其中加入不同含有亚硝酸根的样品,1分钟后,观察其颜色变化,同时用紫外-可见吸收光谱和荧光发射光谱,记录其吸收和发射光谱的变化,通过颜色和光谱性质的改变测定亚硝酸根的含量。
探针合成后用核磁共振波谱仪对产物进行测试,得到其氢谱图1,证明有25个氢原子,其化学位移数据为:
1hnmr(400mhz,cdcl3)δ=8.59,8.57,8.45,8.17,8.15,7.67,7.65,7.63,7.38,7.36,7.36,7.34,7.26,6.83,6.81,6.79,6.79,6.78,6.77,6.77,5.21,4.19,4.17,4.16,3.00,1.74,1.73,1.72,1.71,1.70,1.70,1.69,1.68,1.47,1.45,1.43,1.41,1.25,0.98,0.96,0.95.
得到其碳谱图2,证明有24个碳原子其化学位移数据为:
13cnmr(100mhz,cdcl3)δ=166.15,165.72,152.74,147.45,140.08,136.47,132.50,131.45,130.48,128.64,126.63,124.98,124.62,121.83,118.45,114.60,113.48,113.10,78.83,78.51,78.19,42.01,41.52,31.82,21.92,15.39.
高分辨质谱图3显示其分子量为esi-msm/z(m+h+)=388.2016。
以上表征证明了化合物3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺合成成功。
下面,本发明通过高分辨质谱、紫外吸收光谱、荧光发射光谱实验对紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺对亚硝酸根的检测性能进行了试验。
1.高分辨质谱试验
合成成功后,首先本发明研究了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺分子与亚硝酸根的作用机理。
向3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺中加入20μm的no2﹣,室温条件下孵化1min(hcl:1mol/l)后,在m/z:399.1816处出现11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的分子离子峰(图4),分子离子峰的出现证明了11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的形成,这与推测的反应机理的是一致。
2.紫外荧光试验
测定3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的紫外-可见吸收光谱和荧光发射光谱。
在酸性条件下测定(hcl:1mol/l)3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣作用前后的紫外和荧光性质变化,首先本发明测定了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺和11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的紫外-可见吸收光谱,如图5所示,在酸性条件下,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在445nm处有强烈的紫外吸收。而3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣作用生成11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮后,图6显示3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在445nm处的紫外吸收降低,同时在360nm和550nm处出现新的紫外吸收峰。确定了该条件下3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺和11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的紫外-可见吸收光谱后,本发明测定了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺和11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的荧光发射光谱,图7显示3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在540nm处有强烈的荧光发射,而从图8可以看出11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮在600nm处有强烈的荧光发射。
3.响应时间实验
确定了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺和11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的吸收和发射光谱性质后,本发明对3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣的作用时间进行了研究。图9表明,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺可以在60s内与no2-达到反应平衡,其600nm处的荧光增强达到最大值(λex=570nm)。
4.选择性实验
为了研究3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺探针对no2﹣的识别能力,本发明将3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺分别与被分析物so42﹣,no3﹣,hpo4﹣,ac﹣,clo4﹣,br﹣,n3﹣,cl﹣,co32﹣,hco3﹣,so32﹣,k+,al3+,mn2+,zn2+,fe3+,fe2+,mg2+,ca2+,cu2+,na+,co2+孵化1min,孵化完成后,用紫外-可见分光光度计记录紫外吸收光谱,用荧光分光光度计记录3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在570nm激发波长下在600nm的荧光发射光谱。如图10所示,当3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺与no2﹣作用时,其紫外吸收光谱在370nm和550nm处出现新的吸收峰,荧光发射光谱在600nm处出现发射峰(图11λex=570nm),而与其他被分析物作用后,其紫外和荧光光谱均无变化。这一结果证明,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺可以对no2-实现特异性的识别。
5.浓度滴定实验
考察了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的响应时间和选择性以后,本发明研究了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺对于no2﹣的定量检测能力。本发明分别用紫外吸收和荧光发射光谱对其定量性能进行了考察。向不同体积的1mmol/lnano2中分别加入2.0μl3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺(10mm),用1mol/l的hcl定容至1ml,,孵化1min。孵化完成后,用紫外-可见分光光度计记录3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺及其与亚硝酸钠反应后的产物11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的紫外吸收光谱,用荧光分光光度计记录3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在570nm激发波长下的荧光发射光谱。由图12可以看出,随着no2﹣浓度的增加,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺在445nm处的紫外吸收降低,在370nm和550nm处出现新的紫外吸收峰,并且逐渐增强,此外,550nm处的吸收强度与no2﹣(0-30μmol/l)的浓度呈现出了良好的线性关系(回归方程y=0.01+0.011×[no2﹣],r=0.992),检出限(lod,s/n=3)可以达到0.39μm(σ=0.00144)(图13)。
同时,如图14所示,其荧光发射光谱也展现出了相同的趋势,随着no2﹣的加入,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺分子在540nm处的荧光发射降低,其600nm处的荧光发射逐渐增强,并且与no2﹣(0-30μmol/l)的浓度呈现出了良好的线性关系(回归方程y=69.65+10.91×[no2﹣],r=0.993),检出限(lod,s/n=3)可以达到52nm(σ=0.19)(图15)。这一结果表明,3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺可以在紫外-可见吸收和荧光发射两种模式下对no2﹣进行定量分析。
6.黄河水、自来水、猪肉、鸡肉中亚硝酸根的含量测定实验
在系统的研究了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺的光学性质以后,本发明将其应用于实际样品中no2﹣的含量测定。为此,本发明直接测定了黄河水样中no2﹣的含量,并且采用加标回收的方法测定了自来水样和肉类样品中no2﹣的含量。实验测得的四种不同实际样品中no2﹣的含量与传统的griess方法测定的结果相近(见表1,2)。
表1,表2证明了3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺可以应用于实际样品中no2﹣的定量测试。具体方法为:
a.样品处理
黄河水样取自黄河兰州段,所取得水样用0.45μm的微孔滤膜过滤;
自来水样取自实验室用水,向50ml的自来水样中加入250μlnano2(10mm),用0.45μm的微孔滤膜过滤;精确称取2.3806g的猪肉,搅碎,用超纯水定容至80ml,超声15min后,75oc下加热5min,冷却至室温,取出45ml,用超纯水定容至50ml,离心(800r,5min),用0.45μm的微孔滤膜过滤后备用;精确称取2.3596g的猪肉,搅碎,加入500μlnano2(10mm),用超纯水定容至80ml,超声15min后,75oc下加热5min,冷却至室温,取出45ml,用超纯水定容至50ml,离心(800r,5min),用0.45μm的微孔滤膜过滤后备用;精确称取2.3432g的鸡肉,搅碎,用超纯水定容至80ml,超声15min后,75oc下加热5min,冷却至室温,取出45ml,用超纯水定容至50ml,离心(800r,5min),用0.45μm的微孔滤膜过滤后备用;精确称取2.3571g的鸡肉,搅碎,加入500μlnano2(10mm),用超纯水定容至80ml,超声15min后,75oc下加热5min,冷却至室温,取出45ml,用超纯水定容至50ml,离心(800r,5min),用0.45μm的微孔滤膜过滤后备用。
b.本发明与griess法测定实际样品中no2﹣含量的比照:
griess试剂配制:
称取50mg对氨基苯磺酰胺,用超纯水定容至50ml得1%的对氨基苯磺酰胺;称取500mg萘乙二胺,用5%的磷酸定容至50ml得到1%的萘乙二胺。将1%对氨基苯磺酰胺与1%萘乙二胺按照体积比1:1混合,得到griess试剂,避光冷藏储存,半小时内用完。
标准曲线建立,向100μl的griess试剂中,分别加入(0,15,30,75,150,225,300.0μl)的nano2(1mm),用超纯水定容至1ml,摇匀,室温孵化30min后,记录其在波长为548nm处的吸光度数值。并根据浓度与吸光度的关系绘制标准曲线。
建立曲线后,取2.9ml上述处理好的实际样品,加入100μl的griess试剂,摇匀,室温孵化30min,记录其在波长为548nm处的吸光度数值。根据标准曲线计算实际样品中的亚硝酸根含量。
本发明用紫外吸收光谱法和荧光发射光谱法测定实际样品中no2﹣含量
紫外法测定实际样品中no2﹣含量
取2.9ml上述处理好的实际样品,分别加入2μl的3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,摇匀,室温孵化1min,用紫外-可见分光光度计记录其紫外吸收光谱。
荧光法测定实际样品中no2﹣含量
取2.9ml上述处理好的实际样品,分别加入2μl的3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺,摇匀,室温孵化1min,用荧光分光光度计记录570nm的激发波长下的荧光发射光谱。
测试结果表明黄河水中的亚硝酸根含量为:
表1.黄河水样中的no2﹣含量测定
测试结果表明自来水、猪肉、鸡肉中的亚硝酸根含量分别为:
通过对紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺及其与亚硝酸反应生成的产物11-正丁基-2-二甲氨基-10h-苯基甲酰[c]异喹啉[4,5-gh]邻二氮萘-10,12(11h)-二酮的光学性质研究,证明了本发明合成的紫外荧光分子探针3-二甲氨基苯基-4-氨基-n-丁基-1,8-萘二甲酸亚胺可以通过紫外-可见吸收光谱和荧光发射光谱的分析方式实现对no2﹣的测定,相比传统的griess方法,本发明光学性质稳定,特异性好,灵敏度高,响应迅速,仅需一步即可以完成对亚硝酸根的检测,探针更易于保存,操作更加简单,是一种快捷的检测亚硝酸根的简便方法。
- 还没有人留言评论。精彩留言会获得点赞!