一种戈氏梭菌特异性PCR检测引物及方法与流程
本发明涉及一种戈氏梭菌特异性PCR检测引物及方法,属于生物检测技术领域。
背景技术:
戈氏梭菌(Clostridium ghonii)为革兰氏阳性菌,严格厌氧菌,可存在土壤、水中沉积物、动物和人肠道中。目前戈氏梭菌的研究主要集中于利用其趋肿瘤内低氧特性(仅可在肿瘤乏氧区大量繁殖),并分泌多种水解酶和诱导机体抗肿瘤免疫反应,抑制肿瘤组织生长的作用,进行细菌溶瘤药物一类新药的研发。
中国专利文献CN104473973A(申请号201410803072.X)公开了一株驯化戈氏梭菌MW-DCG-HNCv-18菌株在制备治疗非小细胞肺癌药物中的应用。该发明还公开了驯化戈氏梭菌MW-DCG-HNCv-18菌株和多西他赛为药效成分联用的药物。该发明首次发现MW-DCG-HNCv-18菌株对非小细胞肺癌具有特异性抑制作用,对非小细胞肺癌抑制效果显著优于现有已知的其他类似菌株,并通过筛选发现其与多西他赛注射液联用时,对非小细胞肺癌抑制效果更加突出,为治疗非小细胞肺癌提供了新的途径。
此外美国专利文献141397,293、欧洲专利文献13780960.4、澳大利亚专利文献2013252495等均公开了戈氏梭菌临床前抗肿瘤作用的有效性,显示出较好的药物开发前景。但是,戈氏梭菌体内组织分布的高特异性、高灵敏性的快速检测仍是未解决的难题,也是临床检测的难点。
目前,主要采用染色镜检、生理生化反应和16S rRNA测序和组织切片革兰氏染色进行细菌分布研究和临床检测,检测结果仍存在步骤复杂、特异性不强、灵敏度不高、易误判的问题。
采用PCR技术来进行细菌的体内分布和临床检测,具有操作简单、特异性强、灵敏度高、结果易判的特点。但由于戈氏梭菌目前尚未检测获得其基因组序列,且对该菌株研究较少,相关研究仅限于菌株整体应用,对于其分子水平的研究较少,从而限制了PCR技术对其进行检测技术的开发。
技术实现要素:
本发明针对现有技术的不足,提供一种戈氏梭菌特异性PCR检测引物及方法。该引物可用于戈氏梭菌的PCR检测,具有检测时间短,成本低,检测结果特异性高,灵敏度强,结果易判断,实用性强。
本发明是通过以下的技术方案实现:
戈氏梭菌硫氧还蛋白编码基因Trx,核苷酸序列如SEQ ID NO.3所示。
戈氏梭菌硫氧还蛋白(Thioredoxin,Trx)是一类高度保守的低分子量蛋白质,广泛分布于植物、细菌、酵母和动物中,在许多还原反应中作为氢供体,参与氧化还原反应。但发明人通过研究发现,戈氏梭菌硫氧还蛋白的编码基因Trx与Clostridium Novyi、Clostridium beijerinckii、Clostridium sporogenes等亲缘关系接近的其他梭菌属厌氧菌硫氧还蛋白基因序列相似度不高,分别仅为25.23%、34.60%和33.38%,这为利用该基因进行戈氏梭菌的特异性检测创造了条件。
一种戈氏梭菌特异性PCR检测引物,该引物为一对,正向引物核苷酸序列如SEQ ID NO.1所示,反向引物核苷酸序列如SEQ ID NO.2所示。
正向引物F:5’-ATGGCTAAAACAATAAATACAGGGA-3’ SEQ ID NO.1
反向引物R:5’-TTATAAATGAGCTTCTACTTTTGCT-3’ SEQ ID NO.2
利用上述戈氏梭菌特异性PCR检测引物进行PCR检测的方法,步骤如下:
(1)提取组织样品中的RNA;
(2)将步骤(1)提取获得的RNA进行反转录,制得cDNA;
(3)以步骤(2)制得的cDNA为模板,上述戈氏梭菌特异性PCR检测引物为特异引物,进行PCR扩增,获得扩增产物;
(4)取步骤(3)制得的扩增产物,经电泳检测,如果检测结果在315bp处出现条带,则组织样品中含有戈氏梭菌,如果检测结果中未在315bp处出现条带,则组织样品中不含戈氏梭菌。
根据本发明优选的,所述步骤(3)中,PCR扩增体系如下,总体积20μL:
最后用灭菌双蒸水补至20μL。
根据本发明优选的,所述步骤(3)中,PCR扩增程序如下:
94℃预变性3min;94℃变性30s,60℃退火30s,72℃延伸20s,32个循环;72℃延伸5min,4℃保存。
根据本发明优选的,所述步骤(4)中,所述电泳检测为采用质量百分比为1.5%的琼脂糖凝胶电泳检测。
上述步骤(1)中的组织样品中的RNA提取及步骤(2)中的反转录均可采用本领域常规技术;如RNA提取可采用Trizol法进行提取,反转录可采用TaKaRa公司生产的TaKaRa PrimeScriptTMRT-PCR kit(RR014A)反转录试剂盒进行反转录。
有益效果
本发明首次公开了戈氏梭菌硫氧还蛋白的编码基因Trx不同于Clostridium Novyi、Clostridium beijerinckii、Clostridium sporogenes等亲缘关系接近的其他梭菌属厌氧菌硫氧还蛋白基因序列高度保守的规律,并根据该发现设计出戈氏梭菌特异性PCR检测引物,解决了PCR技术进行戈氏梭菌体内分布和临床检测的技术难题;本发明检测的靶点具有特异性,检测结果特异,易于判定;为戈氏梭菌抗肿瘤药物研发、临床戈氏梭菌快速检测和流行病学调查提供技术支撑。
附图说明
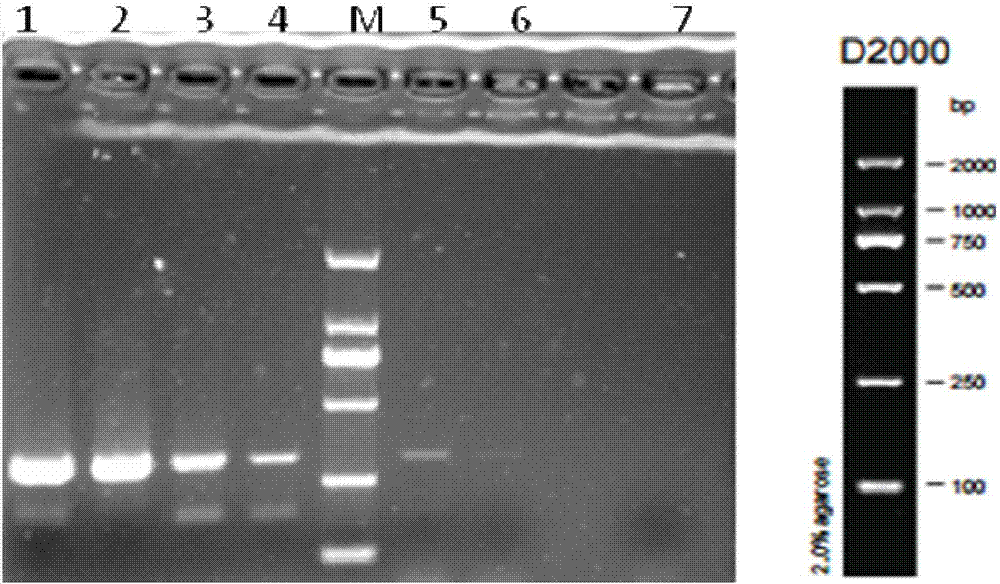
图1为实施例中PCR检测方法特异性评估实验凝胶电泳结果图;
图中:泳道1为肠,泳道2为胃,泳道3为大肠杆菌,泳道M为Marker(D2000),泳道4为肺,泳道5为戈氏梭菌,泳道6为戈氏梭菌芽孢,泳道7为灭菌双蒸水;
图2为实施例中PCR检测方法灵敏度评价实验凝胶电泳结果图;
图中:泳道M为Marker(D2000),泳道1为戈氏梭菌的阳性对照,泳道2为初始模板cDNA的101倍稀释液PCR扩增结果,泳道3为初始模板cDNA的102倍稀释液PCR扩增结果,泳道4为初始模板cDNA的103倍稀释液PCR扩增结果,泳道5为初始模板cDNA的104倍稀释液PCR扩增结果,泳道6为初始模板cDNA的10 5倍稀释液PCR扩增结果,泳道7为灭菌双蒸水。
图3为实施例中PCR检测方法特异性检测戈氏梭菌和Clostridium Novyi凝胶电泳结果图;
图中:泳道1为戈氏梭菌,泳道2为Clostridium Novyi,泳道M为Marker(D2000),泳道3为灭菌双蒸水。
具体实施方法
下面结合具体实施例,进一步阐述本发明。应理解,这些实施例仅用于说明本发明而不用于限制本发明的范围。
实施例中未注明具体条件的实验方法,通常按照常规条件例如Sambrook等分子克隆:实验室手册(New York:Cold Spring Habor Laboratory Press,1989)中所述的条件,或按照制造厂商所建议的条件。
实施例中所述戈氏梭菌来源于澳大利亚国家计量研究院,菌株保藏号V12/001485。
实施例中所述Clostridium Novyi来源于ATCC,菌种保藏号编号ATCC7659。
实施例1戈氏梭菌特异性PCR检测引物的开发
发明人通过前期对戈氏梭菌全基因组测序和对测序结果的分析发现,该菌含有编码硫氧还蛋白的基因序列,核苷酸序列如SEQ ID NO.3所示。
利用DNAMAN软件比对发现,该菌硫氧还蛋白基因序列与Clostridium Novyi、Clostridium beijerinckii、Clostridium sporogenes等亲缘关系接近的其他梭菌属厌氧菌硫氧还蛋白基因序列相似度不高,分别仅为25.23%、34.60%和33.38%,这不同于梭菌属厌氧菌硫氧还蛋白基因序列高度保守的规律。根据编码戈氏梭菌硫氧还蛋白的基因序列的高特异性设计并合成特异扩增戈氏梭菌的引物。
实施例2
步骤一,设计并合成戈氏梭菌特异性PCR检测引物,核苷酸序列如下所示:
F:5’-ATGGCTAAAACAATAAATACAGGGA-3’; SEQ ID NO.1
R:5’-TTATAAATGAGCTTCTACTTTTGCT-3’; SEQ ID NO.2
步骤二,RNA模板制备
将戈氏梭菌接种于6ml RCM液体培养基(购自BD公司)中,于37℃厌氧工作站中培养12h后,取1m L菌液,6000r/min离心5min,弃尽上清,加入100μL灭菌双蒸水,用移液器轻轻吹打,重悬菌体;将菌液放入液氮充分预冷的研钵中研磨至粉末,加入1mL Trizol进行RNA提取。
步骤三,RNA反转录成cDNA
按照TaKaRa PrimeScriptTMRT-PCR kit(RR014A)试剂盒说明书进行反转录,制得cDNA模板,测定cDNA模板浓度。
步骤四,戈氏梭菌特异性PCR检测方法建立
PCR检测体系为:
2×Taq MasterMix 10μL,10μM的正向引物F 1Μl,10μM的反向引物R 1μL,cDNA模板1μL,灭菌双蒸水补至20μL;
PCR检测程序为:
94℃预变性3min;94℃变性30s,60℃退火30s,72℃延伸20s,32个循环;72℃延伸5min,4℃保存。
步骤五,PCR扩增结果凝胶电泳判定
所述判断具体为:质量百分比浓度为1.5%凝胶电泳检测扩增产物,紫外灯照射下观察电泳结果,如果出现315bp的扩增条带,则说明样本中含有戈氏梭菌;反之,则样本中不含戈氏梭菌。
实施例3PCR检测方法特异性评价试验
按实施例2所述方法制备cDNA模板与PCR检测,对戈氏梭菌、大肠杆菌、胃、肠等样本中的细菌进行PCR扩增反应。
特异性检测结果如图1所示,图1结果显示只有戈氏梭菌在315bp处有特异性条带,而其它泳道均未出现特异性条带。
PCR检测方法灵敏度评价试验
接种戈氏梭菌于6mL RCM液体培养基中,置于37℃厌氧工作站中培养12h后,取1ml菌液,用无菌1×PBS缓冲液进行10倍梯度稀释后,平板法计数,细菌浓度为108CFU/mL。取1mL菌液按实施例提取RNA,进行反转录,并检测cDNA浓度,以灭菌双蒸水稀释cDNA,稀释倍数为101-105,以梯度稀释的cDNA为模板进行PCR扩增,凝胶电泳检测扩增产物,如图2所示。由图2可知,在泳道6可以看到清晰条带,其相对应检测细菌浓度为50CFU/mL,从而证明本申请所述方法具有较高的灵敏度。
实施例4
取戈氏梭菌和与戈氏梭菌遗传关系较近的Clostridium Novyi,分别按照实施例2所述方法制备cDNA模板与PCR检测,结果如图3所示。
由图3结果可以看出仅戈氏梭菌经PCR检测后在315bp处扩增出能够体现戈氏梭菌硫氧还蛋白基因的特异条带,而以Clostridium Novyi经PCR检测后未在315bp处扩增出特异条带。以上结果说明本申请设计的戈氏梭菌特异性PCR检测引物可以有效将与戈氏梭菌亲缘关系接近的菌检测区分。
应当理解的是,对本领域普通技术人员来说,可以根据上述说明加以改进或变换,而所有这些改进和变换都应属于本发明所附权利要求的保护范围。
SEQUENCE LISTING
<110> 山东新创生物科技有限公司
<120> 一种戈氏梭菌特异性PCR检测引物及方法
<160> 3
<170> PatentIn version 3.5
<210> 1
<211> 25
<212> DNA
<213> 人工合成
<400> 1
atggctaaaa caataaatac aggga 25
<210> 2
<211> 25
<212> DNA
<213> 人工合成
<400> 2
ttataaatga gcttctactt ttgct 25
<210> 3
<211> 315
<212> DNA
<213> Clostridium ghonii
<400> 3
atggctaaaa caataaatac agggaatttt agaggtgcag tagaagataa taaaggtgtt 60
gttgttgtag acttttttgc aacatggtgt gggccttgta agatgttagc tccagtattt 120
gaaagtgttt catcagaagt agataatgct aaatttgtta aagtagatat tgatgaaagt 180
ttagagttgg ctcaaaaatt tggaatctca acagtaccaa ctatgatgat atttaaagat 240
ggtaaagtag ttgataaatt agttggattt atgccaaaag aaagtttaaa agcaaaagta 300
gaagctcatt tataa 315
- 还没有人留言评论。精彩留言会获得点赞!
- 用于检测AEDs引起的SJS/TEN的引物、试剂盒及方法与制造工艺
- 检测植原体的LAMP引物组及其试剂盒和应用的制造方法与工艺
- 用于多重PCR检测致腹泻寄生虫的引物组及试剂盒的制造方法与工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种基于特异性SS-COI引物的丽草蛉PCR快速检测方法与制造工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 紫苑石斛的分子特异性标记引物及检测方法
- 一种检测牛hcd携带者的特异性pcr引物、试剂盒及检测方法
- 检测植原体的LAMP引物组及其试剂盒和应用的制造方法与工艺
- 用于多重PCR检测致腹泻寄生虫的引物组及试剂盒的制造方法与工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 紫苑石斛的分子特异性标记引物及检测方法
- 一种检测牛hcd携带者的特异性pcr引物、试剂盒及检测方法
- 用于检测牛源性成分的lamp引物及其设计方法
- 七种不同种属来源细胞的pcr检测引物和检测方法与应用
- 玉米低镁条件下特异性转运镁离子基因ZmMGT10及其应用的制造方法与工艺
- CRISPR‑Cas9特异性敲除猪SLA‑3基因的方法及用于特异性靶向SLA‑3基因的sgRNA与制造工艺
- 毛酸浆的分子特异性标记引物及鉴别方法与制造工艺
- 一种检测CYP2C9基因多态性的ARMS引物的制造方法与工艺
- 构建在海马体区域特异性敲除IKKα基因的小鼠模型的方法及打靶载体和试剂盒与制造工艺
- 使用重叠非等位基因特异性引物和等位基因特异性阻断剂寡核苷酸的组合物进行等位基因特异性扩增的制造方法与工艺
- 一种利用线粒体D-loop区特异区域鉴定鼋的标记引物及方法
- 一种用于检测大豆拟茎点种腐病菌的特异性lamp引物组合物及其应用
- 一种针对膨胀污泥中Eikelboom Type 0092型丝状菌群特异性引物和方法
- 脯氨酸特异性蛋白酶基因及其应用